文档内容
第一章 物质及其变化
专题2 化学键 分子间作用力和氢键
课时作业
基础达标
1.下列关于化学键的说法中,不正确的是
A.化学反应过程包含反应物中化学键断裂和生成物中化学键形成
B.氯化氢气体溶解于水产生氢离子和氯离子的过程中有离子键被破坏
C.化学键是相邻原子或离子间的强烈的相互作用
D.非极性键属于一种化学键
【答案】B
【解析】A.化学反应的实质是反应物中旧化学键的断裂和生成物中新化学键的形
成,故A正确;B.氯化氢气体溶解于水产生氢离子和氯离子的过程中H原子和Cl原子形
成的共价键断裂,故B错误;C.化学键包括共价键和离子键,为物质中直接相邻的原子
或离子间的强烈的相互作用,故C正确;D.非极性键是同种元素之间形成的共价键,属
于化学键,故D正确;综上所述答案为B。
2.下列叙述正确的是( )
A.离子键、共价键、分子间作用力均属于化学键
B.氯气中含离子键
C.共价化合物中一定含有共价键
D.所有物质一定含有化学键
【答案】C
【解析】A. 分子间作用力不属于化学键,A项错误;B. 离子键只存在于离子化合物
中,氯气是非金属单质,不含离子键,B项错误;C. 共价化合物中的原子以共价键相结
合,C项正确;D. 稀有气体中没有化学键,D项错误。答案选C。
3.下列每组中各物质内既有离子键又有共价键的一组是( )
A.NaOH、HSO 、(NH )SO B.MgO、NaSO 、NH HCO
2 4 4 2 4 2 4 4 3
C.NaO、KOH、NaSO D.HCl、Al O、MgCl
2 2 2 4 2 3 2
【答案】C
【解析】A中HSO 内只有共价键;B中MgO内只有离子键;D中HCl内只有共价
2 4键,Al O、MgCl 内只有离子键。
2 3 2
4.下列说法错误的是( )
A.稀有气体分子中不存在化学键
B.离子化合物中不一定含有金属元素
C.含有非极性键的化合物,不一定是共价化合物
D.阴、阳离子通过静电引力所形成的化学键叫离子键
【答案】D
【解析】A.稀有气体分子为单原子分子,不存在化学键,故A正确;B.离子化合物
中不一定含有金属元素,如NH Cl,故B正确;C.含有非极性键的化合物,不一定是共
4
价化合物,如NaO 等,故C正确;D.阴、阳离子通过静电作用力所形成的化学键叫离子
2 2
键,这种静电作用力既包括静电吸引力,又包括静电排斥力,故D错误;故选D。
5.实验室利用反应2NH Cl+Ca(OH) =====CaCl2+2HO制取氨气。在Pt催化条件下,
4 2 2
NH 可发生催化氧化反应:4NH +5O =====4NO+6H O。下列关于NH Cl说法正确的是
3 3 2 2 4
A.只含离子键 B.只含共价键
C.既含离子键也含共价键 D.既不含离子键也不含共价键
【答案】C
【解析】NH Cl中NH + 和Cl-以离子键结合,NH +内N原子和H原子形成共价键,所
4 4 4
以NH Cl既含离子键也含共价键,答案选C。
4
6.下列说法正确的是( )
A.分子间作用力与化学键的大小相当
B.分子间作用力的大小远大于化学键,是一种很强的作用力
C.分子间作用力主要影响物质的化学性质
D.分子内部的相邻原子之间强烈的相互作用称为化学键,而分子之间也存在相互作
用,称为分子间作用力
【答案】 D
【解析】 化学键是指使离子相结合或原子相结合的强烈的相互作用力,分子间作用
力是指分子间存在的将分子聚集在一起的作用力,分子间作用力比化学键弱得多,A、B
项错误,D项正确;分子间作用力主要影响物质的物理性质,如熔点、沸点和溶解性等,
C项错误。
7.下列说法正确的是 ( )
A.HO分子间存在氢键,所以HO比HS稳定
2 2 2
B.He、CO 和CH 都是由分子构成,它们中都存在共价键
2 4
C.PCl 中各微粒最外层均达到8电子稳定结构
5D.NaHCO 受热分解生成NaCO、CO 和HO,既破坏了离子键,也破坏了共价键
3 2 3 2 2
【答案】D
【解析】A. H O分子间存在氢键,影响水的沸点,稳定性是化学性质,沸点是物理性
2
质,所以稳定性与氢键无关,故A错误;B. CO 和CH 都是由分子构成,它们中都存在共
2 4
价键,He中不存在共价键,故B错误;C. PCl 中Cl的最外层电子数为7,成键电子数为
5
1,都达到8电子稳定结构,PCl 分子中P原子最外层电子数为5,成键电子数为5,达到
5
10电子结构,故C错误;D. NaHCO 受热分解生成NaCO、CO 和HO,受热分解的过程
3 2 3 2 2
中,既有离子键被破坏又有共价键被破坏,故D正确;
8.下列说法正确的是( )
A.碘晶体受热转变为碘蒸气,吸收的热量用于克服碘原子间的作用力
B.硫酸钾和硫酸溶于水都电离出硫酸根离子,所以它们在熔融状态下都能导电
C.在N、CO 和SiO 物质中,都存在共价键,它们都是由分子构成
2 2 2
D.H 和Cl 在光照条件反应生成HCl,一定有共价键的断裂和形成
2 2
【答案】D
【解析】碘晶体受热转变为碘蒸气,吸收的热量用于克服碘分子间的作用力,A项错
误;硫酸属于共价化合物,熔融状态下不导电,B项错误; SiO 属于原子晶体,C项错
2
误;H 和Cl 在光照条件反应生成HCl,H-H和Cl-Cl键断裂,形成H-Cl,D项正确。
2 2
9.短周期主族元素X、Y、Z、W原子序数依次增大,其中只有Y、Z处于同一周期
且相邻,Z是地壳中含量最多的元素,W是短周期中金属性最强的元素。下列说法正确的
是( )
A.原子半径:
B.X、Y、Z三种元素可以组成共价化合物或离子化合物
C.Y的单质的氧化性比Z的强
D.Y的气态氢化物稳定性强于Z气态氢化物
【答案】B
【解析】A. 同周期从左到右原子半径减小Z<Y,原子半径:r(X)T
C.K与T形成的两种化合物中,阴、阳离子个数比不同
D.K在T单质中燃烧所生成的化合物是淡黄色的 固体
【答案】D
【解析】A.K、L、M三种元素即Na、Mg、Al同一周期从左往右元素的金属性逐渐
减弱,故K、L、M三种元素的金属性逐渐减弱,A错误;B.Q为S,T为O,同主族元
素从上到下非金属性增强,非金属性:O>S,非金属性越强,其简单气态氢化物稳定性越
强,则稳定性:T>Q,B错误;C.K为Na,T为O,形成的两种化合物NaO、NaO,
2 2 2
阴、阳离子个数比都是1:2,C错误;D.K在T单质中燃烧即Na在O 中燃烧,所生成的
2
化合物是淡黄色的NaO,D正确;故答案为:D。
2 2
14.下表是元素周期表的一部分,请参照元素①-⑩在表中的位置,回答下列问题。
族 IA ⅡA ⅢA ⅣA ⅤA ⅥA ⅦA 0周期
2 ① ② ③ ④
3 ⑤ ⑥ ⑦ ⑧ ⑨ ⑩
(1)②的原子结构示意图是____。
(2)化学性质最不活泼的元素是_____(填元素符号)。
(3)在③、④、⑤、⑥这些元素形成的最简单离子中,离子半径由大到小的顺序是
_______________________。(填离子符号)。
(4)在这些元素的最高价氧化物对应的水化物中,酸性最强的物质与碱性最强的物质在
水溶液中发生的化学方程式为___________________________________________________。
(5)由元素③、⑤、⑨形成的一种常见的杀菌消毒剂中存在的化学键有
________________。
(6)由元素⑧和⑨形成的某种化合物可表示为XY(其中各原子均满足8电子稳定结
2 2
构),写出XY 的电子式:__________________________________。
2 2
【答案】 Ar )O2->F->Na+>Al3+ NaOH+HClO =NaClO +H O
4 4 2
共价键、离子键
【解析】由元素在周期表位置可知,①为C,②为N,③为O,④为F,⑤为Na,⑥
为Al,⑦为Si,⑧为S,⑨为Cl,⑩为Ar元素,然后结合原子结构与元素性质及元素周
期律分析解答。
(1)②为N元素,其原子核外电子排布为2、5,所以原子结构示意图为 ;
(2)0族元素Ar原子最外层有8个电子,既不容易失去电子,也不容易得到电子,化学
性质最不活泼,最稳定;
(3)根据元素在周期表的位置可知:③为O,④为F,⑤为Na,⑥为Al,这几种元素形
成的离子核外电子排布都是2、8,电子层结构相同。对于电子层结构相同的离子,核电荷
数越大,离子半径越小,所以这几种元素形成的离子中,离子半径由大到小的顺序是:O2-
>F->Na+>Al3+;
(4)同一周期元素随原子序数的增大,元素的金属性逐渐减弱,非金属性逐渐增强;同一主族元素,原子序数越大,元素的金属性越强,非金属性越弱。在上述元素中金属性最
强的是Na元素,其形成的最高价氧化物对应的水化物是NaOH;能够形成含氧酸的非金属
性最强的元素是Cl元素,其形成的最高价含氧酸是HClO,二者在水溶液中发生反应产生
4
NaClO 和HO,反应的化学方程式为:NaOH+HClO =NaClO +H O;
4 2 4 4 2
(5)③为O,⑤为Na,⑨为Cl,由这三种元素形成的一种常见的杀菌消毒剂是
NaClO,该物质是离子化合物,Na+与ClO-通过离子键结合,在阴离子ClO-中,Cl与O原
子之间通过共价键结合,故该化合物中存在的化学键有离子键、共价键;
(6)⑧为S,⑨为Cl,由元素⑧和⑨形成的某种化合物可表示为XY 是SCl,2个S原
2 2 2 2
子通过一个共价键结合,每个S原子分别与1个Cl原子结合,从而使分子中各个原子都达
到最外层8个电子的稳定结构,其电子式为: 。
直击高考
15.X、Y、Z、M是四种短周期主族元素,其中X、Y位于同一主族,Y与M、X与Z
位于同一周期。X原子的最外层电子数是其电子层数的3倍,Z原子的核外电子数比X原
子的少1。M是同周期主族元素中半径最大的。下列说法错误的是( )
A.X、Y的最简单氢化物中,X的最简单氢化物沸点更高
B.四种元素简单离子的半径大小为Y>X>Z>M
C.Y的最高价氧化物对应水化物的化学式可表示为HYO
2 4
D.X、Y、M可以组成多种离子化合物
【答案】B
【解析】A.X为O元素,对应最简单氢化物水中含有氢键,常温下为液态,而硫化
氢为气态,故水的沸点更高,故A正确;B.离子的核外电子层数越多半径越大,S2-半径
最大,Na+、O2-、N3-核外电子排布相同,核电荷数越大,离子半径越小,则四种元素简单
离子的半径大小为Y >Z>X >M,故B错误;C.S的最高价氧化物对应水化物的化学式可
表示为HSO ,故C正确;D.O、S、Na可以组成NaSO 、NaSO 等离子化合物,故D
2 4 2 4 2 3
正确;答案选B。
16.已知短周期元素M、N、X、Y、Z分布在三个周期,N、X最外层电子数相同,
物质A由原子序数依次增大的元素X、Y、Z组成,其中Z的简单离子半径在同周期中最小,X、Y、Z简单离子的核外电子排布相同,物质A的结构式如下图所示:
回答下列问题:
(1)请写出YM的电子式:__________________。
(2)N、X、Y、Z简单离子的半径由大到小的顺序(用对应离子符号表示):
_______________。
(3)在YZO 与YX的混合液中,通入足量CO,是工业制取A的一种方法,写出该反
2 2
应的化学方程式:__________________________________________。
(4)镓( Ga)与Z为同主族元素,氮化镓(GaN)和砷化镓(GaAs)作为第三代半导体材料,
31
具有耐高温、耐高电压等特性,随着5G技术的发展,它们的商用价值进入“快车道”。
下列有关说法正确的是__________________。
a. Ga位于元素周期表第四周期IVA族
b. GaN为新型无机非金属材料
c. Ga的最高价氧化物对应水化物的碱性比Z元素最高价氧化物对应水化物的碱性强
d. 酸性:HAsO >H PO >HNO
3 4 3 4 3
(5)YZM 是有机合成的重要还原剂,其合成路线如图所示
4
利用YZM 遇水反应生成的氢气的体积测定YZM 样品纯度。
4 4
①其反应的化学方程式为___________________________________________________。
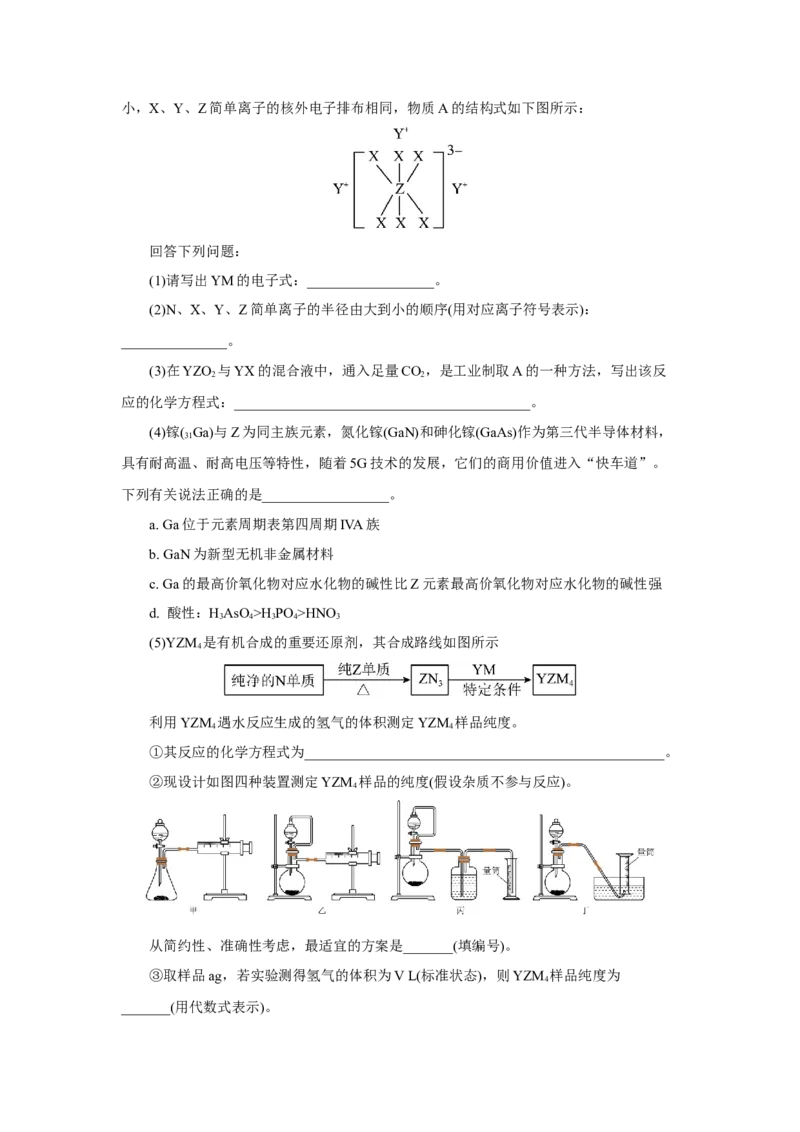
②现设计如图四种装置测定YZM 样品的纯度(假设杂质不参与反应)。
4
从简约性、准确性考虑,最适宜的方案是_______(填编号)。
③取样品ag,若实验测得氢气的体积为V L(标准状态),则YZM 样品纯度为
4
_______(用代数式表示)。【答案】(1)
(2)Cl->F-> Na+>Al3+
(3)NaAlO +6NaF+4CO +2H O=Na AlF+4NaHCO
2 2 2 3 6 3
(4)bc
(5) NaAlH +2H O=NaAlO +4H ↑ 乙 %
4 2 2 2
【解析】(1)根据分析可知,Y为钠,M为H; YM为NaH,其电子式为
;故答案为 ;
(2)N、X、Y、Z分别为Cl、F、Na、Al;简单离子的核外排布不同时,电子层数越
多,半径越大,核外排布相同时,核电荷数越小,半径越大;所以N、X、Y、Z简单离子
的半径由大到小的顺序Cl->F-> Na+>Al3+,故答案为Cl->F-> Na+>Al3+;
(3)A是Na[AlF ],工业上,在NaAlO 与NaF的混合液中,通入足量CO,即可制
3 6 2 2
得Na[AlF ],写出该反应的化学方程式为NaAlO +6NaF+4CO +2H O=Na AlF+4NaHCO,
3 6 2 2 2 3 6 3
故答案为NaAlO +6NaF+4CO +2H O=Na AlF+4NaHCO;
2 2 2 3 6 3
(4)a.Ga位于元素周期表第四周期ⅢA族,故a错误;b.GaN为新型的无机非金
属材料,故b正确;c.Ga的金属性大于铝的金属性,故Ga的最高价氧化物对应水化物的
碱性比铝元素最高价氧化物对应水化物的碱性强,故c正确;d.非金属性:N>P>As,
故酸性:HAsO <HPO <HNO,故d错误;故答案为bc;
3 4 3 4 3
(5)YZM 是NaAlH ,其中含有的氢元素为−1价,遇水反应生成的氢气;
4 4
①根据原子守恒和化合价升降守恒,可得反应的化学方程式为
NaAlH +2H O=NaAlO +4H ↑,故答案为NaAlH +2H O=NaAlO +4H ↑;
4 2 2 2 4 2 2 2
②根据题给的装置图,从简约性、准确性考虑,最适宜的方案是乙,故答案为乙;