文档内容
第二章 海水中的重要元素—钠和氯
第二节 氯及其化合物 课时作业
专题 氯及其化合物的应用
基础达标
1.下列关于氯水的叙述正确的是( )
A.新制氯水可使蓝色石蕊试纸先变红后褪色
B.新制氯水中只含Cl 和HO 分子
2 2
C.光照氯水有气泡逸出,该气体是Cl
2
D.氯水放置数天后pH值将变大
2.下列说法正确的是( )
A.漂白粉是纯净物,84消毒液是混合物,两者都可以长期保存
B.漂白粉中含有次氯酸,所以漂白粉能使有机色质褪色
C.工业上将氯气通入澄清石灰水中制取漂白粉
D.漂白粉在空气中容易失效的原因是Ca(ClO) 与CO、HO反应生成的HClO不稳定
2 2 2
3.近期埃博拉病毒在非洲各国肆虐,严重威胁了非洲人民的生命。在此期间,环境消
毒是极其关键的,常常喷洒一种名为“84”的消毒液,其有效成分为NaClO。下列有关
“84”消毒液的说法正确的是( )
A.“84”的消毒液属于纯净物
B.“84”的消毒液除能杀菌消毒外,还可作漂白剂
C.“84”消毒液中的NaClO比较稳定,不需密封保存
D.“84”消毒液杀菌消毒过程中并未发生氧化还原反应
4.氯化碘(ICl)的化学性质跟氯气相似,预计它跟水反应的最初生成物是( )
A.HI和HCl B.HCl和HIO
C.HClO 和HIO D.HClO和HIO
3
5.关于氯化钠、氯化钙、氯化钾的下列说法正确的是( )
A.工业上利用钠与氯气反应制取氯化钠
B.向氯化钠的饱和溶液中加入少量钠无明显现象
C.氯化钙是漂白粉的有效成分
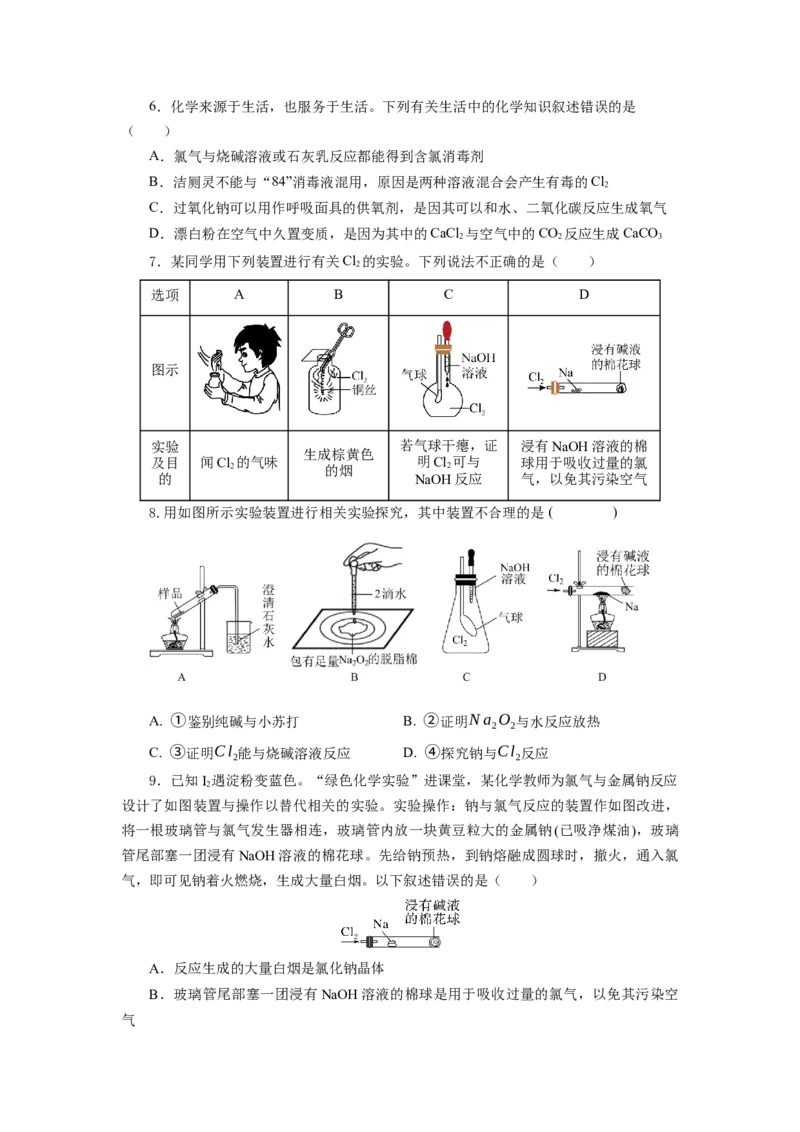
D.向氯化钠、氯化钙、氯化钾的溶液中分别加入少量硝酸银溶液,均出现白色沉淀6.化学来源于生活,也服务于生活。下列有关生活中的化学知识叙述错误的是
( )
A.氯气与烧碱溶液或石灰乳反应都能得到含氯消毒剂
B.洁厕灵不能与“84”消毒液混用,原因是两种溶液混合会产生有毒的Cl
2
C.过氧化钠可以用作呼吸面具的供氧剂,是因其可以和水、二氧化碳反应生成氧气
D.漂白粉在空气中久置变质,是因为其中的CaCl 与空气中的CO 反应生成CaCO
2 2 3
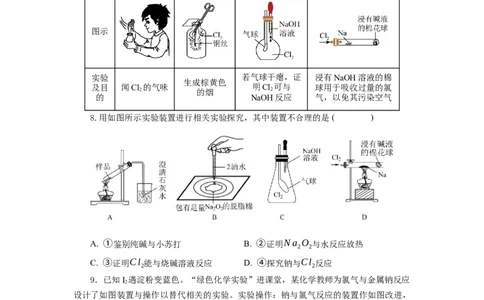
7.某同学用下列装置进行有关Cl 的实验。下列说法不正确的是( )
2
选项 A B C D
图示
实验 若气球干瘪,证 浸有NaOH溶液的棉
生成棕黄色
及目 闻Cl 的气味 明Cl 可与 球用于吸收过量的氯
2 的烟 2
的 NaOH反应 气,以免其污染空气
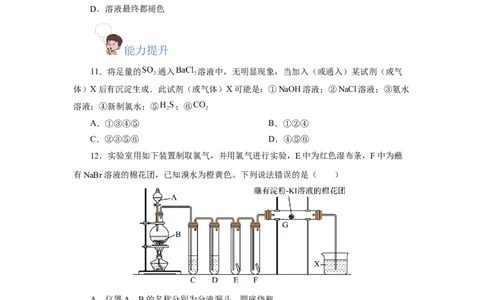
8.用如图所示实验装置进行相关实验探究,其中装置不合理的是( )
A. ①鉴别纯碱与小苏打 B. ②证明Na O 与水反应放热
2 2
C. ③证明Cl 能与烧碱溶液反应 D. ④探究钠与Cl 反应
2 2
9.已知I 遇淀粉变蓝色。“绿色化学实验”进课堂,某化学教师为氯气与金属钠反应
2
设计了如图装置与操作以替代相关的实验。实验操作:钠与氯气反应的装置作如图改进,
将一根玻璃管与氯气发生器相连,玻璃管内放一块黄豆粒大的金属钠(已吸净煤油),玻璃
管尾部塞一团浸有NaOH溶液的棉花球。先给钠预热,到钠熔融成圆球时,撤火,通入氯
气,即可见钠着火燃烧,生成大量白烟。以下叙述错误的是( )
A.反应生成的大量白烟是氯化钠晶体
B.玻璃管尾部塞一团浸有NaOH溶液的棉球是用于吸收过量的氯气,以免其污染空
气C.钠着火燃烧产生苍白色火焰
D.若在棉球外沿滴一滴淀粉碘化钾溶液,据其颜色变化判断氯气是否被碱液完全吸
收
10.向紫色石蕊溶液中分别加入过量的Cl、Na和NaO 粉末,振荡,下列叙述正确
2 2 2
的是( )
A.溶液最终分别呈红色、蓝色、蓝色,且加入后溶液中均有气体产生
B.通入Cl,溶液先变红后褪色,是由于Cl 的漂白作用
2 2
C.加入足量NaO 粉末的溶液先变蓝后褪色
2 2
D.溶液最终都褪色
能力提升
11.将足量的 通入 溶液中,无明显现象,当加入(或通入)某试剂(或气
体)X后有沉淀生成.此试剂(或气体)X可能是:①NaOH溶液;②NaCl溶液;③氨水
溶液;④新制氯水;⑤ ;⑥
A.①③④⑤ B.①②④
C.②③⑤⑥ D.④⑤⑥
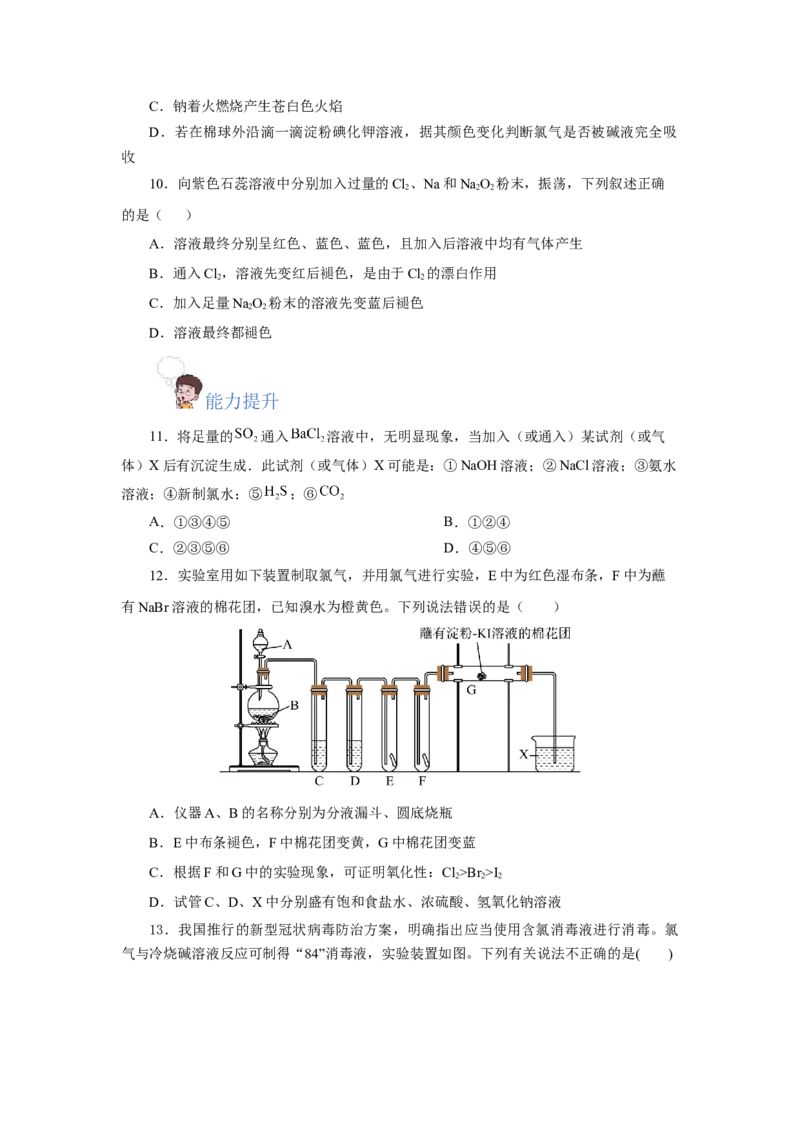
12.实验室用如下装置制取氯气,并用氯气进行实验,E中为红色湿布条,F中为蘸
有NaBr溶液的棉花团,已知溴水为橙黄色。下列说法错误的是( )
A.仪器A、B的名称分别为分液漏斗、圆底烧瓶
B.E中布条褪色,F中棉花团变黄,G中棉花团变蓝
C.根据F和G中的实验现象,可证明氧化性:Cl>Br >I
2 2 2
D.试管C、D、X中分别盛有饱和食盐水、浓硫酸、氢氧化钠溶液
13.我国推行的新型冠状病毒防治方案,明确指出应当使用含氯消毒液进行消毒。氯
气与冷烧碱溶液反应可制得“84”消毒液,实验装置如图。下列有关说法不正确的是( )A.甲中盛放的试剂可以是高锰酸钾固体
B.乙中可采用热水浴,有利于加快反应速率
C.在甲、乙之间加入饱和食盐水洗气,可提高NaOH利用率
D.在乙之后再连接NaOH溶液吸收尾气,更加符合绿色化学思想
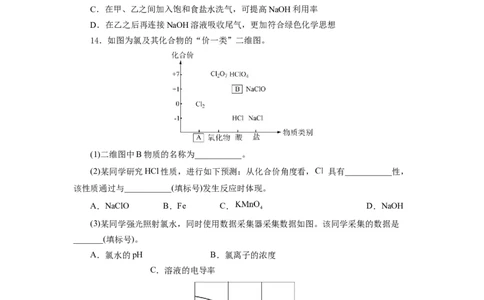
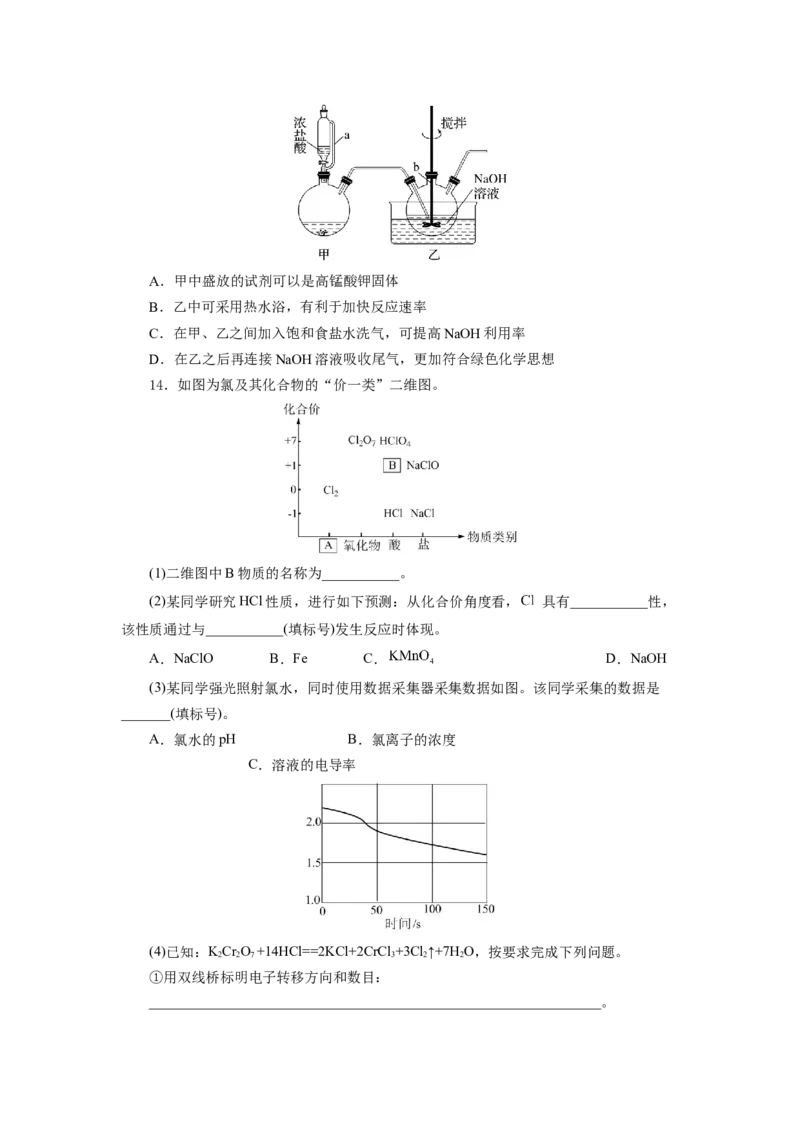
14.如图为氯及其化合物的“价一类”二维图。
(1)二维图中B物质的名称为___________。
(2)某同学研究HCl性质,进行如下预测:从化合价角度看, 具有___________性,
该性质通过与___________(填标号)发生反应时体现。
A.NaClO B.Fe C. D.NaOH
(3)某同学强光照射氯水,同时使用数据采集器采集数据如图。该同学采集的数据是
_______(填标号)。
A.氯水的pH B.氯离子的浓度
C.溶液的电导率
(4)已知:KCr O +14HCl==2KCl+2CrCl +3Cl↑+7H O,按要求完成下列问题。
2 2 7 3 2 2
①用双线桥标明电子转移方向和数目:
________________________________________________________________。②该反应中,氧化剂是___________(填化学式),还原剂是___________(填化学式)。
③被氧化的HCl与参加反应的HCl的质量之比___________。
直击高考
15.将氯气分别通入下列物质的溶液中,对于反应现象、原因和有关化学方程式的表
述中错误的是( )
①NaBr ②FeCl ③AgNO ④NaHCO
2 3 3
反应现象 原因 化学方程式
① 溶液变成橙色 Br-被Cl 氧化为Br 2NaBr+Cl =2NaCl+Br
2 2 2 2
溶液由浅绿色变
② Fe2+被Cl 氧化为Fe3+ 2FeCl +Cl=2FeCl
成黄色 2 2 2 3
③ 有白色沉淀生成 Ag+与Cl- 反应生成沉淀 AgNO+HCl=AgCl↓+HNO
3 3
HCO - 与HClO 反应产
④ 有气体产生 3 NaHCO +HClO=NaC1O+CO ↑+H O
生气体 3 2 2
A.① B.② C.③ D.④
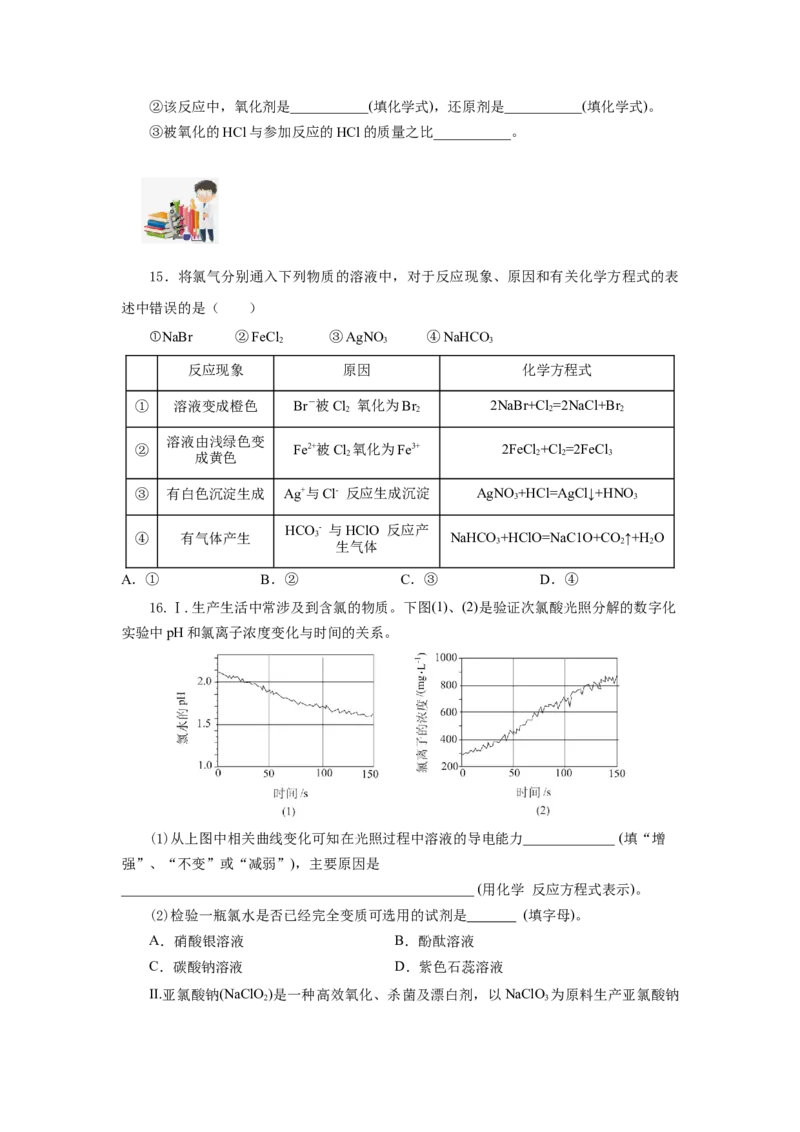
16.Ⅰ.生产生活中常涉及到含氯的物质。下图(1)、(2)是验证次氯酸光照分解的数字化
实验中pH和氯离子浓度变化与时间的关系。
(1)从上图中相关曲线变化可知在光照过程中溶液的导电能力_____________ (填“增
强”、“不变”或“减弱”),主要原因是
__________________________________________________ (用化学 反应方程式表示)。
(2)检验一瓶氯水是否已经完全变质可选用的试剂是 (填字母)。
A.硝酸银溶液 B.酚酞溶液
C.碳酸钠溶液 D.紫色石蕊溶液
Ⅱ.亚氯酸钠(NaClO)是一种高效氧化、杀菌及漂白剂,以NaClO 为原料生产亚氯酸钠
2 3的工艺流程如下:
(1)过程I在生成ClO 的同时,还会得到另一种常见的盐,请写出其化学方程式:
2
_______________________________________________________________________。
(2)过程I中常伴有少量Cl 生成。结合下表信息,设计实验方案除去ClO 中的Cl
2 2 2
_______________________________________________________________________。
ClO Cl
2 2
在水中的溶解性 易溶 溶
在CCl 中的溶解性 难溶 溶
4
(3)过程Ⅱ中HO 的作用是_______(填“氧化剂”或“还原剂”)
2 2