文档内容
第三章 铁 金属材料
第一节 铁及其化合物 课时作业
专题2 检验食品中的铁元素
基础达标
1.为检验FeCl 溶液中是否含有Fe3+,可选择的试剂是( )
2
A.稀盐酸 B.AgNO 溶液 C.KSCN溶液 D.HO
3 2 2
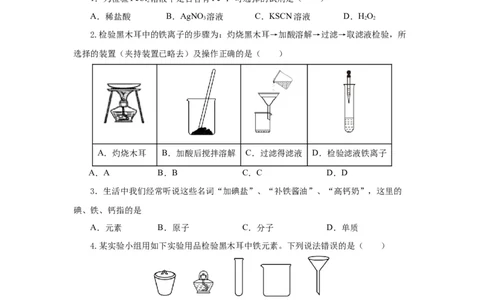
2.检验黑木耳中的铁离子的步骤为:灼烧黑木耳→加酸溶解→过滤→取滤液检验,所
选择的装置(夹持装置已略去)及操作正确的是( )
A.灼烧木耳 B.加酸后搅拌溶解 C.过滤得滤液 D.检验滤液铁离子
A.A B.B C.C D.D
3.生活中我们经常听说这些名词“加碘盐”、“补铁酱油”、“高钙奶”,这里的
碘、铁、钙指的是
A.元素 B.原子 C.分子 D.单质
4.某实验小组用如下实验用品检验黑木耳中铁元素。下列说法错误的是( )
A.将黑木耳灼烧灰化,选用的仪器有①、②、⑥、⑦和⑨
B.用浓硝酸溶解木耳灰并获得滤液,选用的仪器有④、⑤、⑦和⑩C.检验滤液中的 ,选用③、⑧和⑩
D.利用上述仪器也可进行硫酸铜结晶水含量的测定
5.证明某溶液只含有Fe2+而不含有Fe3+的实验方法是( )
A.只需滴加硫氰化钾溶液
B.先滴加硫氰化钾溶液,不显红色,再滴 加氯水后显红色
C.先滴加氯水,再滴加硫氰化钾溶液后显红色杨sir化学,侵权必究
D.滴加氢氧化钠溶液,立即产生红褐色沉淀
6.随着人们生活节奏的加快,方便的包装食品已被广泛接受,为了防止副食品氧化变
质,延长食品食品的保质期,在包装袋中常放入抗氧化物质,下列不属于抗氧化物质的是(
)
A.生石灰 B.亚硫酸钠 C.铁粉 D.硫酸亚铁
7.铁及其化合物是中学化学中重要的物质。下列有关铁及其化合物说法正确的是(
)
A.被腐蚀的铁制品属于可回收垃圾 B.不能通过物理方法将铁粉和铝粉分离
C.铁锈的主要成分是Fe(OH) D.指南针中因含有FeO而可以指定方位
3
8.下列有关说法正确的是( )
A.厨房可用食醋除水垢,食醋的作用是作氧化剂
B. 某食品包装袋内装有一包铁粉,它的主要作用是作干燥剂
C.病人补铁( )的同时需补维生素C,维生素C的作用是作还原剂
D.疫情期间常用酒精对物品和手部进行消毒,乙醇的作用是作氧化剂
9.化学与生活等密切相关,下列说法不正确的是( )
A.葡萄糖注射液不能产生丁达尔效应
B.“铁质菜刀生锈”与氧化还原反应有关
C.为防止中秋月饼等富脂食品因被氧化而变质,常在包装袋中放入生石灰
D.维生素C可将 转变为 ,所以维生素C具有还原性
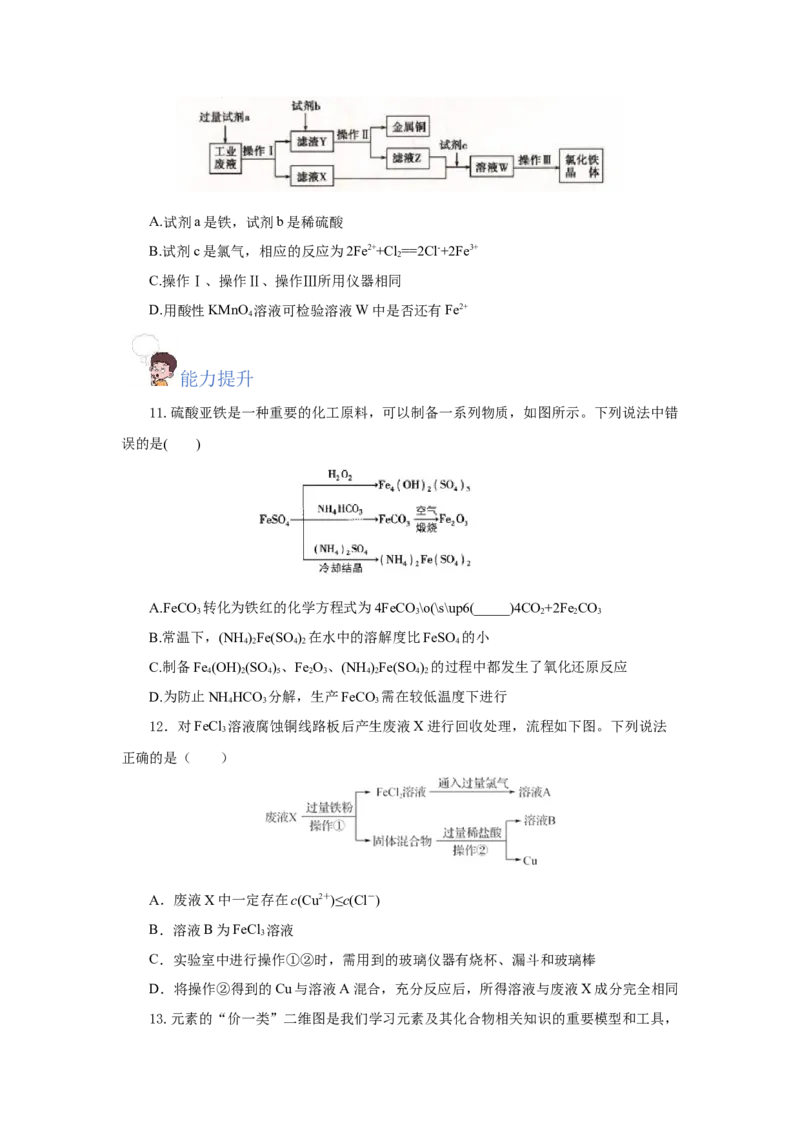
10.从某含有FeCl 、FeCl 、CuCl 的工业废液中回收铜并制备氯化铁晶体的流程如
2 3 2
图,则下列说法正确的是( )A.试剂a是铁,试剂b是稀硫酸
B.试剂c是氯气,相应的反应为2Fe2++Cl==2Cl-+2Fe3+
2
C.操作Ⅰ、操作Ⅱ、操作Ⅲ所用仪器相同
D.用酸性KMnO 溶液可检验溶液W中是否还有Fe2+
4
能力提升
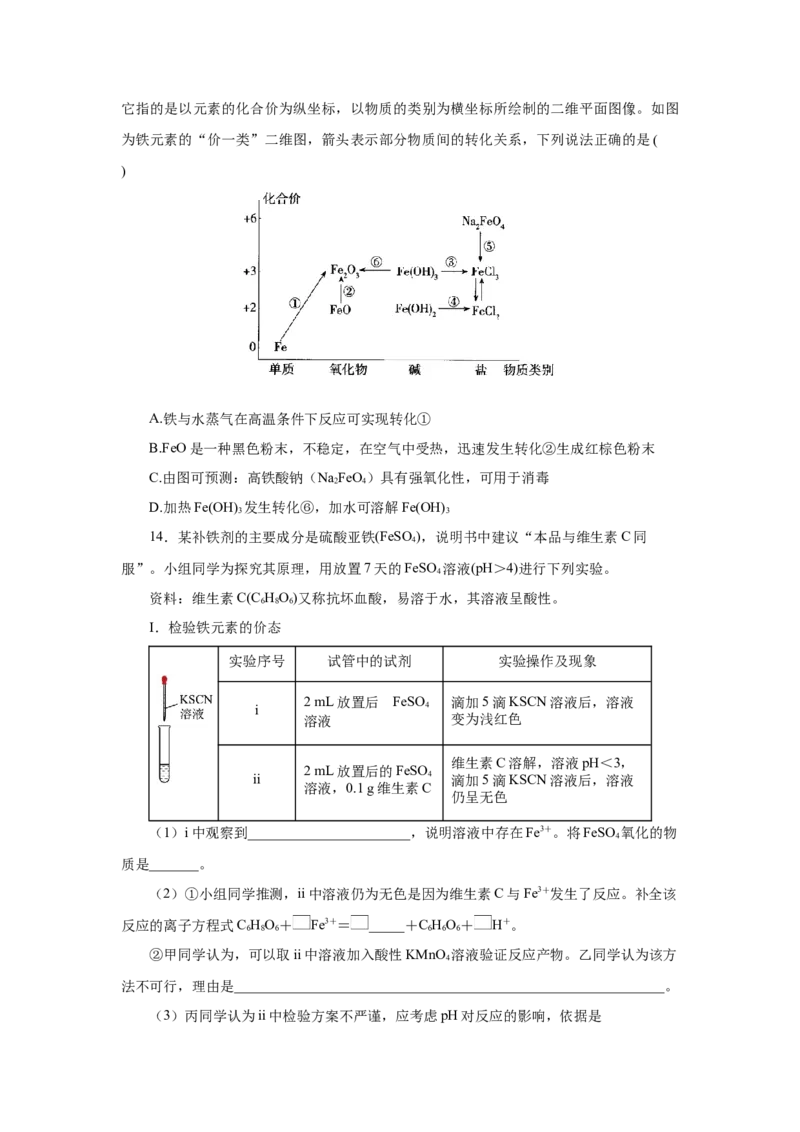
11.硫酸亚铁是一种重要的化工原料,可以制备一系列物质,如图所示。下列说法中错
误的是( )
A.FeCO 转化为铁红的化学方程式为4FeCO\o(\s\up6(_____)4CO+2Fe CO
3 3 2 2 3
B.常温下,(NH )Fe(SO ) 在水中的溶解度比FeSO 的小
4 2 4 2 4
C.制备Fe (OH) (SO )、Fe O、(NH )Fe(SO ) 的过程中都发生了氧化还原反应
4 2 4 5 2 3 4 2 4 2
D.为防止NH HCO 分解,生产FeCO 需在较低温度下进行
4 3 3
12.对FeCl 溶液腐蚀铜线路板后产生废液X进行回收处理,流程如下图。下列说法
3
正确的是( )
A.废液X中一定存在c(Cu2+)≤c(Cl-)
B.溶液B为FeCl 溶液
3
C.实验室中进行操作①②时,需用到的玻璃仪器有烧杯、漏斗和玻璃棒
D.将操作②得到的Cu与溶液A混合,充分反应后,所得溶液与废液X成分完全相同
13.元素的“价一类”二维图是我们学习元素及其化合物相关知识的重要模型和工具,它指的是以元素的化合价为纵坐标,以物质的类别为横坐标所绘制的二维平面图像。如图
为铁元素的“价一类”二维图,箭头表示部分物质间的转化关系,下列说法正确的是(
)
A.铁与水蒸气在高温条件下反应可实现转化①
B.FeO是一种黑色粉末,不稳定,在空气中受热,迅速发生转化②生成红棕色粉末
C.由图可预测:高铁酸钠(NaFeO)具有强氧化性,可用于消毒
2 4
D.加热Fe(OH) 发生转化⑥,加水可溶解Fe(OH)
3 3
14.某补铁剂的主要成分是硫酸亚铁(FeSO ),说明书中建议“本品与维生素C同
4
服”。小组同学为探究其原理,用放置7天的FeSO 溶液(pH>4)进行下列实验。
4
资料:维生素C(C HO)又称抗坏血酸,易溶于水,其溶液呈酸性。
6 8 6
I.检验铁元素的价态
实验序号 试管中的试剂 实验操作及现象
2 mL放置后 的FeSO 滴加5滴KSCN溶液后,溶液
i 4
溶液 变为浅红色
维生素C溶解,溶液pH<3,
2 mL放置后的FeSO
ii 4 滴加5滴KSCN溶液后,溶液
溶液,0.1 g维生素C
仍呈无色
(1)i中观察到_______________________,说明溶液中存在Fe3+。将FeSO 氧化的物
4
质是_______。
(2)①小组同学推测,ii中溶液仍为无色是因为维生素C与Fe3+发生了反应。补全该
反应的离子方程式C HO+ Fe3+= _____+C HO+ H+。
6 8 6 6 6 6
②甲同学认为,可以取ii中溶液加入酸性KMnO 溶液验证反应产物。乙同学认为该方
4
法不可行,理由是_____________________________________________________________。
(3)丙同学认为ii中检验方案不严谨,应考虑pH对反应的影响,依据是______________。
II.探究pH对ii中反应的影响
小组同学补充了如下实验,继续探究pH对ii中反应的影响。
实验序号 试剂 实验操作及现象
滴加5滴KSCN溶液后,溶液变
iii
为浅红色,浅红色比i中加深
(4)判断下列关于实验结论的说法是否正确(填“对”或“错”)。
①pH对Fe3+与SCN-的显色反应有影响。_______
②加维生素C后pH<3,导致ii中未末检测出Fe3+。_______
(5)反思实验i~iii,下列说法合理的是_____________(填序号)。
a.维生素C具有氧化性和酸性
b.同服维生素C可减缓补铁剂中FeSO 被氧化
4
c.使用KSCN检验Fe3+时,宜先将溶液酸化
直击高考
15.一种利用废旧镀锌铁皮制备Fe O 纳米粒子的工艺流程如下:
3 4
已知:Zn及其化合物与Al及其化合物的性质相似。下列说法不正确的是( )
A.“碱洗”的目的是为了去除废旧镀锌铁皮表面的油污及锌
B.“氧化”时发生反应的离子方程式为2Fe2++ClO-+2H+=2Fe3++Cl-+HO
2
C.“氧化”后的溶液中主要存在的金属阳离子:Fe3+、Na+
D.“加热沉铁”时通入N 是防止空气中的O 对产品造成影响
2 2
16.已知K[Fe(CN)]溶液遇 Fe2+生成蓝色沉淀,可检验溶液中的Fe2+。某实验小组
3 6
测定菠菜和黑木耳中的铁元素。实验如下:
I.水煮菠菜(铁元素主要以难溶的 FeC O 形式存在)检验法:
2 4II.灼烧检验法:
(1)操作i中起分离作用的仪器名称为 ;溶液A中未能检测出
Fe2+的可能原因是 。
(2)甲同学取少量无色溶液B,滴加酸性KMnO 溶液,振荡后,溶液紫色消失,因
4
此得出结论,溶液B含有Fe2+。乙同学认为甲同学的实验方法不严谨,理由是
。
有研究表明,黑木耳中铁的含量约为13.93mg/100g,是菠菜含铁量的10倍以上。
III.测定木耳铁中元素含量。
(3)称取2.00g干黑木耳置于 (填仪器名称)中灼烧。经过一系列操作后配
制成100mL待测液。过程中,用到盐酸羟胺(在溶液中可完全电离出NH OH+与Cl-)将溶
3
液中Fe3+还原Fe2+,同时产生一种无污染的气体。该反应的离子方程式为
;配制100mL一定物质的量浓度的酸性高锰酸钾溶液时,所需要的玻璃仪器除量筒、玻璃
棒、烧杯外还有 。
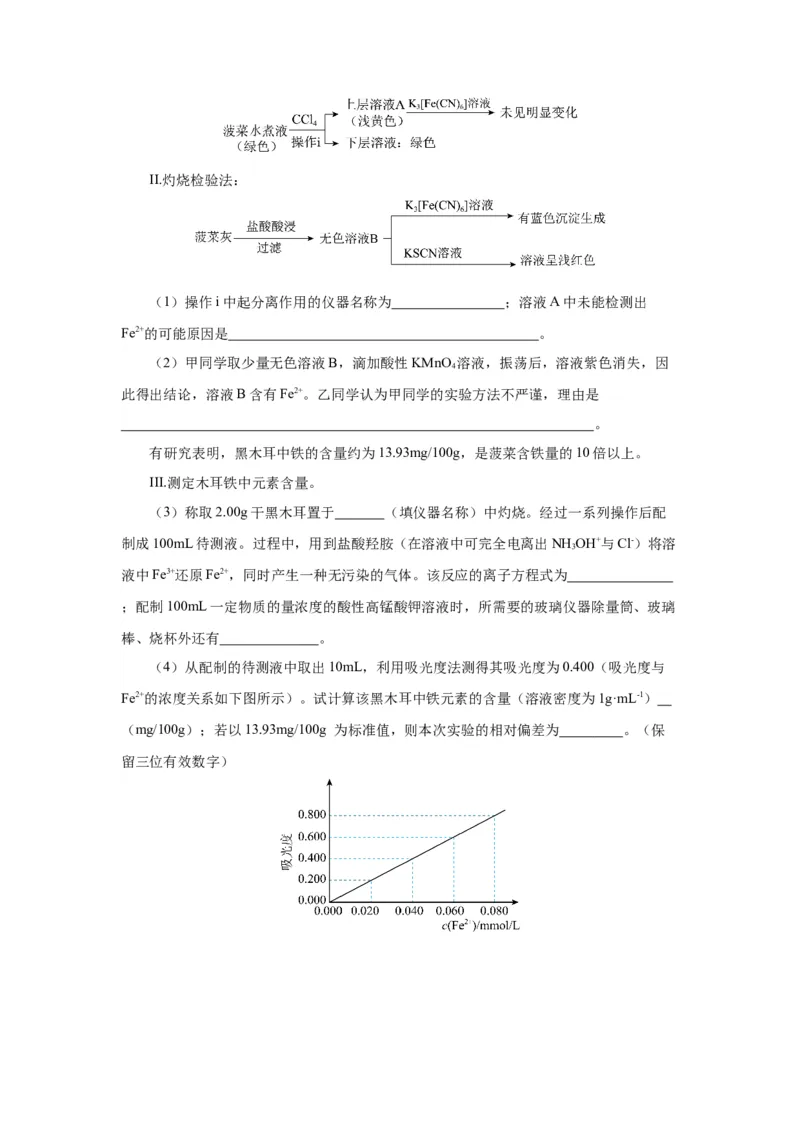
(4)从配制的待测液中取出10mL,利用吸光度法测得其吸光度为0.400(吸光度与
Fe2+的浓度关系如下图所示)。试计算该黑木耳中铁元素的含量(溶液密度为1g·mL-1)
(mg/100g);若以13.93mg/100g 为标准值,则本次实验的相对偏差为 。(保
留三位有效数字)