文档内容
课程基本信息
课题 《分子的空间结构》(第三课时)
书名:物质结构与性质
教科书
出版社:人民教育出版社 出版日期: 2020年5月
教学目标
教学目标:
结合实例了解杂化轨道理论的要点和类型(sp3、sp2、sp),能运用杂化轨道理论解释
简单共价分子和离子的空间结构
教学重点:判断杂化轨道类型
教学难点:应用杂化轨道理论解释分子的空间结构
教学过程
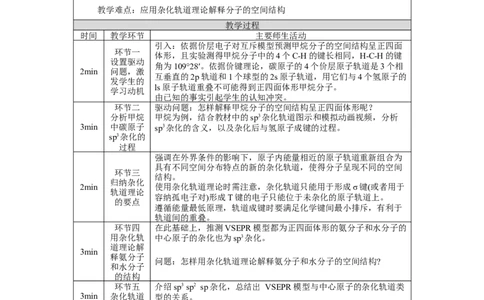
时间 教学环节 主要师生活动
引入:依据价层电子对互斥模型预测甲烷分子的空间结构呈正四面
环节一
体形,且实验测得甲烷分子中的4个C-H的键长相同,H-C-H的键
设置驱动
角为109°28′。依据价键理论,碳原子的4个价层原子轨道是3个相
2min 问题,激
互垂直的2p轨道和1个球型的2s原子轨道,用它们与4个氢原子的
发学生的
ls原子轨道重叠不可能得到正四面体形甲烷分子。
学习动机
由已知的事实引起学生的认知冲突。
环节二 驱动问题:怎样解释甲烷分子的空间结构呈正四面体形呢?
分析甲烷 甲烷为例,结合教材中的sp3杂化轨道图示和模拟动画视频,分析
3min 中碳原子 sp3杂化的含义,以及杂化后与氢原子成键的过程。
sp3杂化的
过程
强调在外界条件的影响下,原子内能量相近的原子轨道重新组合为
具有不同空间分布特点的新的杂化轨道,使得分子呈现不同的空间
环节三
结构。
归纳杂化
2min 使用杂化轨道理论时需注意,杂化轨道只能用于形成σ键(或者用于
轨道理论
容纳孤电子对)形成T键的电子只能位于未杂化的原子轨道上。
的要点
遵循能量最低原理,轨道成键时要满足化学键间最小排斥,有利于
轨道间的重叠。
环节四 在此基础上,推测VSEPR模型都为正四面体形的氨分子和水分子的
用杂化轨 中心原子的杂化也为sp3杂化。
道理论解
3min
释氨分子
问题:怎样用杂化轨道理论解释氨分子和水分子的空间结构?
和水分子
的结构
环节五 介绍sp3 sp2 sp杂化,总结出 VSEPR模型与中心原子的杂化轨道类
3min 杂化轨道 型的关系。
类型
先计算价层电子对数,然后确定分子或离子的VSEPR理想模型,最
环节六 后就可以比较方便地确定中心原子的杂化轨道类型。
VSEPR模
10min 型和杂化
预测和解释BF、乙烯、乙炔的空间结构,以及中心原子的杂化轨
轨道理论 3
道类型,并分析杂化过程。
联用
明确它们功能和关系:分子的空间结构可以通过光谱测定,VSEPR
环节七
1min 模型是预测模型,杂化轨道理论是解释模型。将VSEPR模型和杂化
总结提升
轨道理论联用可以很好地预测和解释简单分子或离子的空间结构。