文档内容
第五章 化工生产中的重要非金属元素 4. H SO
2 4
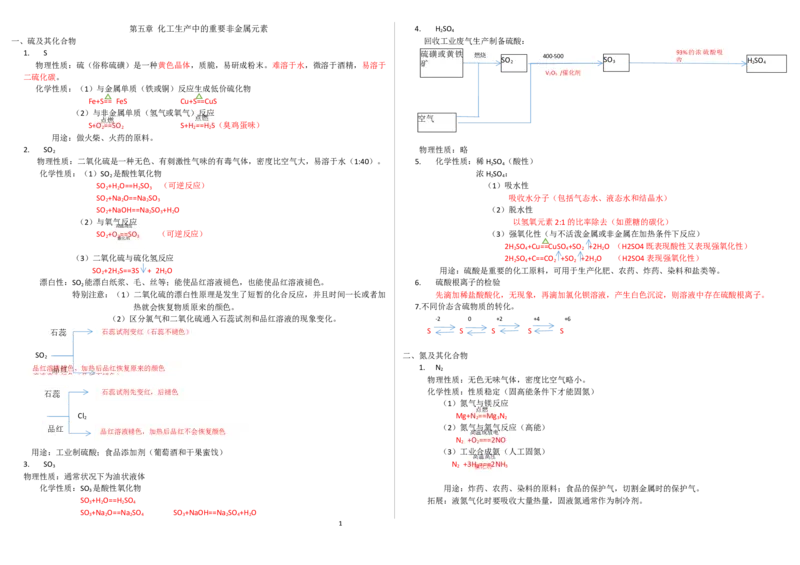
一、硫及其化合物 回收工业废气生产制备硫酸:
1. S 硫磺或黄铁 燃烧 400-500 93%的浓硫酸吸
物理性质:硫(俗称硫磺)是一种黄色晶体,质脆,易研成粉末。难溶于水,微溶于酒精,易溶于 矿 SO 2 SO 3 收 H 2 SO 4
VO /催化剂
二硫化碳。 2 5
化学性质:(1)与金属单质(铁或铜)反应生成低价硫化物
Fe+S== FeS Cu+S==CuS
(2)与非金属单质(氢气或氧气)反应
点燃 空气
点燃
S+O ==SO S+H ==H S(臭鸡蛋味)
2 2 2 2
用途:做火柴、火药的原料。
2. SO 物理性质:略
2
物理性质:二氧化硫是一种无色、有刺激性气味的有毒气体,密度比空气大,易溶于水(1:40)。 5. 化学性质:稀H SO (酸性)
2 4
化学性质:(1)SO 是酸性氧化物 浓H SO :
2 2 4
SO +H O==H SO (可逆反应) (1)吸水性
2 2 2 3
SO +Na O==Na SO 吸收水分子(包括气态水、液态水和结晶水)
2 2 2 3
SO +NaOH==Na SO +H O (2)脱水性
2 2 3 2
(2)与氧气反应 以氢氧元素2:1的比率除去(如蔗糖的碳化)
高温高压
SO +O ==SO (可逆反应) (3)强氧化性(与不活泼金属或非金属在加热条件下反应)
2 催2化剂 3
2H SO +Cu==CuSO +SO +2H O (H2SO4既表现酸性又表现强氧化性)
2 4 4 2 2
(3)二氧化硫与硫化氢反应 2H SO +C==CO +SO +2H O (H2SO4表现强氧化性)
2 4 2 2 2
SO +2H S==3S + 2H O 用途:硫酸是重要的化工原料,可用于生产化肥、农药、炸药、染料和盐类等。
2 2 2
漂白性:SO 能漂白纸浆、毛、丝等;能使品红溶液褪色,也能使品红溶液褪色。 6. 硫酸根离子的检验
2
特别注意:(1)二氧化硫的漂白性原理是发生了短暂的化合反应,并且时间一长或者加 先滴加稀盐酸酸化,无现象,再滴加氯化钡溶液,产生白色沉淀,则溶液中存在硫酸根离子。
热就会恢复物质原来的颜色。 7.不同价态含硫物质的转化。
(2)区分氯气和二氧化硫通入石蕊试剂和品红溶液的现象变化。 -2 0 +2 +4 +6
石蕊 石蕊试剂变红(石蕊不褪色) S S S S S
SO 二、氮及其化合物
2
品红溶品液红褪色,加热后品红恢复原来的颜色 1. N
2
溶液变为红色(品红不褪色)
物理性质:无色无味气体,密度比空气略小。
石蕊 石蕊试剂先变红,后褪色 化学性质:性质稳定(固高能条件下才能固氮)
(1)氮气与镁反应
点燃
Cl Mg+N ==Mg N
2 2 3 2
品红 (2)氮气与氧气反应(高能)
品红溶液褪色,加热后品红不会恢复颜色 高温或放电
N +O ===2NO
2 2
用途:工业制硫酸;食品添加剂(葡萄酒和干果蜜饯) (3)工业合成氨(人工固氮)
高温高压
3. SO N +3H ===2NH
3 2 催2化剂 3
物理性质:通常状况下为油状液体
化学性质:SO 是酸性氧化物 用途:炸药、农药、染料的原料;食品的保护气,切割金属时的保护气。
3
SO +H O==H SO 拓展:液氮气化时要吸收大量热量,固液氮通常作为制冷剂。
3 2 2 4
SO +Na O==Na SO SO +NaOH==Na SO +H O
3 2 2 4 3 2 4 2
12. NO 三、硅及其化合物(拓展、新教材已经删减大部分,但建议理科生掌握)
物理性质:一氧化氮是无色的有毒气体,不溶于水,在常温下很容易与氧气结合。 1. Si
化学性质:(1)与氧气反应 物理性质:黑色晶体(自然界中不存在游离态的硅单质)
2NO+O ==2NO 化学性质:(1)与氢氟酸反应(与其他酸都不反应)
2 2
(2)汽车尾
催
气
化剂
的处理(一) Si+4HF==SiF
4
+2H
2
2NO+2CO==N +2CO (2)与强碱反应
2 2
3. NO Si+2NaOH+H O==Na SiO +2H
2 2 2 3 2
物理性质:二氧化氮是红棕色、有刺激性气味的有毒气体,密度比空气大,易液化 应用:良好的半导体材料,应用于太阳能电池和计算机芯片。
化学性质:(1)工业制硝酸的原理 2. SiO
2
3NO +H O==2HNO +NO 物理性质:不溶于水也不和水反应。
2 2 3
(2)汽车尾气的处理(二) 化学性质:(1)酸性氧化物
催化剂
2NO +4CO==N +4CO SiO +Na O==Na SiO
2 2 2 2 2 2 3
4. NH 和NH +(铵盐) SiO +2NaOH==Na SiO +H O
3 4 2 2 3 2
物理性质:氨是无色、有刺激性气味的气体,密度比空气的小。 (2)与氢氟酸反应(雕刻玻璃的原理)(不与其他酸反应)
化学性质:(1)氨与酸反应(注意与可挥发性酸的反应现象) SiO
2
+4HF==SiF
4
+5H
2
O
NH +HCl==NH Cl(产生白烟) (4)高温下与碳酸钙反应
3 4 高温
(2)氨的催化氧化(工业制硝酸的第一步) SiO +CaCO ==CaSiO +CO
催化剂 2 3 3 2
4NH +5O ==4NO+6H O 应用:良好的材料,是水晶,玛瑙,石英,光导纤维的主要成分。
3 2 2
(3)实验室制氨气 3. H SiO
2 3
2NH Cl+Ca(OH) ==CaCl +2NH +2H O 物理性质:白色絮状沉淀,不溶于水。
4 2 2 3 2
(4)工业合成氨 4. 化学性质:(1)弱酸性,比碳酸酸性还弱(制备H SiO )
高温高压 2 4
N +3H ===2NH Na SiO +CO +H O==Na CO +H SiO
2 催2化剂 3 2 3 2 2 2 3 2 3
(2)与碱性氧化物(或碱)反应
铵根离子的检验 H SiO +Na O==Na SiO +H O
2 3 2 2 3 2
取少量待测液与试管中,滴加氢氧化钠溶液,加热产生使湿润的石蕊试剂变蓝的气体(或取少 H SiO +2NaOH==Na SiO +2H O
2 3 2 3 2
量待测液与试管中,滴加氢氧化钠溶液加热,用沾有浓盐酸的玻璃棒靠近试管口,产生大量白烟) (3)受热分解
应用:制化肥或硝酸的原料;氨易液化,氨气化时需要吸收大量热,故液氨经常用作制冷剂。 H SiO ==SiO +2H O
2 3 2 2
5. HNO (浓硝酸和稀硝酸都有强氧化性) 注意:不能用二氧化硅与水反应直接制得硅酸。
3
物理性质:硝酸是无色、易挥发、有刺激性气味的液体。 应用:常用作干燥剂。
化学性质:(1)浓硝酸的分解 5. SiO 2-(硅酸钠为例)
4
4HNO ==4NO + O +2H O 物理性质:硅酸盐材料具有耐高温、抗腐蚀、硬度高等特点
3或 光照 2 2 2
结构:硅氧四面体结构。
(2)浓硝酸与不活泼金属反应 应用:常用作防火涂料;三大硅酸盐材料(玻璃、陶瓷、水泥)的主要成分。
4HNO (浓)+Cu==Cu(NO ) +2NO +2H O 四、无机非金属材料
3 3 2 2 2
(3)稀硝酸与不活泼金属反应 1 .传统无机非金属材料:玻璃、陶瓷、水泥
8HNO (稀)+3Cu==3Cu(NO ) +2NO +4H O 玻璃:纯碱、石灰石、石英砂为原料。
3 3 2 2
(4)浓硝酸(或浓硫酸)在常温下与金属铝或铁发生钝化现象。 陶瓷:以黏土为主要原料高温烧结而成的
用途:制化肥、炸药和化工的原料 水泥:普通水泥以黏土和石灰石为主要原料。
酸雨:PH<5.6的降水,主要来源是化石燃料的燃烧。 2.新型无机非金属材料:硅和二氧化硅、新型陶瓷(碳化硅、氮化硅)、碳纳米材料(富勒烯、石墨
烯、碳纳米管)
2第六章 化学反应与能量 负极(失电子)发生氧化反应;正极(得电子)发生还原反应。
一、化学反应与能量变化 (4)电子、电流、离子移动的方向(记住电子不入水、离子不上岸)
1. 化学反应与热能 电子:负极经导线流向正极
(1)化学反应往往伴随着能量的变化,化学反应过程中能量变化的主要原因:化学键的断裂与形 电流:正极流向负极
成。 离子:阴离子移向负极;阳离子移向正极。
(2)化学键角度看:反应物断键要吸热,生成物成键要放热。(键能越大物质越稳定,反之键能 (5)原电池正负极的判断
越小越不稳定) 已知电极反应式:
(3)物质自身具有的能量角度:反应物总能量大于生成物总能量要放热,反应物能量小于生成物 失电子的作负极(负失),则另一电机作正极
总能量要吸热。(物质自身具有的能量越高越不稳定,反之物质能量越低越稳定) 未知电极反应式:
活泼金属作负极,不活泼金属(或非金属)作正极。
发生氧化反应的作负极,发生还原反应的作正极。
失电子的作负极,得电子的作正极。
电极质量减少的一极作负极,电极质量增大(或产生气体)的一极作正极。
(6)原电池的种类:
一次电池(锌锰干电池):
(4)物质稳定与自身具有的能量和化学键的关系:物质键能越大,破坏化学键所需能量就越高, 正极(锌) 负极(石墨棒) 电解质(熔融的NH Cl)
4
物质越稳定,则物质自身具有的能量就越低;反之物质键能越小,破坏化学键所需能量就越低,物质 二次电池又称为充电电池(铅蓄电池):电解质(稀H SO )
2 4
越不稳定,则物质自身具有的能量就越高) 正极(Pb): Pb-2e-+SO 2-=PbSO
4 4
(5)常见的吸热反应: 负极(PbO):PbO +2e-+4H++SO 2==PbSO +2H O
2 4 4 2
①二氧化碳与碳的反应 总反应:Pb+PbO +2H SO ==2PbSO +2H O
高温 2 2 4 4 2
CO +C== 2CO 燃料电池:(记住燃料作负极,氧气或空气一极作正极)氢氧燃料电池为例:
2
②铵盐的反应 (酸性电解质)正极(燃料):2H -4e-==4H+
2
2NH
4
Cl+Ca(OH)
2
==CaCl
2
+2NH
3
+2H
2
O 负极(氧气):O
2
+4e-+4H+==2H
2
O
③大多数分解反应 总反应:2H +O ==2H O
2 2 2
NH Cl==NH +HCl (碱性电解质)正极(燃料):2H -4e-+4OH-==2H O
4 3 2 2
(6)常见的放热反应: 负极(氧气):O +4e-+2H O==4OH-
2 2
①所有的燃烧反应 总反应:2H +O ==2H O
2 2 2
②酸碱中和反应 (中性电解质)正极(燃料):2H -4e-==4H+
2
NaOH+HCl==NaCl+H O 负极(氧气):O +4e-+2H O==4OH-
2 2 2
③活泼金属与酸或碱的反应(酸性氧化物或碱性氧化物与水的反应也是放热反应) 总反应:2H +O ==2H O
2 2 2
2Na+2H O==2NaOH+H 其他类电池:根据题意判断出正负极(例如Li电池)
2 2
❹大多数化合反应 二、化学反应速率与限度
高温
CaO+CO ==CaCO 1. 化学反应速率
2 3
注:强酸强碱的稀释都是放热的过程(但不是放热反应) (1)公式
2. 化学反应与电能(原电池)
(1)构成原电池的条件
单位:
活泼性不同的两个电机、电解质溶液、形成闭合回路、自发发生氧化还原反应
(2)能量转化形式 (2)化学反应速率之比等于化学计量数之比。
化学能转化为电能 (3)影响化学反应速率的因素
(3)发生的反应 温度:温度越高,化学反应速率越快。
氧化还原反应 浓度:反应物浓度越大,化学反应速率越快。
3催化剂:高效催化剂能增大反应速率,但是不能增大转化率。 (8)同系物:相同类别的有机物,相差一个或多个—CH 原子团的有机化合物。(判别同系物:原子相同,
2
(有气体参与反应或生成)压强:越强越大,化学反应速率越大(压强对化学反应速率的影响实质 官能团相同且相等,相差一个或多个CH 原子团。)
2
上是对物质浓度的影响) 2.各类有机化合物的性质
其它:如增大反应物接触面积等 (1)烷烃(甲烷为例)
2. 化学反应的限度 甲烷的燃烧
点燃
(1)化学反应的限度 CH +2O ==CO +2H O
4 2 2 2
逆:研究的对象是可逆反应 与氯气光照条件下反应
光照
等:平衡时正逆反应速率相等(但是不等于0) CH +Cl ==CH Cl+HCl
4 2 3
动:平衡时保持动态平衡(反应并没有停止) 注:烷烃不能和强酸强碱、强氧化剂(高锰酸钾)反应。
定:平衡时各物质浓度保持不变 (2)烯烃(乙烯为例)
变:改变外界条件时将打破平衡建立新的平衡 乙烯的燃烧
点燃
(2)达到化学平衡的判断依据:正逆反应速率相等,各物质浓度保持不变(或者是变量不再改变)。 C H +3O ==2CO +2H O
2 4 2 2 2
(3)化学计算中的三段式(反应中消耗或生成的物质的量之比等于化学计量数之比) 乙烯使溴水褪色
A + 2 B == C + 2 D C H +Br ==CH BrCH Br(1,2-二溴乙烷 液体)
2 4 2 2 2
反应开始: xmol ymol 0 0 乙烯水化法制乙醇
催化剂
变化 :amol 2amol amol 2amol C H +H O==CH CH OH
2 4 2 3 2
平衡时: x-a mol y-2mol amol 2amol 乙烯制氯乙烷
C H +HCl==CH CH Cl
2 4 3 2
(4)转化率和产率计算公式 乙烯制聚乙烯
nC H === CH CH
2 4 2— 2 n
注:乙烯有碳碳双键,所以有还原性,能被高锰酸钾等强氧化剂氧化。
(计算时量可以是质量或者物质的量,但是上下单位要一致)
(3)炔烃(拓展)(乙炔为例)
乙炔的燃烧
点燃
2CH +3O ==2CO +2H O
2 2 2 2
(计算时量可以是质量或者物质的量或是气体体积,但是上下单位要一致)
乙炔是溴水褪色:
乙炔制氯乙烯:
注:乙炔有碳碳三键,所以有还原性,能被高锰酸钾等强氧化剂氧化。
第七章 有机化合物 (4)乙醇
一、有机物及其性质 乙醇的燃烧
1.认识有机物及概念 乙醇的催化氧化:(注意现象)
(1)有机物中的碳成键形式:每个碳原子链接4个共价键 乙醇与钠反应:(注意和钠与水反应的现象对比)
(2)有机物的结构:结构式、结构简式、分子式、最简式(或实验室)、球棍模型、空间充填模型。 乙醇被酸性高锰酸钾(或重铬酸钾)氧化
(3)根据碳骨架的不同可以分为碳链和碳环; 注:乙醇不会与氢氧化钠反应。
(4)有机物的熔沸点:(除了新戊烷是气体,一般含碳量小于等于 4的为气态,大于4的液态)含碳量 (5)乙酸
越多,熔沸点越高;链状烷烃支链越多熔沸点越低;对于脂肪酸不饱和键越多熔沸点越低。 乙酸的燃烧
(5)大多数有机物都能燃烧(氧化反应) 乙酸和钠反应
(6)液态有机物:中学常见的大多数液态有机物多为油状液态,不溶水,且密度比水小。(除了特殊的 乙酸和乙醇的反应
有机物乙醇和乙酸等易溶于水;四氯化碳密度比水大等) 注:乙酸是有机酸,是弱酸,但是比碳酸酸性强。
(7)烃:只含碳氢两种元素的有机化合物。 二、有机高分子材料
(8)烃的衍生物:烷烃中氢原子(或原子团)被原子或原子团所取代后形成的有机物。 三大合成材料:塑料、合成纤维、合成橡胶
(7)同分异构体:分子式相同,结构式不同的有机物。 1.塑料:主要成分是合成树脂;合成树脂+添加剂=塑料
42.橡胶:天然橡胶的主要成分是聚异戊二烯。 3.油脂(高级脂肪酸甘油酯)
合成橡胶:硫化橡胶:更好的强度、韧性、弹性和化学稳定性。 组成元素:C、H、O
氟橡胶:耐热、耐酸碱腐蚀 (1)定义:高级脂肪酸和甘油通过酯化反应得到的高级脂肪酸甘油酯。油脂是酯中的一类。
特种橡胶(硅橡胶):耐高温和严寒,特种橡胶在航天航空和国防尖端技术领域中发挥着重要 (2)高级脂肪酸的分类:
的作用。 饱和脂肪酸:硬脂酸(C H COOH)和软脂酸(C H COOH)
17 35 15 31
3.纤维: 天然纤维:棉花、羊毛、蚕丝和麻等。 不饱和脂肪酸:油酸(C H COOH)和亚油酸(C H COOH)
17 33 17 31
合成纤维:以煤、石油、天然气为原料经聚合反应生产合成纤维。 (3)油脂的性质:
三、基本营养物质(包括:糖类、蛋白质、油脂、维生素、无机盐和水) 油脂的水解的最终产物:高级脂肪酸和甘油
1.糖类 (皂化反应) 油脂在碱性条件下水解的产物:高级脂肪酸盐和甘油
组成元素:C、H、O 油脂能够促进脂溶性维生素(A、D、E、K)的吸收。
(1)单糖:葡萄糖和果糖(是同分异构体) (4)人造奶油(又称人造黄油):氢化植物油。
分子式:C H O
6 12 6
检验葡萄糖(还原糖)的方法:
1.与新制氢氧化铜反应: 先加过量氢氧化钠溶液使溶液显碱性,再硫酸铜溶液,煮沸后观
察到砖红色沉淀产生。 第八章 化学与可持续发展
2.银镜反应: 先加过量氢氧化钠溶液使溶液显碱性,再加银氨溶液,水浴加热,观察到试 一、自然资源的开发利用
管内壁有银镜生成。 1.金属矿物的开发利用
(2)二糖:蔗糖和麦芽糖(是同分异构体) (1)金属在自然界中的存在形式:化合态和游离态
分子式:C H O (2)金属的冶炼方式
12 22 11
二糖水解的条件:浓硫酸,加热。 K Ca Na Mg Al :电解法
(3)多糖:淀粉和纤维素(不是同分异构体) Zn Fe Sn Pb Cu :热还原法(或铝热法)
分子式:(C H O ) Hg Ag :热分解法
6 10 5 n
多糖水解的条件和最终产物:葡萄糖 Pt Au :其它方法(富集法)
检验淀粉的试剂:I 2.海水资源的开发利用
2
检验淀粉水解程度的实验: (1)海水中的元素:
取淀粉配置成溶液,滴加稀硫酸加热后加热,滴加碘水,观察现象 1;滴加过量氢氧化钠溶液,加 (2)海水淡化的方法:
入银氨溶液,水浴加热,观察现象2。 (3)工业上常用的一种海水提取溴技术叫做“吹出法”,其过程包括:
现象1 现象2 淀粉水解程度 氧化:氧化(用氯气氧化海水中的溴离子)
变蓝 无明显现象 淀粉未水解 2Br-+Cl ==Br +2 Cl-
2 2
变蓝 有银镜产生 淀粉部分水解 吹出:热空气(用空气将生成的溴吹出)
未变蓝 有银镜产生 淀粉全部水解 吸收:二氧化硫(用二氧化硫作还原剂使溴转化为氢溴酸,以使其与空气分离)
注:纤维素在人体内不能被水解 SO +Br +H O==HBr+H SO
2 2 2 2 4
2.蛋白质 蒸馏:氯气(再用氯气将氢溴酸氧化为溴后蒸馏分离)
组成元素:C、H、O、N、P、S等
(1)蛋白质的性质 3.煤、石油、天然气的开发利用(都是混合物)
蛋白质的变性:强酸、强碱、重金属的盐类都能使蛋白质变性;变性是不可逆的过程。 (1)煤
蛋白质的水解:蛋白质水解的最终产物是氨基酸。 组成:由有机物和少量无机物组成的复杂混合物,其主要以碳元素为主,还含有少量的氢、氧、氮、
颜色(显色)反应:蛋白质遇到浓硝酸会变黄色。 硫等元素
注:绝大多数酶也是蛋白质。 综合利用
(2)氨基酸的性质(既有酸性,又有碱性) 干馏:(化学变化)将煤隔绝空气加热使之分解的过程,工业上也叫煤的焦化。
高温
注:我国科学家在世界上首次完成了具有生命活力的蛋白质——牛结晶胰岛素的全合成。 气化:(化学变化)将煤转化为可燃性气体的过程。C+H O==CO+H
2 2
5液化:(化学变化)煤与氢气作用生成液体燃料。 绿色化学:改变先污染后治理的观念和做法,减少或消除产品在生成和应用中涉及的有害物质,实现从
源头减少或消除环境污染。
(2)石油 4.开发和利用自然资源要遵循的原则减量化、再利用、再循环。:
组成:多种碳氢化合物组成的混合物,成分复杂。
综合利用
分馏:(物理变化)根据各组分沸点的不同,分馏后可以获得汽油、煤油、柴油含碳较少的轻质油。
裂化:将重油裂化为汽油等物质。
裂解:裂化后进一步裂解可得到短链饱和和不饱和烃。
催化重整:使链状烃转化为环状烃。
(3)天然气
组成:
综合利用:作为清洁的化石燃料;化工原料主要用于合成氨和生成甲醇等。
二、化学品的合理使用
化学品分类
大宗化学品:乙烯、硫酸、纯碱和化肥等。
精细化学品:医药、农药、日用化学品、食品添加剂等。
1.农药
2.医药
(1)药物的分类:按照来源分为天然药物和合成药物
(2)阿司匹林:化学名称为乙酰水杨酸,具有解热镇痛的作用。
(3)处方药和非处方药的标识:
非处方药:OTC
处方药:R
3.食品添加剂
(1)着色剂:
天然色素:红曲红、B-胡萝卜素、姜黄、叶绿素铜钠盐、焦糖色等
合成色素:芹菜红、柠檬黄、靛蓝等
(2)曾味剂:味精(化学名称为谷氨酸钠)
味精最早是海带中提取出来的,现在主要以淀粉为原料通过发酵法生产。
(3)膨松剂:碳酸氢铵、碳酸氢钠等。
(4)凝固剂:氯化镁、硫酸钙、葡萄糖酸- ᶞ-内脂等
(5)防腐剂:苯甲酸及其钠盐、山梨酸及其钾盐、亚硝酸钠
亚硝酸钠是防腐剂和护色剂。
(6)抗氧化剂:维生素C(又称抗坏血酸)
(7)营养强化剂:碘酸钾、碳酸钙、硫酸亚铁、硫酸锌、维生素等
三、绿色化学
1.三废:废气、废水、废渣
2.污水的处理
一级处理:通常采用物理方法,处理后达不到排放标准。
二级处理:常采用生物和化学方法,处理后达到排放标准。
三级处理:通常采用化学方法,处理后达到排放标准,通常用于绿化和景观用水等。
6