文档内容
《化学反应与能量变化》第一课时教学设计
课题 《化学反应与能 单元 6 学科 化学 年级 高一
量变化》第一
课时
教材 本节教学内容是人教版高中化学必修第二册第六章《化学反应与能量》第一节《化学反
分析 应与能量变化》的第一课时。本章教材给学生建立一个重要的思想,化学反应中不仅有物质
的变化同时伴随有能量变化,让学生能从物质和能量两个角度认识物质世界的变化规律,
然后展开对化学变化相关理论的学习,如:化学反应的快慢,以及从能否进行到底的角度认
识化学反应,化学平衡状态、勒夏特列原理这些基本理论。搞清楚反应是吸热反应还是放热
反应,是判断温度对化学平衡移动的影响的前提。
本节教材,对于构建学生完整的化学反应体系有重要作用,又是对后边化学平衡移动
的学习作铺垫。化学热力学可以解决化学反应中能量变化的问题,同时可以解决化学反应
进行的方向和进行的限度问题。学生首先利用键能计算几个化学反应中的能量变化,在单
一物质体系的转化中感受“化学键”的局限,仅有它是不够的。让学生在本节内容的学习
中树立起化学反应的能量转化观以及定量研究能量转化的思想,从理论和定量层面更深入
地让学生体会和感受到运用化学变化实现能量转化的重大意义。
本节安排了“吸热和放热反应”,“反应热(焓变)”“反应热的有关计算”“世界能
源”这四部分内容。学生通过学习这部分知识,掌握化学反应与能量的关系以及计算方法,
会根据键能计算化学反应的焓变,能根据图像判断化学反应是吸热还是放热反应。
宏观辨识与微观探析:通过放热和吸热反应的实验,然学生直观的感觉化学反应中的能量
变化,进一步激发学生学习化学的兴趣和求知欲望,启发学生分析产生有关现象的因果关
系和本质联系,从而使学生了解学习和研究化学问题的一般方法和思维过程
证据推理与模型认知:通过揭示问题、讨论释疑、动手实验,学习对比、推断等多种科学探
教学目 究方法,学会由事物的表象分析事物的本质和变化,提高学生的实验能力、观察能力和对实
标与核 验现象的分析、推理及归纳总结能力。
心素养
科学探究与创新意识:从现象和结构出发,设计探究方案,探究硫的转化过程中的化学反应
原理,在探究中互利合作,培养团队精神。
科学精神与社会责任:激发学生透过现象探究本质的兴趣,尊重科学,认真学习科学的学习
方法;通过参与探究过程,培养自身严谨的科学态度和辩证分析能力。
重点 通过键能计算反应热;根据反应物和生成物能量图像判断反应是放热反应还是还是吸热反
难点 应。
教学过程
教学环节 教师活动 学生活动 设计意图
导入新课 火的发现和使用使人类告别了茹毛饮血的时代,从野蛮
走向文明。我们利用的正是燃烧过程中释放的能量,化学反应
不仅仅是物质的变化,还伴随有能量的变化。化学能可以转化
为光能、热能、电能等,当能量以热的形式表现时,化学反应
就分为吸热反应和放热反应。那么化学中都有哪些放热和吸
热反应?
讲授新课 第一节化学反应与能量变化
一、吸热和放热反应
1.实验
【实验6-1】
在一支试管中加入2mL 2mol/L盐酸,并用温度计测量其温度。再向试管中放入用砂纸打磨光亮的镁条,观察现象,并
测量溶液温度的变化。
实验现象:在实验6-1中,镁条不断溶解,有气泡产生,同
时观察到温度计温度升高,说明反应放出了热量。
反应方程式:Mg+2HCl==MgCl +H ↑
2 2
【实验 6-2】将 20gBa(OH) .8HO 晶体研细后与
2 2
10gNH4Cl晶体仪器放入烧杯中,并将烧杯放在滴有几滴水的
木片上。用玻璃棒快速搅拌,闻到气味后迅速用玻璃片盖上烧
杯,用手触摸烧杯壁下部,试着用手拿起烧杯,观察现象。
实验现象:在实验6-2中,用手触摸烧杯壁下部,烧杯壁
冰冷,拿起烧杯,木片上的水滴结冰,和烧杯底部粘结在一
起,说明反应吸收了热量。
反应方程式:
Ba(OH).8HO+2NH Cl==NH3↑+BaCl +10H O
2 2 4 2 2
2.放热反应和吸热反应
化学上把释放热量的化学反应称为放热反应,如镁条、铝
片和盐酸的反应,木炭、氢气、甲烷等在氧气中的燃烧,氢气
与氯气的化合等都是放热反应。
把吸收热量的化学反应称为吸热反应,如氢氧化钡和氯
化铵的反应,盐酸和碳酸氢钠的反应,灼热的炭与二氧化碳的
反应等都是吸热反应。
所有的燃烧
中和反应
常见放热反应 溶液里的置换反应
一般的化合反应
铝热反应
电离
强碱与铵盐
常见的吸热反应 一般的分解反应
特殊的化合反应(C和CO 反应)
2
特殊的置换(C和水蒸气、铁和水蒸
气)
二、反应热(焓变)
1.化学反应过程中所释放或吸收的能量,都可以用热量
(或换算成相应的热量)来表述,叫做反应热,在恒压条件下又
称为焓变。
PS:①符号:△H;单位: kJ/mol 或 kJ·mol-1;
②反应热描述的是化学反应前后的热量变化;
③反应热描述的是一定温度下的热量变化;
④任何化学反应都有反应热,表现为吸热反应或者放热反应;
⑤反应体系的能量降低(即放热反应),则∆H为“-”;
反应体系的能量升高(即 吸热反应),则∆H为
“+”;
2. 热化学方程式
①我们已经认识了反应热,那么如何在化学方程式中正
确反映其热量的变化?---------------热化学方程式
表示参加反应物质的量和反应热的关系的化学方程式,
叫做热化学方程式。
与化学方程式相比,热化学方程式有哪些不同?
正确书写热化学方程式应注意哪几点?
②热化学方程式
能表示参加反应物质的量和反应热的关系的化学方程式
200℃
H(g)+I (g)======2HI(g) △H=-14.9kJ/mol
2 2
101kPa
⑴热化学方程式包含物质变化和能量变化两个部分,二
者缺一不可。
普通化学方程式只包含物质变化一个部分。
⑵热化学方程式需注明反应时的温度和压强。对于 25℃
101kPa时进行的反应可不注明。
普通化学方程式不需注明温度和压强。
⑶热化学方程式需注明各物质的状态。
普通化学方程式不需注明物质的状态。
⑷热化学方程式中化学计量数表示参加反应的各物质的
物质的量,可为整数或分数,其△H与系数对应成比例。
普通化学方程式中化学计量数宏观上表示各物质的物质
的量,微观上表示原子分子数目,只能为整数,不能为分数。
3.书写热化学方程式的注意事项
①化学方程的右边必须写上△H,并用“空格”隔开,
△H:吸热用“+”,放热用:“-”,单位是kJ/mol或J/mol;
②需注明反应的温度和压强,如不注明条件,即指: 25℃
1.01×105Pa;
③物质后需注明物质状态(s固体、l液体、g气体、aq溶
液中);
④热化学方程式中各物质化学式前面的化学计量数仅表
示物质的量并不能表示物质的分子数或原子数,因此化学计
量数可以是整数也可以是分数;
⑤根据焓的性质,若化学方程式中各物质的系数加倍,则
△H的数值也加倍;若反应逆向进行,则△H改变符号,但绝对
值不变;⑥ 热化学方程式一般不要写反应条件。
三、反应热的有关计算
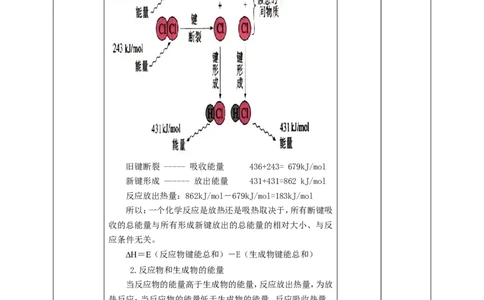
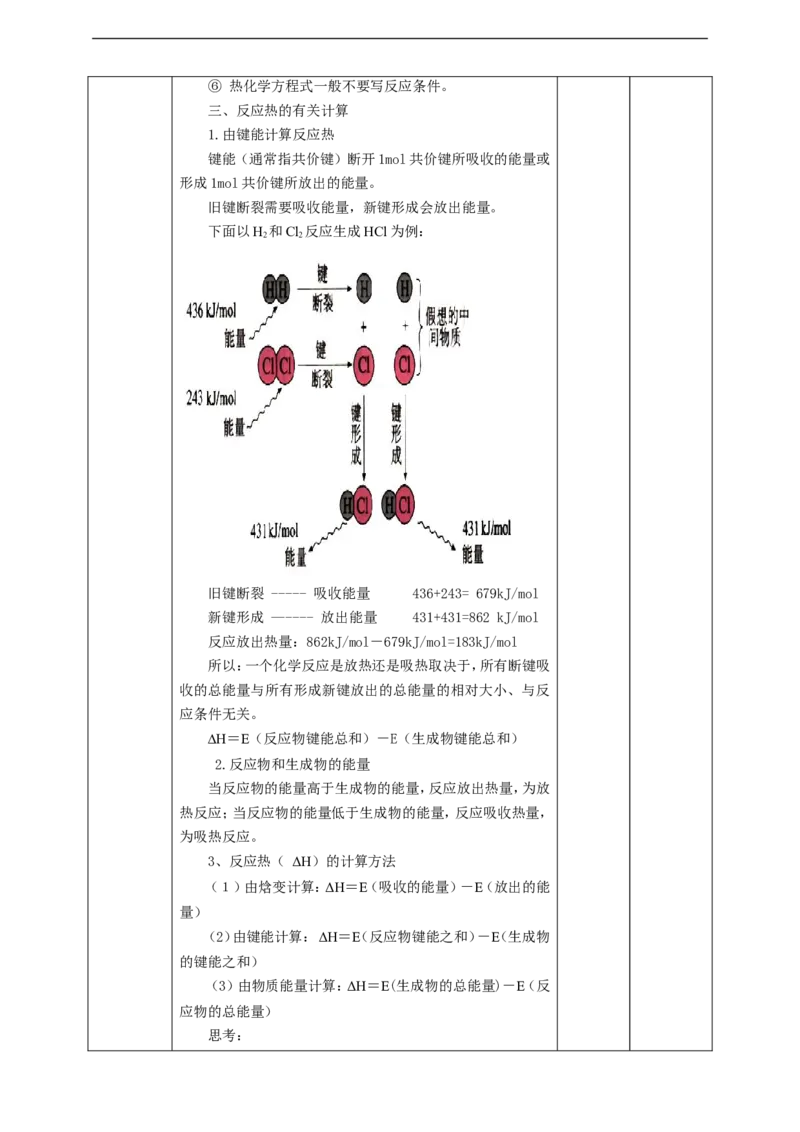
1.由键能计算反应热
键能(通常指共价键)断开1mol共价键所吸收的能量或
形成1mol共价键所放出的能量。
旧键断裂需要吸收能量,新键形成会放出能量。
下面以H 和Cl 反应生成HCl为例:
2 2
旧键断裂 ----- 吸收能量 436+243= 679kJ/mol
新键形成 —---- 放出能量 431+431=862 kJ/mol
反应放出热量:862kJ/mol-679kJ/mol=183kJ/mol
所以:一个化学反应是放热还是吸热取决于,所有断键吸
收的总能量与所有形成新键放出的总能量的相对大小、与反
应条件无关。
∆H=E(反应物键能总和)-E(生成物键能总和)
2.反应物和生成物的能量
当反应物的能量高于生成物的能量,反应放出热量,为放
热反应;当反应物的能量低于生成物的能量,反应吸收热量,
为吸热反应。
3、反应热( ΔH)的计算方法
(1)由焓变计算:ΔH=E(吸收的能量)-E(放出的能
量)
(2)由键能计算: ΔH=E(反应物键能之和)-E(生成物
的键能之和)
(3)由物质能量计算:ΔH=E(生成物的总能量)-E(反
应物的总能量)
思考:物质具有的能量与其稳定性之间存在什么关系?
物质具有的能量越低越稳定。一般原子间的化学键越牢
固,键能越大,物质越稳定。
吸热反应和放热反应的对比
放热反应 吸热反应
△H表现行式 △H﹤0 或△H 为 △H﹥0 或△H 为
“—” “+”
物质总能量变化 生成物的总能量 生成物的总能量
小于反应物的总 大于反应物的总
能量 能量
键能变化 生成物总键能大 生成物总键能小
于反应物总键能 于反应物总键能
联系 键能越大,物质能量越低,越稳定,反
之键能越小,物质能量越高,越不稳
定。
四、世界能源
1.从古到今,人类的能源主要来自于物质的燃烧。进入近
现代社会,煤、石油、天然气等化石 燃料成为主要的能源,但
是化石燃料存在的主要问题:一是不可再生并且储量有限;二
是在燃烧和使用过程中产生了粉尘、SO 、NOx、CO等大气污
2
染物。所以人类必须节约能源并寻找合适的新能源。
2.节能一方面是减少能源使用,另一方面则要提高能源
的利用率。
目前,人类比较理想的新能源,主要包括太阳能、风能、
地热能、海洋能和氢能等。
思考与讨论:
煤、汽油和柴油等作为燃料大量使用会造成空气污染,但
不适用它们又会严重影响现代社会的生产和生活。对此,请从
社会不同人群的角度,提出你的想法和建议,并与同学讨论。
答案提示:让学生从工厂、工人、司机、生活等角度自由
发挥。
信息搜索
(1)利用互联网(如国家统计局网站)搜索近10年我国
每年的能源消费总量和能源矿产储量的数据及变化趋势,体
会节能的重要性和必要性。
(2) 通过查阅书刊或互联网搜索,了解煤和石油产品的
燃烧排放物对环境和气候的影响,以及人类正在采取的应对
措施。
随堂练习:
1.(课本41页第一题)化学反应的本质是有新物质生成,
物质的变化是化学反应的基本特征之一,化学反应的另一基本特征是__________,通常表现为_____的释放或吸收。
答案:化学键的断裂和形成;能量。
2、(课本41页第3题)下列说法错误的是( )
A、化学反应必然伴随发生能量变化
B、化学反应中能量变化的大小与反应物的质量多少无关
C、能量变化必然伴随发生化学变化
D、化学反应中的能量变化主要是由化学键变化引起的
答案为:C
【解析】A、化学反应必然伴随能量变化,故A正确;
B、焓变的数值与化学计量数对应,故B正确;
C、能量变化不一定伴随化学反应,比如浓硫酸溶于水放
热,故C错误;
D、化学反应中的能量变化主要是由化学键的断裂和形成
引起的,故D正确;
3、(课本41页第4题)在一定条件下,石墨转化为金刚石
要吸收能量,在该条件下,下列结论正确的是( )
A、金刚石比石墨稳定
B、等质量的金刚石和石墨完全燃烧释放的热量相同
C、金刚石转化为石墨是吸热反应
D、1molC(金刚石)比1mol(石墨)的总能量高
答案为:D
【解析】A、石墨能量低,能量越低越稳定,A错误;
B、金刚石和石墨能量不同,等质量时,放出的热量不同,
B错误;
C、金刚石转化为石墨要放出热量,C错误;
D、石墨转化为金刚石吸收热量,所以金刚石能量高,D正
确。
4、已知键能: N≡N: 946KJ/mol,H-H :436KJ/mol, H-N
:391KJ/molN (g) + 3H (g)==2NH3(g),从理论上计算△H为(
2 2
)
A.+1800KJ/mol B. + 92KJ/mol
C. – 92KJ/mol D. – 46KJ/mol
答案为:C
【解析】
△H=946kJ/mol+3×436kJ/mol-6×391kJ/mol=-92kJ/mol
5.已知反应A+B=C+D为放热反应,对该反应的下列
说法中正确的是( )
A. A的能量一定高于C
B. B的能量一定高于D
C. A和B的总能量一定高于C和D的总能量D. 该反应为放热反应,故不必加热就一定能发生
答案为:C
【解析】该反应放热,说明反应物的能量和高于生成物的
能量和
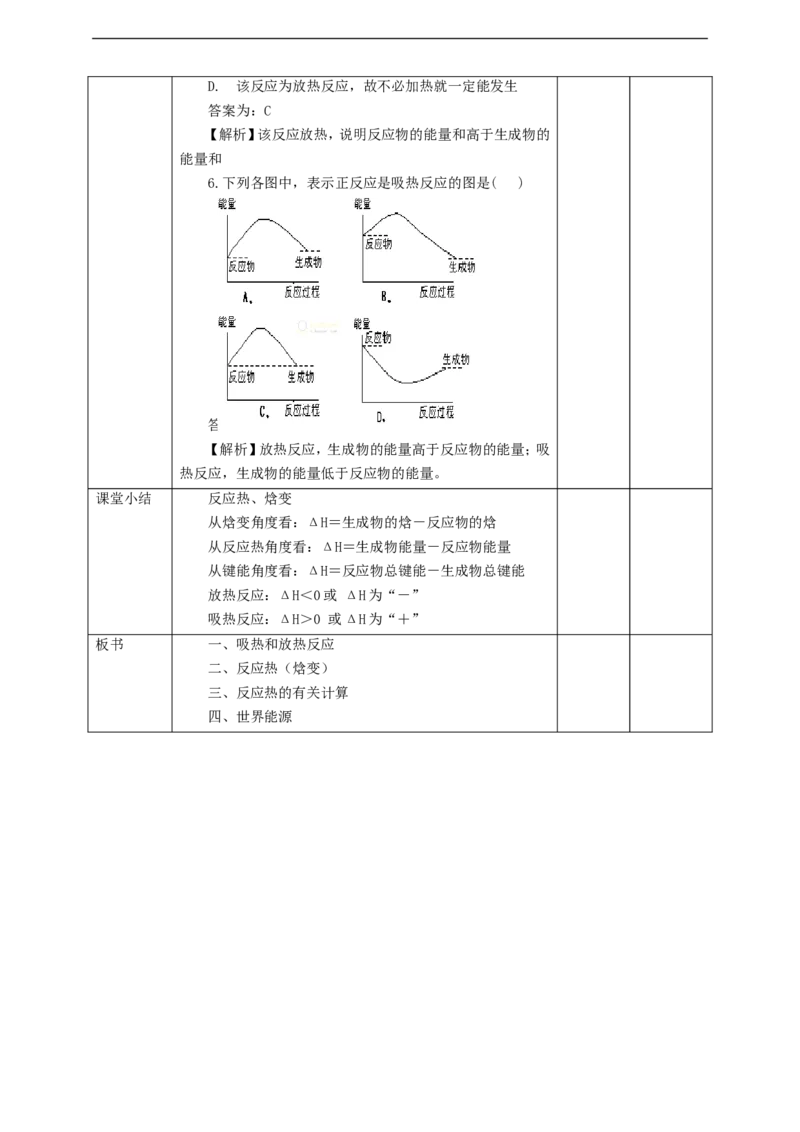
6.下列各图中,表示正反应是吸热反应的图是( )
答案为:A
【解析】放热反应,生成物的能量高于反应物的能量;吸
热反应,生成物的能量低于反应物的能量。
课堂小结 反应热、焓变
从焓变角度看:ΔH=生成物的焓-反应物的焓
从反应热角度看:ΔH=生成物能量-反应物能量
从键能角度看:ΔH=反应物总键能-生成物总键能
放热反应:ΔH<0或 ΔH为“-”
吸热反应:ΔH>0 或ΔH为“+”
板书 一、吸热和放热反应
二、反应热(焓变)
三、反应热的有关计算
四、世界能源