文档内容
第二章 化学物质及其变化
第三节 氧化还原反应
专题:氧化还原反应的应用
【学习目标】1.通过讨论交流、归纳小结,学会判断物质具有氧化性、还原性以及判断氧化性和还
原性强弱的一般方法。
2.通过阅读归纳、练习应用,学会利用氧化性和还原性强弱判断化学反应能否发生,能用氧化还
原反应的相关知识解释生活中的一些化学现象。
3. 通过分析探究,典例剖析,初步建立用氧化还原反应中的“电子守恒”思想解决简单的氧化还原
计算问题的思维模型,培养解决生产生活中的化学问题的能力。
【学习重点】物质氧化性、还原性强弱的判断及应用。
【学习难点】建立利用电子守恒思想解决有关氧化还原反应问题的基本思维模型。
【课前预习】
旧知回顾:1.从元素的价态考虑:最高价态—只有 ,如Fe3+、HSO 、KMnO 等;最低价态
2 4 4
—只有 ,如金属单质、Cl-、S2-等;中间价态—既有 又有 ,如Fe2+、S、Cl 等。
2
2.Fe O +2Al=====Al O +2Fe所属基本反应类型是 。在该反应中____元素的化合价升
2 3 2 3
高,该元素的原子 电子,被_______;而____ ____元素的化合价降低,该元素的原子
电子,被__ __。该反应中,Fe O 发生了__ _反应,Al发生了__ __反应,__ _是氧化产
2 3
物,__ _是还原产物。
新知预习:1.氧化性、还原性的强弱取决于物质得、失电子的 程度,与得、失电
子 无关。
2.已知:①2Fe+3Cl=====2FeCl ②Fe+S FeS。铁元素被氯气氧化为+3价,被硫氧化为+2
2 3
价,则氧化性:氯气 硫。
3.某些氧化剂的氧化性和还原剂的还原性的强弱与 等因素有
关。
【课中探究】
情景导入:氧化还原反应是一类重要的化学反应类型,广泛存在于日常的生产生活中。其中有的反应
是有益于人类活动,例如:金属的冶炼、电镀、燃料的燃烧、植物的光合作用等;有的反应对于人类活动
是有害的,例如:食物的腐败、钢铁的锈蚀等。作为化学工作者我们应该认真学好有关化学知识,才能趋
利避害使之更好的服务于社会。(见PPT图片)
一、物质氧化性、还原性强弱
活动一、探究物质的氧化性和还原性
任务一、请结合氧化性和还原性的定义,思考物质的化合价是如何影响物质的氧化性和还原性的?并
完成表格中的内容:
①定义:氧化性:
还原性:
②物质的氧化性及还原性与核心元素化合价有关。见下表:
核心元素化合价 实例 性质
最高价 KMnO、FeCl、浓HNO、浓HSO
4 3 3 2 4
中间价 SO 、NaSO、FeSO 、S
2 2 3 4
最低价 Fe、Na、KI
任务二、以反应MnO + 4HCl MnCl +Cl↑+2H O为例,在氧化还原反应中如何判断物质的氧化性
2 2 2 2
和还原性、氧化剂和还原剂?
【对应练习】1.下列盐酸参与的反应中,HCl被氧化的是
A.CuO+2HCl=CuCl +H O
2 2
B.Zn+2HCl=ZnCl +H ↑
2 2
C.Ca(ClO) +4HCl=CaCl +2Cl↑+2H O
2 2 2 2
D.CaCO +2HCl=CaCl +CO ↑+H O
3 2 2 2
2.验室制取少量的氮气,常利用的反应是NaNO +NH Cl NaCl+N↑+2HO。关于该反应说法正
2 4 2 2
确的是( )
A.NaNO 是还原剂
2
B.生成1分子N 时转移的电子为6个
2
C.NH Cl中的氮元素被氧化
4
D.N 既是氧化剂又是还原剂
2
活动二、物质氧化性、还原性强弱的判断方法
任务一、讨论交流:根据所学知识,你知道判断物质氧化性、还原性强弱有哪些基本方法?并举例说
明。
①根据氧化还原反应方程式判断:
②根据元素的活动性顺序判断:③根据反应条件判断:
④根据氧化产物的化合价高低判断:
任务二、问题探究:金属阳离子一定只有氧化性吗?已知物质的氧化性或还原性的强弱关系,如何判
断某一氧化还原反应能否发生?
任务三、拓展探究:“钠原子能失去1个电子,铝原子能失去3个电子,所以铝的还原性比钠强。”
这种说法正确吗?物质氧化性或还原性的强弱与哪些因素有关?
【对应练习】1.现有下列几个离子反应:
①Cr O+14H++6Cl-===2Cr3++3Cl↑+7HO
2 2 2
②2Fe2++Br ===2Fe3++2Br-
2
③2Fe3++SO +2HO===2Fe2++SO+4H+
2 2
下列有关性质的比较正确的是( )
A.氧化性:Cr O>Cl>Fe3+
2 2
B.氧化性:Cl>Br >Cr O
2 2 2
C.还原性:SO Cr3+>Fe2+
2.已知I-、Fe2+、SO 、Cl-和HO 均有还原性,它们在酸性溶液中还原性的强弱顺序为SO >I->Fe2+
2 2 2 2
>H O>Cl-,则下列反应不可能发生的是( )
2 2A.2Fe3++SO +2HO===2Fe2++SO+4H+
2 2
B.I+SO +2HO===H SO +2HI
2 2 2 2 4
C.2Fe2++I===2Fe3++2I-
2
D.HO+SO ===H SO
2 2 2 2 4
二、氧化还原反应的规律及应用
活动一、探究氧化还原反应的规律
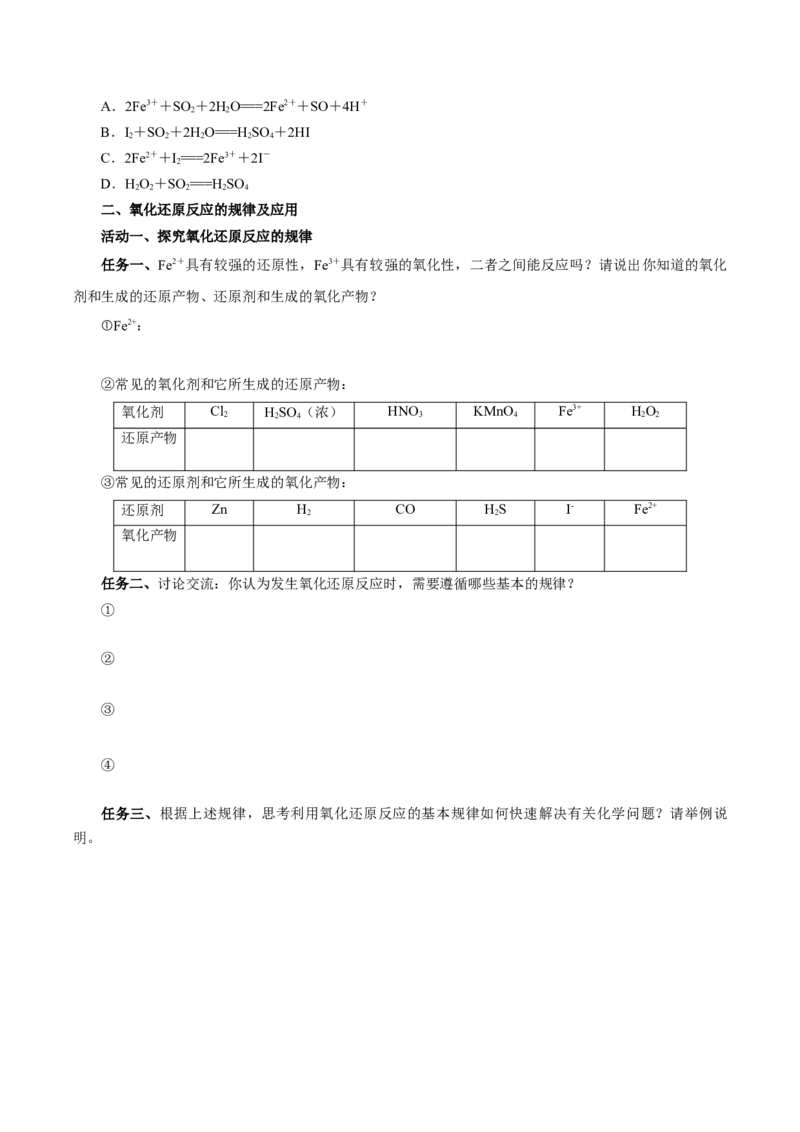
任务一、Fe2+具有较强的还原性,Fe3+具有较强的氧化性,二者之间能反应吗?请说出你知道的氧化
剂和生成的还原产物、还原剂和生成的氧化产物?
①Fe2+:
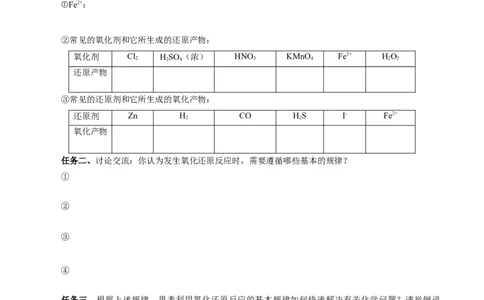
②常见的氧化剂和它所生成的还原产物:
氧化剂 Cl HSO (浓) HNO KMnO Fe3+ HO
2 2 4 3 4 2 2
还原产物
③常见的还原剂和它所生成的氧化产物:
还原剂 Zn H CO HS I- Fe2+
2 2
氧化产物
任务二、讨论交流:你认为发生氧化还原反应时,需要遵循哪些基本的规律?
①
②
③
④
任务三、根据上述规律,思考利用氧化还原反应的基本规律如何快速解决有关化学问题?请举例说
明。【对应练习】1.在含有Cu(NO )、Mg(NO)、AgNO 的溶液中加入适量锌粉,首先置换出的是( )
3 2 3 2 3
A.Mg B.Cu
C.Ag D.H
2
2.PbO 、KMnO 、Cl、FeCl 、CuCl 的氧化性依次减弱。下列反应在水溶液中不可能发生的是( )
2 4 2 3 2
A.Cu+2Fe3+===Cu2++2Fe2+
B.10Cl-+2MnO+16H+===2Mn2++5Cl↑+8HO
2 2
C.2Fe2++Cl===2Fe3++2Cl-
2
D.5Pb2++2MnO+2HO===5PbO+2Mn2++4H+
2 2
活动二、氧化还原反应的应用
任务一、若已知用3个NaSO 恰好将2个XO还原,如何利用“守恒规律”快速判断元素X在产物中
2 3
的化合价?
①基本方法:
②一般步骤:
任务二、已知如下反应:①2BrO+Cl===Br +2ClO,②ClO+5Cl-+6H+===3Cl +3HO,③2FeCl
2 2 2 2 3
+2KI===2FeCl +2KCl+I ,④2FeCl +Cl===2FeCl 。如何利用“强弱规律”快速判断有关物质氧化性或
2 2 2 2 3
还原性的强弱?
任务三、阅读教材P26页最后自然段,回答氧化还原反应在生产、生活中有哪些应用? 并尝试对红
酒中添加二氧化硫的原因作出解释。
任务四、结合教材P26页“思考与讨论”可知,汽车尾气产生的NO (主要指NO和NO )和CO均为
x 2
有毒气体,容易对环境造成污染,思考如何有效消除汽车尾气污染以实现保护环境的目的?【对应训练】1.人体正常的血红蛋白中应含有Fe2+。若误食亚硝酸钠,则导致血红蛋白中Fe2+转化为高
铁血红蛋白而中毒。服用维生素C可解除亚硝酸钠中毒。下列叙述中正确的是( )
A.亚硝酸钠表现还原性 B.维生素C表现了还原性
C.亚硝酸钠被氧化 D.维生素C作为氧化剂
2.近年来随着汽车数量的大幅增长,空气污染越来越严重。汽车尾气装置中,气体在催化转化器中的
催化转化过程如图所示。下列说法正确的是( )
A.催化转化反应中NO为氧化剂,N 为氧化产物
2
B.催化转化反应中氧化剂与还原剂的个数相等
C.催化转化后将生成的CO 处理吸收后尾气才能排放
2
D.催化转化反应中氧化产物与还原产物的个数相等
【课后巩固】1.(中)教材作业:P27-28页练习8、11、13
2.(易)下列各组物质中的氮元素,都既有氧化性又有还原性的是( )
A.N、NO B.NH 、NO
2 2 3
C.NH Cl、NO D.HNO、NO
4 2 3 2 4
3.(易)关于反应2NaClO+Na SO +H SO = 2ClO ↑+2Na SO +H O,说法正确的是( )
3 2 3 2 4 2 2 4 2
A.HSO 是还原剂 B.NaSO 是氧化剂
2 4 2 3
C.NaClO 中氯元素被氧化 D.氧化性:NaClO>NaSO
3 3 2 4
4.(易)已知还原性I->Fe2+>Br->Cl-,氧化性Cl>Br >Fe3+>I ,下列反应的化学方程式或叙述不成立
2 2 2
的是( )
A.Br +2HI = I +2HBr
2 2
B.2FeCl +Cl = 2FeCl
2 2 3
C.2FeCl +2HCl+I = 2FeCl +2HI
2 2 3
D.Cl 通入NaBr和NaI的混合溶液中,I-先被氧化
25.(中)氧化还原反应实际上包含氧化和还原两个过程。(1)向氯酸钠的酸性水溶液中通入二氧化
硫,该反应中氧化过程的反应式为SO +2H O—2e-→SO 2-+4H+;(2)向亚氯酸钠(NaClO )固体中通入
2 2 4 2
用空气稀释的氯气,该反应中还原过程的反应式为Cl2+2e-→2Cl-。在(1)和(2)反应中均会生成产物
X,则X的化学式为( )
A. NaClO B.NaClO
4
C. HClO D.ClO
2 2
6.(中)青铜是铜锡合金,明代宋应星所著的《天工开物》曾记载了炼锡的方法,其化学方程式为:
2C+SnO\o(\s\up6(_____)Sn+2CO↑。下列有关说法不正确的是( )
2
A.该反应中,C体现了还原性
B.该化学反应后,固体质量减小
C.SnO 在该过程中发生了氧化反应
2
D.一氧化碳有毒,可以用气球收集来进行尾气处理
7.(难)将磁性氧化铁放入稀硝酸中可发生如下反应:3Fe O +28HNO(稀)===9Fe(NO) +NO↑+
3 4 3 3 x
14HO,下列判断合理的是( )
2
A.Fe(NO ) 中的x为2
3 x
B.稀硝酸在反应中只表现氧化性
C.反应中每还原2 个氧化剂,就有6个电子转移
D.磁性氧化铁中的所有铁元素全部被氧化
8.(中)已知下列反应:
①Cl+2NaBr=2NaCl+Br ;②2KI+Br =2KBr+I ;③NaS+I =2NaI+S↓。
2 2 2 2 2 2
(1)Cl-、Br-、I-、S2-四种离子的还原性由强到弱的顺序是________________________。
(2)判断Cl 与NaS能否反应?___________________________________(填“否”或书写离子反应方程
2 2
式)。
(3)判断I 与NaBr能否反应?_____________(填“否”或书写离子反应方程式)。
2
(4)已知实验室制取氯气反应为:MnO +4HCl(浓) MnCl +Cl↑+2H O,由此分析:MnO 在反应中
2 2 2 2 2
________电子,所含元素化合价_________,发生__________反应。
(5)在硫酸溶液中,NaClO 和NaSO 能按粒子个数比1:2完全反应,生成一种棕黄色气体X,同时
3 2 3
NaSO 被氧化为NaSO ,则X为___________。
2 3 2 4
A.ClO B.ClO C.ClO D.Cl
2 7 2 2 2