文档内容
第四章 物质结构 元素周期律
第三节 化学键
第1课时 离子键
(1)以典型物质为例认识离子键形成,建立离子键的概念。
(2)能用电子式对离子键进行表征。
(3)能从宏观现象及化学键等不同角度对物质进行分类。能对典型物质的微粒间相互作用进行分析,能
从物质的构成微粒及相互作用角度说明物质性质的共性、差异及其原因,解释同类物质性质变化的规律。
【内容分析】
初中化学中讨论了离子的概念,学生知道带正电的Na+与带负电的Cl-形成了NaCl,也知道了物质是
由分子、原子或离子构成的,但学生并不知道离子化合物、共价化合物的概念,也不知道它们是如何形成
的。本节从微观粒子间相互作用的视角,讨论物质的构成,并揭示化学反应的本质。
学生已经知道活泼的金属钠与活泼的非金属氯可以反应生成氯化钠,所以,本节从学生非常熟悉的物
质人手,提出"从原子结构的角度来看,钠原子和氯原子是怎样形成氯化钠的呢"这一问题,接下来从微粒
间相互作用的视角,讨论钠原子和氯原子如何相互作用以达到稳定结构,来解释 NaCI的形成,从而引出
离子键的概念。
教材引入了电子式、分子结构模型等,以帮助学生形象地认识微观、抽象的概念,电子式的呈现突出
其工具性,以使学生易于理解原子核外电子排布,说明物质的形成过程。
化学键对于学生来说是个新的概念,在必修阶段学业要求不高,教材只介绍了简单的离子化合物和共
价化合物中的化学键类型。例如,关于离子键,只以NaCI的形成为例,并只说明"由活泼金属与活泼非金属形成离子化合物",列举的也是简单的物质。必修阶段的化学键内容只是为了使学生更好地认识分子的结
构和微粒间的相互作用,并没有深入讨论,更多相关内容将在选择性必修课程中做系统介绍。
【教学重点和难点】
重点∶离子键、离子化合物的概念;电子式的书写。
难点∶从微粒间相互作用的视角,认识化学反应的本质。
【教学流程】
【问题引入】
从元素周期表可以看出,到目前为止,已经发现的元素有一百多种。然而,由这一百多种元素的原子
构成的物质已超过1亿种。那么,元素的原子之间通过什么作用形成如此丰富的物质呢?
【学习任务一】宏观角度,感受化学键的存在
【思考与交流】
(1)观看钠在氯气中燃烧的实验视频,描述实验现象,写出化学方程式。
【设计意图】通过观看钠与氯气反应,从宏观的角度感受在化学反应中化学键的存在。
【学习任务二】微观探析,认识离子键的形成
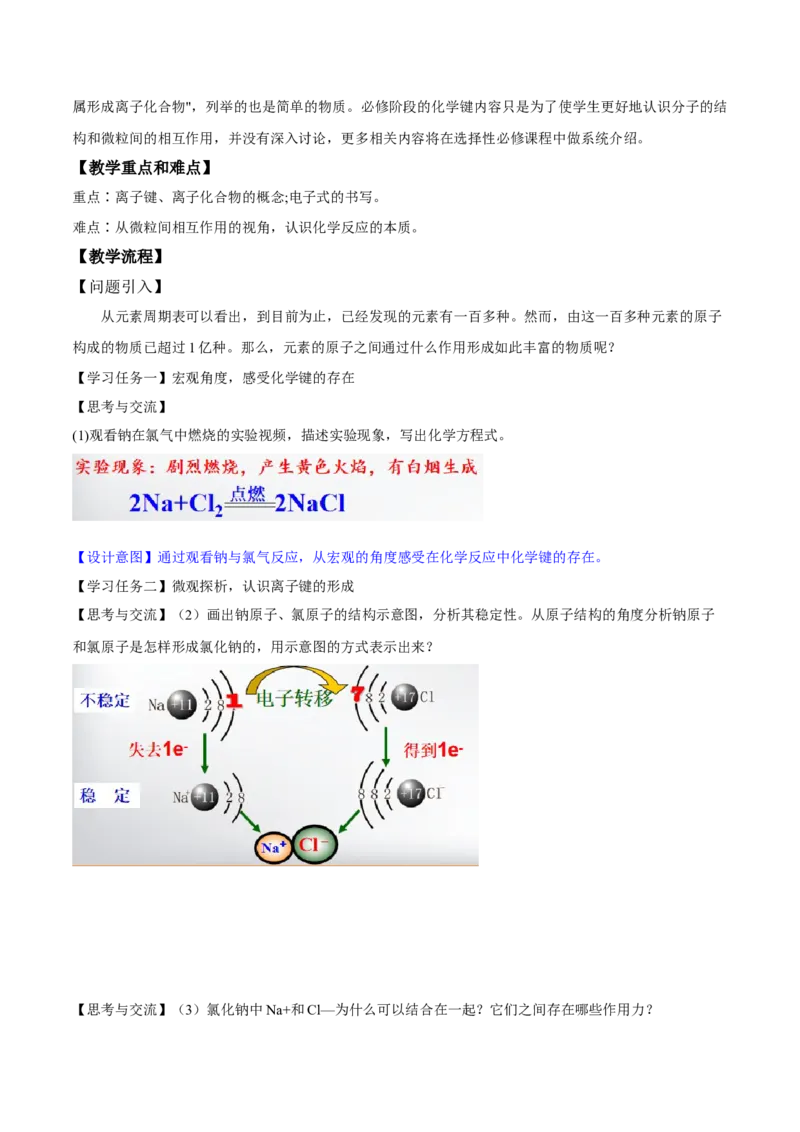
【思考与交流】(2)画出钠原子、氯原子的结构示意图,分析其稳定性。从原子结构的角度分析钠原子
和氯原子是怎样形成氯化钠的,用示意图的方式表示出来?
【思考与交流】(3)氯化钠中Na+和Cl—为什么可以结合在一起?它们之间存在哪些作用力?静电作用
(1) 异性电荷(Na+和Cl—)间的静电引力;
(2) 同性电荷(电子与电子、原子核与原子核)间的静电斥力
【设计意图】结合原子结构示意图从微观的角度认识离子键的形成过程,得出离子键的概念。
【新概念】
1、离子键——使阴、阳离子之间结合成化合物的静电作用叫做离子键。
【概念的运用】离子键存在哪些化合物之中?请举例说明。
NaCl、MgCl 、KCl、NaO、MgO、NaOH、NaSO 、NH Cl等等。
2 2 2 4 4
2、离子化合物———由离子键构成的化合物。
【小结】离子键存在范围(物质类别)——强碱、大多数盐及金属氧化物
【概念辨析】
判断正误:(1)离子化合物一定含有离子键?
(2)含有离子键的化合物一定是离子化合物?
【学习评价】1、2
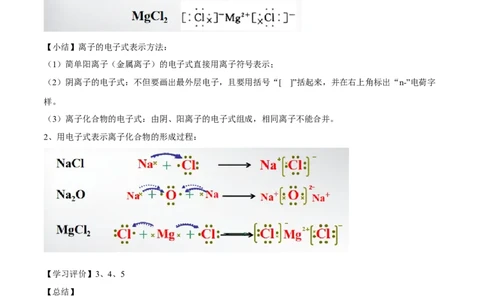
【学习任务三】符号表征——用电子式表示离子化合物的形成过程
电子式: 在元素符号周围用小黑点 · (或×)来表示粒子最外层电子的式子。
1、微粒的电子式表示方法:【小结】离子的电子式表示方法:
(1)简单阳离子(金属离子)的电子式直接用离子符号表示;
(2)阴离子的电子式:不但要画出最外层电子,且要用括号“[ ]”括起来,并在右上角标出“n-”电荷字
样。
(3)离子化合物的电子式:由阴、阳离子的电子式组成,相同离子不能合并。
2、用电子式表示离子化合物的形成过程:
【学习评价】3、4、5
【总结】【问题情景素材】
【思考与交流】
(1)观察钠在氯气中燃烧的实验,描述实验现象,写出化学方程式。
(2)画出钠原子、氯原子的结构示意图,分析其稳定性。从原子结构的角度分析钠原子和氯原子是怎样
形成氯化钠的,用示意图的方式表示出来?
(3)氯化钠中Na+和Cl—为什么可以结合在一起?它们之间存在哪些作用力?
【使用建议】本节概念、理论较多。要设计好问题的梯度,应低起点、小台阶设计教学,逐步突破教学难
点、重点。
【实验素材】
1、【实验3-4】在一支试管中加入5mL盐酸,再向试管中放入一小块铝片。观察现象。过一段时间后,将
点燃的木条放在试管口,你观察到什么现象?
2、【实验3-5】在两支试管中分别加入少量的NaOH溶液,然后向其中一支试管中放入一小块铝片,向另
一支试管中放入用砂纸仔细打磨过(除去表面的氧化膜)的一小块铝片。观察现象。过一段时间后,将点
燃的木条分别放在两支试管口,你观察到什么现象?
【练习素材】
1、下列物质中,属于离子化合物的是___________________。
① KOH ② ZnSO ③ HO ④ NH Cl ⑤ CO ⑥ MgO ⑦ HCl
4 2 4 2
⑧NH ·H O
3 2
【答案】①②④⑥
2、下列性质中,能证明某化合物内一定存在离子键的是( )
A.可溶于水 B.具有较高的熔点
C.水溶液能导电 D.熔融状态能导电【答案】D
3、用电子式表示下列微粒或物质的核外电子结构。
(1)Ca _______________ (2)S _________________
(3)Ca2+_______________ (4)S2-_________________
(5)CaCl ______________ (6)NaS_______________
2 2
【答案】略
4、下列化合物电子式书写正确的是( )
【答案】D
5、用电子式表示下列物质的形成过程。
(1)KCl
(2)MgF
2
(3)BaCl
2
(4)MgO
【答案】略