文档内容
倒卖拉黑不更新,淘宝唯一免费更新店铺: 知二教育
2021-2022 学年高二化学重难点专题突破
模块三 晶体结构与性质
习题课 晶胞的计算
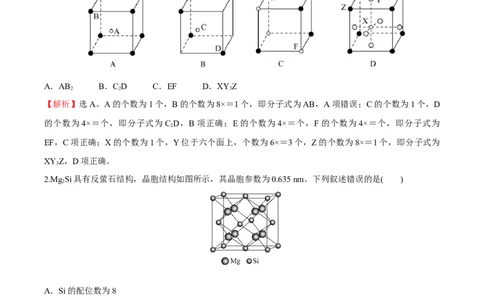
1.根据离子晶体的晶胞结构(如图),判断化学式不正确的是( )
A.AB B.C D C.EF D.XY Z
2 2 3
【解析】选A。A的个数为1个,B的个数为8×=1个,即分子式为AB,A项错误;C的个数为1个,D
的个数为4×=个,即分子式为 C D,B项正确;E的个数为4×=个,F的个数为4×=个,即分子式为
2
EF,C项正确;X的个数为1个,Y位于六个面上,个数为6×=3个,Z的个数为8×=1个,即分子式为
XY Z,D项正确。
3
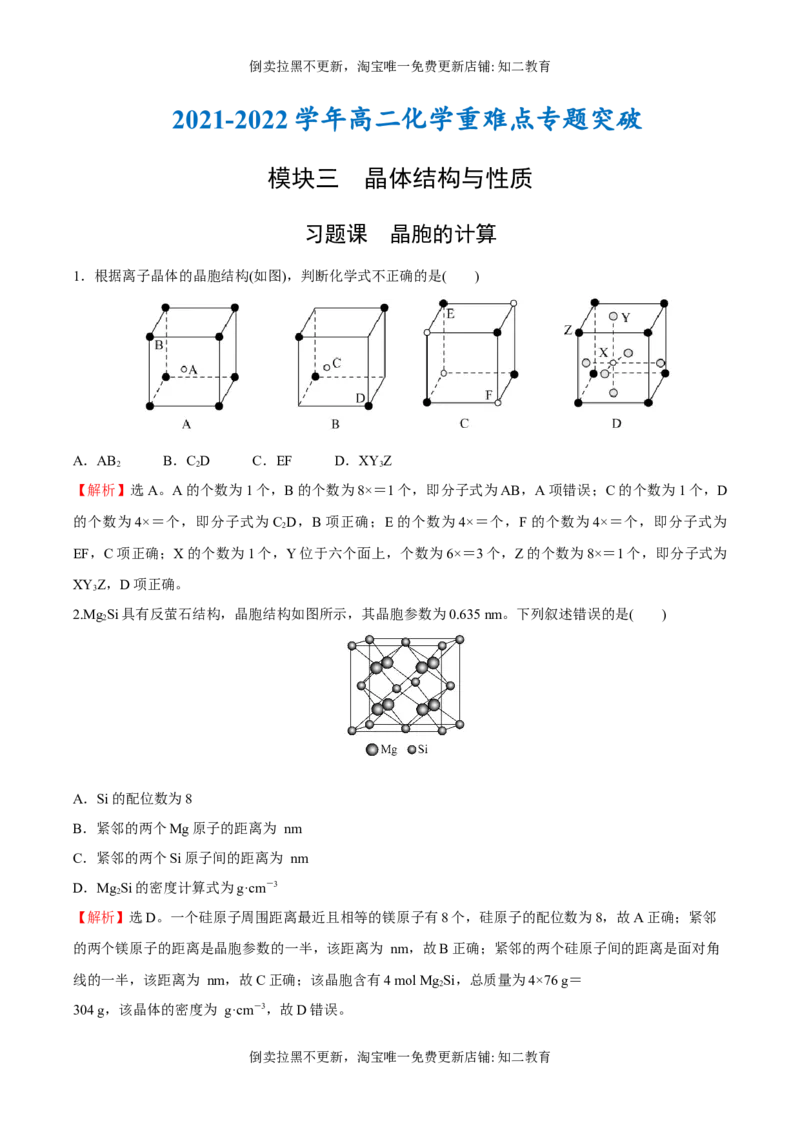
2.Mg Si具有反萤石结构,晶胞结构如图所示,其晶胞参数为0.635 nm。下列叙述错误的是( )
2
A.Si的配位数为8
B.紧邻的两个Mg原子的距离为 nm
C.紧邻的两个Si原子间的距离为 nm
D.MgSi的密度计算式为g·cm-3
2
【解析】选D。一个硅原子周围距离最近且相等的镁原子有8个,硅原子的配位数为8,故A正确;紧邻
的两个镁原子的距离是晶胞参数的一半,该距离为 nm,故B正确;紧邻的两个硅原子间的距离是面对角
线的一半,该距离为 nm,故C正确;该晶胞含有4 mol Mg Si,总质量为4×76 g=
2
304 g,该晶体的密度为 g·cm-3,故D错误。
倒卖拉黑不更新,淘宝唯一免费更新店铺: 知二教育倒卖拉黑不更新,淘宝唯一免费更新店铺: 知二教育
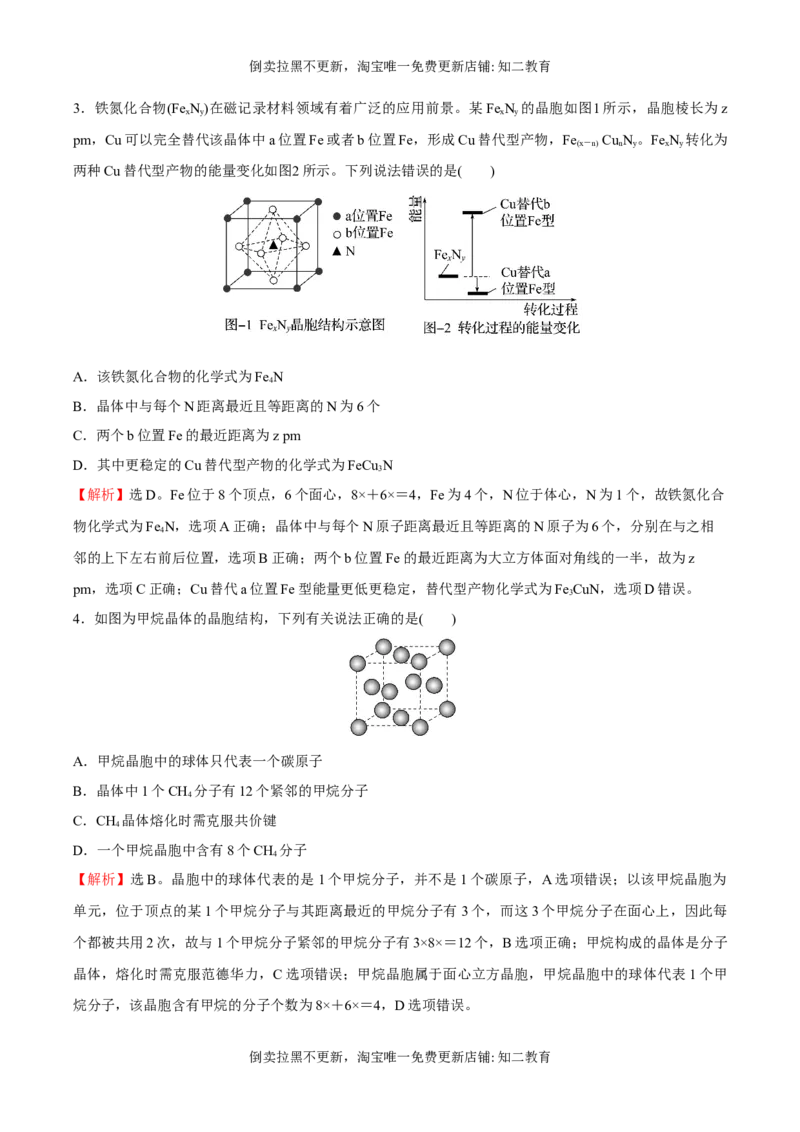
3.铁氮化合物(Fe N)在磁记录材料领域有着广泛的应用前景。某Fe N 的晶胞如图1所示,晶胞棱长为z
x y x y
pm,Cu可以完全替代该晶体中a位置Fe或者b位置Fe,形成Cu替代型产物,Fe Cu N 。Fe N 转化为
(x-n) n y x y
两种Cu替代型产物的能量变化如图2所示。下列说法错误的是( )
A.该铁氮化合物的化学式为Fe N
4
B.晶体中与每个N距离最近且等距离的N为6个
C.两个b位置Fe的最近距离为z pm
D.其中更稳定的Cu替代型产物的化学式为FeCu N
3
【解析】选D。Fe位于8个顶点,6个面心,8×+6×=4,Fe为4个,N位于体心,N为1个,故铁氮化合
物化学式为Fe N,选项A正确;晶体中与每个N原子距离最近且等距离的N原子为6个,分别在与之相
4
邻的上下左右前后位置,选项B正确;两个b位置Fe 的最近距离为大立方体面对角线的一半,故为z
pm,选项C正确;Cu替代a位置Fe型能量更低更稳定,替代型产物化学式为Fe CuN,选项D错误。
3
4.如图为甲烷晶体的晶胞结构,下列有关说法正确的是( )
A.甲烷晶胞中的球体只代表一个碳原子
B.晶体中1个CH 分子有12个紧邻的甲烷分子
4
C.CH 晶体熔化时需克服共价键
4
D.一个甲烷晶胞中含有8个CH 分子
4
【解析】选B。晶胞中的球体代表的是1个甲烷分子,并不是1个碳原子,A选项错误;以该甲烷晶胞为
单元,位于顶点的某1个甲烷分子与其距离最近的甲烷分子有3个,而这3个甲烷分子在面心上,因此每
个都被共用2次,故与1个甲烷分子紧邻的甲烷分子有3×8×=12个,B选项正确;甲烷构成的晶体是分子
晶体,熔化时需克服范德华力,C选项错误;甲烷晶胞属于面心立方晶胞,甲烷晶胞中的球体代表1个甲
烷分子,该晶胞含有甲烷的分子个数为8×+6×=4,D选项错误。
倒卖拉黑不更新,淘宝唯一免费更新店铺: 知二教育倒卖拉黑不更新,淘宝唯一免费更新店铺: 知二教育
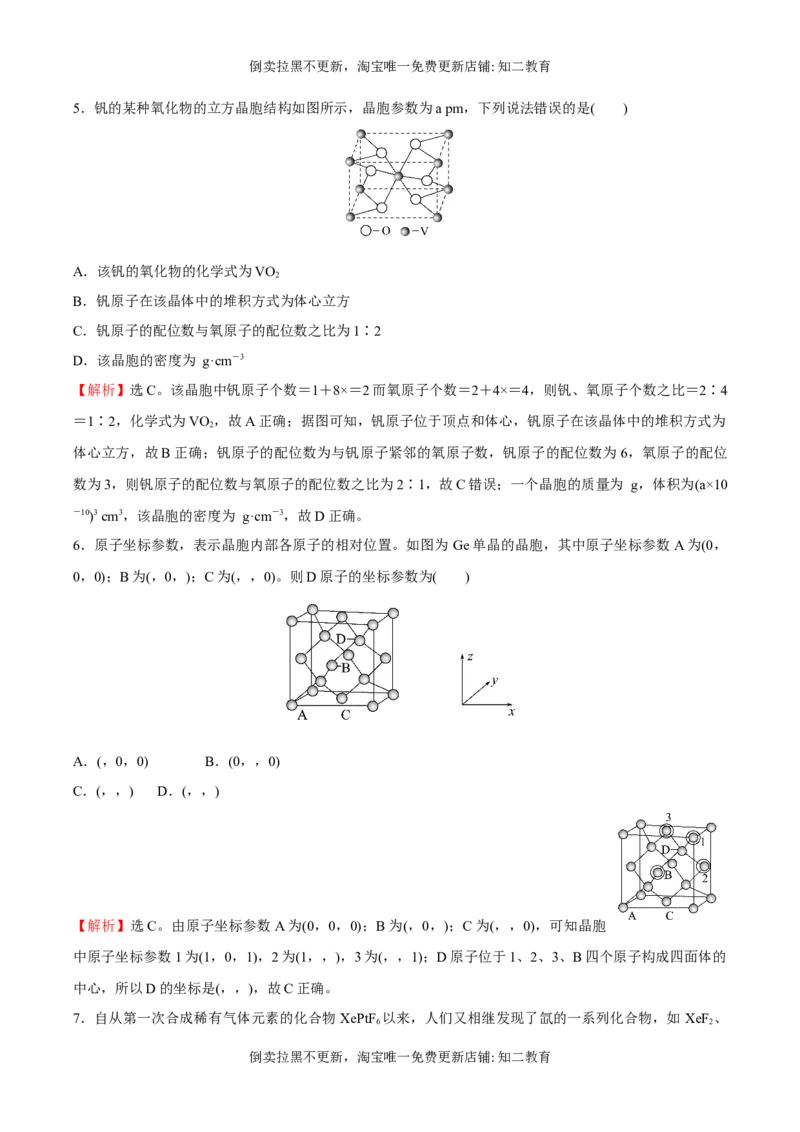
5.钒的某种氧化物的立方晶胞结构如图所示,晶胞参数为a pm,下列说法错误的是( )
A.该钒的氧化物的化学式为VO
2
B.钒原子在该晶体中的堆积方式为体心立方
C.钒原子的配位数与氧原子的配位数之比为1∶2
D.该晶胞的密度为 g·cm-3
【解析】选C。该晶胞中钒原子个数=1+8×=2而氧原子个数=2+4×=4,则钒、氧原子个数之比=2∶4
=1∶2,化学式为VO ,故A正确;据图可知,钒原子位于顶点和体心,钒原子在该晶体中的堆积方式为
2
体心立方,故B正确;钒原子的配位数为与钒原子紧邻的氧原子数,钒原子的配位数为6,氧原子的配位
数为3,则钒原子的配位数与氧原子的配位数之比为2∶1,故C错误;一个晶胞的质量为 g,体积为(a×10
-10)3 cm3,该晶胞的密度为 g·cm-3,故D正确。
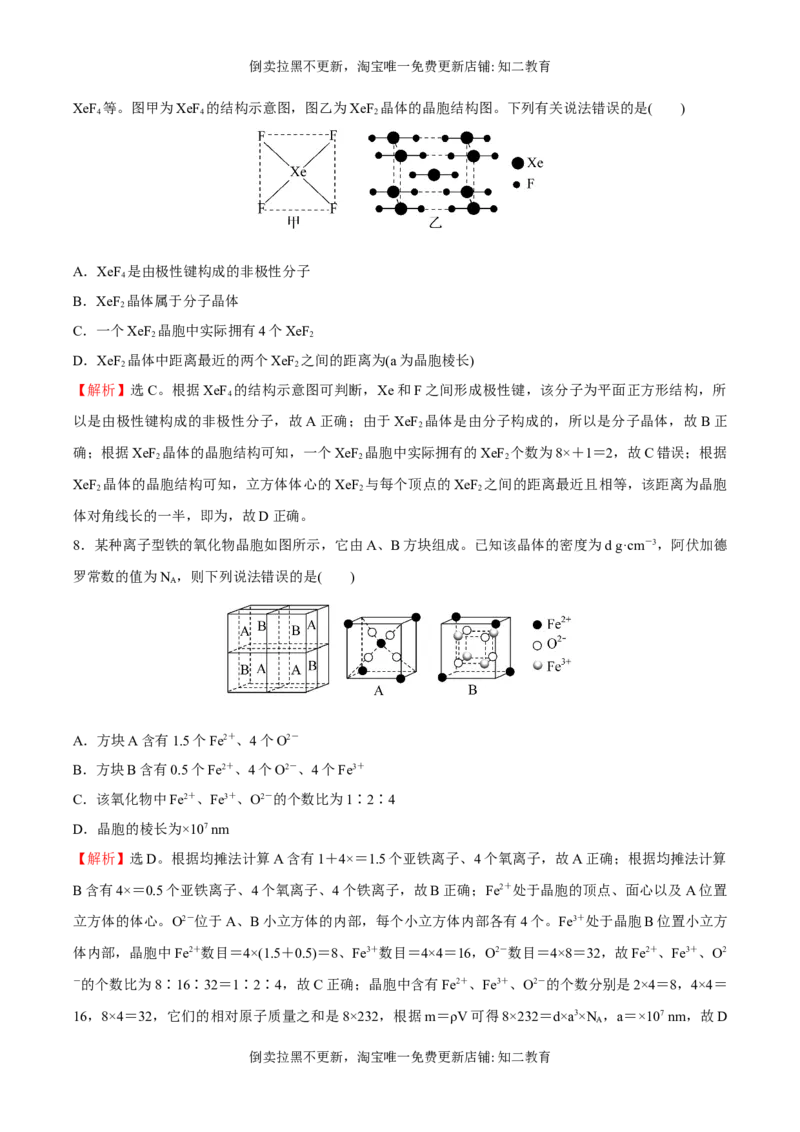
6.原子坐标参数,表示晶胞内部各原子的相对位置。如图为 Ge单晶的晶胞,其中原子坐标参数A为(0,
0,0);B为(,0,);C为(,,0)。则D原子的坐标参数为( )
A.(,0,0) B.(0,,0)
C.(,,) D.(,,)
【解析】选C。由原子坐标参数A为(0,0,0);B为(,0,);C为(,,0),可知晶胞
中原子坐标参数1为(1,0,1),2为(1,,),3为(,,1);D原子位于1、2、3、B四个原子构成四面体的
中心,所以D的坐标是(,,),故C正确。
7.自从第一次合成稀有气体元素的化合物XePtF 以来,人们又相继发现了氙的一系列化合物,如 XeF 、
6 2
倒卖拉黑不更新,淘宝唯一免费更新店铺: 知二教育倒卖拉黑不更新,淘宝唯一免费更新店铺: 知二教育
XeF 等。图甲为XeF 的结构示意图,图乙为XeF 晶体的晶胞结构图。下列有关说法错误的是( )
4 4 2
A.XeF 是由极性键构成的非极性分子
4
B.XeF 晶体属于分子晶体
2
C.一个XeF 晶胞中实际拥有4个XeF
2 2
D.XeF 晶体中距离最近的两个XeF 之间的距离为(a为晶胞棱长)
2 2
【解析】选C。根据XeF 的结构示意图可判断,Xe和F之间形成极性键,该分子为平面正方形结构,所
4
以是由极性键构成的非极性分子,故A正确;由于XeF 晶体是由分子构成的,所以是分子晶体,故B正
2
确;根据XeF 晶体的晶胞结构可知,一个XeF 晶胞中实际拥有的XeF 个数为8×+1=2,故C错误;根据
2 2 2
XeF 晶体的晶胞结构可知,立方体体心的XeF 与每个顶点的XeF 之间的距离最近且相等,该距离为晶胞
2 2 2
体对角线长的一半,即为,故D正确。
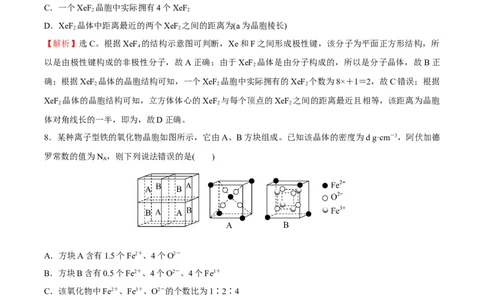
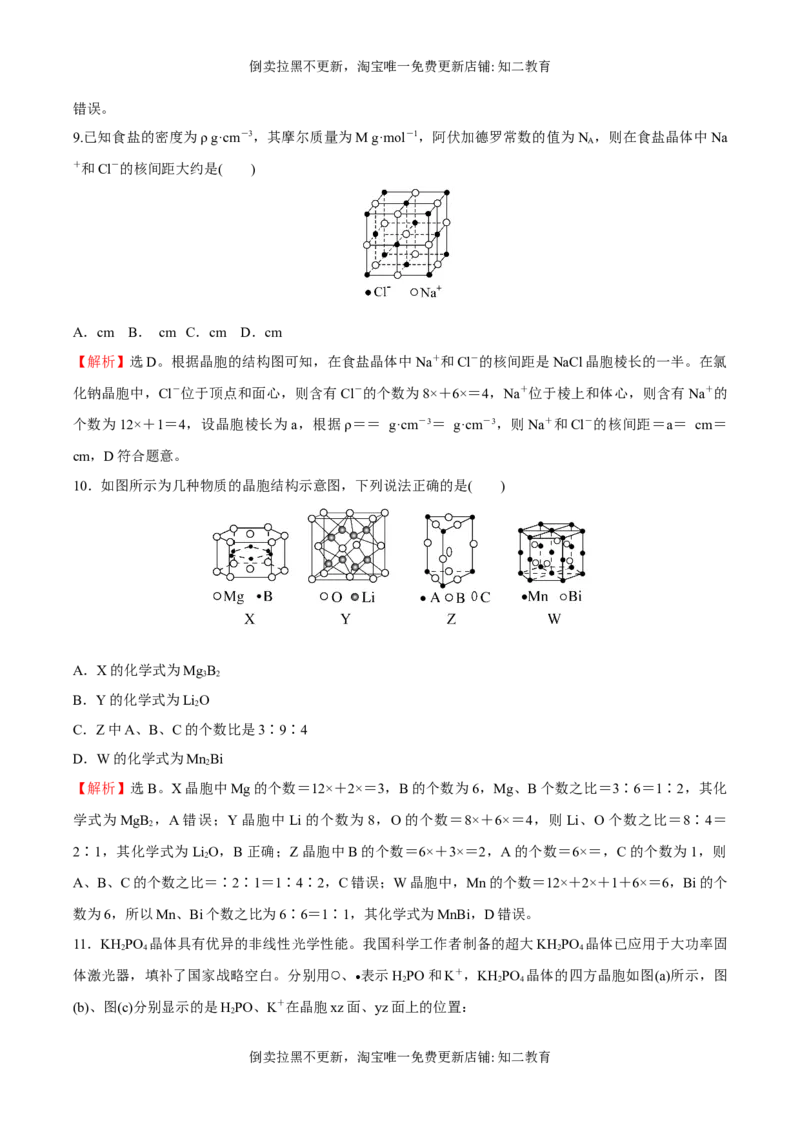
8.某种离子型铁的氧化物晶胞如图所示,它由A、B方块组成。已知该晶体的密度为d g·cm-3,阿伏加德
罗常数的值为N ,则下列说法错误的是( )
A
A.方块A含有1.5个Fe2+、4个O2-
B.方块B含有0.5个Fe2+、4个O2-、4个Fe3+
C.该氧化物中Fe2+、Fe3+、O2-的个数比为1∶2∶4
D.晶胞的棱长为×107 nm
【解析】选D。根据均摊法计算A含有1+4×=1.5个亚铁离子、4个氧离子,故A正确;根据均摊法计算
B含有4×=0.5个亚铁离子、4个氧离子、4个铁离子,故B正确;Fe2+处于晶胞的顶点、面心以及A位置
立方体的体心。O2-位于A、B小立方体的内部,每个小立方体内部各有4个。Fe3+处于晶胞B位置小立方
体内部,晶胞中Fe2+数目=4×(1.5+0.5)=8、Fe3+数目=4×4=16,O2-数目=4×8=32,故Fe2+、Fe3+、O2
-的个数比为8∶16∶32=1∶2∶4,故C正确;晶胞中含有Fe2+、Fe3+、O2-的个数分别是2×4=8,4×4=
16,8×4=32,它们的相对原子质量之和是8×232,根据m=ρV可得8×232=d×a3×N ,a=×107 nm,故D
A
倒卖拉黑不更新,淘宝唯一免费更新店铺: 知二教育倒卖拉黑不更新,淘宝唯一免费更新店铺: 知二教育
错误。
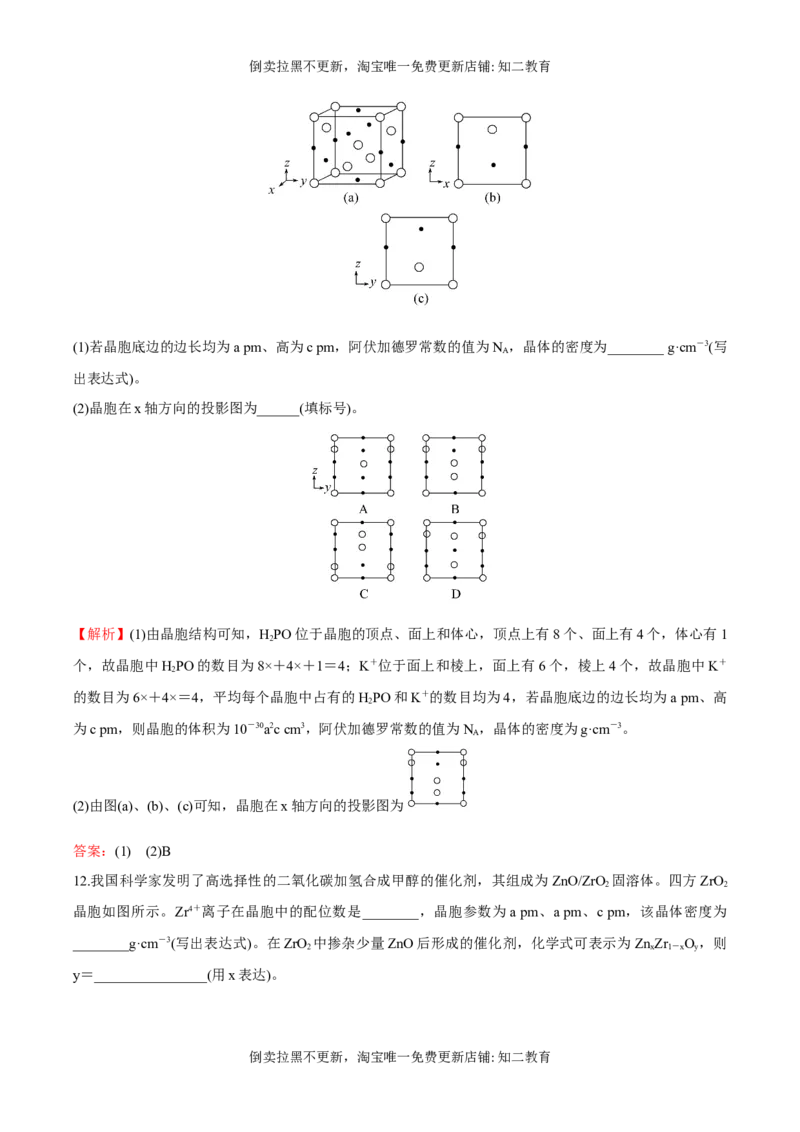
9.已知食盐的密度为ρ g·cm-3,其摩尔质量为M g·mol-1,阿伏加德罗常数的值为N ,则在食盐晶体中Na
A
+和Cl-的核间距大约是( )
A.cm B. cm C.cm D.cm
【解析】选D。根据晶胞的结构图可知,在食盐晶体中Na+和Cl-的核间距是NaCl晶胞棱长的一半。在氯
化钠晶胞中,Cl-位于顶点和面心,则含有Cl-的个数为8×+6×=4,Na+位于棱上和体心,则含有Na+的
个数为12×+1=4,设晶胞棱长为a,根据ρ== g·cm-3= g·cm-3,则Na+和Cl-的核间距=a= cm=
cm,D符合题意。
10.如图所示为几种物质的晶胞结构示意图,下列说法正确的是( )
A.X的化学式为MgB
3 2
B.Y的化学式为LiO
2
C.Z中A、B、C的个数比是3∶9∶4
D.W的化学式为MnBi
2
【解析】选B。X晶胞中Mg的个数=12×+2×=3,B的个数为6,Mg、B个数之比=3∶6=1∶2,其化
学式为MgB ,A错误;Y晶胞中Li的个数为8,O的个数=8×+6×=4,则Li、O个数之比=8∶4=
2
2∶1,其化学式为LiO,B正确;Z晶胞中B的个数=6×+3×=2,A的个数=6×=,C的个数为1,则
2
A、B、C的个数之比=∶2∶1=1∶4∶2,C错误;W晶胞中,Mn的个数=12×+2×+1+6×=6,Bi的个
数为6,所以Mn、Bi个数之比为6∶6=1∶1,其化学式为MnBi,D错误。
11.KH PO 晶体具有优异的非线性光学性能。我国科学工作者制备的超大KH PO 晶体已应用于大功率固
2 4 2 4
体激光器,填补了国家战略空白。分别用 、 表示HPO和K+,KH PO 晶体的四方晶胞如图(a)所示,图
2 2 4
(b)、图(c)分别显示的是HPO、K+在晶胞xz面、yz面上的位置:
2
倒卖拉黑不更新,淘宝唯一免费更新店铺: 知二教育倒卖拉黑不更新,淘宝唯一免费更新店铺: 知二教育
(1)若晶胞底边的边长均为a pm、高为c pm,阿伏加德罗常数的值为N ,晶体的密度为________ g·cm-3(写
A
出表达式)。
(2)晶胞在x轴方向的投影图为______(填标号)。
【解析】(1)由晶胞结构可知,HPO位于晶胞的顶点、面上和体心,顶点上有8个、面上有4个,体心有1
2
个,故晶胞中HPO的数目为8×+4×+1=4;K+位于面上和棱上,面上有6个,棱上4个,故晶胞中K+
2
的数目为6×+4×=4,平均每个晶胞中占有的HPO和K+的数目均为4,若晶胞底边的边长均为a pm、高
2
为c pm,则晶胞的体积为10-30a2c cm3,阿伏加德罗常数的值为N ,晶体的密度为g·cm-3。
A
(2)由图(a)、(b)、(c)可知,晶胞在x轴方向的投影图为
答案:(1) (2)B
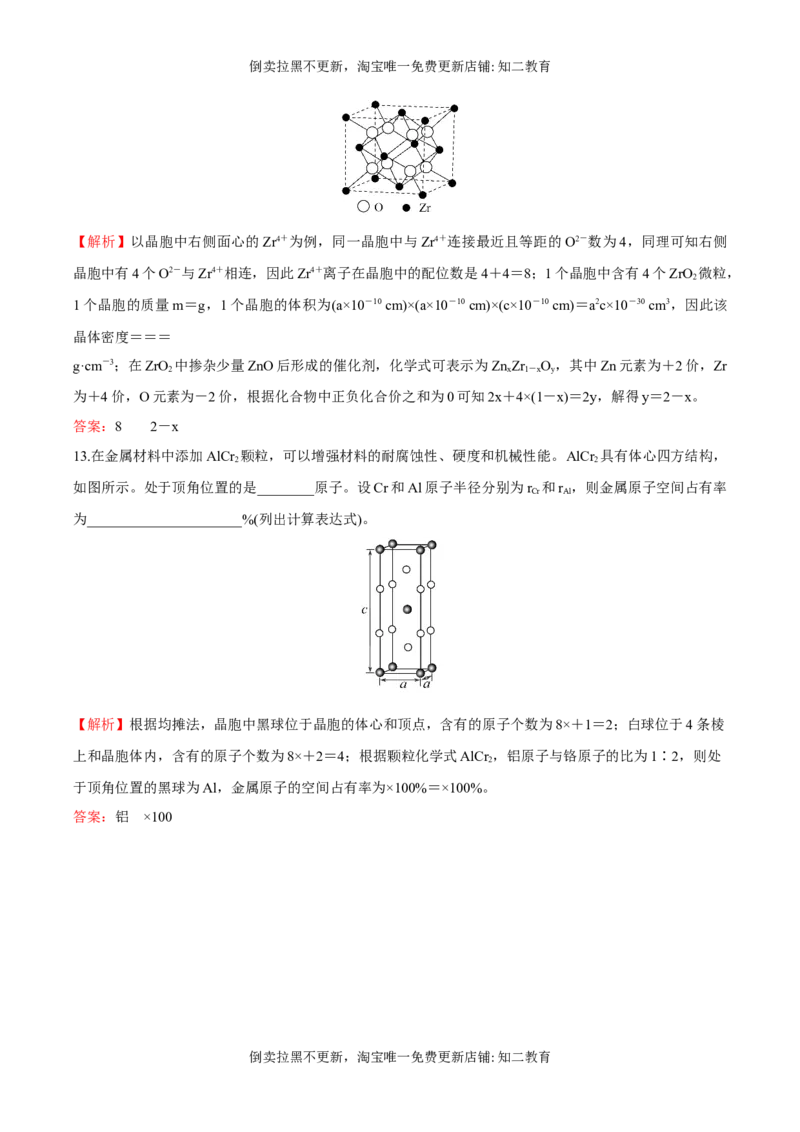
12.我国科学家发明了高选择性的二氧化碳加氢合成甲醇的催化剂,其组成为ZnO/ZrO 固溶体。四方ZrO
2 2
晶胞如图所示。Zr4+离子在晶胞中的配位数是________,晶胞参数为a pm、a pm、c pm,该晶体密度为
________g·cm-3(写出表达式)。在ZrO 中掺杂少量ZnO后形成的催化剂,化学式可表示为ZnZr O ,则
2 x 1-x y
y=________________(用x表达)。
倒卖拉黑不更新,淘宝唯一免费更新店铺: 知二教育倒卖拉黑不更新,淘宝唯一免费更新店铺: 知二教育
【解析】以晶胞中右侧面心的Zr4+为例,同一晶胞中与Zr4+连接最近且等距的O2-数为4,同理可知右侧
晶胞中有4个O2-与Zr4+相连,因此Zr4+离子在晶胞中的配位数是4+4=8;1个晶胞中含有4个ZrO 微粒,
2
1个晶胞的质量m=g,1个晶胞的体积为(a×10-10 cm)×(a×10-10 cm)×(c×10-10 cm)=a2c×10-30 cm3,因此该
晶体密度===
g·cm-3;在ZrO 中掺杂少量ZnO后形成的催化剂,化学式可表示为ZnZr O,其中Zn元素为+2价,Zr
2 x 1-x y
为+4价,O元素为-2价,根据化合物中正负化合价之和为0可知2x+4×(1-x)=2y,解得y=2-x。
答案:8 2-x
13.在金属材料中添加AlCr 颗粒,可以增强材料的耐腐蚀性、硬度和机械性能。AlCr 具有体心四方结构,
2 2
如图所示。处于顶角位置的是________原子。设Cr和Al原子半径分别为r 和r ,则金属原子空间占有率
Cr Al
为______________________%(列出计算表达式)。
【解析】根据均摊法,晶胞中黑球位于晶胞的体心和顶点,含有的原子个数为8×+1=2;白球位于4条棱
上和晶胞体内,含有的原子个数为8×+2=4;根据颗粒化学式AlCr ,铝原子与铬原子的比为1∶2,则处
2
于顶角位置的黑球为Al,金属原子的空间占有率为×100%=×100%。
答案:铝 ×100
倒卖拉黑不更新,淘宝唯一免费更新店铺: 知二教育倒卖拉黑不更新,淘宝唯一免费更新店铺: 知二教育
倒卖拉黑不更新,淘宝唯一免费更新店铺: 知二教育