文档内容
元素周期表
【学习目标】
1、知道元素周期表的发展历程,能说出元素周期表的编排原则及其结构
2、能根据原子序数确定元素在周期表中的位置
【主干知识梳理】
一、元素周期表的编排原则
1、元素周期表的发展历程
诞生⇒1869年,俄国化学家门捷列夫编制出第一张元素周期表
↓
依据⇒按照相对原子质量由小到大的顺序依次排列,将化学性质相似的元素放在同一纵行
↓
意义⇒揭示了化学元素间的内在联系,成为化学发展史上的重要里程碑之一
↓
发展⇒随着科学的发展,元素周期表中为未知元素留下的空位先后被填满
↓
现行⇒当原子的组成及结构的奥秘被发现后,编排依据由相对原子质量改为原子的核电荷数,形成现行的元
素周期表
2、元素周期表的编排原则
(1)横行原则:把电子层数目相同的元素,按原子序数递增的顺序从左到右排列
(2)纵行原则:把不同横行中最外层电子数相同的元素,按电子层数递增的顺序由上而下排列
(3)原子序数:按照元素在周期表中的顺序给元素编的序号
(4)原子序数与元素的原子结构之间的关系:原子序数=核电荷数=质子数=核外电子数
【即学即练1】
1、下列说法正确的是( )
A.我们常用的元素周期表中元素排序的依据是元素的相对原子质量
B.元素周期表中同一横行元素原子的电子层数相同
C.元素周期表有16个纵行
D.元素周期表已发展成一个稳定的形式,它不可能再有新的变化了
2、已知元素的原子序数,不可以推断元素原子的( )
A.质子数 B.核电荷数 C.核外电子数 D.离子所带的电荷数
二、元素周期表的结构——“七行十八列”、七周期十六族
1、周期
(1)含义:把电子层数相同的元素,按原子序数递增的顺序从左到右排列的一横行,叫做一个周期
(2)数目:元素周期表有7 个横行,每一横行称为一个周期,元素周期表共有7 个周期
(3)特点:周期序数=该周期元素原子的电子层数
(4)分类:
包括元 核外电 稀有气体原
类别 周期序数 起止元素 位置与结构的关系
素种数 子层数 子序数
一 H~He 2 1 2
短周期 二 Li~Ne 8 2 10
三 Na~Ar 8 3 18
四 K~Kr 18 4 36 周期序数=电子层数
五 Rb~Xe 18 5 54
长周期
六 Cs~Rn 32 6 86
七 Fr~118号 32 7 118
2、族
(1)含义:把最外层电子数相同的元素,按电子层数递增的顺序,从上至下排成的纵行,叫做一个族
(2)数目:元素周期表18个纵行中,除中间8、9、10三个纵行为一族外,其余每一纵行为一族,即:有16 个族(3)特点:主族元素的族序数=该主族元素原子的最外层电子数
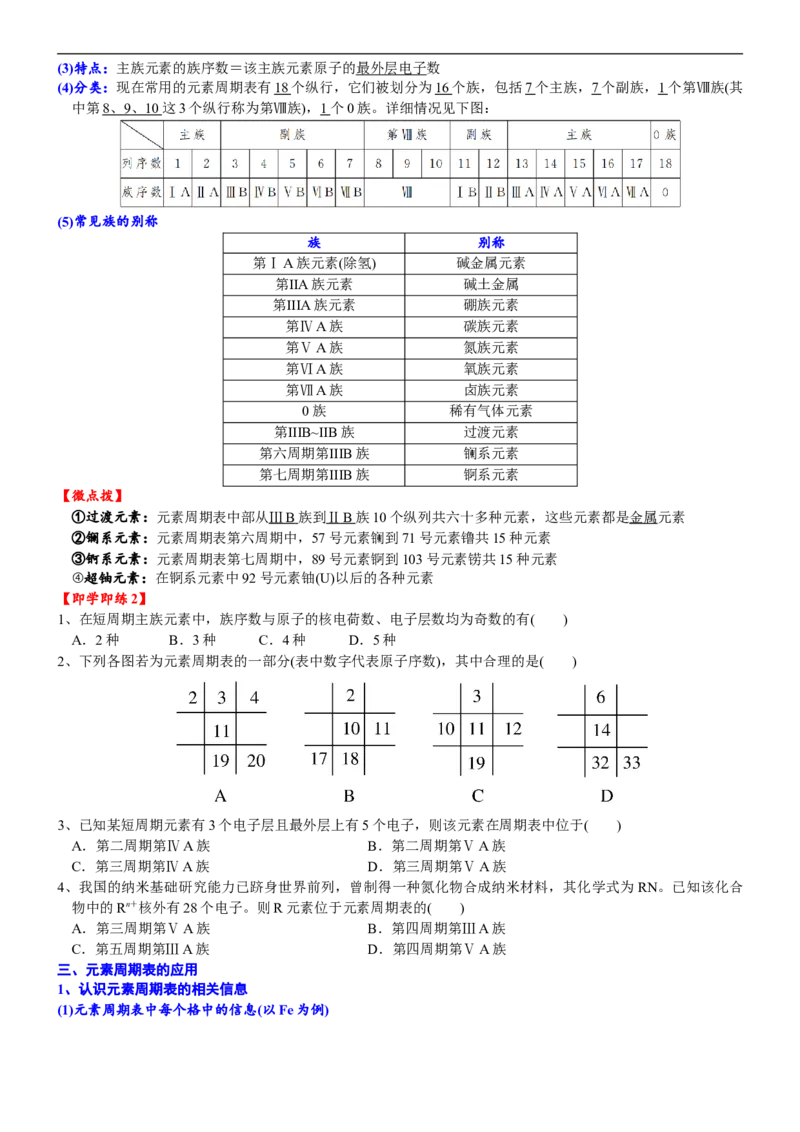
(4)分类:现在常用的元素周期表有18 个纵行,它们被划分为16 个族,包括7 个主族,7 个副族,1 个第Ⅷ族(其
中第 8 、 9 、 10 这3个纵行称为第Ⅷ族),1 个0族。详细情况见下图:
(5)常见族的别称
族 别称
第ⅠA族元素(除氢) 碱金属元素
第IIA族元素 碱土金属
第IIIA族元素 硼族元素
第ⅣA族 碳族元素
第ⅤA族 氮族元素
第ⅥA族 氧族元素
第ⅦA族 卤族元素
0族 稀有气体元素
第IIIB~IIB族 过渡元素
第六周期第IIIB族 镧系元素
第七周期第IIIB族 锕系元素
【微点拨】
①过渡元素:元素周期表中部从 Ⅲ B 族到 Ⅱ B 族10个纵列共六十多种元素,这些元素都是金属元素
②镧系元素:元素周期表第六周期中,57号元素镧到71号元素镥共15种元素
③锕系元素:元素周期表第七周期中,89号元素锕到103号元素铹共15种元素
④超铀元素:在锕系元素中92号元素铀(U)以后的各种元素
【即学即练2】
1、在短周期主族元素中,族序数与原子的核电荷数、电子层数均为奇数的有( )
A.2种 B.3种 C.4种 D.5种
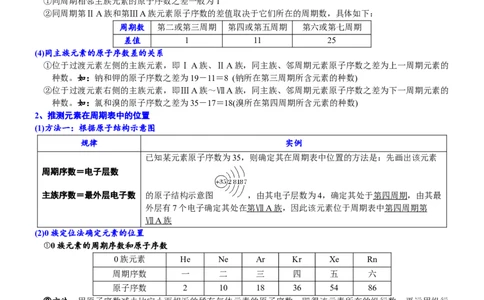
2、下列各图若为元素周期表的一部分(表中数字代表原子序数),其中合理的是( )
3、已知某短周期元素有3个电子层且最外层上有5个电子,则该元素在周期表中位于( )
A.第二周期第ⅣA族 B.第二周期第ⅤA族
C.第三周期第ⅣA族 D.第三周期第ⅤA族
4、我国的纳米基础研究能力已跻身世界前列,曾制得一种氮化物合成纳米材料,其化学式为 RN。已知该化合
物中的Rn+核外有28个电子。则R元素位于元素周期表的( )
A.第三周期第ⅤA族 B.第四周期第ⅢA族
C.第五周期第ⅢA族 D.第四周期第ⅤA族
三、元素周期表的应用
1、认识元素周期表的相关信息
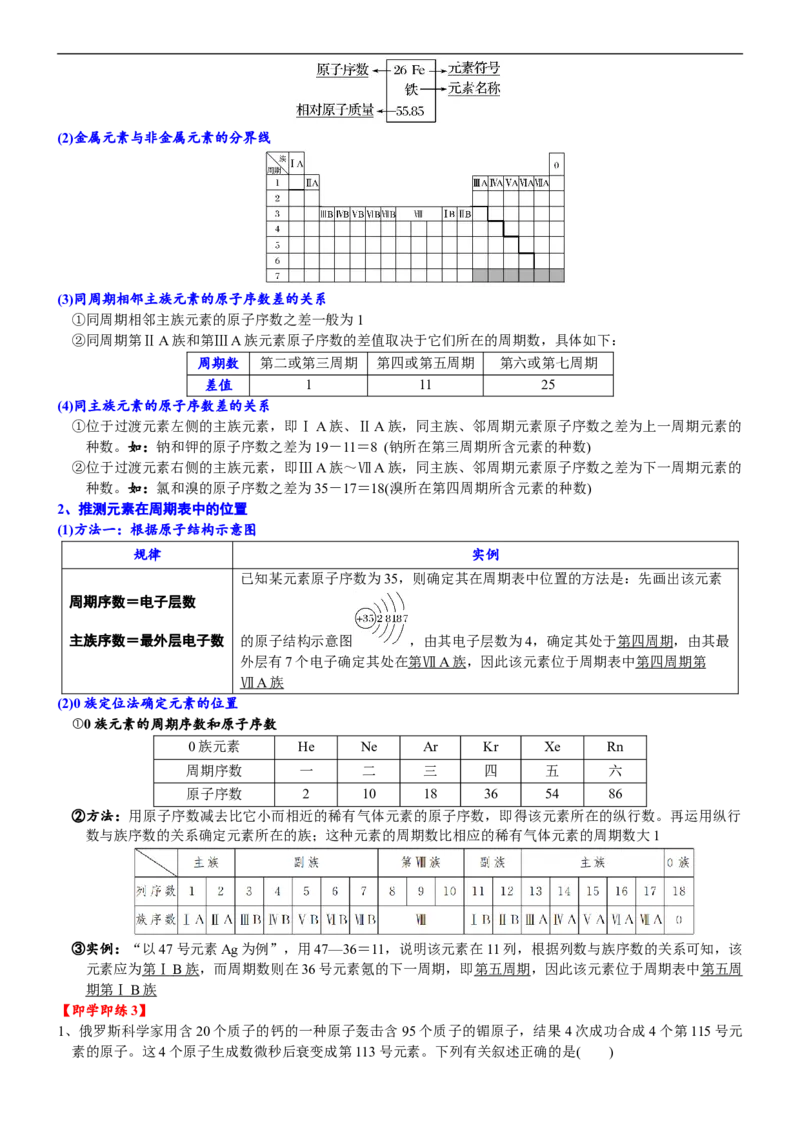
(1)元素周期表中每个格中的信息(以Fe为例)(2)金属元素与非金属元素的分界线
(3)同周期相邻主族元素的原子序数差的关系
①同周期相邻主族元素的原子序数之差一般为1
②同周期第ⅡA族和第ⅢA族元素原子序数的差值取决于它们所在的周期数,具体如下:
周期数 第二或第三周期 第四或第五周期 第六或第七周期
差值 1 11 25
(4)同主族元素的原子序数差的关系
①位于过渡元素左侧的主族元素,即ⅠA族、ⅡA族,同主族、邻周期元素原子序数之差为上一周期元素的
种数。如:钠和钾的原子序数之差为19-11=8 (钠所在第三周期所含元素的种数)
②位于过渡元素右侧的主族元素,即ⅢA族~ⅦA族,同主族、邻周期元素原子序数之差为下一周期元素的
种数。如:氯和溴的原子序数之差为35-17=18(溴所在第四周期所含元素的种数)
2、推测元素在周期表中的位置
(1)方法一:根据原子结构示意图
规律 实例
已知某元素原子序数为35,则确定其在周期表中位置的方法是:先画出该元素
周期序数=电子层数
主族序数=最外层电子数 的原子结构示意图 ,由其电子层数为4,确定其处于 第 四 周期 ,由其最
外层有7个电子确定其处在 第 Ⅶ A 族 ,因此该元素位于周期表中 第 四 周期第
Ⅶ A 族
(2)0族定位法确定元素的位置
①0族元素的周期序数和原子序数
0族元素 He Ne Ar Kr Xe Rn
周期序数 一 二 三 四 五 六
原子序数 2 10 18 36 54 86
②方法:用原子序数减去比它小而相近的稀有气体元素的原子序数,即得该元素所在的纵行数。再运用纵行
数与族序数的关系确定元素所在的族;这种元素的周期数比相应的稀有气体元素的周期数大1
③实例:“以47号元素Ag为例”,用47—36=11,说明该元素在11列,根据列数与族序数的关系可知,该
元素应为 第Ⅰ B 族 ,而周期数则在36号元素氪的下一周期,即第五周期,因此该元素位于周期表中 第 五 周
期第Ⅰ B 族
【即学即练3】
1、俄罗斯科学家用含20个质子的钙的一种原子轰击含95个质子的镅原子,结果4次成功合成4个第115号元
素的原子。这4个原子生成数微秒后衰变成第113号元素。下列有关叙述正确的是( )A.115号元素在第六周期 B.113号元素在第七周期ⅢA族
C.115号和113号元素都是非金属元素 D.镅元素和115号元素不在同一周期
2、下列说法正确的是( )
A.原子序数之差为2的两种元素不可能位于同一主族
B.D-核外有36个电子,则元素D位于第四周期第ⅦA族
C.位于同一主族相邻的甲、乙两种元素,甲的原子序数为x,则乙的原子序数可能为x+4
D.位于同一周期的甲、乙两种元素,甲位于第ⅠA族,原子序数为x,乙位于第ⅢA族,则乙原子序数可能
为x+19
3、原子序数为x的元素位于周期表中的ⅡA族,则原子序数为x+1的元素不可能处在( )
A.ⅢA族 B.ⅠA族 C.镧系 D.ⅢB族
4、两种短周期元素X和Y,可以组成化合物XY ,当Y的原子序数为m时,X的原子序数为( )
3
①m-4 ②m+4 ③m+8 ④m-2 ⑤m+6 ⑥m-12 ⑦m+14
A.①②④⑤ B.①②③⑤ C.①②③④⑤ D.①②③④⑤⑥⑦
5、核反应不仅能发电也能制造元素。2016年初国际上确认,利用原子核间的撞击已制造出原子序数分别为
113、115、117和118的四种新元素,填补了目前元素周期表的空白,其中113号元素与Al元素处于同一主
族。下列说法正确的是( )
A.核反应发电实现了化学能到电能的转化 B.115号元素一定是处于ⅤA族的非金属元素
C.117号元素与F、Cl、Br、I均处于ⅦA族 D.四种新元素位于元素周期表中的不同周期
四、常见的等电子微粒
1、常见的“10电子”粒子
(1)分子:Ne、HF、HO、NH 、CH
2 3 4
(2)阳离子:Na+、Mg2+、Al3+、NH、HO+
3
(3)阴离子:N3-、O2-、F-、OH-、NH
2、常见的“18电子”粒子
(1)分子:Ar、HCl、HS、PH 、SiH、F、HO、NH
2 3 4 2 2 2 2 4
(2)阳离子:K+、Ca2+
(3)阴离子:P3-、S2-、HS-、Cl-
【即学即练4】
1、A+、B+、C-、D、E五种粒子(分子或离子)中,每个粒子均有10个电子。已知:
①A++C-===D+E↑;②B++C-===2D。请回答:
(1)C-的电子式是________________
(2) 分 别 写 出 A + 和 D 反 应 、 B + 和 E 反 应 的 离 子 方 程 式 _______________________ 、
___________________________
(3)除D、E外,请再写出两种含10个电子的分子的分子式_________
(4)除A+、B+外,请再写出两种含10个电子的阳离子________
【课后作业】
1、1869年,俄国化学家门捷列夫制作出了第一张元素周期表,揭示了化学元素间的内在联系,成为化学史上
的重要里程碑之一。下列有关元素周期表的说法正确的是( )
A.元素周期表含元素最多的族是第ⅢB族 B.元素周期表有18个族
C.第ⅠA族的元素全部是金属元素 D.短周期是指第一、二、三、四周期2、下列关于元素周期表的说法正确的是( )
A.在元素周期表中,每一列就是一个族 B.主族元素都是短周期元素
C.副族元素都是金属元素 D.元素周期表每个长周期均包含32种元素
3、下列说法正确的是( )
A.常用元素周期表中元素排序的依据是原子的核电荷数
B.元素周期表有16个纵行,也就是16个族
C.原子的最外层电子数相同的元素,一定属于同一族
D.电子层数相同的粒子,对应元素一定属于同一周期
4、在现行元素周期表中,所含元素种数最多的族和周期分别是( )
A.第ⅠA族 第六周期 B.第Ⅷ族 第六周期
C.第ⅢB族 第六周期 D.第ⅢA族 第六周期
5、主族元素在周期表中的位置取决于该元素的( )
A.相对原子质量和核外电子数 B.电子层数和最外层电子数
C.相对原子质量和最外层电子数 D.电子层数和次外层电子数
6、若把周期表原先的主、副族号取消,由左到右按原顺序编为 18纵行。如碱金属为第1纵行,稀有气体为第
18纵行,按这个规定,下列说法不正确的是( )
A.计算机芯片的组成元素位于第14纵行 B.第10纵行元素全部是金属元素
C.第18纵行元素单质全部是气体 D.只有第2纵行元素的原子最外层有2个电子
7、几种粒子具有相同的核电荷数,则可说明( )
A.可能属于同一种元素 B.一定是同一种元素
C.一定有相同的原子序数 D.核外电子数一定相等
8、某短周期元素原子最外层只有2个电子,则该元素( )
A.一定是第ⅡA族元素 B.一定是金属元素
C.一定在化合物中呈+2价 D.可能是金属元素,也可能是非金属元素
9、据国外有关资料报道,在“独居石”(一种共生矿,化学成分为Ce、La、Nd等的磷酸盐)中,查明有尚未命
名的116、124、126号元素。试判断116号元素应位于周期表中的( )
A.第六周期ⅣA族 B.第七周期ⅥA族
C.第七周期ⅦA族 D.第八周期ⅥA族
10、下图各为元素周期表的一部分(数字为原子序数),其中X为35的是( )
11、A、B、C均为短周期元素,它们在周期表中的位置如图所示,已知 B、C两元素在周期表中族序数之和是
A元素族序数的2倍;B、C两元素的原子序数之和是A元素原子序数的4倍,则符合A、B、C的一组元素
是( )
A.Be、Na、Al B.B、Mg、Si C.O、P、Cl D.C、Al、P
12、原子序数为x的元素E在周期表中位于A、B、C、D四种元素中间(如图所示),则A、B、C、D四种元素
的原子序数之和不可能是(镧系、锕系、0族元素除外)( )
A.4x B.4x+6 C.4x+10 D.4x+1413、Ⅰ.已知A、B、C、D是中学化学中常见的四种不同微粒。它们之间存在如下图中转化关系:
如果A、B、C、D均是10电子的微粒,请写出:A的化学式________;D的化学式________
Ⅱ.用A+、B-、C2-、D、E、F和G分别表示含有18个电子的七种微粒(离子或分子),请回答:
(1)A元素是________,B元素是________,C元素是________(用元素符号表示)
(2)D是由两种元素组成的双原子分子,其分子式是________
(3)F是由两种元素组成的三原子分子,其分子式是________,将其通入足量的NaOH溶液,反应的离子方程式
为__________________________________
(4)G分子中含有4个原子,其分子式是________
14、A、B、C为短周期元素,在周期表中所处的位置如右图所示。A、C两元素的原子核外电子数之和等于B
原子的质子数。B原子核内质子数和中子数相等。
(1)写出A、B、C三种元素的名称________、________、________。
(2)B位于元素周期表中第________周期________族。
(3)C的原子结构示意图为________。
15、下表是元素周期表的一部分,针对表中的①~⑨9种元素,填写下列空白:
主族
ⅠA ⅡA ⅢA ⅣA ⅤA ⅥA ⅦA 0
周期
二 ① ② ③
三 ④ ⑤ ⑥ ⑦ ⑧
四 ⑨
(1)写出元素符号和名称:①________,②________,⑧________,⑨________
(2)写出下列反应的化学方程式:
⑦的单质跟④的氢氧化物溶液反应:_____________________
⑤的氧化物跟④的氢氧化物溶液反应:________________
⑥的单质在③的单质中燃烧:__________________
【元素周期表】答案
【即学即练1】
1、B
2、D。解析:根据原子序数=核电荷数=质子数=核外电子数,故选D。
【即学即练2】
1、D。解析:在短周期主族元素中,族序数与原子的核电荷数、电子层数均为奇数的有 H、Na、Al、P、Cl,
共5种。
2、D。解析:本题要求熟记周期表的结构,知道1~18号元素在周期表中的具体位置。解题时可根据稀有气体2号、10号元素应在周期表的最右端和3号元素在周期表的最左端排除A、B、C三项。
3、D。解析:短周期元素中电子层数即周期序数,最外层电子数即主族的族序数,因此,该元素位于元素周期
表中第三周期第ⅤA族。
4、B。解析:据氮化物的化学式为RN知,N为-3价,则R为+3价,所以R的原子序数为28+3=31;大于
31且最邻近的0族元素原子序数为36(氪:第四周期),31-36=-5,因此R元素也在第四周期,8-|-5|=3,
则R在第ⅢA族。
【即学即练3】
1、B。解析:95号元素镅、115号元素、113号元素,原子序数都大于86而小于118,所以都在第七周期;115
号元素比118号元素原子序数少3,应在第ⅤA族,113号元素在第ⅢA族;113号元素和115号元素都是金属
元素。
2、B。解析:氢和锂两种元素的原子序数之差为2,却同位于第ⅠA族,A错误;简单阴离子的核外电子与同
周期的稀有气体相同,D-核外有36个电子,即与第四周期的0族元素Kr处于同一周期,且D比Kr少一个电
子,即在第ⅦA族,B正确;甲、乙同主族,若甲的原子序数为x,则根据元素周期表结构可知乙的原子序数
可能为x+2或x+8或x+18或x+32,C错误;同一周期的第ⅠA族和第ⅢA族的元素的原子序数之差分为三
种情况:①第二、三周期为2;②第四、五周期为2+10;③第六、七周期为2+24,D错误。
3、B。解析:原子序数为x+1的元素应位于ⅡA族右侧相邻的族,在短周期中为ⅢA族,长周期中为ⅢB族,
镧系元素属于ⅢB族。
4、D。解析:两种短周期元素X和Y可组成化合物XY ,则X为ⅢA族元素时,Y为ⅤⅡA族元素;或X、Y
3
均为ⅥA族元素;还有可能为X在ⅤA族,Y为ⅤⅡA族或H;①若Y为Cl,X为Al,则X的原子序数为m
-4,故①正确;②若Y为F,X为Al,则X的原子序数为m+4,故②正确;③若Y为S,X为O,则X的原
子序数为m+8,故③正确;④若Y为Cl,X为P,则X的原子序数为m-2,故④正确;⑤若Y为H,X为
N,则X的原子序数为m+6,故⑤正确;⑥若Y为Cl,X为N,则X的原子序数为m-12,故⑥正确;⑦若Y
为H,X为P,则X的原子序数为m+14,故⑦正确;故答案为D。
5、C。解析:核反应发电是核能转化成电能,故A错误;115号元素是位于第七周期第ⅤA族的金属元素,故
B错误;117号元素是位于第七周期第ⅦA族的元素,故C正确;四种新元素都在第七周期,故D错误。
【即学即练4】
1、(1)NH+OH-=====HO+NH ↑
2 3
HO++OH-===2H O
3 2
(2)Ne、CH (合理即可)
4
(3)Na+、Mg2+(合理即可)
解析:先列出常见的10电子粒子,对照分析找出其转化关系。
①分子:Ne、HF、HO、NH 、CH
2 3 4
②阳离子:Na+、Mg2+、Al3+、NH、HO+
3
③阴离子:F-、O2-、OH-、N3-、NH。
其中发生题给模式的反应分别为NH+OH-=====NH ↑+HO,HO++OH-===2H O,故A+为NH,B+为
3 2 3 2
HO+,C-为OH-,D为HO,E为NH 。
3 2 3
【课后作业】
1、A。解析:第ⅢB族中包含锕系与镧系元素,共有32种元素,A正确;元素周期表中共有18个纵行,16个
族,B错误;第ⅠA族中H为非金属元素,C错误;短周期包括第一、二、三周期,D错误。
2、C。解析:A项,第8、9、10三列为第Ⅷ族;B项,主族元素由短周期元素和长周期元素共同组成;D项,
第四、五周期均有18种元素。
3、A。解析:元素周期表中有18个纵行,16个族,第Ⅷ族占3个纵行;Be和He的最外层电子数都是2,但不
属于同一族;Ne和Na+的电子层数都是2,但不属于同一周期。
4、C。解析:现行元素周期表中,第六、七周期ⅢB族分别为镧系和锕系元素,各有15种元素,由于第七周
期未排满(不涉及人工合成元素),故元素种类最多的分别为第ⅢB族和第六周期。
5、B 。解析:对主族元素而言,其电子层数就是该元素在元素周期表中的周期序数;其最外层上的电子数就是
该元素在周期表中的族序数;由该元素在周期表中的周期和族决定元素的位置。
6、D。解析:本题实际上考查了对元素周期表结构的掌握状况。芯片的组成元素为硅,位于第ⅣA族,为第14
纵行,A项正确;第10纵行为过渡金属元素,B项正确;第18纵行元素为稀有气体元素,单质全部为气体,C项正确;D项中除第2纵行元素的原子最外层有2个电子外,其他如He、部分过渡金属元素最外层也是2个电
子。
7、A。解析:粒子可能是分子、原子、离子,虽然具有相同的核电荷数,但不一定是同一种元素,如 CH 与
4
HO,B错误。核外电子数不一定相等,如Na与Na+、F与F-等,D错误。粒子种类未确定,则不能判定一定
2
是原子,故C不正确。
8、D。解析:元素原子最外层只有2个电子,若为主族元素则在周期表中处于第ⅡA族,为金属元素,在化合
物中呈+2价;若为He,则为0族元素。
9、B。解析:第七周期若排满,118号元素应为0族元素,则116号元素位于从0族开始向左数第三纵行,故应
为第七周期ⅥA族元素,故选B。
10、D。解析:依据“稀有气体定位法”先写出各周期中稀有气体原子序数:2、10、18、36、54、86;其次根
据第五周期有18种元素,即可确定元素X(35号)应为D中位置。
11、C。解析:解答本题首先确定三种元素在元素周期表中的相对位置,再根据元素周期表中结构的关系列式
求解。由于A、B、C为短周期元素,从A、B、C的图中位置看,A只能处在第二周期,而B、C处在第三周期。
设A的原子序数为x,则B的原子序数为x+8-1=x+7,C的原子序数为x+8+1=x+9,则x+7+x+9=
4x,x=8。所以,A、B、C的原子序数分别为8、15、17,对应的元素分别为O、P、Cl,代入族序数关系:5
+7=2×6成立。
12、B。解析:在A、B、C、D四种元素中,同周期的A、C两种元素的原子序数之和为2x,又因同主族各周
期相邻的两元素之间的原子序数相差8、18、32。所以四种元素中,同主族的B、D两种元素的原子序数之和可
能为2x、2x+10或2x+14。则四种元素的原子序数之和可能为4x、4x+10或4x+14,故只有B项不可能。
13、Ⅰ.NH HO
2
Ⅱ.(1)K Cl S (2)HCl (3)H S HS+2OH-===S2-+2HO (4)H O(或PH)
2 2 2 2 2 3
解析:Ⅰ.如果A、B、C、D均是10电子的微粒,结合10电子微粒的结构性质特征,可知A为NH,B为OH
-,C为NH ,D为HO。
3 2
Ⅱ.常见的18e-微粒有:
阳离子:K+、Ca2+;阴离子:P3-、S2-、HS-、Cl-;分子有Ar、HCl、HS、PH 、SiH 、F 、HO 、
2 3 4 2 2 2
NH、C H 等。结合题目所给条件,不难确定答案。
2 4 2 6
14、(1)氮 硫 氟 (2)三 ⅥA (3)
15、(1)①C碳 ②N氮 ⑧Ar氩 ⑨K钾
(2)Cl+2NaOH===NaCl+NaClO+HO
2 2
Al O+2NaOH===2NaAlO +HO S+O=====SO
2 3 2 2 2 2