文档内容
卤族元素的结构和性质
【学习目标】
1、知道卤族元素在周期表中的位置及其原子结构特点,能说出卤族元素性质的相似性和递变性
2、进一步掌握结构与性质的内在联系
【主干知识梳理】
一、卤族元素的原子结构特点
1、概念:在元素周期表中,与氯元素处于同一纵行——第VIIA族的元素氟(F)、氯(Cl)、溴(Br)、碘(I)、砹(At)
都能与Na、K、Ca、Mg等金属化合成盐,所以统称为卤素(成盐元素之意)
2、成员:氟(F)、氯(Cl)、溴(Br)、碘(I)、砹(At)
元素名称 氟(F) 氯(Cl) 溴(Br) 碘(I)
原子序数 9 17 35 53
原子结构示意图
最外层电子数 7 7 7 7
电子层数 2 3 4 5
原子半径 由小到大
3、原子结构的特点
(1)相似性:最外层电子数都是7,容易得到一个电子
(2)递变性:从F到I,核电荷数逐渐增大,电子层数逐渐增多,原子半径逐渐增大
【即学即练1】
1、已知某微粒的结构示意图为 ,则下列说法正确的是( )
A.该元素位于第三周期0族 B.该元素位于第四周期ⅠA族
C.该元素是非金属元素 D.该元素是金属元素
2、关于卤族元素,下列说法正确的是( )
A.所有卤族元素的微粒都易得电子 B.和F同一主族的元素都是非金属元素
C.化合物中卤族元素都显负价 D.卤族元素原子的原子半径从上到下逐渐减小
二、卤素单质的物理性质
卤素单质 颜色和状态 密度 熔点/℃ 沸点/℃
F 淡黄绿色气体 1.69 g·L-1(15 ℃) -219.6 -188.1
2
Cl 黄绿色气体 3.214 g·L-1(0 ℃) -101 -34.6
2
Br 深红棕色液体 3.119 g·cm-3(20 ℃) -7.2 58.78
2
I 紫黑色固体 4.93 g·cm-3 113.5 184.4
2
1、相似性:都有颜色,有毒,在水中溶解度不大,易溶于苯、汽油、四氯化碳、酒精等有机溶剂
2、递变性:从F 到I,颜色逐渐加深,熔、沸点逐渐升高,密度逐渐增大,在水中的溶解度逐渐减小
2 2
【微点拨】
①Cl、Br 、I 在水中的溶解能力比较小,但较易溶于有机溶有剂(汽油、苯、四氯化碳、酒精)中
2 2 2
水 CCl 汽油(苯)
4
Cl 黄绿色 黄绿色 黄绿色
2
Br 橙色 橙红色 橙红色
2
I 棕黄色 紫红色 紫红色
2
②溶液的颜色与溶液的浓稀有关,浓溶液颜色深,稀溶液颜色浅,如:饱和溴水为红棕色,而很稀的溴水则
为浅黄色
二、卤素单质的化学性质
1、卤素单质与H 反应
2
卤素单质 反应条件 化学方程式 产物稳定性
F 暗处 H+F===2HF 很稳定
2 2 2Cl 光照或点燃 H+Cl========2HCl 较稳定
2 2 2
Br 加热 H+Br =====2HBr 不如氯化氢稳定
2 2 2
I 不断加热 H+I 2HI 不稳定
2 2 2
①与H 反应的难易程度:越来越困难
2
②生成气态氢化物的稳定性:依次减弱
结论
③与H 反应所需要的条件:逐渐升高
2
④与H 反应剧烈程度:逐渐减弱
2
⑤卤素的非金属性强弱:F>Cl>B r > I)
2、卤素单质间的置换反应
实验操作 实验现象 化学方程式
静置后,液体分层,上层无色,
2NaBr+Cl===2NaCl+Br
下层橙红色 2 2
静置后,液体分层,上层无色,
2KI+Br ===2KBr+I
下层紫红色 2 2
静置后,液体分层,上层无色,
2KI+Cl===2KCl+I
下层紫红色 2 2
①卤素单质的氧化性由强到弱的顺序是Cl > B r > I
结论 2 2 2
②卤素离子的还原性由强到弱的顺序是 I - > Br - > Cl -
3、卤素单质与金属反应:F 和所有金属都能反应;Cl 和绝大多数金属反应;Br 和较活泼金属反应;I 只和活
2 2 2 2
泼金属反应
2Na+X=====2NaX (X=F、Cl、Br、I)
2
2Fe+3Cl=====2FeCl 2Fe+3Br =====2FeBr Fe+I===FeI (碘水生烟)
2 3 2 3 2 2
4、卤素单质与水反应:X+HO=== HX + HXO (X为Cl、Br、I)
2 2
2F+2HO===4HF+O
2 2 2
Cl +HO HCl+HClO
2 2
Br +HO HBr+HBrO
2 2
5、卤素单质与碱反应:2NaOH+X===NaX+NaXO+HO (X=Cl、Br、I)
2 2
Cl +2NaOH===NaCl+NaClO+HO
2 2
Br +2NaOH===NaBr+NaBrO+HO
2 2
I+2NaOH===NaI+NaIO+HO (也可生成NaI和NaIO )
2 2 3
6、卤素单质与Fe2+、SO 、Na SO 、Na S等还原性物质反应
2 2 3 2
(1)与Fe2+反应:2Fe2++Cl ===2Cl-+2Fe3+
2
2Fe2++Br ===2Br-+2Fe3+
2
I 不能与Fe2+反应 (但I-与Fe3可以反应:2Fe3++2I-===I +2Fe2+)
2 2
(2)与SO 、Na SO 反应: SO +X+2HO===2HX+H SO (X=Cl、Br、I)
2 2 3 2 2 2 2 4
SO+X+HO===SO+2X-+2H+ (X=Cl、Br、I)
2 2
(3)与Na S反应:X+S2-===2X-+S↓ (X=Cl、Br、I)
2 2
【即学即练2】
1、随着卤族元素原子序数递增,下列说法正确的是( )A.单质的熔、沸点逐渐降低 B.最高价氧化物对应水化物的酸性逐渐减弱(F除外)
C.单质的氧化性逐渐增强 D.气态氢化物的稳定性逐渐增强
2、下列对卤素的说法不符合递变规律的是( )
A.F、Cl、Br 、I 的氧化性逐渐减弱 B.HF、HCl、HBr、HI的热稳定性逐渐减弱
2 2 2 2
C.F-、Cl-、Br-、I-的还原性逐渐增强 D.卤素单质按F、Cl、Br 、I 的顺序颜色变浅,密度增大
2 2 2 2
3、下列关于卤素(用X表示)的叙述中,正确的是( )
A.卤素单质与水反应均可用X+HO===HXO+HX表示
2 2
B.HX的热稳定性随卤素核电荷数增加而增强
C.卤素单质的颜色F→I 随相对分子质量增大而加深
2 2
D.卤素单质越活泼,其熔点和沸点就越高
四、卤族元素性质的相似性和递变性
1、相似性
(1)单质均为双原子分子
(2)主要化合价为—1价,最高正价为+7价(氟无正价)
(3)具有强氧化性
2、递变性:随着原子序数的递增,原子半径逐渐增大,原子核对最外层电子的引力逐渐减小,卤素原子得电子
的能力逐渐减弱,非金属性逐渐减弱
(1)原子半径和离子半径逐渐增大:F<Cl<Br<I;F-<Cl-<Br-<I-
(2)单质的氧化性逐渐减弱:F>Cl>Br >I
2 2 2 2
(3)卤离子还原性逐渐增强:F-<Cl-<Br-<I-
(4)元素的非金属性逐渐减弱:F>Cl>Br>I
(5)与H 化合或水反应由易到难
2
(6)气态氢化物的稳定性逐渐减弱:HF>HCl>HBr>HI
(7)气态氢化物的还原性:HF<HCl<HBr<HI
(8)最高价氧化物的水化物的酸性逐渐减弱:HClO>HBrO >HIO ,HClO 是已知含氧酸中酸性最强的酸
4 4 4 4
(9)前面元素的单质能把后面的元素置换出来
(10)单质颜色变深,熔沸点升高,密度增大,溶解性减小
【即学即练3】
1、下列有关卤族元素的叙述不正确的是( )
A.卤素单质从F 到I,颜色加深,熔沸点升高
2 2
B.卤族元素从Cl到I,最高价氧化物对应水化物的酸性减弱
C.卤族元素从F到I,HX水溶液酸性增强
D.卤素单质氧化性F>Cl>Br >I ,因此排在前面的卤素单质可将排在后面的卤素从它的盐溶液中置换出来
2 2 2 2
2、砹是原子序数最大的卤族元素,根据卤素性质的递变规律,对砹及其化合物的叙述,正确的是 ( )
A.与H 化合能力:At >I B.砹在常温下为白色固体
2 2 2
C.砹原子的最外电子层上有7个电子 D.砹能从NaCl溶液中置换出氯单质
五、卤素及其化合物的特性
①无正价,无含氧酸,氧化性最强,F-的还原性最弱
氟 ②2F +2HO===4HF+O,与H 反应在暗处即爆炸
2 2 2 2
③HF是弱酸,能腐蚀玻璃,故应保存在铅制器皿或塑料瓶中;有毒
①Br 在常温下是唯一的一种液态非金属单质,红棕色,易挥发
2
溴 ②Br 易溶于有机溶剂
2
③盛溴的试剂瓶中加水,进行水封,保存液溴时不能用橡皮塞
①I 遇淀粉变蓝色
2
②I 加热时易升华
碘 2
③I 易溶于有机溶剂
2
④食用盐中加入KIO 可防治甲状腺肿大
3
六、卤素离子的检验1、AgNO 溶液——沉淀法
3
未知液 生成
2、置换——萃取法
未知液 有机层呈
3、氧化——淀粉法检验I-
未知液 蓝色溶液,表明含有I−
七、卤化氢
1、物理性质:卤化氢均为无色有刺激性气味的气体,易溶于水,易挥发与空气中水蒸气结合形成白雾
2、氢化物三大性质比较
①热稳定性:HF>HCl>HBr>HI
②酸性:HF(弱)<HCl<HBr<HI
③还原性:HF<HCl<HBr<HI
3、卤化氢的制备——难挥发酸制挥发性酸
①CaF +HSO (浓)=====CaSO+2HF↑ (萤石和浓硫酸在铅皿中)
2 2 4 4
②NaCl+HSO (浓)=====NaHSO +HCl↑ 2NaCl+HSO (浓)=====NaSO +2HCl↑
2 4 4 2 4 2 4
③NaBr+HPO (浓)=====NaHPO +HBr↑
3 4 2 4
④NaI+HPO (浓)=====NaHPO +HI↑
3 4 2 4
八、重要化合物
1、卤化银(AgX):只有AgF可溶,其余均难溶于水。AgX(除AgF)见光易分解成银和卤素单质。 AgBr和AgI
可做感光材料或变色镜。反应及现象为:2AgCl===2Ag+Cl ;2AgBr===2Ag+Br ;2AgI===2Ag+I 固体逐
2 2 2
渐变成黑色,这是单质银的小颗粒。AgX均具感光性,AgBr作感光材料,AgI作人工降雨材料
2、CaX :只有CaF (萤石)不溶于水,CaCl 具有吸湿性,常作干燥剂
2 2 2
3、NaX:只有NaF有毒可用作农药;纯净的食盐不潮解,粗盐中因混有等杂质,易潮解
4、碘酸钾:加碘盐的配料,受热时易分解
九、卤素互化物—— (n=1,3,5,7)其化学性质与卤素单质相似,具有强氧化性
1、概念:由两种卤素化合而成的物质
2、组成:有一个较重的卤素原子和奇数个较轻的卤素原子组成的,如:IBr(s)、ICl(s)、ICl (s)、BrF(l)、ClF (g)
3 3 3
3、化学性质:与卤素单质相似,具有强氧化性
(1)与金属的反应:2Mg+2IBr===MgI +MgBr 2BrF +4Zn===ZnBr +3ZnF
2 2 3 2 2
(2)与水的反应:ICl+HO===HCl+HIO(该反应不是氧化还原反应,各元素化合价不变)
2
十、拟(类)卤素:一些多原子分子与卤素单质性相似,其阴离子又与卤素阴离子性质相似,常称为拟卤素。如:
(CN) 、(SCN) 、(SeCN) 、(OCN) 等。请写出下列化学方程式:
2 2 2 2
(CN) +H O—— Fe+(SCN) ——
2 2 2
MnO +HSCN
2
【课后作业】
1、卤素按F、Cl、Br、I的顺序其非金属性逐渐减弱的原因是( )
A.原子核内质子数增多起主要作用 B.相对原子质量逐渐增大起主要作用
C.其单质的密度增大起主要作用 D.随着核电荷数增加电子层数增大起主要作用
2、下列说法正确的是( )
A.F、Cl、Br的最外层电子数都是7,次外层电子数都是8
B.从HF、HCl、HBr、HI酸性递增的事实,推出F、Cl、Br、I的非金属性递增规律
C.卤素按F、Cl、Br、I的顺序,其非金属性逐渐减弱的原因是随着核电荷数增加电子层数增大起主要作用
D.砹是原子序数最大的卤族元素,根据卤素性质的递变规律,砹易溶于水,难溶于CCl
4
3、关于卤素(用X表示)的下列叙述正确的是( )
A.卤素单质与水反应均可用X+HO===HXO+HX表示
2 2B.HX都极易溶于水,它们的热稳定性随核电荷数增加而增强
C.卤素单质的颜色从F→I 按相对分子质量增大而加深
2 2
D.X-的还原性依次为F-HCl>HBr>HI B.稳定性:HFBr >I >F D.密度:FS2->Br- B.原子的氧化性由强到弱的顺序是:Br>I>S
C.离子的还原性由强到弱的顺序是:Br->I->S2- D.元素的非金属性由强到弱的顺序是:Br>S>I
18、已知常温下KClO 与HCl(浓)反应放出氯气,现按下图进行卤素的性质实验。玻璃管内装有分别滴有不同溶
3
液的白色棉球,反应一段时间后,对图中指定部位颜色描述正确的是( )
① ② ③ ④
A 黄绿色 橙色 蓝色 白色
B 无色 橙色 紫色 白色
C 黄绿色 橙色 蓝色 无色
D 黄绿色 无色 紫色 白色
19、(CN) 、(OCN) 、(SCN) 等化合物的性质与卤素相似,称为“类卤素”。已知卤素和“类卤素”的氧化性由
2 2 2
强到弱的顺序如下:F、(OCN) 、Cl、Br 、(CN) 、(SCN) 、I、(SeCN) 。下列叙述正确的是( )
2 2 2 2 2 2 2 2
A.反应I+2SCN-===2I-+(SCN) 能自发进行
2 2
B.反应Cl+2CN-===2Cl-+(CN) 不能自发进行
2 2
C.氧化性:F-<OCN-<Br-<SCN-
D.类卤素在碱性溶液中会发生自身氧化还原反应
20、向NaBr和KI的混合溶液中,通入足量的Cl 后,将溶液蒸干并灼烧,最后得到的物质是( )
2
A.NaBr和KI B.NaBr和KCl C.NaCl和KCl D.NaCl、KCl和I
2
21、如图在盛有溴水的三支试管中分别加入少量的苯、四氯化碳和酒精,振荡后静置,出现下列现象,正确的
结论是(提示:苯是一种有机溶剂,不溶于水,密度比水小)( )
A.①加入的是CCl ,②加入的是苯,③加入的是酒精
4
B.①加入的是酒精,②加入的是CCl ,③加入的是苯
4
C.①加入的是苯,②加入的是CCl ,③加入的是酒精
4
D.①加入的是苯,②加入的是酒精,③加入的是CCl
4
22、某学生往一支试管里按一定次序分别加入下列几种物质:A.KI溶液 B.淀粉溶液 C.NaOH溶液
D.氯水,发现溶液颜色按下面次序变化:①无色→②棕黄色→③蓝色→④无色。依据溶液颜色的变化回答
下列问题:
(1)加入以上药品的顺序是___________________________________________________
(2)写出①→②的离子反应方程式:_____________________________________________
(3)写出③→④的化学反应方程式:______________________________________________________
23、氰(CN) 、硫氰(SCN) 的化学性质和卤素(X )类似,化学上称为拟卤素[如(SCN) +HO===HSCN+
2 2 2 2 2
HSCNO]。它们的阴离子还原性强弱顺序为Cl-At,所以At 不能从NaCl溶液中置换出Cl,D错误。
2 2 2 2
【课后作业】
1、D。解析:F、Cl、Br、I元素非金属性逐渐减弱的原因主要是由于核外电子层数增多,原子核对最外层电子
的吸引能力减弱所致。
2、C。解析:F的次外层电子数为2,Br的次外层电子数为18,A项错误;元素的非金属性强弱可以根据其最
高价氧化物对应水化物的酸性强弱比较,B项错误;由碘微溶于水,
易溶于四氯化碳,可推知,砹微溶于水,易溶于CCl ,D项错误。
43、C。解析:A项,F 与HO反应为2F +2HO===4HF+O ,不可用X +HO===HXO+HX表示;B项,HX
2 2 2 2 2 2 2
的热稳定性随核电荷数的增加而减弱;D项,F 性质极为活泼,遇盐溶液先和水反应,故不能将相对分子质量
2
大的卤素从它的盐溶液里置换出来。
4、C。解析:因为此X显-1价,所以X元素的气态氢化物的化学式为HX,但由于X的非金属性很弱,所以
HX在常温下很不稳定,A错误;X单质氧化性比碘弱,不可与KI发生置换反应,B错误;类比Br 、I 等,C
2 2
正确;类比AgCl、AgBr等,D错误。
5、B。解析:此题是一道信息题,题中给出了三点信息:①溴化碘(IBr)暗示Br呈-1价,I呈+1价;②IBr性
质与卤素相似;③IBr与水反应生成HIO和HBr。由②可知,IBr是一种强氧化剂。分析IBr中各元素的化合价,
确定碘为+1价,溴为-1价。再结合③,可知IBr与水的反应不是氧化还原反应,而是复分解反应。因此,
A、C、D正确,B不正确。
6、C。解析:卤素原子最外层有7个电子,而不是单质最外层有7个电子,A项错误;卤素原子从F到I,电子
层数依次增多,半径依次增大,原子核对最外层电子吸引能力依次减弱,原子得电子能力依次减弱,故 B项错
误,C项正确;单质与H 化合由易到难顺序为F>Cl>Br >I ,D项错误。
2 2 2 2 2
7、D。解析:A项应为HI>HBr>HCl>HF;B项应为HF>HCl>HBr>HI;C项应为F>Cl>Br >I 。
2 2 2 2
8、C。解析:F 、Cl 、Br 、I 氧化性依次减弱,其对应的阴离子F-、Cl-、Br-、I-的还原性依次增强,故①
2 2 2 2
叙述错误,⑤叙述正确;F 、Cl 、Br 、I 的颜色由淡黄绿色→黄绿色→深红棕色→紫黑色逐渐加深,②叙述正
2 2 2 2
确;HF、HCl、HBr、HI的稳定性逐渐减弱,③叙述错误;F 、Cl 、Br 、I 在通常情况下其状态变化为气→液
2 2 2 2
→固,则沸点逐渐升高,④叙述正确,C正确。
9、B。解析:碘化钾中加入氯水发生反应2KI+Cl===2KCl+I,加入CCl 后由于碘易溶于CCl ,CCl 层(下层)
2 2 4 4 4
呈现紫红色。
10、C。解析:单质碘可使淀粉变蓝,故加入物质中如含有单质碘或能与 KI反应生成单质碘的,均可使湿润的
淀粉-KI试纸变蓝。溴水和氯水中分别存在Br 、Cl,可与KI反应置换出碘单质;碘酒是碘的酒精溶液,碘以
2 2
I 分子形式溶解在酒精中;酸性高锰酸钾溶液具有强氧化性,可将I-氧化生成碘单质;氯化钾不与KI反应,没
2
有碘单质生成。
11、B。解析:凡能使KI中碘离子氧化为I 的气体均能使淀粉变蓝,如Br 蒸气、臭氧(O )等,碘蒸气当然也能
2 2 3
使该试纸中的淀粉变蓝;氟气与NaCl溶液相遇时,F 先与水反应生成HF和O ,不能置换出氯气,但题述的不
2 2
是水溶液而是熔融状态下的NaCl,可置换出氯气:F+2NaCl(熔融)===2NaF+Cl;碘受热易升华,而NH Cl分
2 2 4
解后得到的NH 和HCl会重新化合,故用加热的方法不能分离二者;用棕色瓶正确,但滴瓶有胶头,溴会严重
3
腐蚀橡胶,所以不能用胶头滴瓶,D不正确。
12、D。解析:由碱金属元素和卤族元素的递变性可知,同主族元素从上到下金属性递增,非金属性递减,最
高价氧化物对应的水化物碱性增强,金属活动性增强,非金属气态氢化化物稳定性减弱,A、B、C错误;同主
族随核电荷数增大,原子半径增大,D正确。
13、D。解析:稀有气体很不活泼,跟一般物质不反应,所以与稀有气体反应的物质应是非常活泼的。
14、A。解析:用于雕刻玻璃的只有氢氟酸;而见光能够分解的物质不仅为卤素的化合物,硝酸盐类物质及硝
酸见光也容易分解;C项说法本身错误(碘单质使淀粉变为蓝色);非极性分子在水中和汽油中的溶解度均不同。
15、B
16、C
17、B。解析:发生反应的离子方程式 Br +2I-===I +2Br-,I +S2-===S+2I-。氧化性(或非金属性)顺序
2 2 2
Br>I>S,还原性顺序S2->I->Br-。
18、A。解析:在锥形瓶中,KClO 与HCl(浓)反应产生Cl ,所以①处为黄绿色;Cl 在②处与Br-反应生成
3 2 2
Br ,所以②处为橙色;Cl(可能还有挥发的Br )在③处与I-反应生成I ,淀粉遇I 变蓝,所以③处为蓝色;
2 2 2 2 2
Cl(可能还有挥发的Br )全部被NaOH溶液吸收,所以④处是白色棉球的本色(析出的NaCl、NaClO固体均为白
2 2
色)。
19、D。解析:氧化性(SCN) 强于I ,故A错误;Cl 氧化性强于(CN) ,反应Cl +2CN-===2Cl-+(CN) 能自发
2 2 2 2 2 2
进行,B错;还原性:F-<OCN-<Br-<SCN-,C错;D显然正确;答案为D。
20、C。解析:NaBr、KI与足量的Cl 反应,得到NaCl、KCl、Br 、I ,蒸干灼烧时生成的Br 易挥发、I 易升
2 2 2 2 2
华,最后只有NaCl、KCl。
21、C。解析:苯和四氯化碳都能萃取溴,苯的密度比水小,在水的上层,而四氯化碳在水的下层,酒精与溴
水互溶,故不分层22、(1)A、D、B、C
(2)2I-+Cl ===I +2Cl-
2 2
(3)3I +6NaOH===5NaI+NaIO +3HO
2 3 2
23、(1)(CN) +2KOH===KCN+KCNO+HO
2 2
(2)2SCN-+(CN) ===(SCN) +2CN-
2 2
解析:(1)根据题给信息,拟卤素氰(CN) 的化学性质跟Cl 的性质相似,故可以按照Cl 与KOH溶液反应的化学
2 2 2
方程式进行类推。(2)由于还原性强弱为 Cl-Br >(CN) >(SCN) >I 。因此NaBr和KSCN的混合溶液中通入(CN) ,能发生反应(被氧化)的只有SCN-,
2 2 2 2 2 2
(CN) 不能氧化Br-。
2
24、H O Cl HBr HCl
2 2 2
解析:由已知条件,C是Cl ,A和C混合爆炸,A是H ;C、D混合瓶壁上出现橙色小液滴为Br ,则D是
2 2 2
HBr,E是HCl。
25、(1)1:4 (2)2:1 (3)7:6
解析:本题主要考查Cl-、Br-、I-的还原性强弱,通入Cl 时,Cl 先氧化还原性较强的I-,I-被氧化完后,再
2 2
氧化Br-。(1)设原Cl-、Br-、I-的物质的量为2 mol、3 mol、4 mol,当变为4 mol、3 mol、2 mol时,Br-没减
少,I-减少2 mol,消耗Cl 1 mol,故通入Cl 的物质的量是原溶液中I-物质的量的。
2 2
(2)当I-被氧化完时,消耗2 mol Cl ,生成4 mol Cl-,此时Cl-和Br-的物质的量之比为6:3,即2:1。
2
(3)当Br-和I-被全部氧化时,3 mol Br-消耗Cl 1.5 mol、4 mol I-消耗Cl 2 mol,则通入Cl 的物质的量与原Br
2 2 2
-的物质的量之比为3.5:3,即7:6。
26、(1)试管,量筒
(2)萃取剂,使生成的Br 、I 溶于其中,便于观察现象
2 2
(3)由无色逐渐变为橙红色
(4)不能证明溴的氧化性强于碘 再做一组实验④,步骤为:KI溶液+溴水+1 mL CCl ,振荡,静置,观
4
察CCl 层颜色
4
解析:利用非金属单质间的转换反应来比较单质的氧化性强弱。Cl 能置换出Br ,I ,Br 能置换出I ,则
2 2 2 2 2
说明氧化性Cl>Br >I 。
2 2 2
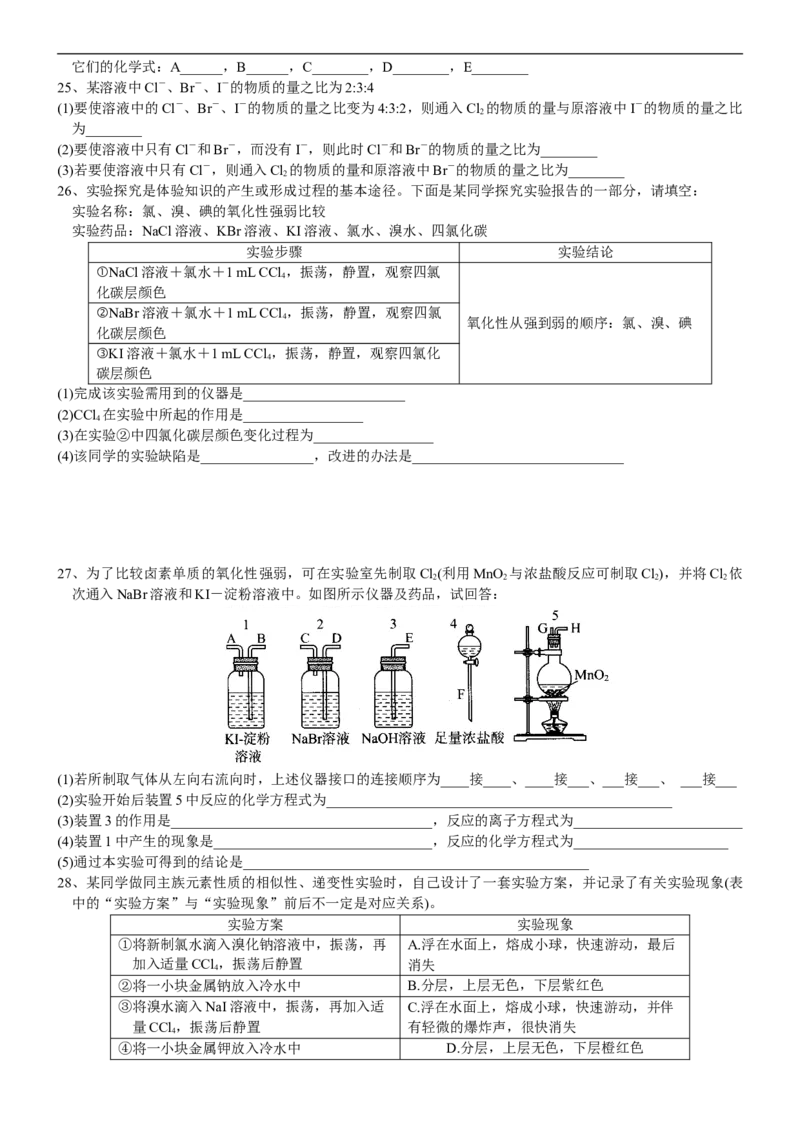
27、(1)F G H D C B A E
(2)MnO +4HCl(浓)=====MnCl +Cl ↑+2HO
2 2 2 2
(3)吸收未反应完的Cl ,以免污染空气
2
Cl +2OH-===Cl-+ClO-+HO
2 2
(4)溶液显蓝色 Cl +2KI===I +2KCl
2 2
(5)同主族元素随着核电荷数的增加,元素的非金属性和单质的氧化性逐渐减弱
28、(2)试管 胶头滴管
(3)
实验方案 实验现象 化学方程式
① D Cl +2NaBr===2NaCl+Br
2 2
② A 2Na+2HO===2NaOH+H↑
2 2
③ B Br +2NaI===2NaBr+I
2 2
④ C 2K+2HO===2KOH+H↑
2 2
(4)同主族元素性质相似;自上到下元素原子失去电子的能力增强,得到电子的能力减弱
解析:钾的金属性比钠强,钾与冷水反应比钠与冷水反应剧烈,产生的H 能发生燃烧或轻微的爆炸;将新制氯
2
水滴入NaBr溶液中,发生反应:Cl +2NaBr===Br +2NaCl,用CCl 萃取,液体分层下层呈橙红色。将溴水滴
2 2 4
入NaI溶液中发生反应:Br +2NaI===I +2NaBr,用CCl 萃取,液体分层,下层呈紫红色。
2 2 4