文档内容
碱金属元素的结构和性质
【学习目标】
1、知道碱金属元素的原子结构及特点,能说出碱金属元素化学性质的相似性及递变性
2、初步学会根据原子结构的特点,推测元素的化学性质
【主干知识梳理】
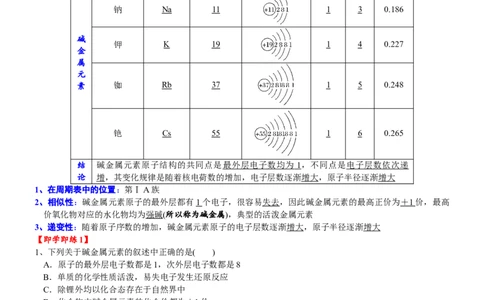
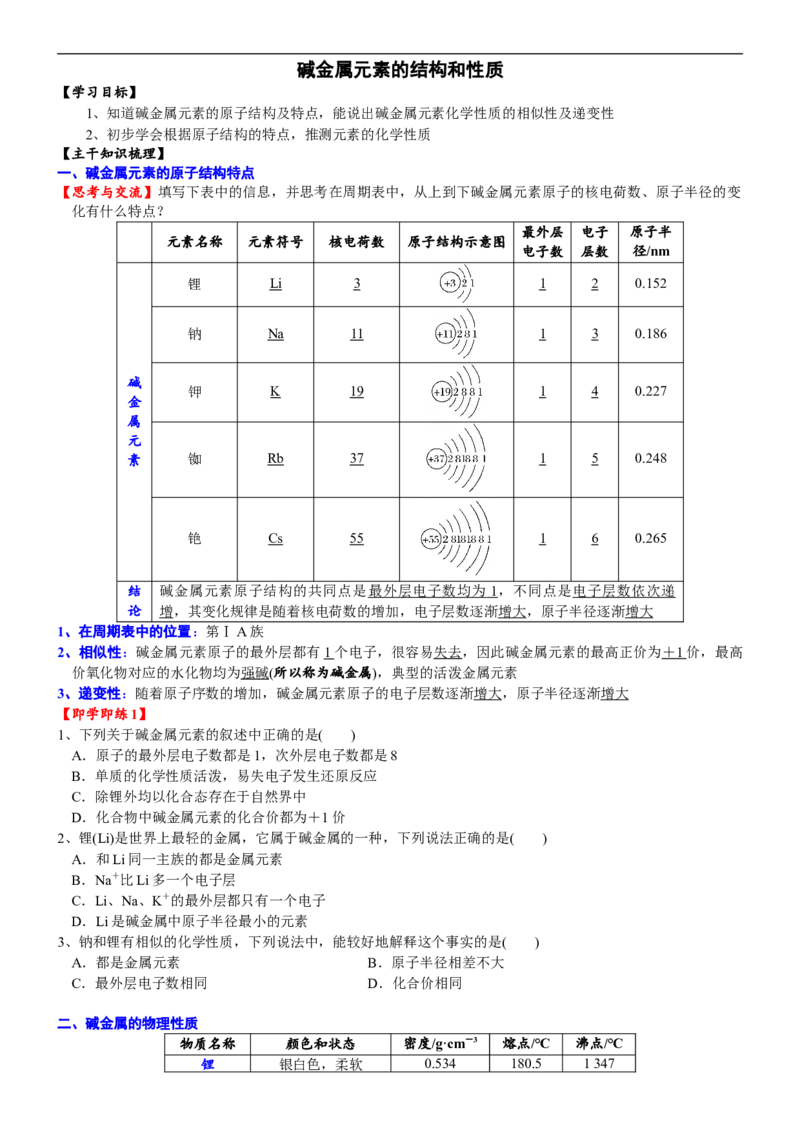
一、碱金属元素的原子结构特点
【思考与交流】填写下表中的信息,并思考在周期表中,从上到下碱金属元素原子的核电荷数、原子半径的变
化有什么特点?
最外层 电子 原子半
元素名称 元素符号 核电荷数 原子结构示意图
电子数 层数 径/nm
锂 Li 3 1 2 0.152
钠 Na 11 1 3 0.186
碱
钾 K 19 1 4 0.227
金
属
元
素 铷 Rb 37 1 5 0.248
铯 Cs 55 1 6 0.265
结 碱金属元素原子结构的共同点是 最外层电子数均为 1 ,不同点是电子层数依次递
论 增,其变化规律是随着核电荷数的增加,电子层数逐渐增大,原子半径逐渐增大
1、在周期表中的位置:第ⅠA族
2、相似性:碱金属元素原子的最外层都有1 个电子,很容易失去,因此碱金属元素的最高正价为 + 1 价,最高
价氧化物对应的水化物均为强碱(所以称为碱金属),典型的活泼金属元素
3、递变性:随着原子序数的增加,碱金属元素原子的电子层数逐渐增大,原子半径逐渐增大
【即学即练1】
1、下列关于碱金属元素的叙述中正确的是( )
A.原子的最外层电子数都是1,次外层电子数都是8
B.单质的化学性质活泼,易失电子发生还原反应
C.除锂外均以化合态存在于自然界中
D.化合物中碱金属元素的化合价都为+1价
2、锂(Li)是世界上最轻的金属,它属于碱金属的一种,下列说法正确的是( )
A.和Li同一主族的都是金属元素
B.Na+比Li多一个电子层
C.Li、Na、K+的最外层都只有一个电子
D.Li是碱金属中原子半径最小的元素
3、钠和锂有相似的化学性质,下列说法中,能较好地解释这个事实的是( )
A.都是金属元素 B.原子半径相差不大
C.最外层电子数相同 D.化合价相同
二、碱金属的物理性质
物质名称 颜色和状态 密度/g·cm-3 熔点/℃ 沸点/℃
锂 银白色,柔软 0.534 180.5 1 347钠 银白色,柔软 0.97 97.81 882.9
钾 银白色,柔软 0.86 63.65 774
铷 银白色,柔软 1.532 38.89 688
略带金色光泽,柔
铯 1.879 28.40 678.4
软
1、相似性:碱金属单质都有银白色的金属光泽(铯略带金色光泽)、硬度小、密度小、熔沸点较低,良好的导电、
导热性,有延展性,钠钾合金为液态,可做原子反应堆的导热剂
2、递变性:在碱金属内,随着元素原子核电荷数的增加,单质的熔点和沸点逐渐降低,密度呈增大趋势(但ρ
Na
>ρ ),且Li、Na、K的密度小于1;Rb、Cs的密度大于1
K
三、碱金属的化学性质——与钠相似
1、碱金属与O 反应
2
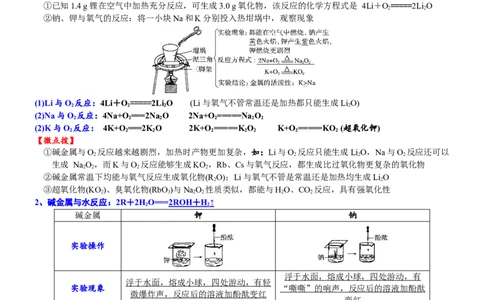
【思考与交流】
①已知1.4 g锂在空气中加热充分反应,可生成3.0 g氧化物,该反应的化学方程式是 4Li+O=====2LiO
2 2
②钠、钾与氧气的反应:将一小块Na和K分别投入热坩埚中,观察现象
(1)Li与O 反应:4Li+O=====2LiO (Li与氧气不管常温还是加热都只能生成LiO)
2 2 2 2
(2)Na与O 反应:4Na+O ===2Na O 2Na+O =====Na O
2 2 2 2 2 2
(2)K与O 反应: 4K+O ===2KO 2K+O =====KO K+O =====KO (超氧化钾)
2 2 2 2 2 2 2 2
【微点拨】
①碱金属与O 反应越来越剧烈,加热时产物更加复杂,如:Li与O 反应只能生成LiO,Na与O 反应还可以
2 2 2 2
生成 NaO,而K与O 反应能够生成KO ,Rb、Cs与氧气反应,都生成比过氧化物更复杂的氧化物
2 2 2 2
②碱金属常温下均能与氧气反应生成氧化物(R O);Li与氧气不管是常温还是加热均生成LiO
2 2
③超氧化物(KO )、臭氧化物(RbO)与NaO 性质类似,都能与HO、CO 反应,具有强氧化性
2 3 2 2 2 2
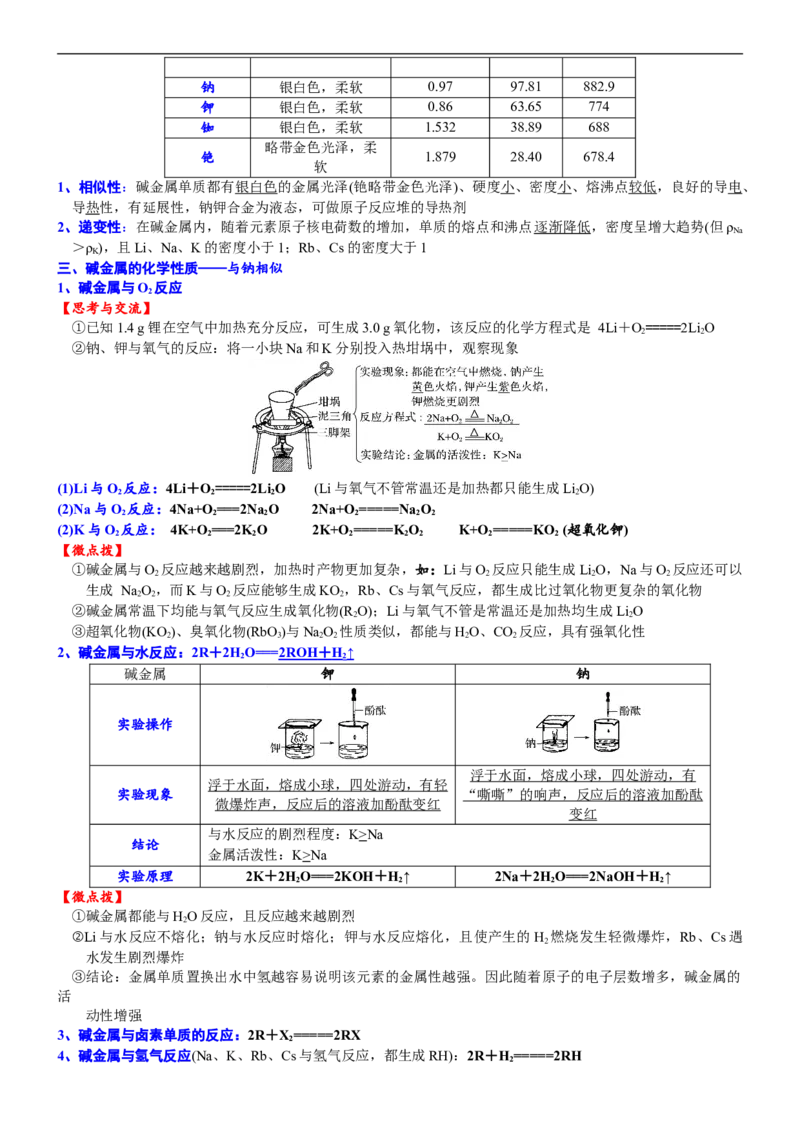
2、碱金属与水反应:2R+2HO=== 2ROH + H ↑
2 2
碱金属 钾 钠
实验操作
浮于水面,熔成小球,四处游动,有
浮于水面,熔成小球,四处游动,有轻
实验现象 “嘶嘶”的响声,反应后的溶液加酚酞
微爆炸声,反应后的溶液加酚酞变红
变红
与水反应的剧烈程度:K>Na
结论
金属活泼性:K>Na
实验原理 2K+2HO===2KOH+H↑ 2Na+2HO===2NaOH+H↑
2 2 2 2
【微点拨】
①碱金属都能与HO反应,且反应越来越剧烈
2
②Li与水反应不熔化;钠与水反应时熔化;钾与水反应熔化,且使产生的H 燃烧发生轻微爆炸,Rb、Cs遇
2
水发生剧烈爆炸
③结论:金属单质置换出水中氢越容易说明该元素的金属性越强。因此随着原子的电子层数增多,碱金属的
活
动性增强
3、碱金属与卤素单质的反应:2R+X=====2RX
2
4、碱金属与氢气反应(Na、K、Rb、Cs与氢气反应,都生成RH):2R+H=====2RH
25、碱金属与硫反应:2R+S=====RS
2
6、与常见盐溶液反应的离子方程式:碱金属与盐溶液反应,都是先与水反应,若符合复分解反应发生的条件,
则生成的氢氧化物继续同盐发生复分解反应。碱金属均不能在水溶液中置换另外的金属单质
7、碱金属的原子结构与化学性质的关系
(1)相似性:碱金属元素原子在结构上的相似性,决定了锂、钠、钾、铷、铯在性质上的相似性,碱金属原子都
容易失去最外层的一个电子,化学性质活泼,它们的单质都具有较强的还原性。具体表现在:
①碱金属都能与O、Cl(卤素单质)、S等非金属单质及水反应
2 2
②碱金属都能与水反应,反应的通式为2R+2HO=== 2ROH + H ↑ (R表示碱金属元素)
2 2
③碱金属都能与酸反应
(2)递变性:随着原子核外电子层数的增多,原子半径逐渐增大,原子核对最外层电子的引力逐渐减小,失去电
子的能力逐渐增强,单质的还原性增强,元素的金属性增强,最高价氧化物对应的水化物的碱性增强 (如:
CsOH>RbOH>KOH>NaOH>LiOH)
【即学即练2】
1、下列关于碱金属的叙述中,不正确的是( )
A.钾元素比钠元素的金属性强
B.钾和钠的焰色分别为紫色和黄色
C.碱金属都能和水发生反应,生成氢氧化物并放出氢气
D.碱金属的熔点随着电子层数的增加而升高
2、下列各组比较中不正确的是( )
A.锂与水反应不如钠与水反应剧烈
B.还原性:K>Na>Li,故K可以从NaCl溶液中置换出金属钠
C.熔、沸点:Li>Na>K
D.碱性:LiOH<NaOH<KOH
3、下列对碱金属性质的叙述中,正确的是( )
A.碱金属元素的单质具有强还原性,可置换出硫酸铜溶液中的铜单质
B.单质在空气中燃烧生成的都是过氧化物
C.碱金属单质与水反应生成碱和氢气
D.单质熔、沸点随着原子序数递增而升高
4、关于铯及其化合物的下列说法中不正确的是( )
A.氢氧化铯是一种强碱,比KOH的碱性强
B.铯与水或酸溶液反应剧烈,都生成氢气
C.Cs的还原性比Na强,故Na+的氧化性大于Cs+
D.Al的金属性大于Cs的金属性
5、随着碱金属元素原子序数的增大,下列递变规律正确的是( )
A.原子半径逐渐增大 B.碱性逐渐减弱
C.单质熔、沸点逐渐升高 D.单质的氧化性逐渐增强
四、碱金属中的一般和特殊之处
1、Na、K需保存于煤油中,但Li的密度比煤油小,所以Li必须保存在密度更小的石蜡油中或密封于石蜡
2、碱金属中,从Li→Cs,密度呈增大的趋势,但ρ(K)NaOH>KOH>RbOH B.金属性:Rb>K>Na>Li
C.和酸反应时Fe能失2e-,Na失e-,所以Fe的金属性强于Na D.Rb不易与水反应放出H
2
13、下列对碱金属的叙述,其中完全不正确的组合是( )
①K通常保存在煤油中,以隔绝与空气的接触
②碱金属常温下呈固态,取用时可直接用手拿
③碱金属中还原性最强的是钾
④碱金属阳离子,氧化性最强的是Li+
⑤碱金属的原子半径和离子半径都随核电荷数的增大而增大
⑥从Li到Cs,碱金属的密度越来越大,熔、沸点越来越高
A.②③⑥ B.②③④ C.④⑤⑥ D.①③⑤
14、已知锂及其化合物的许多性质与碱金属差异较大,却与镁相似。下面有关锂及其化合物性质的叙述错误的
是( )
A.LiCO 受热可以分解 B.少量锂保存在煤油中
2 3
C.在相同温度下,溶解度LiCO 小于LiHCO D.锂在过量氧气中燃烧,主要产物是LiO,不是LiO
2 3 3 2 2 2
15、钠、钾和铯都是碱金属,下列有关叙述中不正确的是( )
A.在一般的实验条件下做铯与水反应的实验是很危险的
B.三种金属中铯的金属活动性最强
C.由于钠钾合金比钠、钾有更强的还原性,故用钠钾合金作原子反应堆的导热剂
D.将钠钾合金与煤油混合,液体明显分为两层
16、关于Li原子结构和性质的判断如下:①与HO反应比Na剧烈;②它的原子半径比Na小;③它的氧化物暴
2
露在空气中易吸收CO ;④它的阳离子最外层电子数和钠离子的最外层电子数相同;⑤它是还原剂;⑥Li应
2
保存在煤油中,以隔绝空气;⑦Li在空气中燃烧生成LiO。其中错误的组合是( )
2 2
A.①④⑥⑦ B.①②③ C.③⑤⑥ D.①②⑦
17、以下各项叙述中错误的是( )
A.原子半径由小到大的顺序是Li25,则另一种碱金属的相对原子
r
质量应小于25,可能为Li或Na。
22、(1)
(2)干燥H,防止H 带走水蒸气,引起实验误差
2 2
(3)偏小 H 将带走部分水蒸气,使测得的H 质量偏大,计算出的相对原子质量则偏小
2 2
解析:在此装置中加入某碱金属后,碱金属与水反应产生 H ,H 的质量为原装置及碱金属的总质量与反
2 2
应后装置总质量的差,利用此差量即可求出碱金属元素的相对原子质量。设该碱金属为 R,相对原子质量为
Ar,则
2R+2HO===2ROH+H↑
2 2
2A 2
r
bg (a+b-c)g
A=
r
无水CaCl 有吸水作用,在此一定是干燥H ,防止H 带走水蒸气。若不用CaCl 干燥,H 将带走部分水
2 2 2 2 2
蒸气,使测得的H 质量即(a+b-c)偏大,则计算出的相对原子质量偏小。
2