文档内容
原子结构与核素
【学习目标】
1、知道核外电子能量高低与分层排布的关系
2、能够根据核外电子排布规律写出常见简单原子的原子结构示意图
3、知道元素、核素、质量数、同位素的含义
【主干知识梳理】
一、原子的表示方法、质量数及原子结构
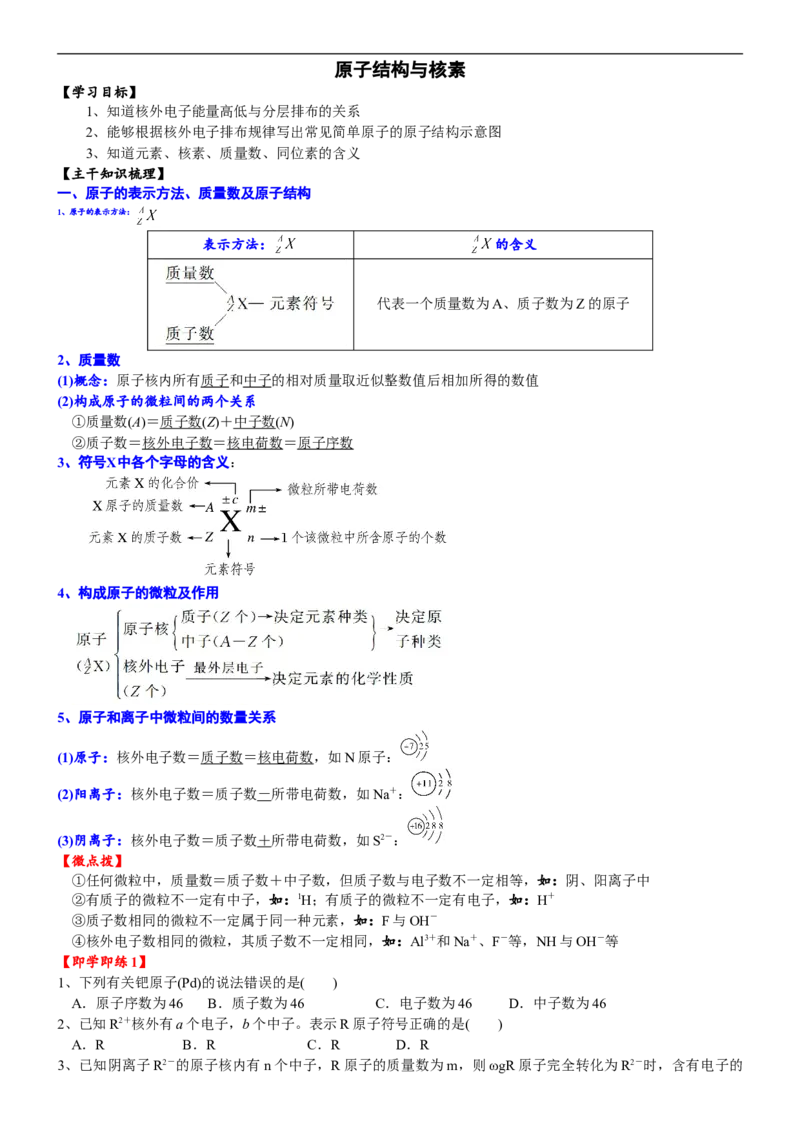
1、原子的表示方法:
表示方法: 的含义
代表一个质量数为A、质子数为Z的原子
2、质量数
(1)概念:原子核内所有质子和中子的相对质量取近似整数值后相加所得的数值
(2)构成原子的微粒间的两个关系
①质量数(A)=质子数(Z)+中子数(N)
②质子数=核外电子数=核电荷数=原子序数
3、符号X中各个字母的含义:
4、构成原子的微粒及作用
5、原子和离子中微粒间的数量关系
(1)原子:核外电子数=质子数=核电荷数,如N原子:
(2)阳离子:核外电子数=质子数-所带电荷数,如Na+:
(3)阴离子:核外电子数=质子数+所带电荷数,如S2-:
【微点拨】
①任何微粒中,质量数=质子数+中子数,但质子数与电子数不一定相等,如:阴、阳离子中
②有质子的微粒不一定有中子,如:1H;有质子的微粒不一定有电子,如:H+
③质子数相同的微粒不一定属于同一种元素,如:F与OH-
④核外电子数相同的微粒,其质子数不一定相同,如:Al3+和Na+、F-等,NH与OH-等
【即学即练1】
1、下列有关钯原子(Pd)的说法错误的是( )
A.原子序数为46 B.质子数为46 C.电子数为46 D.中子数为46
2、已知R2+核外有a个电子,b个中子。表示R原子符号正确的是( )
A.R B.R C.R D.R
3、已知阴离子R2-的原子核内有n个中子,R原子的质量数为m,则ωgR原子完全转化为R2-时,含有电子的物质的量是( )
A.mol B.mol C.ω() mol D.(m-n+2) mol
4、某元素的一种同位素X的原子质量数为A,含N个中子,它与1H原子组成H X分子,在agH X中所含质子
m m
的物质的量是( )
A.(A-N+m)mol B.(A-N)mol C.(A-N)mol D.(A-N+m)mol
二、原子核外电子的排布规律
1、电子的能量
(1)在多电子原子里,电子的能量不同
(2)在离核近的区域运动的电子的能量较低,在离核远的区域运动的电子的能量较高
2、电子层
(1)概念:在多电子原子里,把电子运动的能量不同的区域简化为不连续的壳层,称作电子层
(2)不同电子层的表示及能量关系
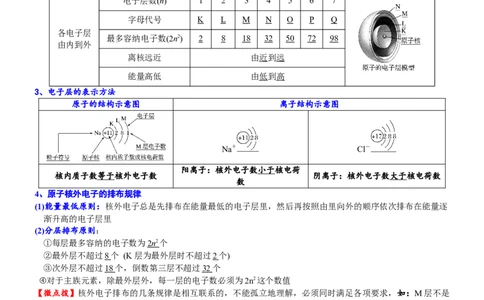
电子层数(n) 1 2 3 4 5 6 7
字母代号 K L M N O P Q
各电子层
最多容纳电子数(2n2) 2 8 18 32 50 72 98
由内到外
离核远近 由近到远
能量高低 由低到高
3、电子层的表示方法
原子的结构示意图 离子结构示意图
Na+ Cl-
阳离子:核外电子数小于核电荷
核内质子数等于核外电子数 阴离子:核外电子数大于核电荷数
数
4、原子核外电子的排布规律
(1)能量最低原则:核外电子总是先排布在能量最低的电子层里,然后再按照由里向外的顺序依次排布在能量逐
渐升高的电子层里
(2)分层排布原则:
①每层最多容纳的电子数为 2 n 2 个
②最外层不超过8 个 (K层为最外层时不超过2 个)
③次外层不超过18 个,倒数第三层不超过32 个
④对于主族元素,除最外层外,每一层的电子数必须为2n2这个数值
【微点拨】核外电子排布的几条规律是相互联系的,不能孤立地理解,必须同时满足各项要求,如:M层不是
最外层时,最多能容纳18个电子,当M层为最外层时,最多容纳8个电子
【即学即练2】
1、分别写出质子数为37、56、35、84、114的元素的原子结构示意
1、按要求填空 (前三周期元素,1~18号元素) (填元素符号)
(1)最外层电子数为1的元素有____________
(2)最外层电子数为2的元素有____________
(3)最外层电子数与次外层电子数相等的元素有____________
(4)最外层电子数是次外层电子数2倍的元素是_______________
(5)最外层电子数是次外层电子数3倍的元素是____________(6)次外层电子数是最外层电子数2倍的元素有____________
(7)内层电子总数是最外层电子数2倍的元素有____________
(8)电子层数与最外层电子数相等的元素有____________
(9)最外层电子数是电子层数2倍的元素有____________
(10)最外层电子数是电子层数3倍的元素有____________
3、下列叙述正确的是( )
A.电子的能量越低,运动区域离核越远 B.核外电子的分层排布即是核外电子的分层运动
C.稀有气体元素原子的最外层都排有8个电子 D.当M层是最外层时,最多可排布18个电子
4、在第n电子层中,当它作为原子的最外电子层时,最多容纳的电子数与(n-1)层相同,当它作为原子的次外
层时,其电子数比(n+1)层最多能多10个,则此电子层是( )
A.K层 B.L层 C.M层 D.N层
5、两种元素原子的核外电子层数之比与最外层电子数之比相等,则在周期表的前10号元素中,满足上述关系
的元素共有( )
A.1对 B.2对 C.3对 D.4对
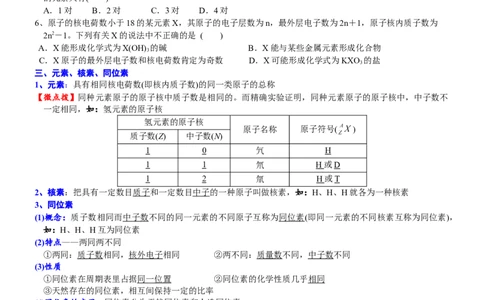
6、原子的核电荷数小于18的某元素X,其原子的电子层数为n,最外层电子数为2n+1,原子核内质子数为
2n2-1。下列有关X的说法中不正确的是 ( )
A.X能形成化学式为X(OH) 的碱 B.X能与某些金属元素形成化合物
3
C.X原子的最外层电子数和核电荷数肯定为奇数 D.X可能形成化学式为KXO 的盐
3
三、元素、核素、同位素
1、元素:具有相同核电荷数(即核内质子数)的同一类原子的总称
【微点拨】同种元素原子的原子核中质子数是相同的。而精确实验证明,同种元素原子的原子核中,中子数不
一定相同,如:氢元素的原子核
氢元素的原子核
原子名称 原子符号( )
质子数(Z) 中子数(N)
1 0 氕 H
1 1 氘 H 或D
1 2 氚 H 或T
2、核素:把具有一定数目质子和一定数目中子的一种原子叫做核素,如:H、H、H就各为一种核素
3、同位素
(1)概念:质子数相同而中子数不同的同一元素的不同原子互称为同位素(即同一元素的不同核素互称为同位素),
如:H、H、H互为同位素
(2)特点——两同两不同
①两同:质子数相同,核外电子相同 ②两不同:质量数不同,中子数不同
(3)性质
①同位素在周期表里占据同一位置 ②同位素的化学性质几乎相同
③天然存在的同位素,相互间保持一定的比率
(4)同位素的应用:同位素分为天然同位素和人造同位素
(1)核能:H 和H 是制造氢弹的原料,;U用于制造原子弹、核发电
(2)考古:根据C遗留数量的多少可以推断生物体的存在年代
(3)医疗:利用放射性同位素释放的射线治疗癌症和肿瘤等
4、元素、核素、同位素的判断方法
(1)判断元素、核素和同位素时,要抓住各种粒子的本质。质子数相同的原子就是同种元素;质子数和中子数均
相同的就是同种原子,也称为核素,同种元素的不同核素互称同位素
(2)分析原子表示符号的几组数字。X,只要Z相同,就是同种元素;Z和A均相同,是同种核素;Z相同,A不
相同的互称同位素;Z不相同的不论A是否相同,均不是同种元素,更不能称为同位素
5、元素、核素、同位素的区别与联系
元素 核素 同位素
质子数、中子数都一定 质子数相同、中子数不同的同一元
本质 质子数相同的一类原子
的原子 素的不同原子之间的相互称谓同类原子,存在游离
范畴 原子 原子
态、化合态两种形式
特性 只有种类,没有个数 化学反应中的最小微粒 化学性质几乎完全相同
决定因素 质子数 质子数、中子数 质子数、中子数
H、H、H、K、Ca属于
举例 O、O、O2-都属氧元素 U、U、U互为同位素
5种不同核素
联系
【即学即练3】
1、填空
(1)有5种单核粒子,它们分别是□、□、□+、□2+、□(“□”内元素符号未写出),则它们所属元素的种类有___
种
(2)1H、2H、3H三种微粒都属于________,因为它们是具有相同______________的同一类原子
(3)在H、H、H、C、C、C、N、N中,核素、元素的种数分别为______种、______种
(4)C、C、C的关系为__________,因为它们是具有___________________________________________的同一元
素的不同原子。其化学性质几乎完全相同
2、判断正误,正确的划“√”,错误的划“×”
(1)一种元素可以有多种核素,也可能只有一种核素,有多少种核素就有多少种原子( )
(2)不同的核素可能具有相同的质子数,可能具有相同的中子数,可能具有相同的质量数,也可能质子数、中子
数、质量数均不相同( )
(3)核聚变如H+H―→He+n,因为有新微粒生成,所以该变化是化学变化( )
3、有六种微粒,它们分别是M、N、X、Q+、Y2+、Z-,它们所属元素的种类为( )
A.3种 B.4种 C.5种 D.6种
4、下列说法错误的是( )
A.H、H、H+和H 是氢元素的四种不同粒子
2
B.Ca和Ca、石墨和金刚石均为同素异形体
C.H和H是不同的核素
D.12C和14C互为同位素,物理性质不同,但化学性质几乎完全相同
5、2015年12月31日,日本获得第113号元素的正式命名权。这种原子(记作Ja)是由30号元素Zn连续轰击83
号元素Bi获得的。下列说法不正确的是( )
A.获得新核素Ja的过程,发生的是化学变化 B.题中涉及的三种元素,都属于金属元素
C.这种超重核素Ja的中子数与质子数之差为52 D.这种新核素,是同主族元素中原子半径最大的
四、原子的相对原子质量与元素的相对原子质量
1、原子(或核素)的相对原子质量:以一个12C原子质量的作为标准,X原子的质量跟它相比所得的数值即为X
的相对原子质量,即:M(核素)=,取该值的正整数即为该核素的质量数
2、元素的相对原子质量:因天然元素往往不只一种原子,因而用上述方法定义元素的相对原子质量就不合适了。
元素的相对原子质量是该元素的各种核素的原子数百分比与其相对原子质量的乘积所得的平均值
如:A、B、C…为某元素的不同核素,其原子数百分比分别为a%、b%、c%…则该元素的相对原子质量为
M ·a%+M ·b%+M ·c%+…其中M 、M 、M …分别表示核素A、B、C…的相对原子质量
A B C A B C
3、元素的近似相对原子质量:若用同位素的质量数替代其相对原子量进行计算,其结果就是元素的近似相对原
子质量(计算结果通常取整数)。我们通常采用元素的近似相对原子质量进行计算
【即学即练4】
1、将某文献资料上记载的相对原子质量数据摘录如下:
35Cl 34.969 75.77% 35Cl 35 75.77%37Cl 36.966 24.23% 37Cl 37 24.23%
平均 35.453 平均 35.485
试回答下列问题:
(1) 34.969是表示 ; (2) 35.453是表示 ;
(3) 35是表示 ;(4) 35.485是表示 ;
(5) 24.23%是表示
【课后作业】
1、判断正误,正确的划“√”,错误的划“×”
(1)34S原子核内中子数为16( )
(2)2H+核外电子数为2( )
(3)1HO的摩尔质量为20g·mol-1( )
(4)13C和15N核内中子数相差1( )
(5)H O+和OH-中具有相同的质子数和电子数( )
3
(6)O和S2-具有相同的质子数和电子数( )
(7)多电子原子中,在离核较近的区域内运动的电子能量较高 ( )
(8)稀有气体元素的原子最外层都有8个电子( )
(9)M层为最外层时容纳的最多电子数不超过8个( )
(10)原子核外各电子层容纳的电子数为2n2个( )
(11)中子数=质量数-质子数( )
2、根据硅原子的结构示意图 可知,在硅原子的核外电子层中,电子没有出现的电子层为( )
A.K层 B.L层 C.M层 D.N层
3、下列是几种粒子的结构示意图,有关说法不正确的是( )
A.①和②属同种元素 B.②属于稀有气体元素
C.①和③的化学性质相似 D.④属于金属元素
4、某元素的原子核外有三个电子层,M层的电子数是L层电子数的,则该元素的原子是 ( )
A.Li B.Al C.Si D.K
5、1996年2月,德国某研究所在高能加速器中,将Zn撞入一个Pb的原子核并释放出一个中子后,合成一种人
造超重元素的原子,该元素原子内中子数为( )
A.278 B.277 C.166 D.165
6、根据元素周期表判断,下列叙述不正确的是( )
A.K层电子为奇数的所有元素所在族的序数与该元素原子的K层电子数相等
B.L层电子为偶数的所有主族元素所在族的序数与该元素原子L层电子数相等
C.L层电子为奇数的所有主族元素所在族的序数与该元素原子L层电子数相等
D.M层电子为奇数的所有主族元素所在族的序数与该元素原子M层电子数相等
7、下列关于原子核外电子排布规律的说法错误的是( )
A.K层是能量最低的电子层 B.原子失电子时先失去能量低的电子
C.核外电子总是优先排布在能量较低的电子层上 D.N层为次外层时,最多可容纳的电子数为18
8、下列说法正确的是( )
A.原子核外各层电子数相等的元素是非金属元素
B.原子最外层只有1个电子的元素一定是金属元素C.最外层电子数比次外层电子数多的元素一定位于第二周期
D.某元素的离子最外层电子数与次外层电子数相同,该元素一定位于第三周期
9、短周期元素中,A元素原子最外层电子数是次外层电子数的2倍;B元素原子最外层电子数是其内层电子总
数的3倍;C元素原子M层电子数等于其L层电子数的一半;D元素原子最外层有1个电子,D的阳离子与
B的阴离子电子层结构相同,则4种元素原子序数关系中正确的是( )
A.C>D>B>A B.D>B>A>C C.A>D>C>B D.B>A>C>D
10、I是常规核裂变产物之一,可以通过测定大气或水中I的含量变化来检测核电站是否发生放射性物质泄漏。
下列有关I的叙述中错误的是( )
A.I的化学性质与I相同 B.I的原子序数为53
C.I的原子核外电子数为78 D.I的原子核内中子数多于质子数
11、有 Xn+和 Ym-两种元素的简单离子,若它们的电子层结构相同,则下列关系正确的是( )
a b
A.b-a=n+m B.a-b=n-m C.核电荷数YX
12、某短周期元素的原子最外层电子数是次外层电子数的3倍,那么该原子( )
A.有3个电子层 B.有2个电子层 C.最外层电子数是8 D.核电荷数是10
13、某元素原子的最外层电子数是次外层的m倍(m为大于1的整数),则该原子的核外电子总数为( )
A.2m B.2m+10 C.2m+2 D.m+2
14、下面关于多电子原子的核外电子的运动规律的叙述正确的是( )
①核外电子是分层运动的 ②所有电子在同一区域里运动
③能量高的电子在离核近的区域内运动 ④ 能量低的电子在离核近的区域内运动
A.①④ B.②③ C.①③ D.②④
15、排布在下列各电子层上的一个电子,所具有的能量最低的是( )
A.K层 B.L层 C.M层 D.N层
16、下列关于原子结构的叙述中正确的是( )
A.所有的原子核都由质子和中子构成 B.原子的最外层电子数不超过8个
C.稀有气体原子的最外层电子数均为8个 D.原子的次外层电子数都是8个
17、下列关于核外电子排布的说法中不正确的是( )
A.第二电子层最多可容纳的电子数为8 B.次外层最多可容纳的电子数为18
C.最多可容纳2个电子的电子层一定是第一电子层 D.最多可容纳8个电子的电子层一定是第二电子层
18、下列叙述中,正确的是( )
A.核外电子排布完全相同的两种微粒,其化学性质一定相同
B.凡单原子形成的离子,一定具有稀有气体元素原子的核外电子排布
C.核外电子排布相同的两原子一定属于同种元素
D.阴离子的核外电子排布一定与上一周期稀有气体元素原子的核外电子排布相同
19、下列各组中两种微粒所含电子数不相等的是( )
A.HO+和OH- B.CO和N C.HNO 和NO D.CH和NH
3 2 2
20、与NH含有不同电子数的微粒是( )
A.Al3+ B.HO C.OH- D.CH
2 2 4
21、和Na+离子都具有相同电子数的一组微粒是( )
A.Na NH B.CO N C.CH HO D.Mg NH
2 4 2 2 4
22、同温同压下,等容积的两个密闭集气瓶中分别充满12C18O和14N 两种气体。关于这两个容器中气体的说法
2
正确的是( )
A.质子数相等,质量不等 B.分子数和质量都不相等
C.分子数、质量均相等 D.原子数、中子数和质量数均相等
23、在离子RO中,共有x个核外电子,R原子的质量数为A,则R原子核内含有的中子数目是( )
A.A-x+n+48 B.A-x+n+24 C.A-x-n-24 D.A+x-n-24
24、由H和O组成的11 g水中,含有的中子的物质的量为( )
A.4.5 mol B.5 mol C.5.5 mol D.6 mol25、某元素X,其原子的电子层数为(n-1),最外层电子数为(2n-1)。下列有关元素X的说法中正确的是( )
A.X可能是金属元素 B.由X形成的含氧酸均为强酸
C.X不能形成化学式为KXO 的含氧酸盐 D.元素X的气态氢化物一定极易溶于水
4
26、某微粒的结构示意图如图所示:
(1)x表示________,y表示________
(2)当y=7时,若该微粒为中性原子,则x =________
(3)当y=8时,若该微粒带有两个单位负电荷,则该微粒的表示符号为________;若该微粒带有一个单位正电荷,
则该微粒的表示符号为________
27、以下是四种粒子的结构示意图:
(1)上述粒子中其单质具有两性的元素是________(填字母序号),将其加入氢氧化钠溶液反应的离子方程式为:
______________________________________________
(2)C单质与水发生反应的离子方程式为___________
(3)电子层结构与C相同、化学性质最稳定的元素原子的核电荷数是________,用原子结构与元素性质的关系说
明它化学性质稳定的原因_____________________________________
(4)A的一种同位素可用于考古测定文物的年代,这种同位素的符号是_______,这种用途取决于它的________性
28、按要求填空
(1)某元素原子K层和M层电子数相同,该元素的元素符号是________
(2)某元素原子最外层电子数是次外层电子数的2倍,该元素的原子结构示意图是________
(3)某元素原子M电子层的电子数为K、L电子层电子数和的一半,该元素的元素名称是________
29、已知A、B、C三种元素的原子中,质子数为AD>B>A。
10、C。解析:核外电子数=质子数=53。
11、C。解析:因为两种离子的电子层结构相同,即其核外电子数相同,且阴离子的核电荷数(或质子数)小于阳
离子的核电荷数(或质子数)。由此可知:①a-n=b+m,a-b=m+n,A、B选项不正确;②a>b,C正确,D
不正确。
12、B。解析:第一层排满为2个电子,第二层排满为8个电子,第三层为最外层时,最多排8个电子,若该原
子有3个电子层,依题意可知最外层(第3层)要排到24个电子,这不可能,则该原子只有2个电子层,第一层
为2个电子,第二层为6个电子。
13、C。解析:按照原子核外电子排布的一般规律,最外层电子数不超过 8个,最外层电子数是次外层的m倍,
所以次外层电子数<8,即次外层只能为K层,电子数为2,最外层电子数是2m,该原子的核外电子总数为(2m+2)。
14、A。解析:原子核外电子是分层运动的,能量越低离核越近,能量越高离核越远。
15、A
16、B。解析:A项,H不含有中子;C项,He最外层电子为2个;D项,第二周期元素原子的次外层电子数为
2个。
17、D。解析:根据核外电子排布规律可知,第二电子层最多可容纳的电子数为8,A正确;次外层最多可容纳
的电子数为18,B正确;最多可容纳2个电子的电子层一定是第一电子层,即 K层,C正确;由于最外层电子
数不超过8,因此最多可容纳8个电子的电子层不一定是第二电子层,D错误。
18、C。解析:核外电子排布完全相同的两种微粒,化学性质不一定相同,如 K+和Cl-,A项错误;H+核外没
有电子,不具有稀有气体元素原子的核外电子排布,B项错误;阴离子的核外电子排布一般与同一周期稀有气
体元素原子的核外电子排布相同,D项错误。
19、D。解析:HO+和OH-均为10电子微粒,A项错误;CO和N 均为14电子微粒,B项错误;HNO 和NO
3 2 2
均为24电子微粒,C项错误;CH为8电子微粒,NH为10电子微粒,D项正确。
20、B。解析:Al3+中具有13个质子和10个电子,则与NH具有相同电子数,故A不符合题意;HO 中有18
2 2
个质子和18个电子,则与NH具有不相同电子数,故B符合题意;OH-中有9个质子和10个电子,则与NH具
有相同电子数,故C不符合题意;CH 中具有10个质子和10个电子,则与NH具有相同电子数,故D不符合
4
题意;综上所述,故选B。
21、C。解析:Na+离子核外电子总数为10。Na核外电子总数为11,NH核外电子总数为10,故A错误;CO
和N 核外电子总数为14,故B错误;CH 和HO核外电子总数为10,故C正确;Mg核外电子总数为12;NH
2 4 2 2 4
核外电子总数为18,故D错误;故选C。
22、A。解析:由阿伏加德罗定律可知两容器中所盛气体的分子数相等;因 12C18O中原子质量数之和为30,故
其摩尔质量为30 g/mol,而14N 中原子质量数之和为28,故其摩尔质量为28 g/mol,故两容器气体的质量不相
2
等;一个12C18O分子中质子数为14,中子数为(12-6)+(18-8)=16,而一个14N 分子中质子数为7×2=14,中
2
子数为(14-7)×2=14,故两容器气体的中子数不同,质子数相同;故A项正确。
23、B。解析:在离子RO中,共有x个核外电子,则R原子的核外电子数为x-n-24,则R原子核内质子数为
x-n-24,则R原子核内含有的中子数目是A-x+n+24。
24、D。解析:由H和O组成的水相对分子质量为22,1 mol 2HO含12 mol中子,故11 g水中含有中子的物质
的量为×12=6 mol。
25、D。解析:由X原子的最外层电子数为(2n-1)可以推知n≤4,则X的电子层数≤3,X为短周期元素。当n
=4时,X为Cl元素;当n=3时,X为N元素;当n=2时,不符合题意。HNO 和HClO均为弱酸,B项错误;
2
Cl元素能形成KClO,C错误;NH 和HCl均极易溶于水,D正确。
4 3
26、(1)质子数 最外层电子数
(2)17 (3)S2- K+
解析:(1)x表示质子数(或核电荷数),y表示最外层电子数;(2)当y=7时,该微粒为中性原子,则质子数=核
外电子数=2+8+7=17;(3)当y=8时,若该微粒带有两个单位的负电荷,质子数=核外电子数-所带电荷数
=18-2=16,故该微粒为S2-;若该微粒带有一个单位的正电荷,质子数=核外电子数+所带电荷数=18+1
=19,故该微粒为K+。
27、(1)D 2Al+2OH-+2HO===2AlO+3H↑ (2)2Na+2HO===2Na++2OH-+H↑
2 2 2 2
(3)10 该原子最外层已达8电子稳定结构,故化学性质稳定 (4)C 放射
解析:四种粒子按A~D的顺序依次是C、Cl、Na+、Al3+,其中单质具有两性的元素为Al,Al能与NaOH溶
液反应生成H ;Na能与水反应产生H ;电子层结构与Na+相同的原子为Ne,其最外层已达8电子稳定结构,
2 2
故化学性质稳定;考古工作者利用C来测定文物的年代。
28、(1)Mg (2) (3)磷
解析:(1)K层最多容纳2个电子,M层的电子数和K层相同,则M层上有2个电子,其原子结构示意图为
,为镁元素。(2)最外层电子数不超过8,最外层电子数是次外层电子数2倍的元素,其原子结构示意图为。(3)M电子层上有电子,则K、L层已充满电子,电子数分别为2、8,那么M层电子数为5,即是15
号磷元素。
29、(1)碳C 硅Si 氯Cl
(2)
解析:由A元素的原子最外层电子数是次外层电子数的2倍,可知A是碳元素;B元素的原子核外M层电子数
是L层电子数的一半,可知B为硅元素;C元素的原子次外层电子数比最外层电子数多1个,可知C应为氯元
素。
30、(1)7 3 3 1H、2H、3H 234U、235U、238U
(2)40K、40Ca 14N、14C 1H、1H+
解析:(1)本题列出的12种粒子分属H、U、K、Ca、Cl、N、C 7种元素;1H和1H+是同一种核素的不同粒子,
1H、2H、3H属于氢元素的3种不同核素,且互为同位素;234U、235U、238U属于铀元素的3种不同核素,也互为
同位素。
(2)是为“质量数相等的粒子”,而非“质量数相等的原子”,否则“1H和1H+”不能为答案。
31、(1)A-Z (2)A-x-n (3)A-x+n (4)22 (5) mol
解析:(1)根据“质子数+中子数=质量数”的关系,得N=A-Z。(2)AXn+共有x个电子,中性原子X的电子数
为x+n,则N=A-x-n。(3)AXn-共有x个电子,中性原子X的电子数为x-n,则N=A-x+n。(4)12C16O 分子
2
中的中子数为6+8+8=22。(5)A2-所含电子数为m-x+2,则 n g A2-所含电子的物质的量为 mol。
32、(1)222 86 136 (2)AB (3)质子数 质子数和中子数
解析:(1)Rn中的质量数是222,质子数是86,中子数是222-86=136。
(2)Rn、Rn、Rn的质子数相同,属于同种元素,但三者的中子数不同,故三者互为同位素。
(3)其中质子数决定元素种类;质子数和中子数共同决定核素种类。
33、(1)19 26 (2)AC (3)Fe与Fe的核外电子排布相同,化学性质几乎完全相同
解析 (1)Fe的中子数=质量数-质子数=45-26=19,电子数=质子数=26。
(2)Fe与Fe的质子数相同,属同一元素Fe元素,但中子数不同,是两种不同的核素;Fe元素不是一种新元素,
Fe衰变放出两个质子后变为质子数为24的新原子,原子核发生了变化,不是化学变化,因为化学的范畴是在原
子、分子水平上研究物质。