文档内容
微专题突破9 化学反应原理透视
一、选择题
1.(2025·江苏苏州市开学考)第19届杭州亚运会采用石墨烯纳米防滑涂层以增加地面防滑性。
石墨烯属于
A.有机材料 B.无机非金属材料
C.金属材料 D.复合材料
2.(2025·江苏镇江市开学考)室温下通过下列实验探究HC O 的性质。已知K (HC O)=
2 2 4 a1 2 2 4
5.6×10-2,K (HC O)=1.5×10-4。
a2 2 2 4
实验1:配制25 mL 0.1 mol·L-1的HC O 溶液,测得溶液pH=1.3
2 2 4
实验2:取等体积的0.1 mol·L-1 NaOH溶液与实验1所配溶液混合(忽略体积变化),溶液pH=2.8
实验3:向实验2中溶液滴入过量Ba(OH) 溶液,出现白色沉淀
2
下列说法不正确的是
A.实验1所得溶液中:c(OH-)+c(C O2-)+c(HC O-)<c(H+)
2 4 2 4
B.实验2所得溶液中:c(HC O)+c(HC O-)+c(C O2-)=0.05 mol·L-1
2 2 4 2 4 2 4
C.实验3中反应的离子方程式为:Ba2++OH-+HC O-=BaC O↓+HO
2 4 2 4 2
D.实验3反应后上层清液中:c(Ba2+)•c(C O2-)>K (BaC O)
2 4 sp 2 4
的
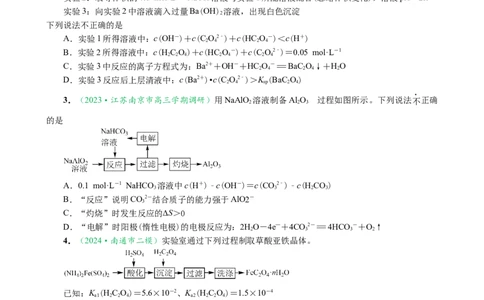
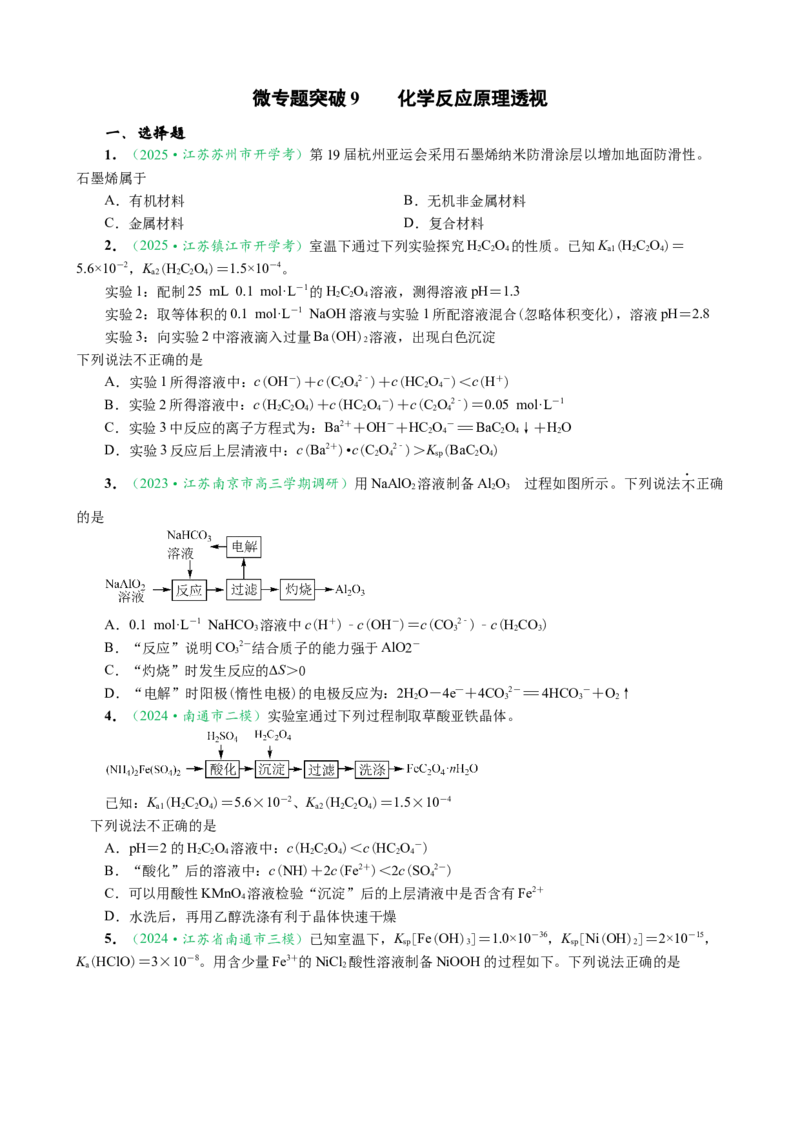
3.(2023·江苏南京市高三学期调研)用NaAlO 溶液制备Al O 过程如图所示。下列说法不正确
2 2 3
的是
A.0.1 mol·L-1 NaHCO 溶液中c(H+)-c(OH-)=c(CO2-)-c(HCO)
3 3 2 3
B.“反应”说明CO2-结合质子的能力强于AlO2-
3
C.“灼烧”时发生反应的∆S>0
D.“电解”时阳极(惰性电极)的电极反应为:2HO-4e—+4CO2-=4HCO -+O↑
2 3 3 2
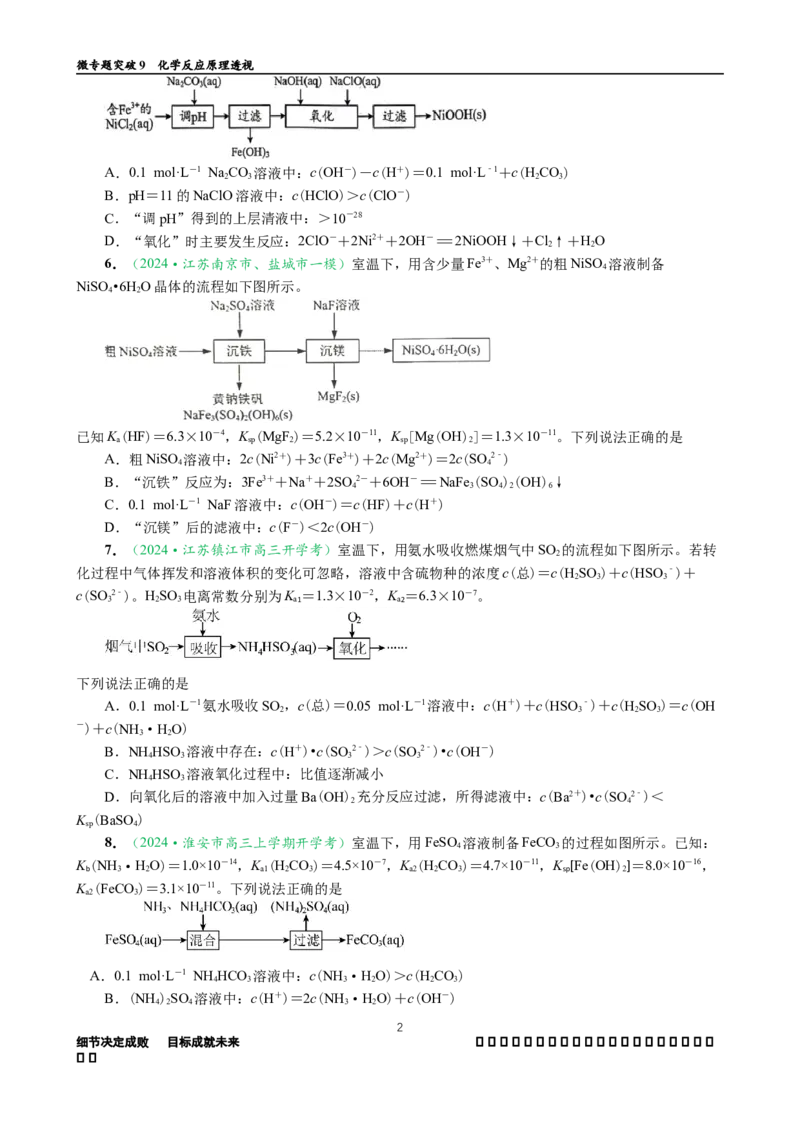
4.(2024·南通市二模)实验室通过下列过程制取草酸亚铁晶体。
已知:K (HC O)=5.6×10-2、K (HC O)=1.5×10-4
a1 2 2 4 a2 2 2 4
下列说法不正确的是
A.pH=2的HC O 溶液中:c(HC O)<c(HC O-)
2 2 4 2 2 4 2 4
B.“酸化”后的溶液中:c(NH)+2c(Fe2+)<2c(SO 2-)
4
C.可以用酸性KMnO 溶液检验“沉淀”后的上层清液中是否含有Fe2+
4
D.水洗后,再用乙醇洗涤有利于晶体快速干燥
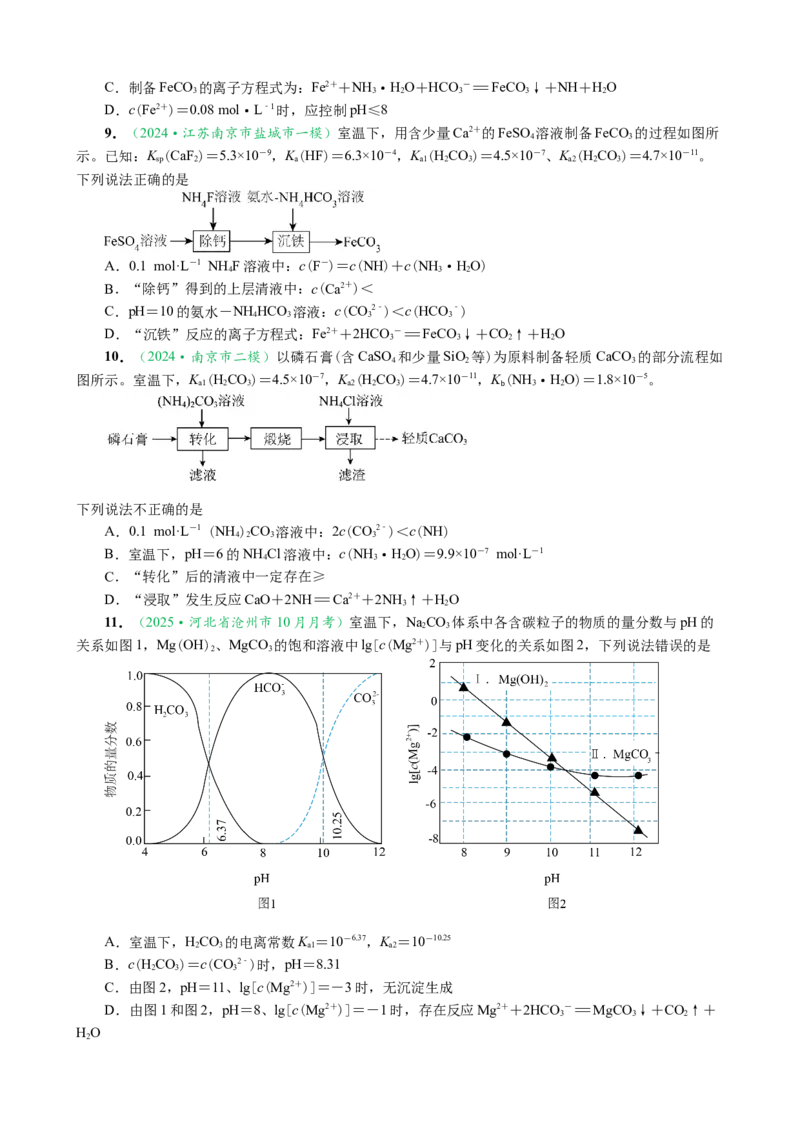
5.(2024·江苏省南通市三模)已知室温下,K [Fe(OH)]=1.0×10-36,K [Ni(OH)]=2×10-15,
sp 3 sp 2
K(HClO)=3×10-8。用含少量Fe3+的NiCl 酸性溶液制备NiOOH的过程如下。下列说法正确的是
a 2微专题突破9 化学反应原理透视
A.0.1 mol·L-1 NaCO 溶液中:c(OH-)-c(H+)=0.1 mol·L-1+c(HCO)
2 3 2 3
B.pH=11的NaClO溶液中:c(HClO)>c(ClO-)
C.“调pH”得到的上层清液中:>10-28
D.“氧化”时主要发生反应:2ClO-+2Ni2++2OH-=2NiOOH↓+Cl↑+HO
2 2
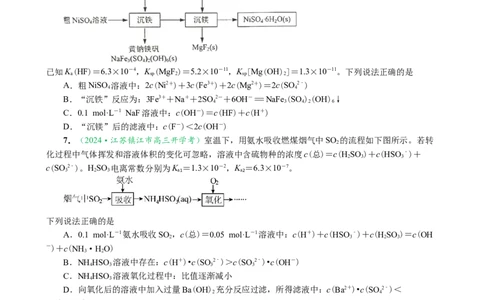
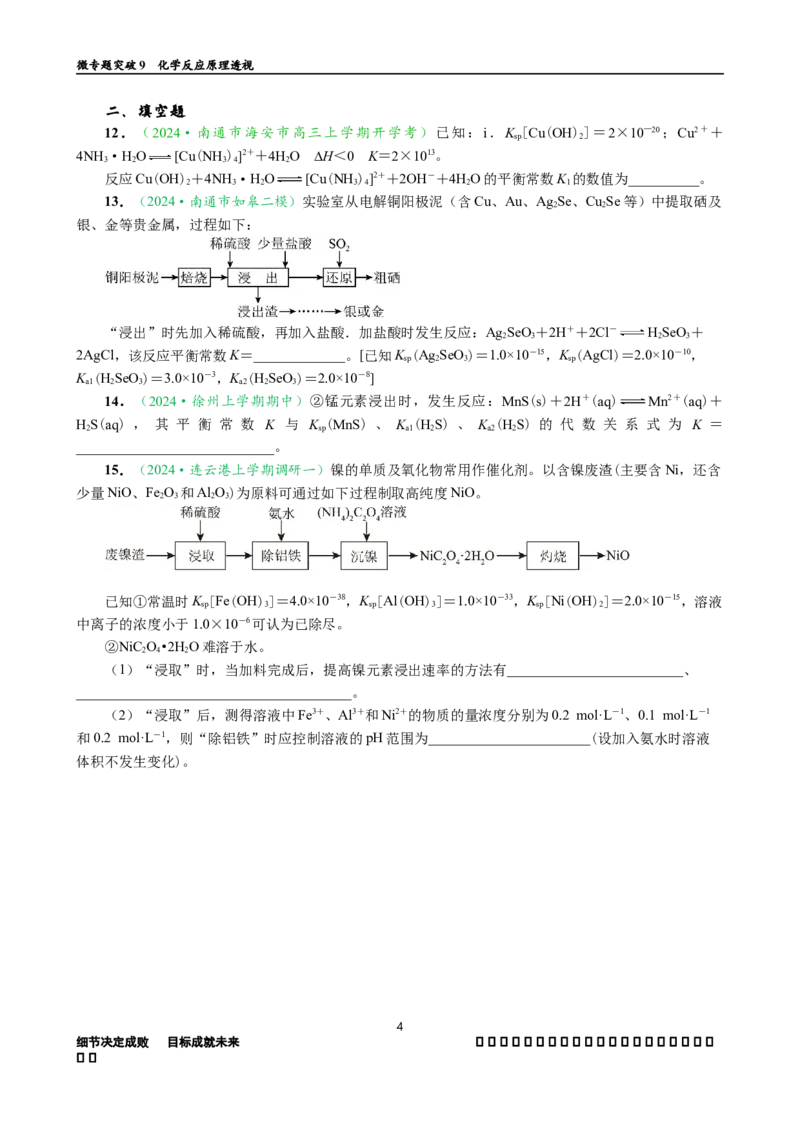
6.(2024·江苏南京市、盐城市一模)室温下,用含少量Fe3+、Mg2+的粗NiSO 溶液制备
4
NiSO •6HO晶体的流程如下图所示。
4 2
已知K(HF)=6.3×10-4,K (MgF )=5.2×10-11,K [Mg(OH)]=1.3×10-11。下列说法正确的是
a sp 2 sp 2
A.粗NiSO 溶液中:2c(Ni2+)+3c(Fe3+)+2c(Mg2+)=2c(SO 2-)
4 4
B.“沉铁”反应为:3Fe3++Na++2SO 2-+6OH-=NaFe (SO )(OH)↓
4 3 4 2 6
C.0.1 mol·L-1 NaF溶液中:c(OH-)=c(HF)+c(H+)
D.“沉镁”后的滤液中:c(F-)<2c(OH-)
7.(2024·江苏镇江市高三开学考)室温下,用氨水吸收燃煤烟气中SO 的流程如下图所示。若转
2
化过程中气体挥发和溶液体积的变化可忽略,溶液中含硫物种的浓度c(总)=c(HSO)+c(HSO -)+
2 3 3
c(SO 2-)。HSO 电离常数分别为K =1.3×10-2,K =6.3×10-7。
3 2 3 a1 a2
下列说法正确的是
A.0.1 mol·L-1氨水吸收SO ,c(总)=0.05 mol·L-1溶液中:c(H+)+c(HSO -)+c(HSO)=c(OH
2 3 2 3
-)+c(NH ·HO)
3 2
B.NH HSO 溶液中存在:c(H+)•c(SO 2-)>c(SO 2-)•c(OH-)
4 3 3 3
C.NH HSO 溶液氧化过程中:比值逐渐减小
4 3
D.向氧化后的溶液中加入过量Ba(OH) 充分反应过滤,所得滤液中:c(Ba2+)•c(SO 2-)<
2 4
K (BaSO)
sp 4
8.(2024·淮安市高三上学期开学考)室温下,用FeSO 溶液制备FeCO 的过程如图所示。已知:
4 3
K (NH ·HO)=1.0×10-14,K (HCO)=4.5×10-7,K (HCO)=4.7×10-11,K [Fe(OH)]=8.0×10-16,
b 3 2 a1 2 3 a2 2 3 sp 2
K (FeCO)=3.1×10-11。下列说法正确的是
a2 3
A.0.1 mol·L-1 NH HCO 溶液中:c(NH ·HO)>c(HCO)
4 3 3 2 2 3
B.(NH )SO 溶液中:c(H+)=2c(NH ·HO)+c(OH-)
4 2 4 3 2
2
细节决定成败 目标成就未来 找找找找找找找找找找找找找找找找找找找找
找找C.制备FeCO 的离子方程式为:Fe2++NH ·HO+HCO -=FeCO↓+NH+HO
3 3 2 3 3 2
D.c(Fe2+)=0.08 mol·L-1时,应控制pH≤8
9.(2024·江苏南京市盐城市一模)室温下,用含少量Ca2+的FeSO 溶液制备FeCO 的过程如图所
4 3
示。已知:K (CaF )=5.3×10-9,K(HF)=6.3×10-4,K (HCO)=4.5×10-7、K (HCO)=4.7×10-11。
sp 2 a a1 2 3 a2 2 3
下列说法正确的是
A.0.1 mol·L-1 NH F溶液中:c(F-)=c(NH)+c(NH ·HO)
4 3 2
B.“除钙”得到的上层清液中:c(Ca2+)<
C.pH=10的氨水-NH HCO 溶液:c(CO2-)<c(HCO -)
4 3 3 3
D.“沉铁”反应的离子方程式:Fe2++2HCO -=FeCO↓+CO↑+HO
3 3 2 2
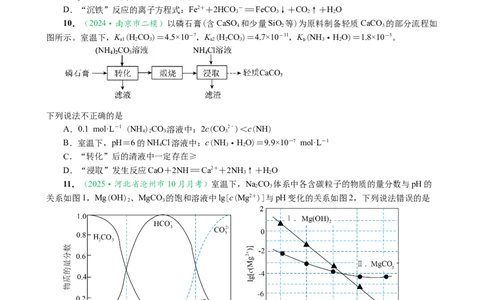
10.(2024·南京市二模)以磷石膏(含CaSO 和少量SiO 等)为原料制备轻质CaCO 的部分流程如
4 2 3
图所示。室温下,K (HCO)=4.5×10-7,K (HCO)=4.7×10-11,K (NH ·HO)=1.8×10-5。
a1 2 3 a2 2 3 b 3 2
下列说法不正确的是
A.0.1 mol·L-1 (NH )CO 溶液中:2c(CO2-)<c(NH)
4 2 3 3
B.室温下,pH=6的NH Cl溶液中:c(NH ·HO)=9.9×10-7 mol·L-1
4 3 2
C.“转化”后的清液中一定存在≥
D.“浸取”发生反应CaO+2NH=Ca2++2NH ↑+HO
3 2
11.(2025·河北省沧州市10月月考)室温下,NaCO 体系中各含碳粒子的物质的量分数与pH的
2 3
关系如图1,Mg(OH)、MgCO 的饱和溶液中lg[c(Mg2+)]与pH变化的关系如图2,下列说法错误的是
2 3
A.室温下,HCO 的电离常数K =10-6.37,K =10-10.25
2 3 a1 a2
B.c(HCO)=c(CO2-)时,pH=8.31
2 3 3
C.由图2,pH=11、lg[c(Mg2+)]=-3时,无沉淀生成
D.由图1和图2,pH=8、lg[c(Mg2+)]=-1时,存在反应Mg2++2HCO -=MgCO ↓+CO↑+
3 3 2
HO
2微专题突破9 化学反应原理透视
二、填空题
12.(2024·南通市海安市高三上学期开学考)已知:i.K [Cu(OH)]=2×10—20;Cu2++
sp 2
4NH ·HO [Cu(NH )]2++4HO ∆H<0 K=2×1013。
3 2 3 4 2
反应Cu(OH)+4NH ·HO [Cu(NH )]2++2OH-+4HO的平衡常数K 的数值为__________。
2 3 2 3 4 2 1
13.(2024·南通市如皋二模)实验室从电解铜阳极泥(含Cu、Au、Ag Se、Cu Se等)中提取硒及
2 2
银、金等贵金属,过程如下:
“浸出”时先加入稀硫酸,再加入盐酸.加盐酸时发生反应:Ag SeO+2H++2Cl- HSeO+
2 3 2 3
2AgCl,该反应平衡常数K=_____________。[已知K (Ag SeO)=1.0×10-15,K (AgCl)=2.0×10-10,
sp 2 3 sp
K (HSeO)=3.0×10-3,K (HSeO)=2.0×10-8]
a1 2 3 a2 2 3
14.(2024·徐州上学期期中)②锰元素浸出时,发生反应:MnS(s)+2H+(aq) Mn2+(aq)+
HS(aq) , 其 平 衡 常 数 K 与 K (MnS) 、 K (HS) 、 K (HS) 的 代 数 关 系 式 为 K =
2 sp a1 2 a2 2
____________________________。
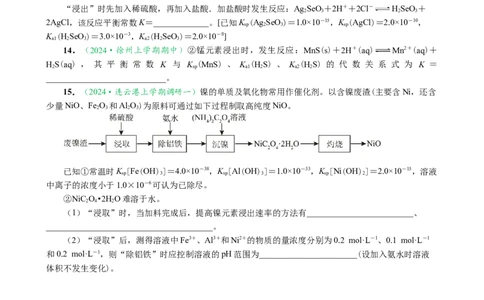
15.(2024·连云港上学期调研一)镍的单质及氧化物常用作催化剂。以含镍废渣(主要含Ni,还含
少量NiO、Fe O 和Al O)为原料可通过如下过程制取高纯度NiO。
2 3 2 3
已知①常温时K [Fe(OH)]=4.0×10-38,K [Al(OH)]=1.0×10-33,K [Ni(OH)]=2.0×10-15,溶液
sp 3 sp 3 sp 2
中离子的浓度小于1.0×10-6可认为已除尽。
②NiC O•2HO难溶于水。
2 4 2
(1)“浸取”时,当加料完成后,提高镍元素浸出速率的方法有_________________________、
_______________________________________。
(2)“浸取”后,测得溶液中Fe3+、Al3+和Ni2+的物质的量浓度分别为0.2 mol·L-1、0.1 mol·L-1
和0.2 mol·L-1,则“除铝铁”时应控制溶液的pH范围为_______________________(设加入氨水时溶液
体积不发生变化)。
4
细节决定成败 目标成就未来 找找找找找找找找找找找找找找找找找找找找
找找