文档内容
微专题突破16 归因类问题考点透视一
一、选择题
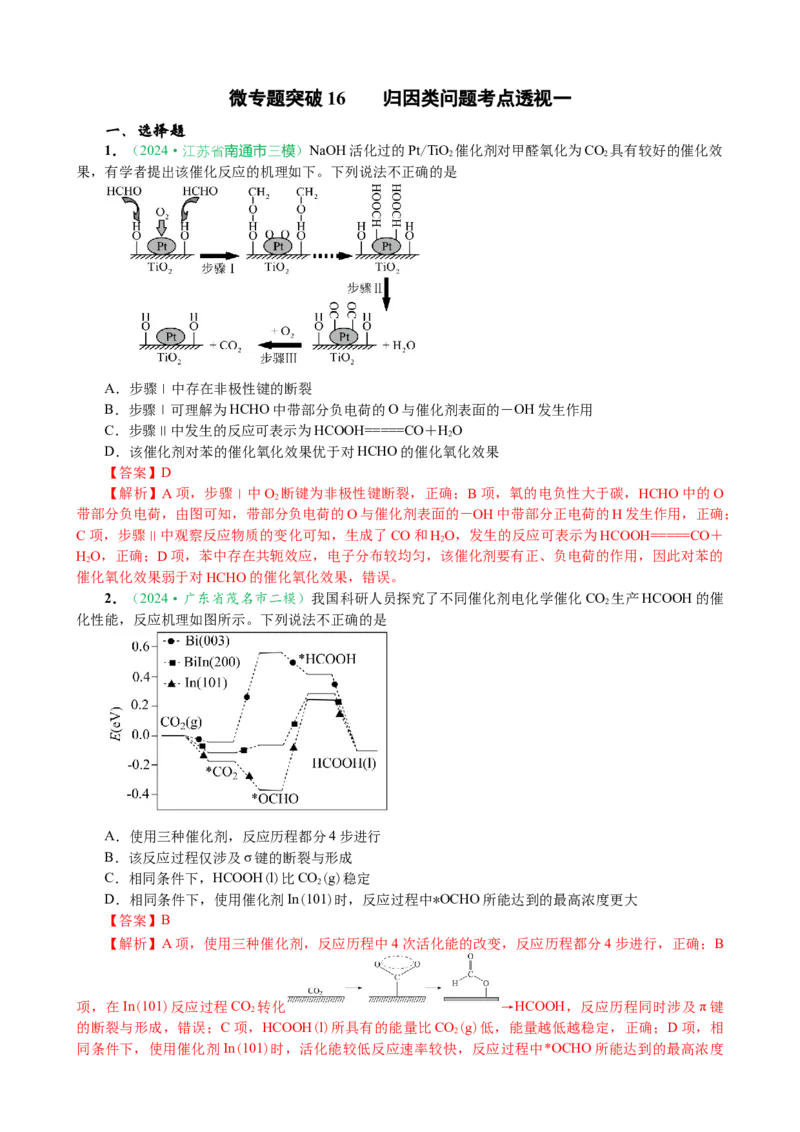
1.(2024·江苏省南通市三模)NaOH活化过的Pt/TiO 催化剂对甲醛氧化为CO 具有较好的催化效
2 2
果,有学者提出该催化反应的机理如下。下列说法不正确的是
A.步骤Ⅰ中存在非极性键的断裂
B.步骤Ⅰ可理解为HCHO中带部分负电荷的O与催化剂表面的-OH发生作用
C.步骤Ⅱ中发生的反应可表示为HCOOH=====CO+HO
2
D.该催化剂对苯的催化氧化效果优于对HCHO的催化氧化效果
【答案】D
【解析】A项,步骤Ⅰ中O 断键为非极性键断裂,正确;B项,氧的电负性大于碳,HCHO中的O
2
带部分负电荷,由图可知,带部分负电荷的O与催化剂表面的-OH中带部分正电荷的H发生作用,正确;
C项,步骤Ⅱ中观察反应物质的变化可知,生成了CO和HO,发生的反应可表示为HCOOH=====CO+
2
HO,正确;D项,苯中存在共轭效应,电子分布较均匀,该催化剂要有正、负电荷的作用,因此对苯的
2
催化氧化效果弱于对HCHO的催化氧化效果,错误。
2.(2024·广东省茂名市二模)我国科研人员探究了不同催化剂电化学催化CO 生产HCOOH的催
2
化性能,反应机理如图所示。下列说法不正确的是
A.使用三种催化剂,反应历程都分4步进行
B.该反应过程仅涉及σ键的断裂与形成
C.相同条件下,HCOOH(l)比CO(g)稳定
2
D.相同条件下,使用催化剂In(101)时,反应过程中*OCHO所能达到的最高浓度更大
【答案】B
【解析】A项,使用三种催化剂,反应历程中4次活化能的改变,反应历程都分4步进行,正确;B
项,在In(101)反应过程CO 转化 →HCOOH,反应历程同时涉及π键
2
的断裂与形成,错误;C项,HCOOH(l)所具有的能量比CO(g)低,能量越低越稳定,正确;D项,相
2
同条件下,使用催化剂In(101)时,活化能较低反应速率较快,反应过程中*OCHO所能达到的最高浓度微专题突破16 归因类问题考点透视一
更大,正确。
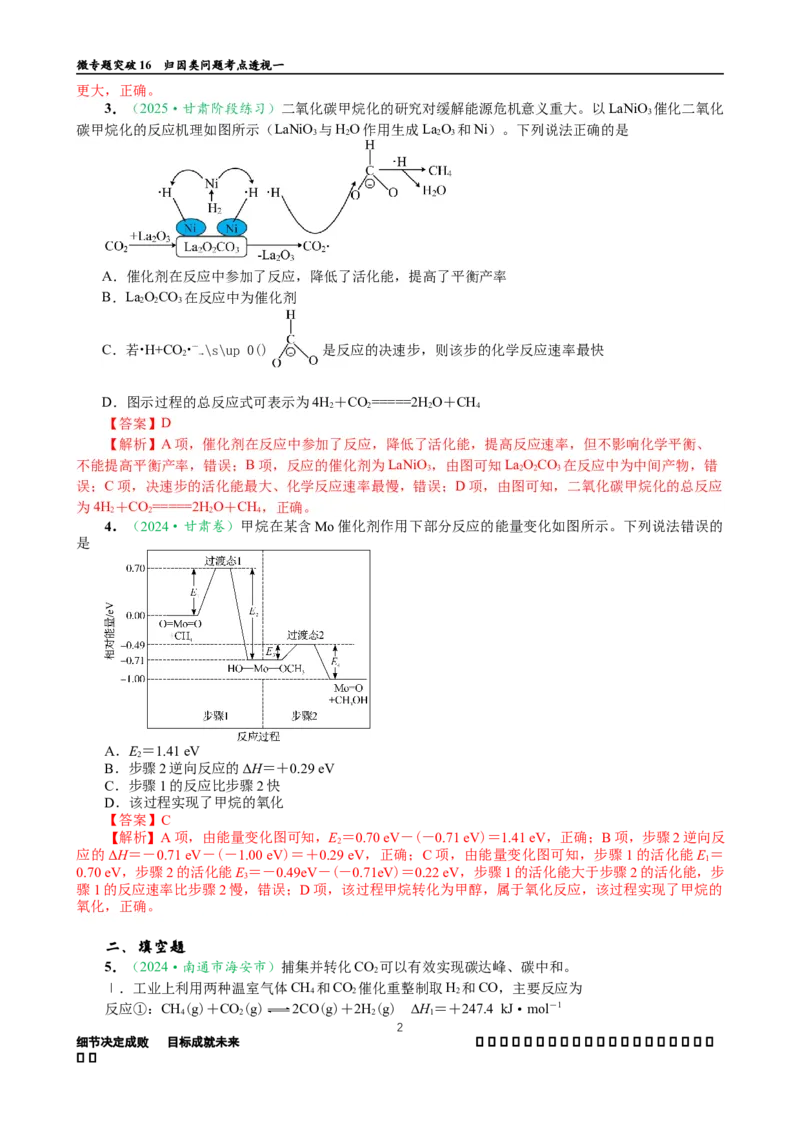
3.(2025·甘肃阶段练习)二氧化碳甲烷化的研究对缓解能源危机意义重大。以LaNiO 催化二氧化
3
碳甲烷化的反应机理如图所示(LaNiO 与HO作用生成LaO 和Ni)。下列说法正确的是
3 2 2 3
A.催化剂在反应中参加了反应,降低了活化能,提高了平衡产率
B.LaOCO 在反应中为催化剂
2 2 3
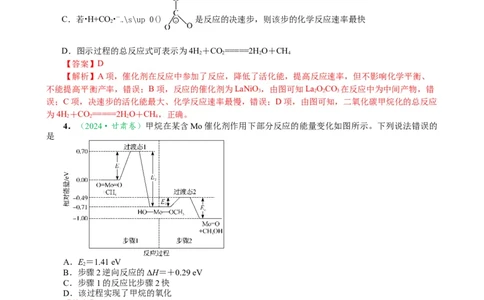
C.若•H+CO•— \s\up 0() 是反应的决速步,则该步的化学反应速率最快
2 →
D.图示过程的总反应式可表示为4H+CO=====2HO+CH
2 2 2 4
【答案】D
【解析】A项,催化剂在反应中参加了反应,降低了活化能,提高反应速率,但不影响化学平衡、
不能提高平衡产率,错误;B项,反应的催化剂为LaNiO ,由图可知LaOCO 在反应中为中间产物,错
3 2 2 3
误;C项,决速步的活化能最大、化学反应速率最慢,错误;D项,由图可知,二氧化碳甲烷化的总反应
为4H+CO=====2HO+CH,正确。
2 2 2 4
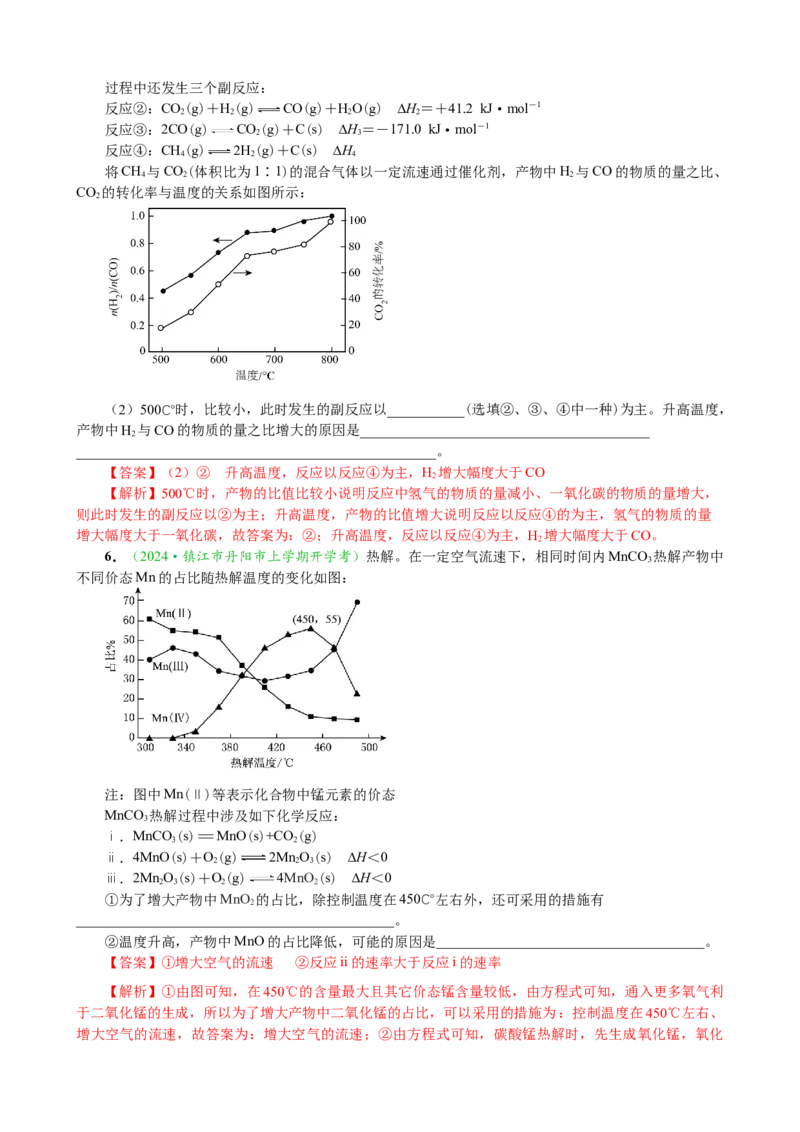
4.(2024·甘肃卷)甲烷在某含Mo催化剂作用下部分反应的能量变化如图所示。下列说法错误的
是
A.E=1.41 eV
2
B.步骤2逆向反应的ΔH=+0.29 eV
C.步骤1的反应比步骤2快
D.该过程实现了甲烷的氧化
【答案】C
【解析】A项,由能量变化图可知,E=0.70 eV-(-0.71 eV)=1.41 eV,正确;B项,步骤2逆向反
2
应的ΔH=-0.71 eV-(-1.00 eV)=+0.29 eV,正确;C项,由能量变化图可知,步骤1的活化能E =
1
0.70 eV,步骤2的活化能E=-0.49eV-(-0.71eV)=0.22 eV,步骤1的活化能大于步骤2的活化能,步
3
骤1的反应速率比步骤2慢,错误;D项,该过程甲烷转化为甲醇,属于氧化反应,该过程实现了甲烷的
氧化,正确。
二、填空题
5.(2024·南通市海安市)捕集并转化CO 可以有效实现碳达峰、碳中和。
2
Ⅰ.工业上利用两种温室气体CH 和CO 催化重整制取H 和CO,主要反应为
4 2 2
反应①:CH(g)+CO(g) 2CO(g)+2H(g) ∆H=+247.4 kJ·mol-1
4 2 2 1
2
细节决定成败 目标成就未来 找找找找找找找找找找找找找找找找找找找找
找找过程中还发生三个副反应:
反应②:CO(g)+H(g) CO(g)+HO(g) ∆H=+41.2 kJ·mol-1
2 2 2 2
反应③:2CO(g) CO(g)+C(s) ∆H=-171.0 kJ·mol-1
2 3
反应④:CH(g) 2H(g)+C(s) ∆H
4 2 4
将CH 与CO(体积比为1∶1)的混合气体以一定流速通过催化剂,产物中H 与CO的物质的量之比、
4 2 2
CO 的转化率与温度的关系如图所示:
2
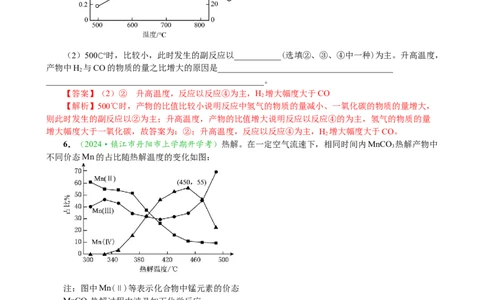
(2)500℃时,比较小,此时发生的副反应以___________(选填②、③、④中一种)为主。升高温度,
产物中H 与CO的物质的量之比增大的原因是_________________________________________
2
___________________________________________________。
【答案】(2)② 升高温度,反应以反应④为主,H 增大幅度大于CO
2
【解析】500℃时,产物的比值比较小说明反应中氢气的物质的量减小、一氧化碳的物质的量增大,
则此时发生的副反应以②为主;升高温度,产物的比值增大说明反应以反应④的为主,氢气的物质的量
增大幅度大于一氧化碳,故答案为:②;升高温度,反应以反应④为主,H 增大幅度大于CO。
2
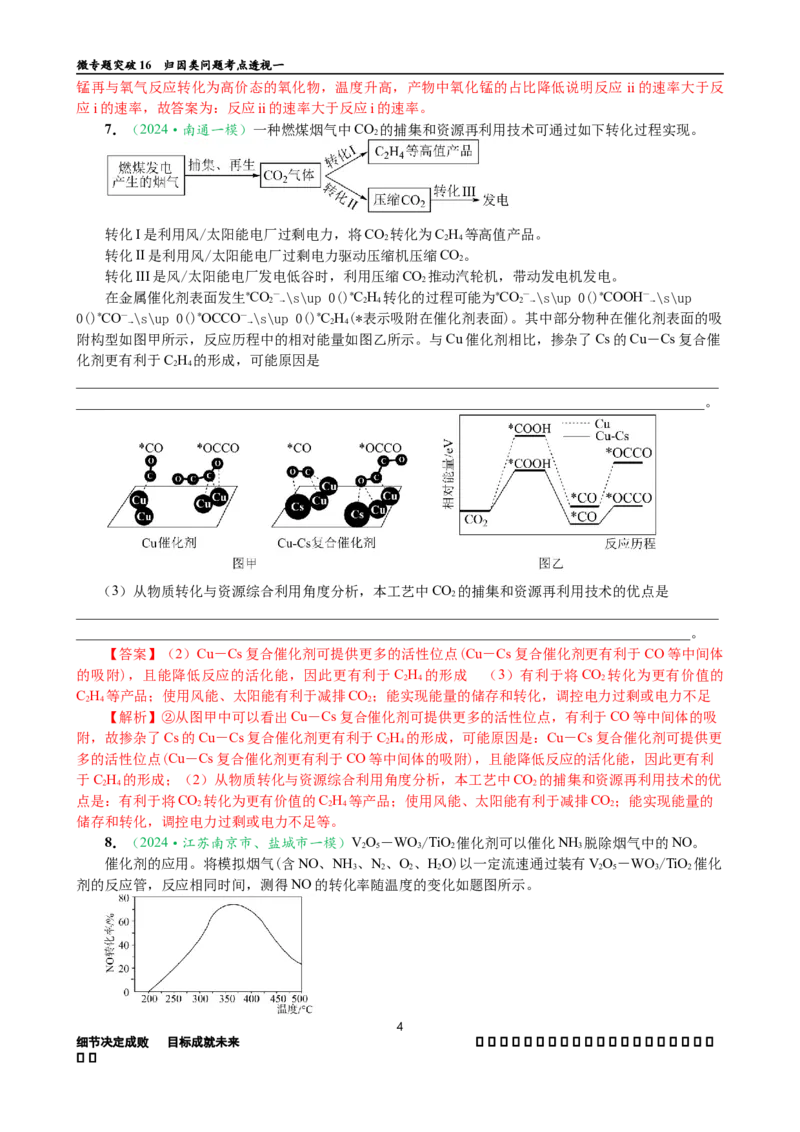
6.(2024·镇江市丹阳市上学期开学考)热解。在一定空气流速下,相同时间内MnCO 热解产物中
3
不同价态Mn的占比随热解温度的变化如图:
注:图中Mn(Ⅱ)等表示化合物中锰元素的价态
MnCO 热解过程中涉及如下化学反应:
3
ⅰ.MnCO(s)=MnO(s)+CO (g)
3 2
ⅱ.4MnO(s)+O(g) 2MnO(s) ∆H<0
2 2 3
ⅲ.2MnO(s)+O(g) 4MnO (s) ∆H<0
2 3 2 2
①为了增大产物中MnO 的占比,除控制温度在450℃左右外,还可采用的措施有
2
_____________________________________________。
②温度升高,产物中MnO的占比降低,可能的原因是______________________________________。
【答案】①增大空气的流速 ②反应ii的速率大于反应i的速率
【解析】①由图可知,在450℃的含量最大且其它价态锰含量较低,由方程式可知,通入更多氧气利
于二氧化锰的生成,所以为了增大产物中二氧化锰的占比,可以采用的措施为:控制温度在450℃左右、
增大空气的流速,故答案为:增大空气的流速;②由方程式可知,碳酸锰热解时,先生成氧化锰,氧化微专题突破16 归因类问题考点透视一
锰再与氧气反应转化为高价态的氧化物,温度升高,产物中氧化锰的占比降低说明反应 ii的速率大于反
应i的速率,故答案为:反应ii的速率大于反应i的速率。
7.(2024·南通一模)一种燃煤烟气中CO 的捕集和资源再利用技术可通过如下转化过程实现。
2
转化I是利用风/太阳能电厂过剩电力,将CO 转化为C H 等高值产品。
2 2 4
转化II是利用风/太阳能电厂过剩电力驱动压缩机压缩CO。
2
转化III是风/太阳能电厂发电低谷时,利用压缩CO 推动汽轮机,带动发电机发电。
2
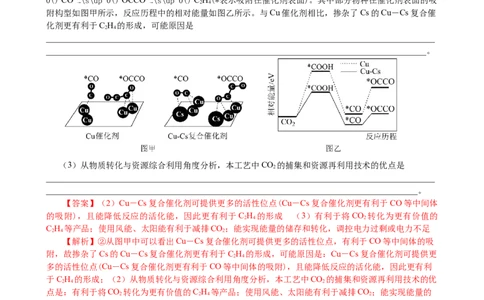
在金属催化剂表面发生*CO— \s\up 0()*C H 转化的过程可能为*CO— \s\up 0()*COOH— \s\up
2 → 2 4 2 → →
0()*CO— \s\up 0()*OCCO— \s\up 0()*C H(*表示吸附在催化剂表面)。其中部分物种在催化剂表面的吸
→ → 2 4
附构型如图甲所示,反应历程中的相对能量如图乙所示。与Cu催化剂相比,掺杂了Cs的Cu-Cs复合催
化剂更有利于C H 的形成,可能原因是
2 4
___________________________________________________________________________________________
_________________________________________________________________________________________。
(3)从物质转化与资源综合利用角度分析,本工艺中CO 的捕集和资源再利用技术的优点是
2
___________________________________________________________________________________________
_______________________________________________________________________________________。
【答案】(2)Cu-Cs复合催化剂可提供更多的活性位点(Cu-Cs复合催化剂更有利于CO等中间体
的吸附),且能降低反应的活化能,因此更有利于C H 的形成 (3)有利于将CO 转化为更有价值的
2 4 2
C H 等产品;使用风能、太阳能有利于减排CO;能实现能量的储存和转化,调控电力过剩或电力不足
2 4 2
【解析】②从图甲中可以看出Cu-Cs复合催化剂可提供更多的活性位点,有利于CO等中间体的吸
附,故掺杂了Cs的Cu-Cs复合催化剂更有利于C H 的形成,可能原因是:Cu-Cs复合催化剂可提供更
2 4
多的活性位点(Cu-Cs复合催化剂更有利于CO等中间体的吸附),且能降低反应的活化能,因此更有利
于C H 的形成;(2)从物质转化与资源综合利用角度分析,本工艺中CO 的捕集和资源再利用技术的优
2 4 2
点是:有利于将CO 转化为更有价值的C H 等产品;使用风能、太阳能有利于减排CO;能实现能量的
2 2 4 2
储存和转化,调控电力过剩或电力不足等。
8.(2024·江苏南京市、盐城市一模)VO-WO/TiO 催化剂可以催化NH 脱除烟气中的NO。
2 5 3 2 3
催化剂的应用。将模拟烟气(含NO、NH 、N、O、HO)以一定流速通过装有VO-WO/TiO 催化
3 2 2 2 2 5 3 2
剂的反应管,反应相同时间,测得NO的转化率随温度的变化如题图所示。
4
细节决定成败 目标成就未来 找找找找找找找找找找找找找找找找找找找找
找找①反应温度高于350℃,NO转化率下降的原因可能是
_____________________________________________________________________________。
②若烟气中含有SO ,则会导致催化剂失活,原因可能是
2
_________________________________________________________________________________________
________________________________________________。
【答案】①催化剂活性下降,反应速率减慢;NH 与O 发生反应生成NO ②SO 会被(VO)催化氧
3 2 2 2 5
化为SO ,SO 与NH 作用生成NH HSO 或(NH )SO ,覆盖(沉积)在催化剂的表面,大大降低了催化剂
3 3 3 4 4 4 2 4
和反应物的接触面积[或SO 与NH 作用生成NH HSO 或(NH )SO ,最终被氧化为NH HSO 或
2 3 4 3 4 2 3 4 4
(NH )SO ,覆盖(沉积)在催化剂的表面,大大降低了催化剂和反应物的接触面积]
4 2 4
【解析】①反应温度高于350℃,催化剂活性下降,反应速率减慢;此外,NH 能与O 发生反应生成
3 2
NO,从而导致NO转化率下降,故答案为催化剂活性下降,反应速率减慢;NH 与O 发生反应生成
3 2
NO;②若烟气中含有 SO ,SO 会被(VO)催化氧化为 SO ,SO 与 NH 作用生成 NH HSO 或
2 2 2 5 3 3 3 4 4
(NH )SO ,覆盖(沉积)在催化剂的表面,大大降低了催化剂和反应物的接触面积,从而导致催化剂失活,
4 2 4
故答案为SO 会被(VO)催化氧化为SO ,SO 与NH 作用生成NH HSO 或(NH )SO ,覆盖(沉积)在催
2 2 5 3 3 3 4 4 4 2 4
化剂的表面,大大降低了催化剂和反应物的接触面积[或SO 与NH 作用生成NH HSO 或(NH )SO ,最
2 3 4 3 4 2 3
终被氧化为NH HSO 或(NH )SO ,覆盖(沉积)在催化剂的表面,大大降低了催化剂和反应物的接触面
4 4 4 2 4
积]。
9.(2025·江苏省泰州中学月考)甲烷是一种重要的化工原料,常用于制H 和CO。
2
(1)甲烷裂解制氢的反应为CH(g)=C(s)+2H(g) ∆H=75 kJ·mol-1,Ni和活性炭均可作该反
4 2
应催化剂。CH 在催化剂孔道表面反应,若孔道堵塞会导致催化剂失活。
4
①Ni催化剂可用NiC O·2HO晶体在氩气环境中受热分解制备,该反应方程式为
2 4 2
_________________________________________________________。
②向反应系统中通入水蒸气可有效减少催化剂失活,其原因是_________________________________
___________________________________________。
③在相同气体流量条件下,不同催化剂和进料比[]对甲烷转化率的影响如图所示。
使用活性炭催化剂,且其他条件相同时,随着进料比的增大,甲烷的转化率逐渐增大的原因是
_______________________________________________________________。
④使用Ni催化剂,且其他条件相同时,随时间增加,温度对Ni催化剂催化效果的影响如下图所示。
使用催化剂的最佳温度为___________,650℃条件下,1 000 s后,氢气的体积分数快速下降的原因为
___________________________________________________________________________。微专题突破16 归因类问题考点透视一
(2)甲烷、二氧化碳重整制CO经历过程I、II。过程I如图所示,可描述为_____________________
___________________________________________________________________________________________
__________________________________________________________________;过程II保持温度不变,再
通入惰性气体,CaCO 分解产生CO,Fe将CO 还原得到CO和Fe O。
3 2 2 3 4
【答案】(1)①NiC O·2HO=====Ni+2CO↑+2HO ②水蒸气与碳反应生成CO(或CO)与氢
2 4 2 2 2 2
气,减少固体碳对孔道的堵塞 ③进入反应的甲烷含量越低,甲烷分子与催化剂接触的几率越大,转化率
越高 ④600℃ 温度升高反应速率加快,催化剂内积碳量增加,催化剂快速失活 (2)CH 和CO 在催
4 2
化剂Ni表面反应,产生CO和H ,H 和CO还原Fe O 生成Fe、CO 和HO,未反应完和生成的CO 与
2 2 3 4 2 2 2
CaO反应生成CaCO
3
【解析】(1)①根据题意可知,在氩气环境中受热分解可得到 Ni,其方程式为:
NiC O·2HO=====Ni+2CO↑+2HO;②向反应系统中通入水蒸气可有效减少催化剂失活,是因为水
2 4 2 2 2
蒸气与碳反应生成CO(或CO)与氢气,减少固体碳对孔道的堵塞;③进料比的增大,进入反应的甲烷含
2
量越低,甲烷分子与催化剂接触的几率越大,转化率越高;④由图可知,在反应后期550℃,600℃,
650℃下,600℃时H 的体积分数最高,即催化效率最高的是600℃时,故答案为:600℃;650℃条件下
2
氢气的体积分数快速下降,是因为温度升高反应速率加快,催化剂内积碳量增加,催化剂快速失活;
(2)由图可知,CH 和CO 在催化剂Ni表面反应,生成CO和H ,H 和CO还原Fe O 生成Fe、CO 和
4 2 2 2 3 4 2
HO,未反应完和生成的CO 与CaO反应生成CaCO 。
2 2 3
10.(2024·泰州市期中)利用CO 制甲烷可实现碳中和,CO 催化加氢合成CH 反应为CO(g)+
2 2 4 2
3H(g) CH(g)+2HO(g) ∆H=-165 kJ·mol-1。
2 4 2 1
(1)CO 催化加氢合成CH 过程中,CO 活化的可能途径如题图1所示, CO是CO 活化的优势中
2 4 2 2
间体,原因是______________________________________________________________________________
_______________________________。
6
细节决定成败 目标成就未来 找找找找找找找找找找找找找找找找找找找找
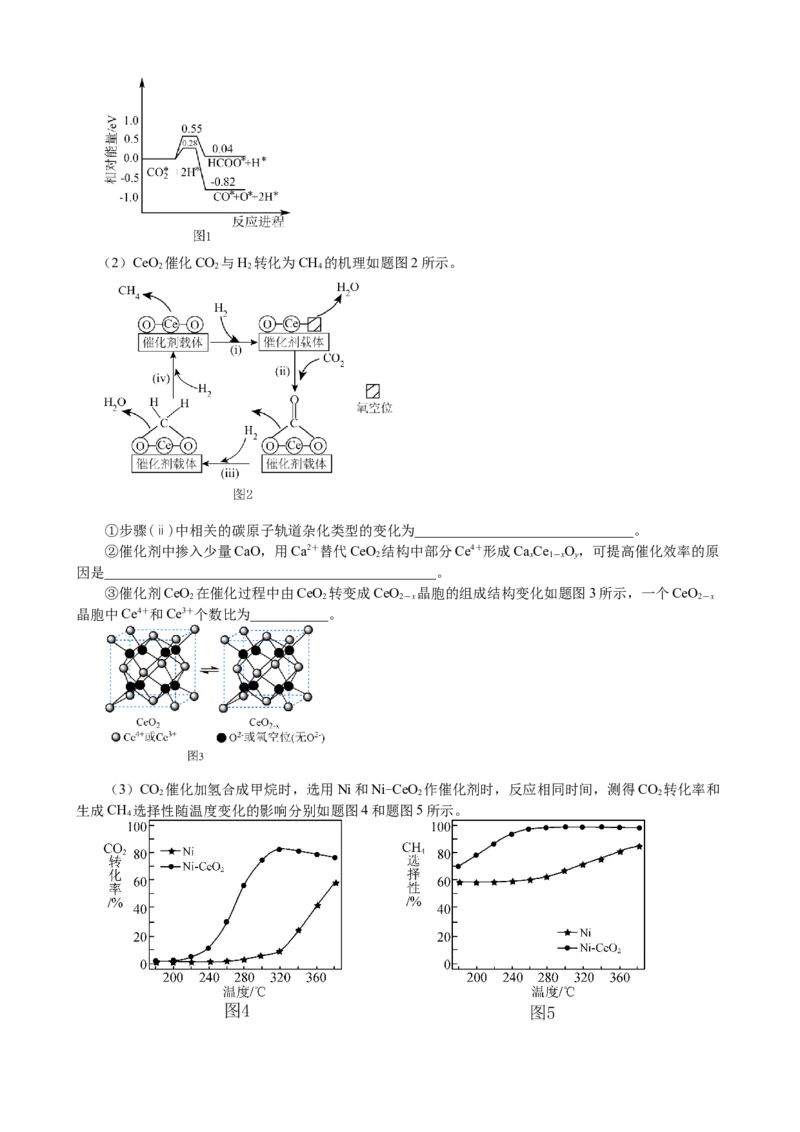
找找(2)CeO 催化CO 与H 转化为CH 的机理如题图2所示。
2 2 2 4
①步骤(ⅱ)中相关的碳原子轨道杂化类型的变化为_______________________________。
②催化剂中掺入少量CaO,用Ca2+替代CeO 结构中部分Ce4+形成CaCe O,可提高催化效率的原
2 x 1-x y
因是_______________________________________________。
③催化剂CeO 在催化过程中由CeO 转变成CeO 晶胞的组成结构变化如题图3所示,一个CeO
2 2 2-x 2-x
晶胞中Ce4+和Ce3+个数比为___________。
(3)CO 催化加氢合成甲烷时,选用Ni和Ni-CeO 作催化剂时,反应相同时间,测得CO 转化率和
2 2 2
生成CH 选择性随温度变化的影响分别如题图4和题图5所示。
4微专题突破16 归因类问题考点透视一
①以Ni为催化剂,高于320℃后,CO 转化率上升的主要原因是_______________________________
2
___________________________________________________________________________________________
________________________________。
②以Ni-CeO 为催化剂,高于320℃后,CO 转化率略有下降的可能原因是
2 2
___________________________________________________________________________________________
_________________________________________________________________________________________。
【答案】(1)生成中间体CO反应的活化能小,反应速率快、CO中间体能量低,稳定,有利于生成
(2)①由sp杂化转变为sp2杂化 ②结构中氧空位增加 ③ (3)①高于320℃后,Ni催化剂活性随温
度升高而增强,和温度升高的共同作用使CO 催化加氢合成甲烷反应速率加快,使CO 转化率上升 ②高
2 2
于320℃后,温度升高对反应速率的影响小于催化剂活性减弱对反应速率的影响,CO 催化加氢合成甲烷
2
反应速率下降;CO 催化加氢合成甲烷反应放热,温度升高不利于提高CO 转化率
2 2
【解析】(1)生成中间体CO反应的活化能小,反应速率快、CO中间体能量低,稳定,有利于生成,
因此CO 催化加氢合成CH 过程中,CO是CO 活化的优势中间体;(2)①步骤(ⅱ)中相关的碳原子由
2 4 2
CO 中的sp杂化转化至CeCO 中CO2-中C为sp2杂化,故轨道杂化类型的变化为由sp杂化转变为sp2杂
2 3 3
化;②催化剂中掺入少量CaO,用Ca2+替代CeO 结构中部分Ce4+形成CaCe O,Ca2+的电荷比Ce4+少,
2 x 1-x y
则可使结构中氧空位增加;③假设CeO 中的Ce4+和Ce3+的个数分别为m和n,则m+n=1,由化合物
2-x
中各元素正、负化合价代数和为0可得4m+3n=4-2x,解得m=1-2x,n=1-m=2x,故一个CeO
2-x
晶胞中Ce4+和Ce3+个数比为;(3)①以Ni为催化剂,高于320℃后,CO 转化率上升的主要原因是高于
2
320℃后,Ni催化剂活性随温度升高而增强,和温度升高的共同作用使CO 催化加氢合成甲烷反应速率加
2
快,使CO 转化率上升;②以Ni-CeO 为催化剂,高于320℃后,CO 转化率略有下降的可能原因是高于
2 2 2
320℃后,温度升高对反应速率的影响小于催化剂活性减弱对反应速率的影响,CO 催化加氢合成甲烷反
2
应速率下降;CO 催化加氢合成甲烷反应放热,温度升高不利于提高CO 转化率。
2 2
8
细节决定成败 目标成就未来 找找找找找找找找找找找找找找找找找找找找
找找