文档内容
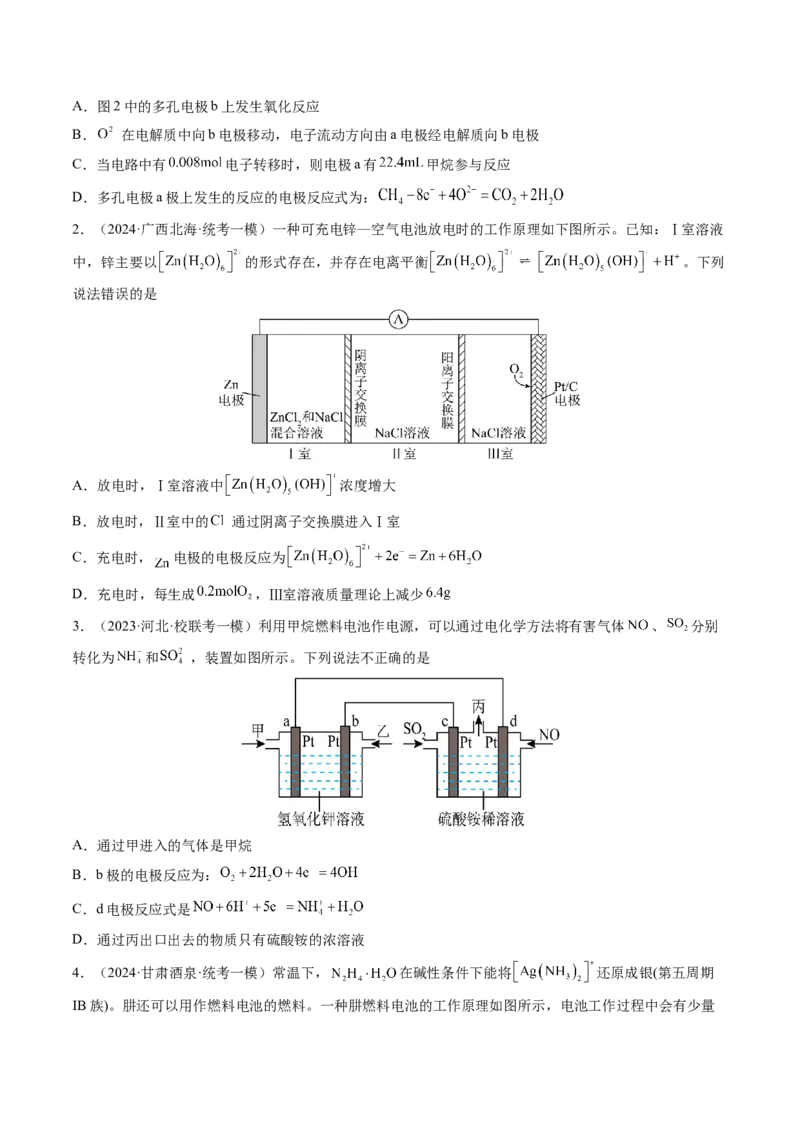
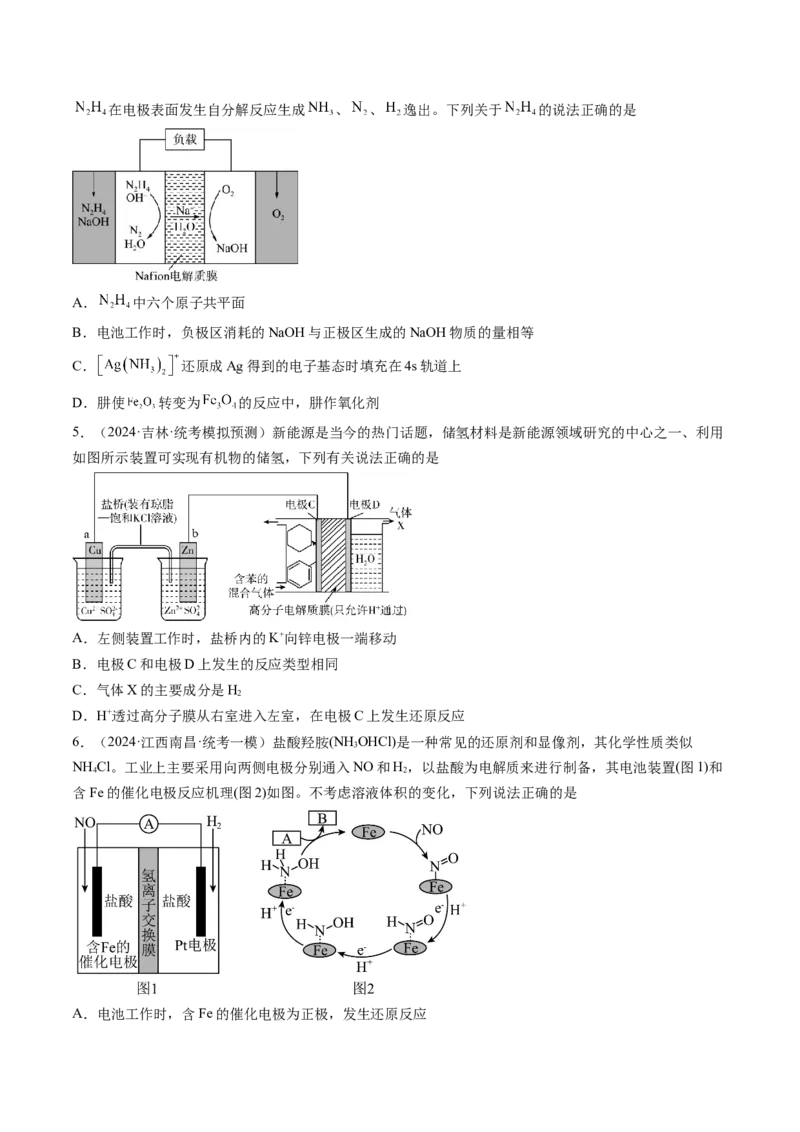
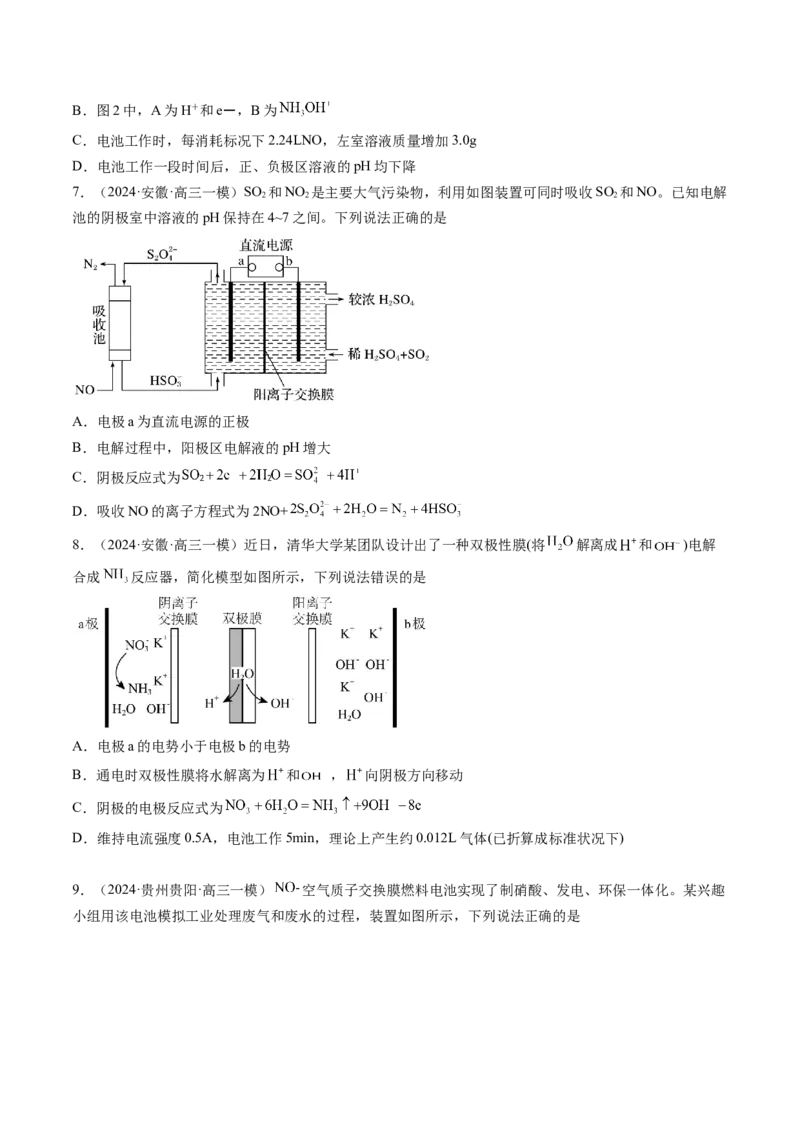
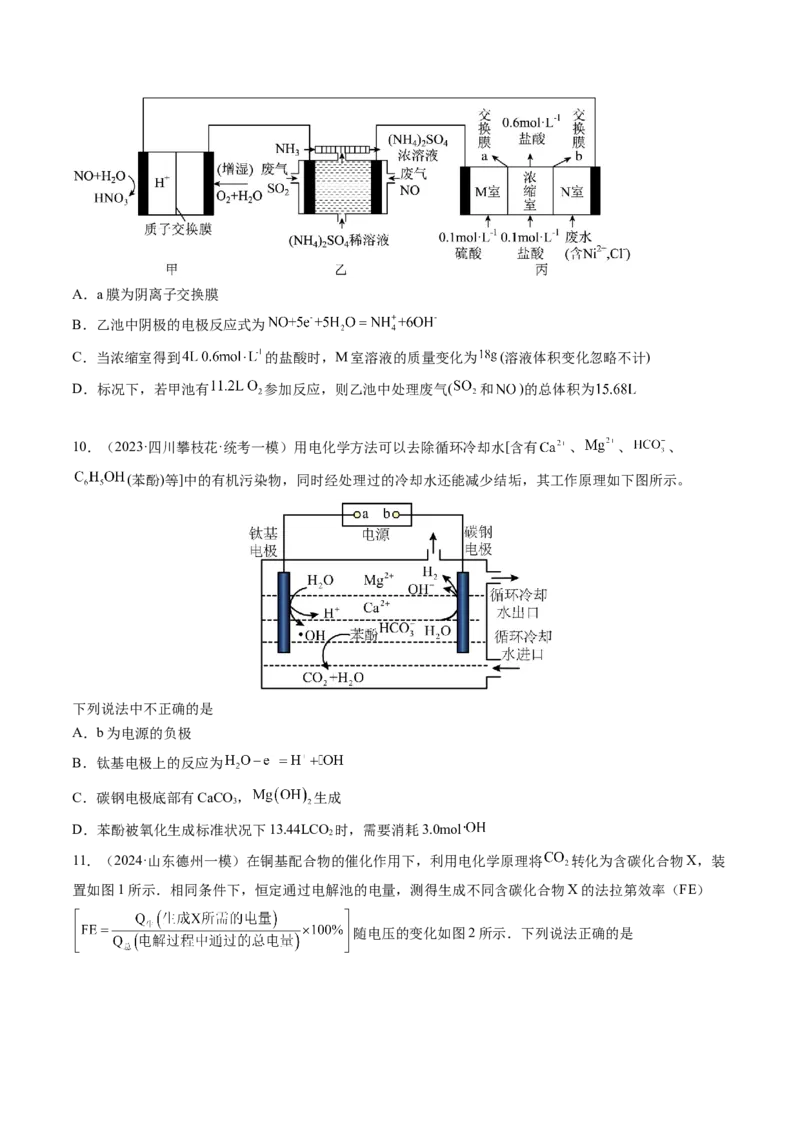
押新高考卷第 13-14 题
电化学原理与应用、电解质溶液曲线
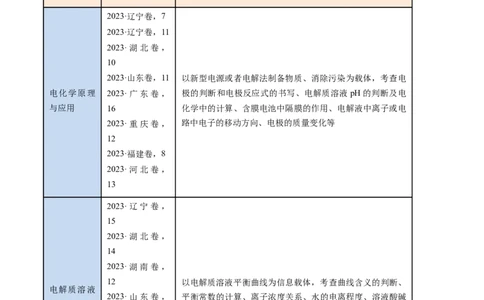
核心考点 考情统计 考向预测
2023·辽宁卷,7
2023·辽宁卷,11
2023·湖北卷,
10
2023·山东卷,11 以新型电源或者电解法制备物质、消除污染为载体,考查电
电化学原理 2023·广东卷, 极的判断和电极反应式的书写、电解质溶液pH的判断及电
与应用 16 化学中的计算、含膜电池中隔膜的作用、电解液中离子或电
2023·重庆卷, 路中电子的移动方向、电极的质量变化等
12
2023·福建卷,8
2023·河北卷,
13
2023·辽宁卷,
15
2023·湖北卷,
14
2023·湖南卷,
12 以电解质溶液平衡曲线为信息载体,考查曲线含义的判断、
电解质溶液
2023·山东卷, 平衡常数的计算、离子浓度关系、水的电离程度、溶液酸碱
曲线
15 性判断及变化等知识
2023·北京卷,
14
2023·福建卷,9
2023·河北卷,
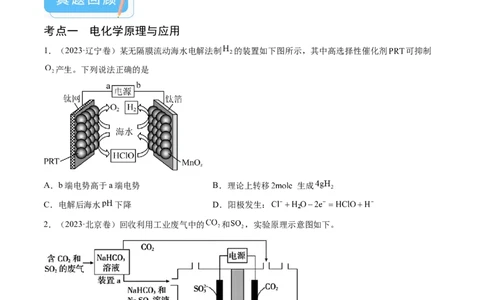
14考点一 电化学原理与应用
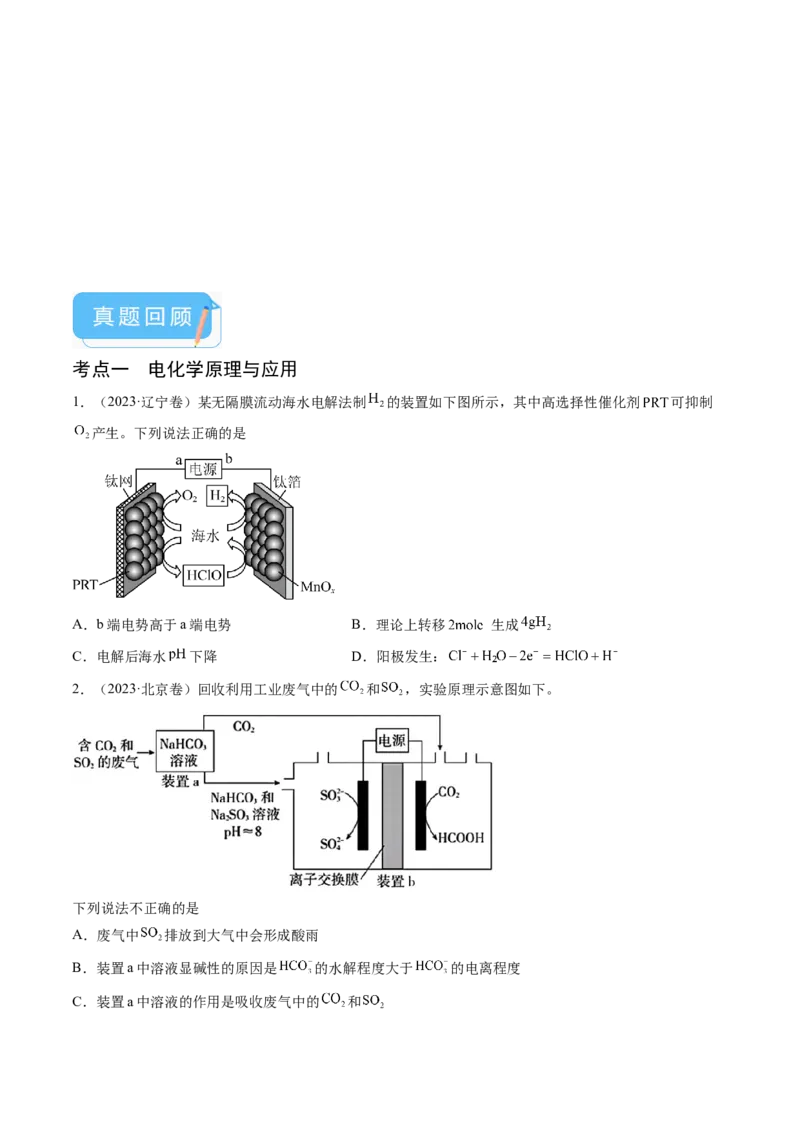
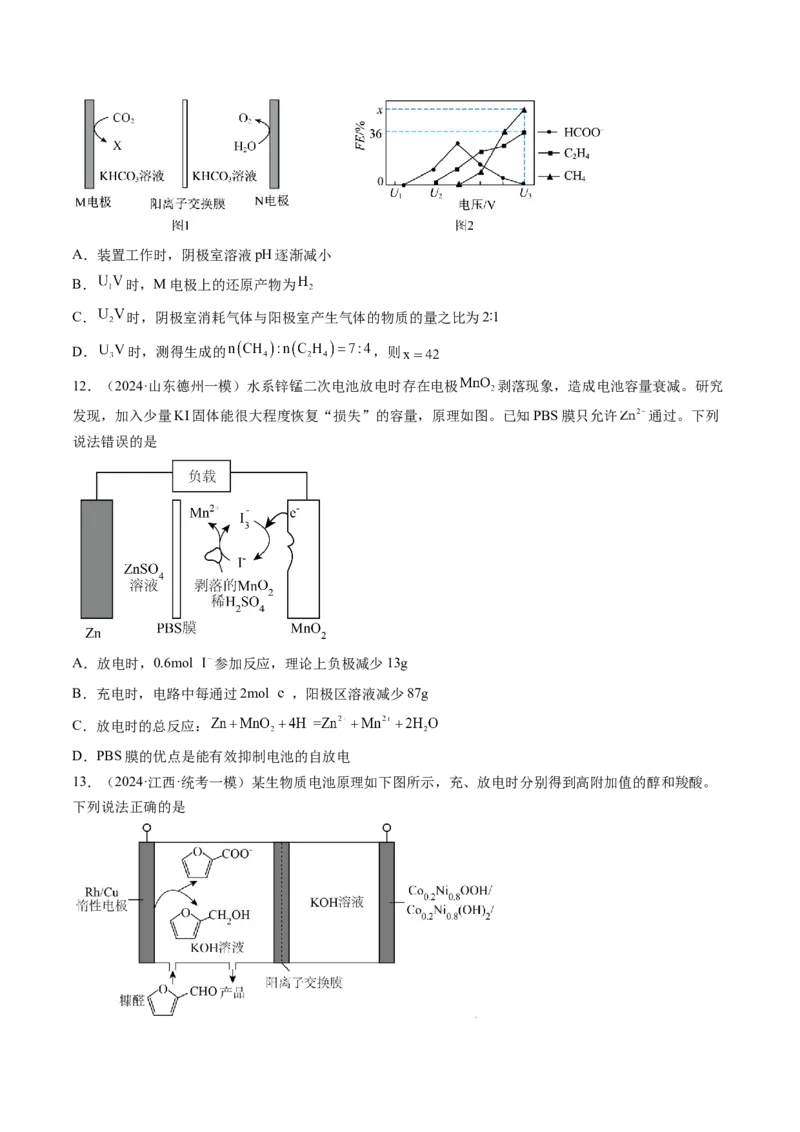
1.(2023·辽宁卷)某无隔膜流动海水电解法制 的装置如下图所示,其中高选择性催化剂 可抑制
产生。下列说法正确的是
A.b端电势高于a端电势 B.理论上转移 生成
C.电解后海水 下降 D.阳极发生:
2.(2023·北京卷)回收利用工业废气中的 和 ,实验原理示意图如下。
下列说法不正确的是
A.废气中 排放到大气中会形成酸雨
B.装置a中溶液显碱性的原因是 的水解程度大于 的电离程度
C.装置a中溶液的作用是吸收废气中的 和D.装置 中的总反应为
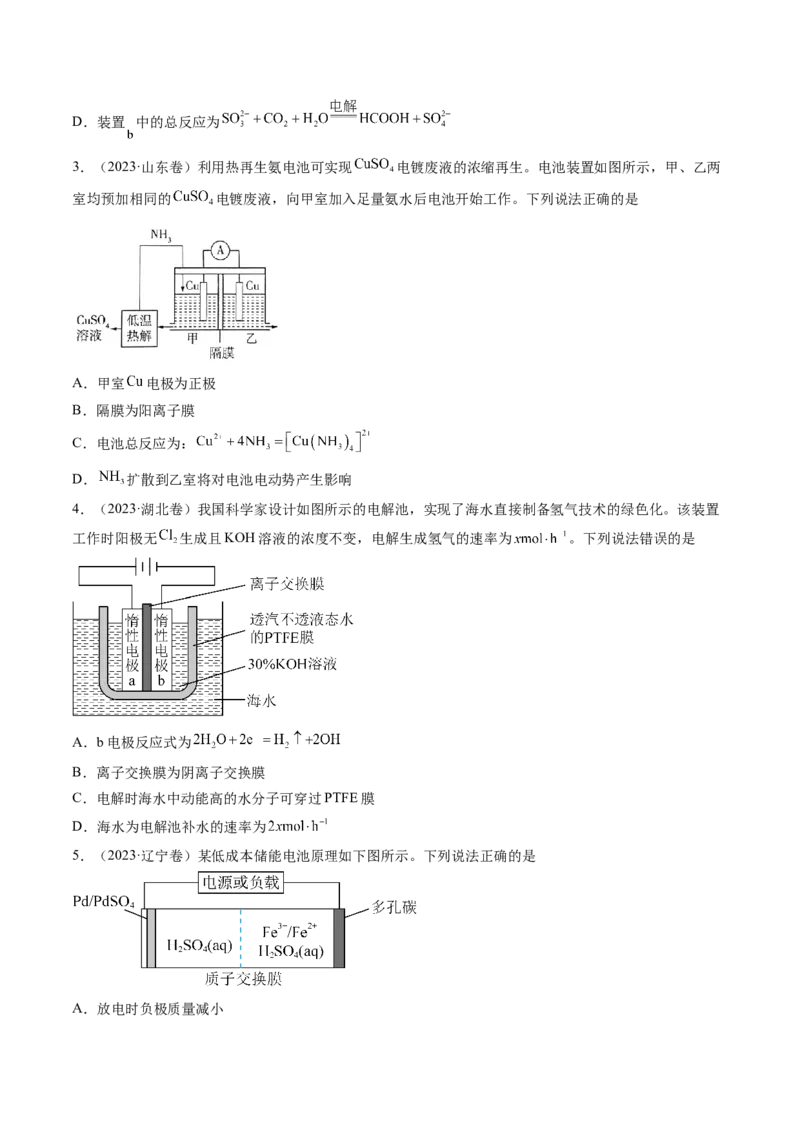
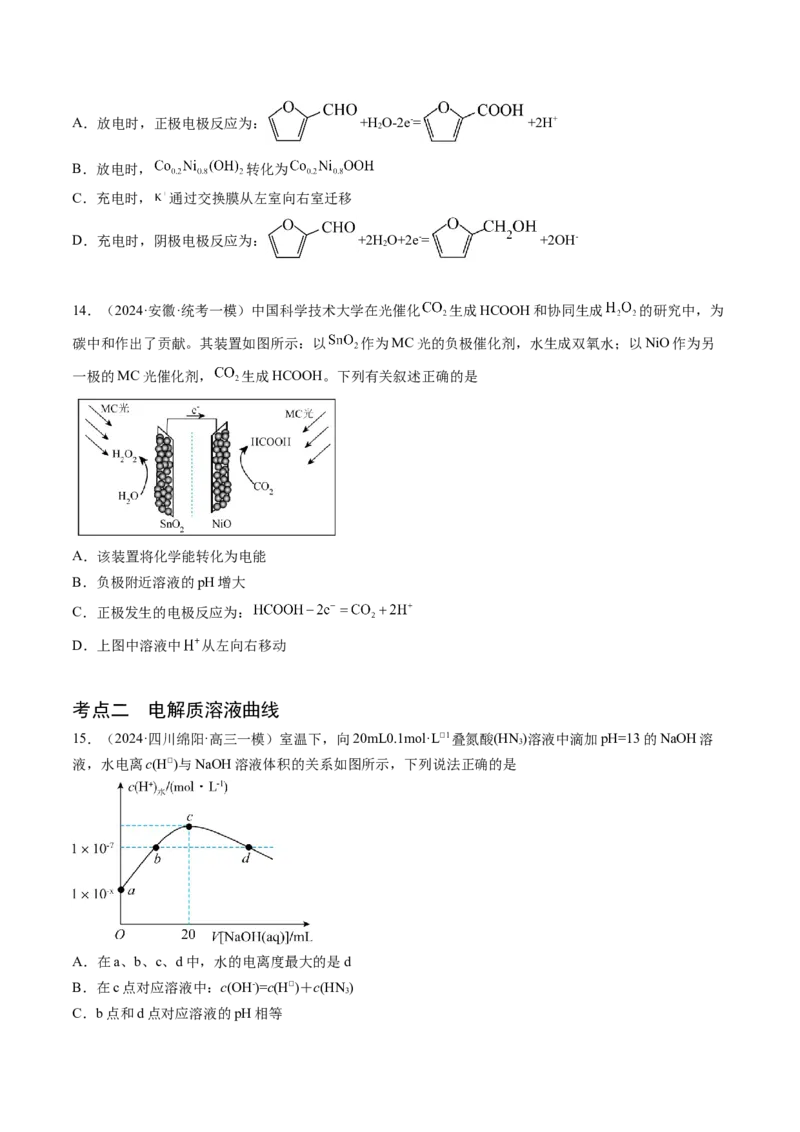
3.(2023·山东卷)利用热再生氨电池可实现 电镀废液的浓缩再生。电池装置如图所示,甲、乙两
室均预加相同的 电镀废液,向甲室加入足量氨水后电池开始工作。下列说法正确的是
A.甲室 电极为正极
B.隔膜为阳离子膜
C.电池总反应为:
D. 扩散到乙室将对电池电动势产生影响
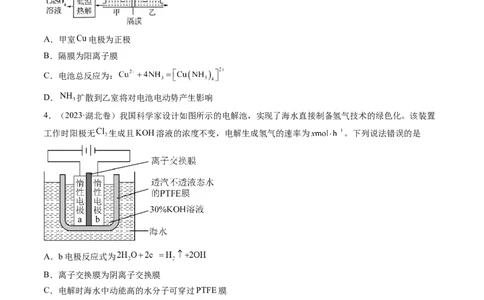
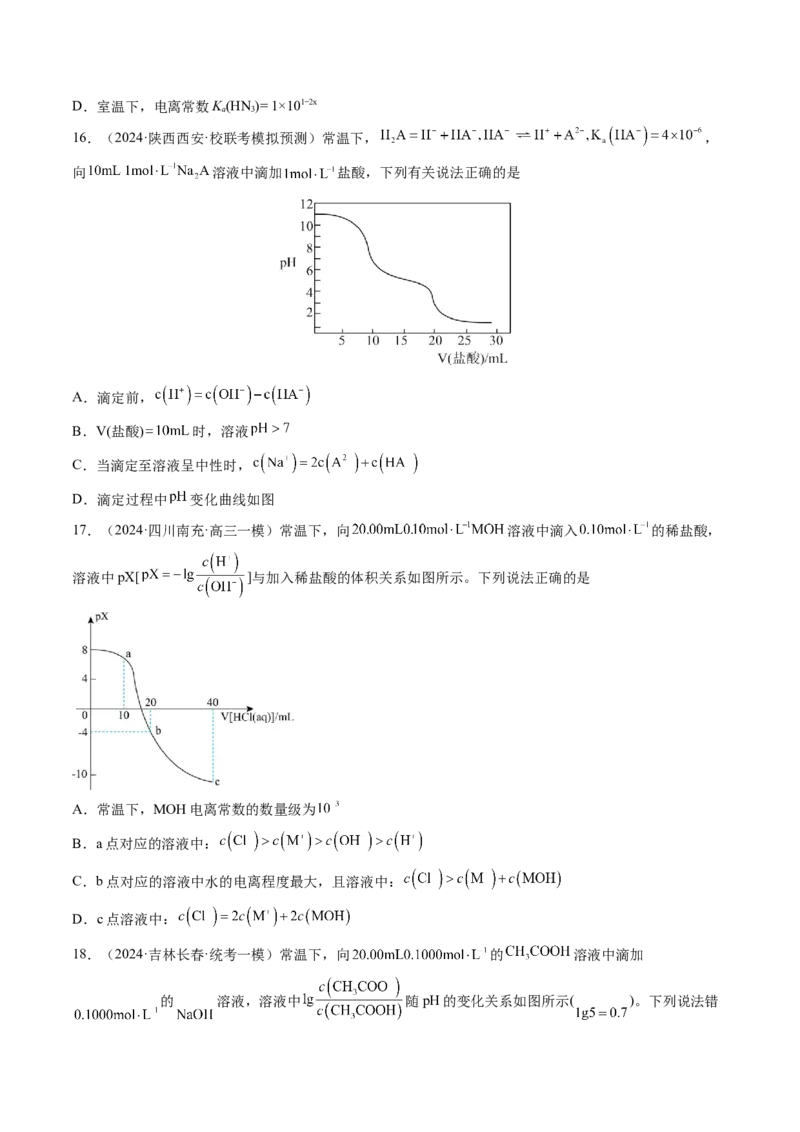
4.(2023·湖北卷)我国科学家设计如图所示的电解池,实现了海水直接制备氢气技术的绿色化。该装置
工作时阳极无 生成且KOH溶液的浓度不变,电解生成氢气的速率为 。下列说法错误的是
A.b电极反应式为
B.离子交换膜为阴离子交换膜
C.电解时海水中动能高的水分子可穿过PTFE膜
D.海水为电解池补水的速率为
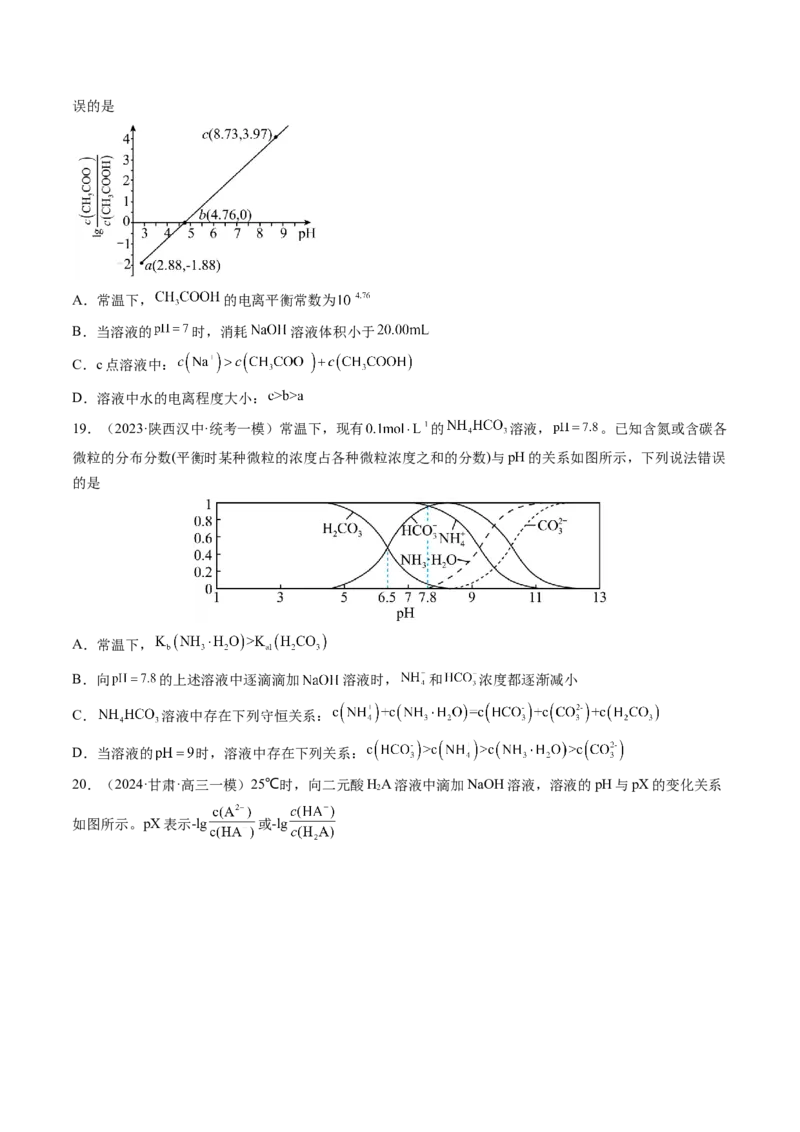
5.(2023·辽宁卷)某低成本储能电池原理如下图所示。下列说法正确的是
A.放电时负极质量减小B.储能过程中电能转变为化学能
C.放电时右侧 通过质子交换膜移向左侧
D.充电总反应:
考点二 电解质溶液曲线
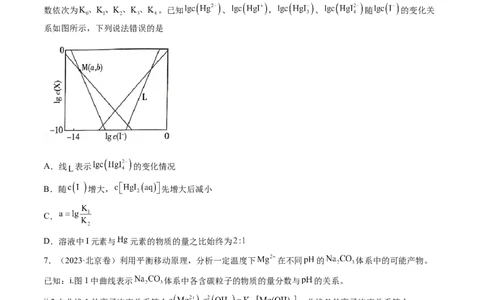
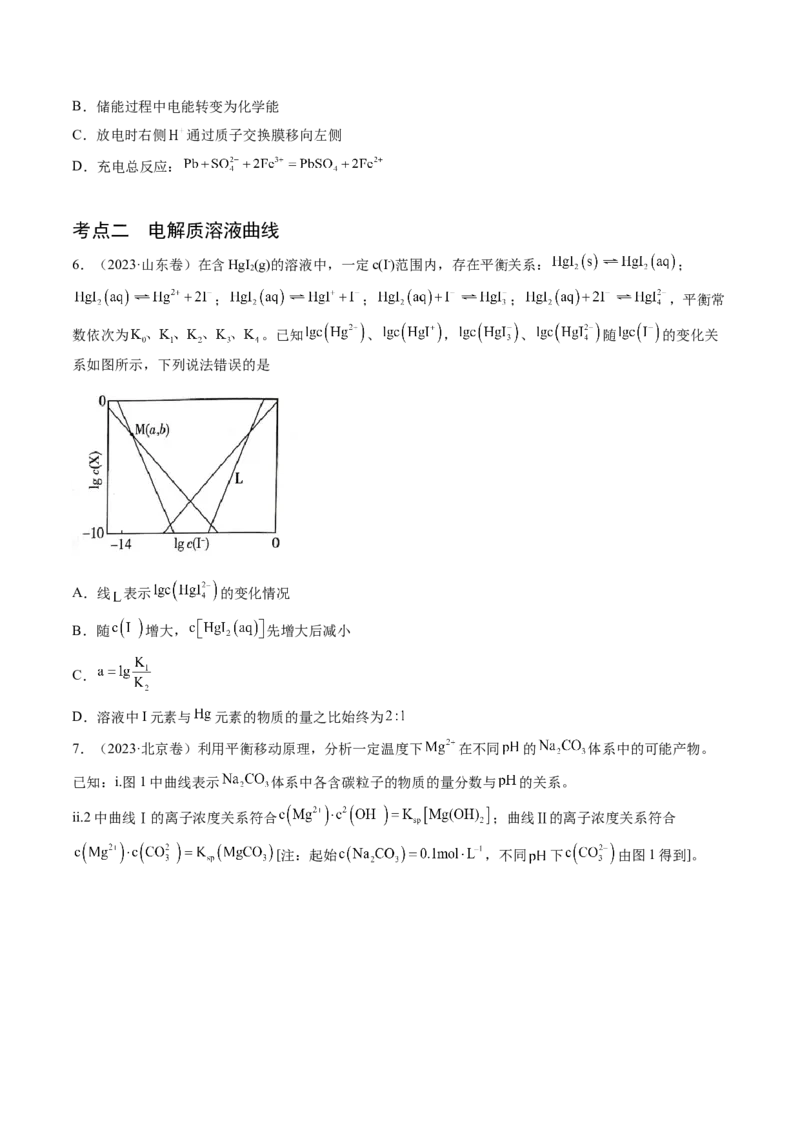
6.(2023·山东卷)在含HgI (g)的溶液中,一定c(I-)范围内,存在平衡关系: ;
2
; ; ; ,平衡常
数依次为 。已知 、 , 、 随 的变化关
系如图所示,下列说法错误的是
A.线 表示 的变化情况
B.随 增大, 先增大后减小
C.
D.溶液中I元素与 元素的物质的量之比始终为
7.(2023·北京卷)利用平衡移动原理,分析一定温度下 在不同 的 体系中的可能产物。
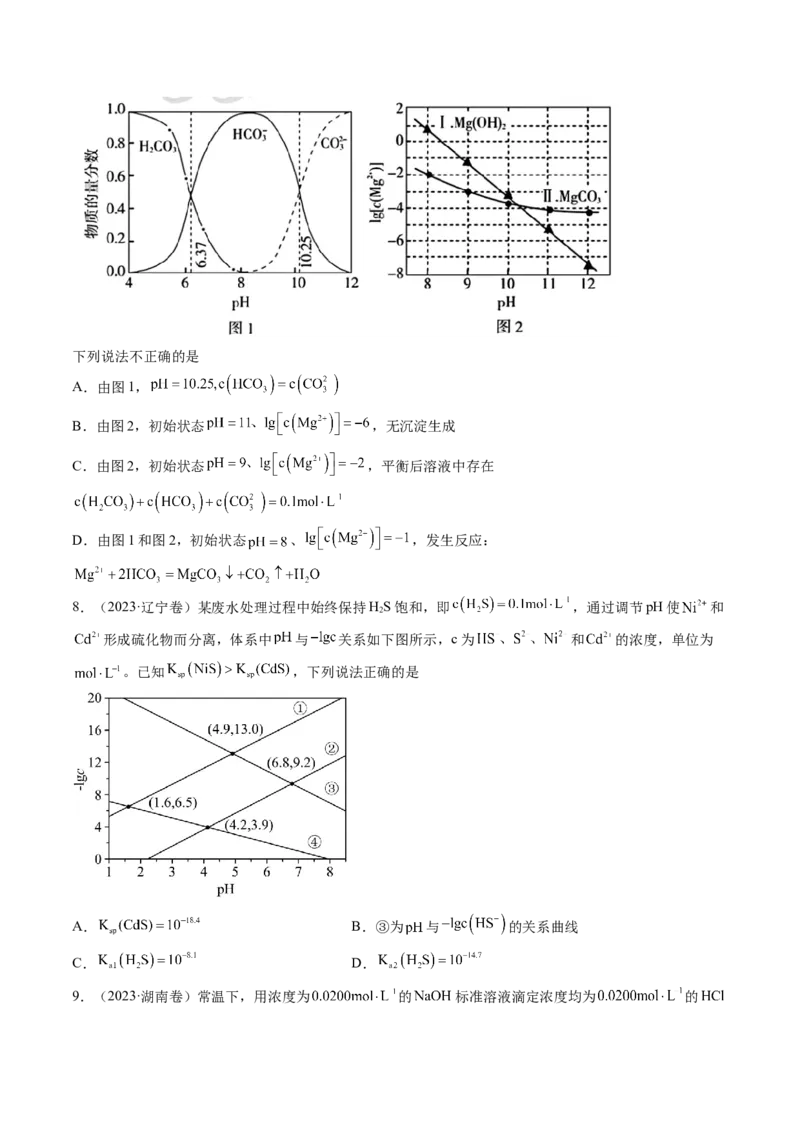
已知:i.图1中曲线表示 体系中各含碳粒子的物质的量分数与 的关系。
ii.2中曲线Ⅰ的离子浓度关系符合 ;曲线Ⅱ的离子浓度关系符合
[注:起始 ,不同 下 由图1得到]。下列说法不正确的是
A.由图1,
B.由图2,初始状态 ,无沉淀生成
C.由图2,初始状态 ,平衡后溶液中存在
D.由图1和图2,初始状态 、 ,发生反应:
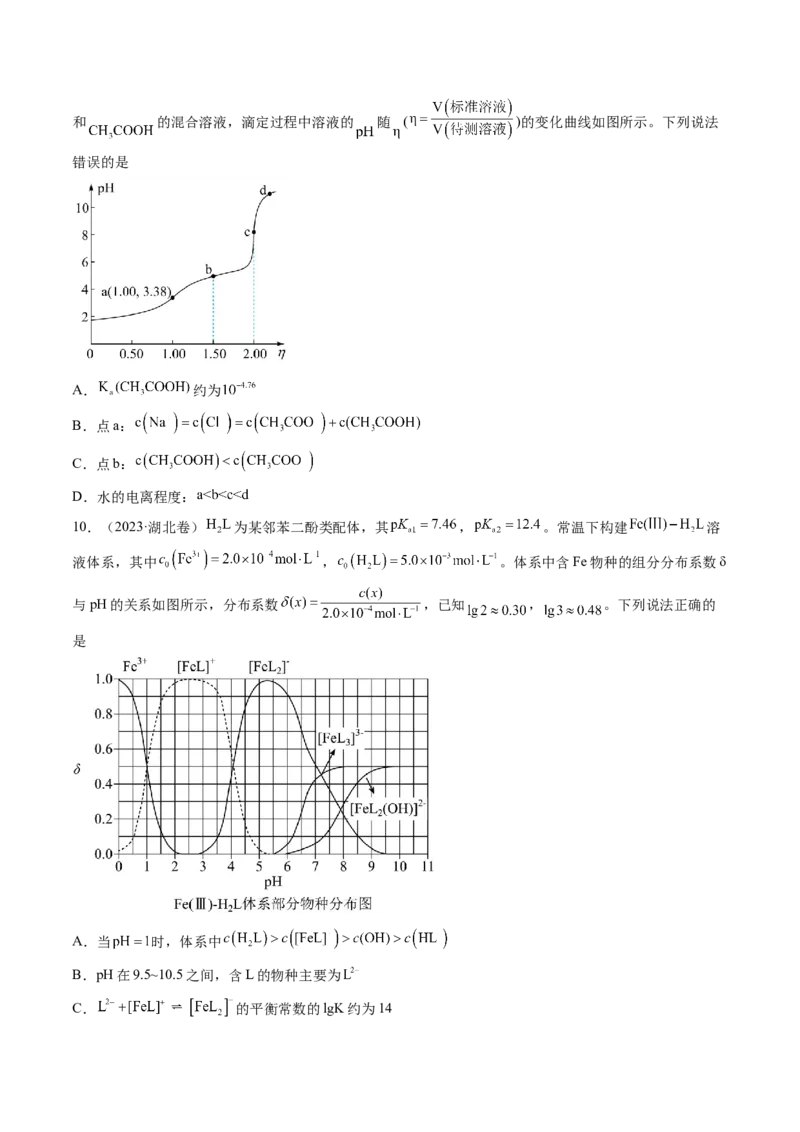
8.(2023·辽宁卷)某废水处理过程中始终保持HS饱和,即 ,通过调节pH使 和
2
形成硫化物而分离,体系中 与 关系如下图所示,c为 和 的浓度,单位为
。已知 ,下列说法正确的是
A. B.③为 与 的关系曲线
C. D.
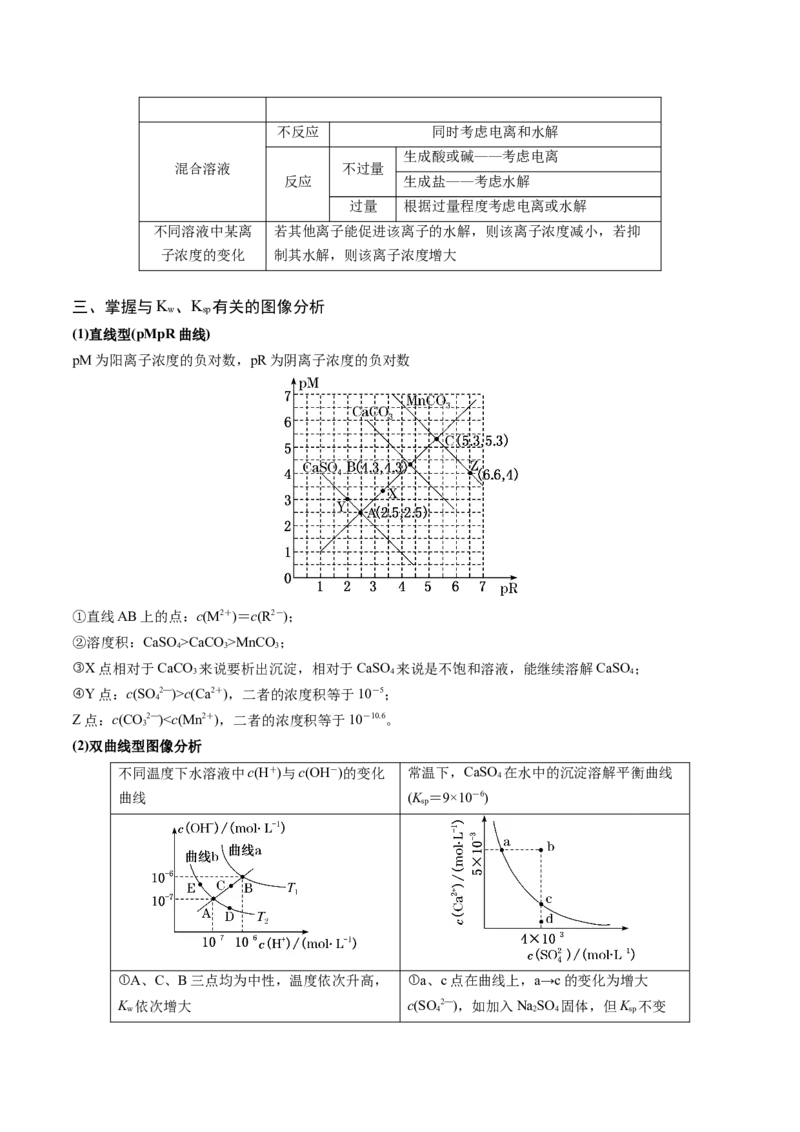
9.(2023·湖南卷)常温下,用浓度为 的 标准溶液滴定浓度均为 的和 的混合溶液,滴定过程中溶液的 随 ( )的变化曲线如图所示。下列说法
错误的是
A. 约为
B.点a:
C.点b:
D.水的电离程度:
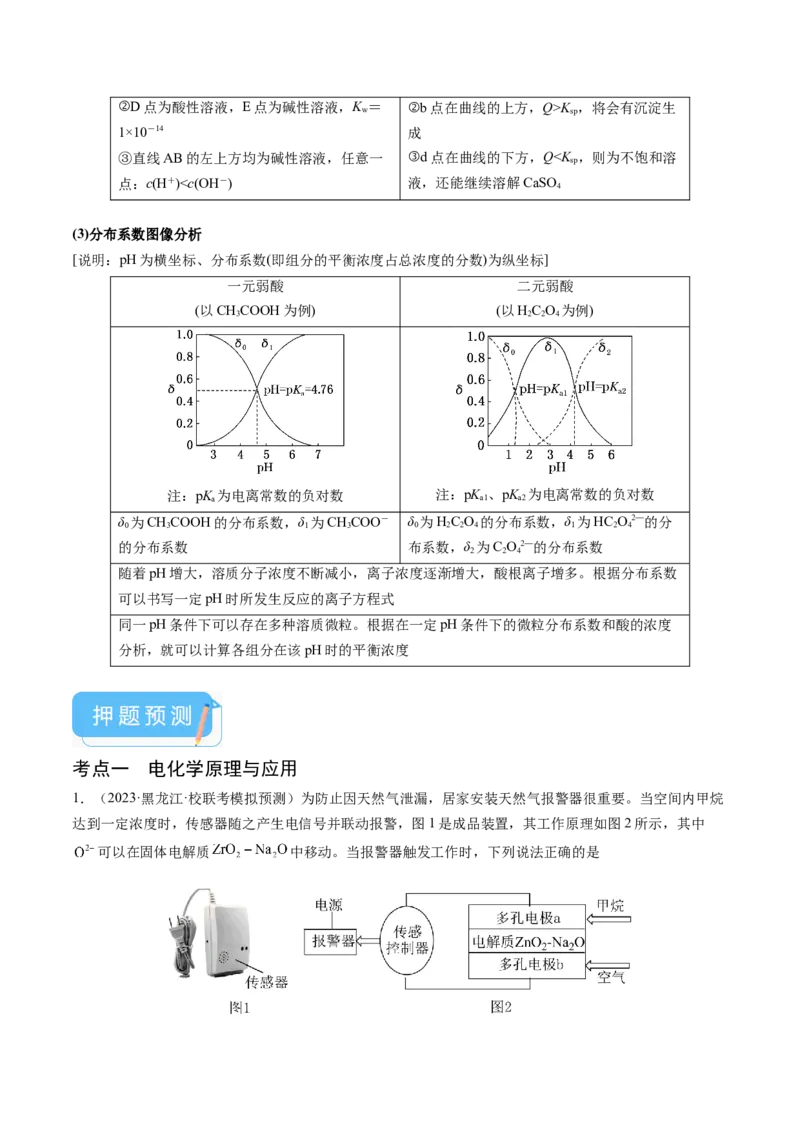
10.(2023·湖北卷) 为某邻苯二酚类配体,其 , 。常温下构建 溶
液体系,其中 , 。体系中含Fe物种的组分分布系数δ
与pH的关系如图所示,分布系数 ,已知 , 。下列说法正确的
是
A.当 时,体系中
B.pH在9.5~10.5之间,含L的物种主要为
C. 的平衡常数的lgK约为14D.当 时,参与配位的
一、溶液中各类平衡常数的计算方法及关系
(1)电离平衡常数(K)与电离度(α)的关系(以一元弱酸HA为例)
a
HA H+ + A-
起始浓度 c 0 0
酸
平衡浓度 c ·(1-α) c ·α c ·α
酸 酸 酸
K==。
a
若α很小,可认为1-α≈1,则K=c ·α2。
a 酸
(2)电离平衡常数与水解平衡常数的关系
①对于一元弱酸HA,K 与K 的关系
a h
HA H++A-,K(HA)=;
a
A-+HO HA+OH-,K (A-)=。
2 h
则K·K =c(H+)·c(OH-)=K ,故K =。
a h w h
②对于二元弱酸HB,K (H B)、K (H B)与K (HB-)、K (B2-)的关系
2 a1 2 a2 2 h h
HB-+HO HB+OH-,
2 2
K (HB-)===。
h
B2-+HO HB-+OH-,
2
K (B2-)===。
h
【特别提示】
常温时,对于一元弱酸HA,当K>1.0×10-7时,K <1.0×10-7,此时将等物质的量浓度的HA溶液与NaA溶
a h
液等体积混合,HA的电离程度大于A-的水解程度,溶液呈酸性;同理,当K<1.0×10-7时,K >1.0×10-
a h
7,A-的水解程度大于HA的电离程度,溶液呈碱性。对于多元弱酸,K =,K 是其阴离子结合一个H+所
h a
形成的粒子的电离平衡常数。
(3)溶度积常数(K )的相关计算
sp
①M(OH) 悬浊液中K 、K 、pH间的关系
n sp w
M(OH) (s) Mn+(aq)+nOH-(aq)
n
K =c(Mn+)·cn(OH-)=·cn(OH-)==。
sp
②K 与溶解度(S)之间的计算关系
sp
对于AB型物质,其K =。
sp
二、浓度大小比较解题思维模型
酸或碱溶液——考虑电离
单一溶液
盐溶液——考虑水解不反应 同时考虑电离和水解
生成酸或碱——考虑电离
混合溶液 不过量
反应 生成盐——考虑水解
过量 根据过量程度考虑电离或水解
不同溶液中某离 若其他离子能促进该离子的水解,则该离子浓度减小,若抑
子浓度的变化 制其水解,则该离子浓度增大
三、掌握与K 、K 有关的图像分析
w sp
(1)直线型(pMpR曲线)
pM为阳离子浓度的负对数,pR为阴离子浓度的负对数
①直线AB上的点:c(M2+)=c(R2-);
②溶度积:CaSO>CaCO >MnCO;
4 3 3
③X点相对于CaCO 来说要析出沉淀,相对于CaSO 来说是不饱和溶液,能继续溶解CaSO;
3 4 4
④Y点:c(SO 2—)>c(Ca2+),二者的浓度积等于10-5;
4
Z点:c(CO2—)K
sp
,将会有沉淀生
1×10-14 成
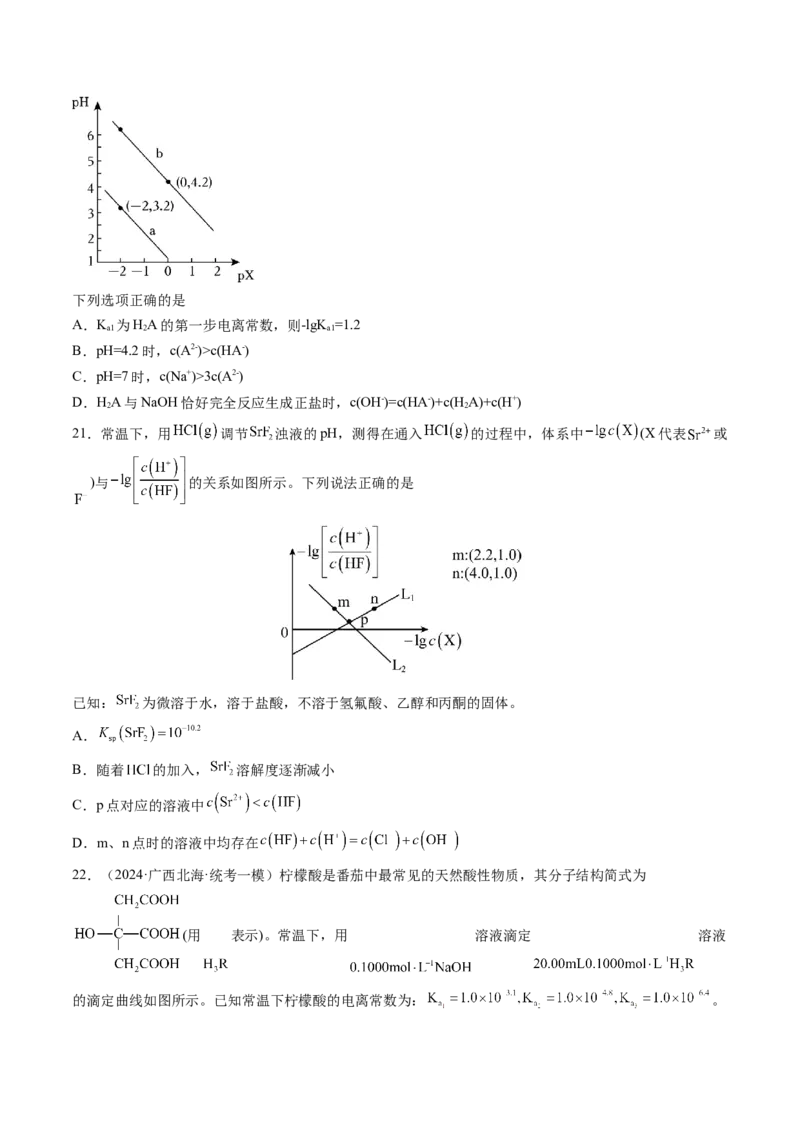
③直线AB的左上方均为碱性溶液,任意一 ③d点在曲线的下方,Qc(HA-)
C.pH=7时,c(Na+)>3c(A2-)
D.HA与NaOH恰好完全反应生成正盐时,c(OH-)=c(HA-)+c(H A)+c(H+)
2 2
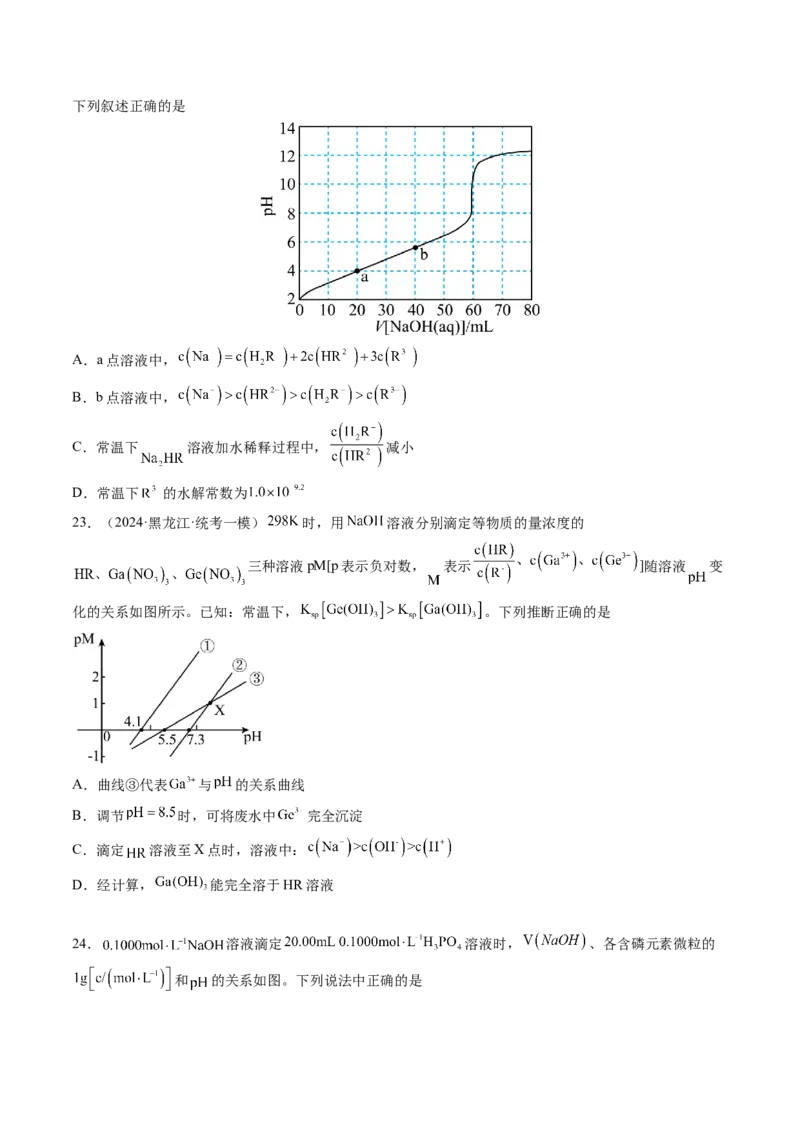
21.常温下,用 调节 浊液的pH,测得在通入 的过程中,体系中 (X代表 或
)与 的关系如图所示。下列说法正确的是
已知: 为微溶于水,溶于盐酸,不溶于氢氟酸、乙醇和丙酮的固体。
A.
B.随着 的加入, 溶解度逐渐减小
C.p点对应的溶液中
D.m、n点时的溶液中均存在
22.(2024·广西北海·统考一模)柠檬酸是番茄中最常见的天然酸性物质,其分子结构简式为
(用 表示)。常温下,用 溶液滴定 溶液
的滴定曲线如图所示。已知常温下柠檬酸的电离常数为: 。下列叙述正确的是
A.a点溶液中,
B.b点溶液中,
C.常温下 溶液加水稀释过程中, 减小
D.常温下 的水解常数为
23.(2024·黑龙江·统考一模) 时,用 溶液分别滴定等物质的量浓度的
三种溶液pM[p表示负对数, 表示 ]随溶液 变
化的关系如图所示。已知:常温下, 。下列推断正确的是
A.曲线③代表 与 的关系曲线
B.调节 时,可将废水中 完全沉淀
C.滴定 溶液至X点时,溶液中:
D.经计算, 能完全溶于HR溶液
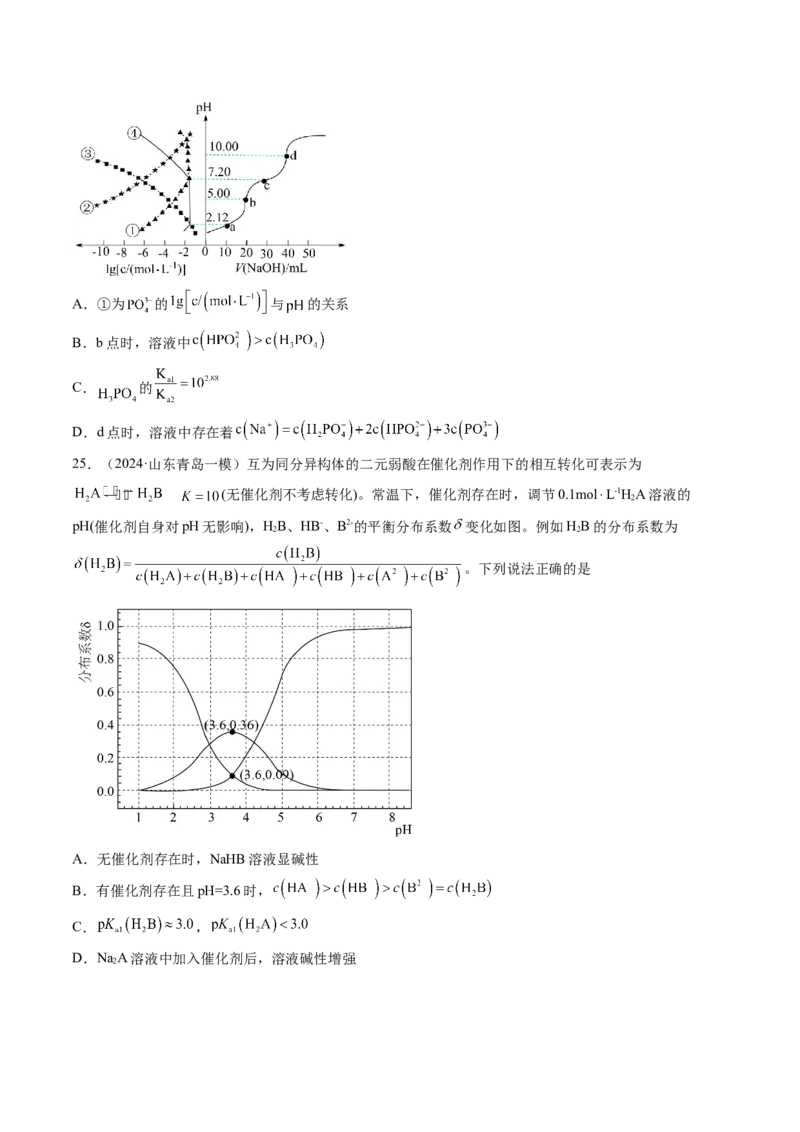
24. 溶液滴定 溶液时, 、各含磷元素微粒的
和 的关系如图。下列说法中正确的是A.①为 的 与 的关系
B.b点时,溶液中
C. 的
D.d点时,溶液中存在着
25.(2024·山东青岛一模)互为同分异构体的二元弱酸在催化剂作用下的相互转化可表示为
(无催化剂不考虑转化)。常温下,催化剂存在时,调节0.1mol⋅L-1HA溶液的
2
pH(催化剂自身对pH无影响),HB、HB-、B2-的平衡分布系数 变化如图。例如HB的分布系数为
2 2
。下列说法正确的是
A.无催化剂存在时,NaHB溶液显碱性
B.有催化剂存在且pH=3.6时,
C. ,
D.NaA溶液中加入催化剂后,溶液碱性增强
2