文档内容
2023 学年度第一学期初三一模
化学试题
(满分100分,考试时间90分钟)
考生注意:请将答案填写在答题卷对应的方框内。
可能用到的相对原子质量:H-1 C-12 O-16 Ca-40
一、选择题(本大题共25小题,共30分)
1~20题均只有一个正确选项
1. 银元素的符号是
A. Ag B. A1 C. Mg D. Hg
2. 空气中体积最大的物质是
A. 氧气 B. 氮气 C. 水蒸气 D. 二氧化碳
3. Fe O 中Fe的化合价是
2 3
A. -3 B. -2 C. +2 D. +3
4. 属于同素异形体的一组物质是
A. 一氧化碳和二氧化碳 B. 水和双氧水
C. 金刚石和石墨 D. 氧气和液氧
5. 物质的命名与化学式一致的是
A. 氯化钙CaCl B. 硫酸钠NaSO C. 碳酸钠NaCO D. 氢氧化钡BaOH
2 2 3 3
6. 能与水形成溶液的是
A. 泥沙 B. 淀粉 C. 豆油 D. 蔗糖
7. 有关碳酸钙的说法,正确的是
A. 蓝色固体 B. 易溶于水 C. 属于氧化物 D. 组成中含原子团
8. 关于粗盐提纯的实验,说法正确的是
A. 粗盐不可以放在烧杯里称量 B. 涉及的分离操作有过滤和蒸发
C. 蒸发皿不可以直接加热 D. 蒸发时发现有固体开始析出,立即停止加热
9. 化学方程式书写正确的是
A. B.
C. D.的
10. 物质在氧气中燃烧 现象描述错误的是
A. 镁:白色火焰 B. 硫:蓝紫色火焰
C. 氢气:淡蓝色火焰 D. 一氧化碳:蓝色火焰
11. 物质的用途只体现其物理性质的是
A. N:作保护气 B. CaO:加热食品 C. CO:冶炼金属 D. CO:作制冷剂
2 2
12. 下列归类正确的是( )
选项 内容 归类
A 风能、太阳能 绿色能源
B PM 、CO 空气污染物
2.5 2
C 胆矾、面粉 晶体
D 稀硫酸、氯化钠溶液 酸性溶液
A. A B. B C. C D. D
13. 如图所示,用启普发生器制取二氧化碳,加入稀盐酸的量,适宜的位置是
A. 甲 B. 乙 C. 丙 D. 丁
14. 对下列宏观事实的微观解释,合理的是
A. 空气湿度增大:单位体积空气中水分子数目增多
B. 石墨一定条件下转变成金刚石:碳原子种类发生改变
C. 二氧化碳制成干冰:二氧化碳分子由运动变为静止
D. 水加热成水蒸气:水分子体积变大
15. 说法正确的是
A. 摩尔是基本物理量 B. 摩尔质量就是指1mol物质的质量
C. 物质的量就是微粒的数量 D. 1mol任何物质含6.02×1023个微粒
16. 有关分子、原子的说法正确的是
A. 分子在化学反应前后不发生改变 B. 同种原子构成的物质是纯净物
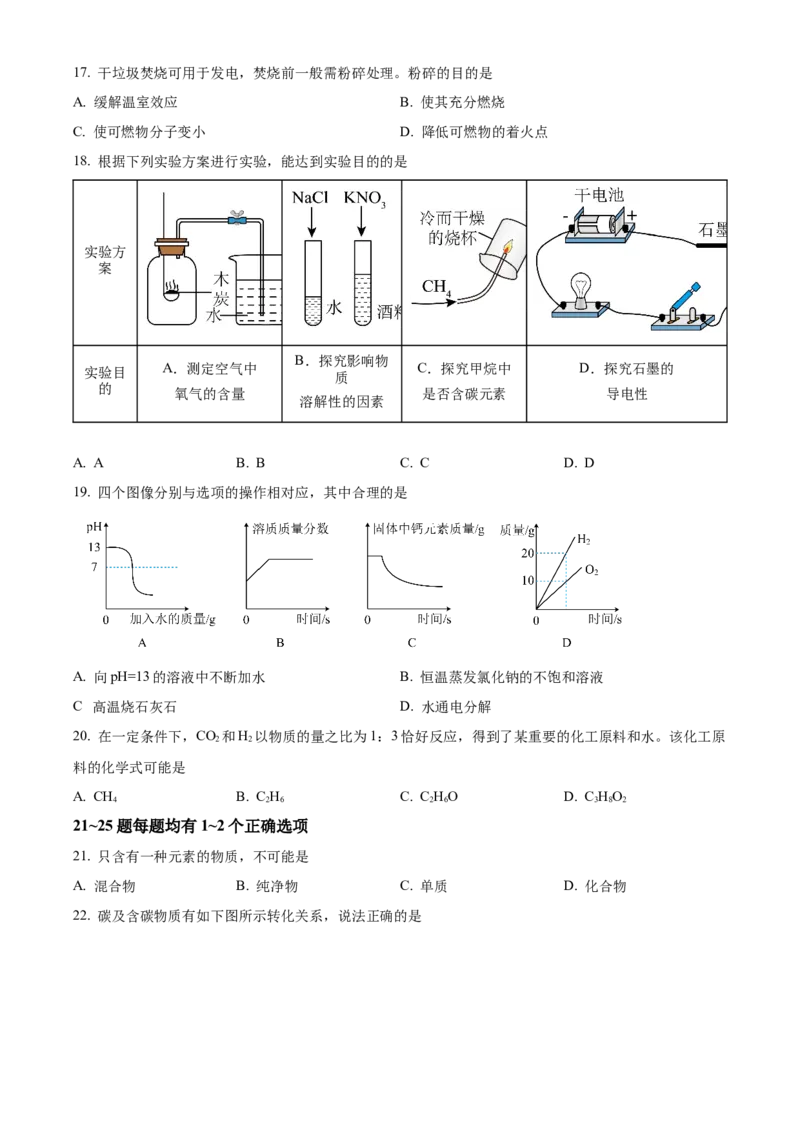
C. 分子的质量可能比原子的质量小 D. 原子是不可再分的最小微粒17. 干垃圾焚烧可用于发电,焚烧前一般需粉碎处理。粉碎的目的是
A. 缓解温室效应 B. 使其充分燃烧
C. 使可燃物分子变小 D. 降低可燃物的着火点
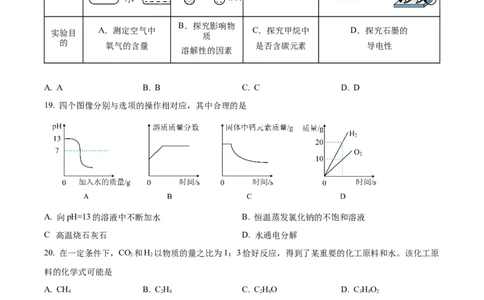
18. 根据下列实验方案进行实验,能达到实验目的的是
实验方
案
B.探究影响物
A.测定空气中 C.探究甲烷中 D.探究石墨的
实验目
质
的
氧气的含量 是否含碳元素 导电性
溶解性的因素
A. A B. B C. C D. D
19. 四个图像分别与选项的操作相对应,其中合理的是
A. 向pH=13的溶液中不断加水 B. 恒温蒸发氯化钠的不饱和溶液
.
C 高温烧石灰石 D. 水通电分解
20. 在一定条件下,CO 和H 以物质的量之比为1:3恰好反应,得到了某重要的化工原料和水。该化工原
2 2
料的化学式可能是
A. CH B. C H C. C HO D. C HO
4 2 6 2 6 3 8 2
21~25题每题均有1~2个正确选项
21. 只含有一种元素的物质,不可能是
A. 混合物 B. 纯净物 C. 单质 D. 化合物
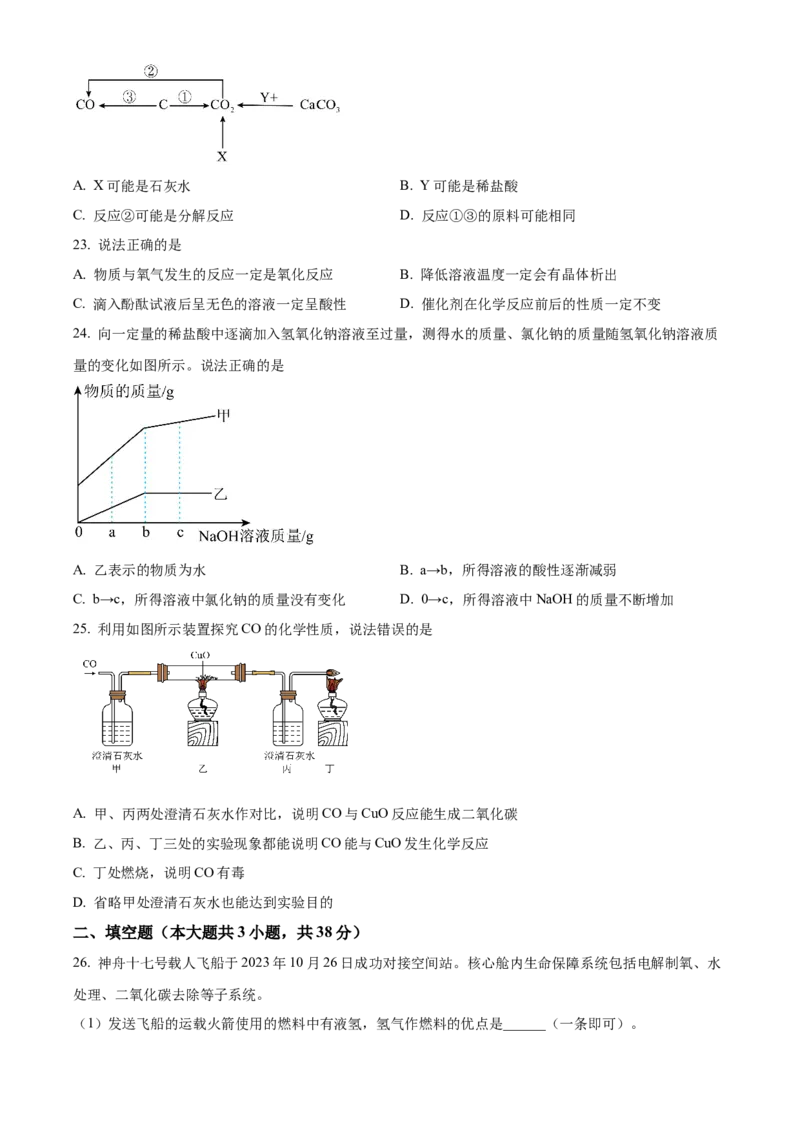
22. 碳及含碳物质有如下图所示转化关系,说法正确的是A. X可能是石灰水 B. Y可能是稀盐酸
C. 反应②可能是分解反应 D. 反应①③的原料可能相同
23. 说法正确的是
A. 物质与氧气发生的反应一定是氧化反应 B. 降低溶液温度一定会有晶体析出
C. 滴入酚酞试液后呈无色的溶液一定呈酸性 D. 催化剂在化学反应前后的性质一定不变
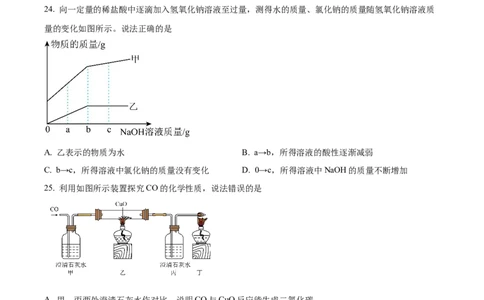
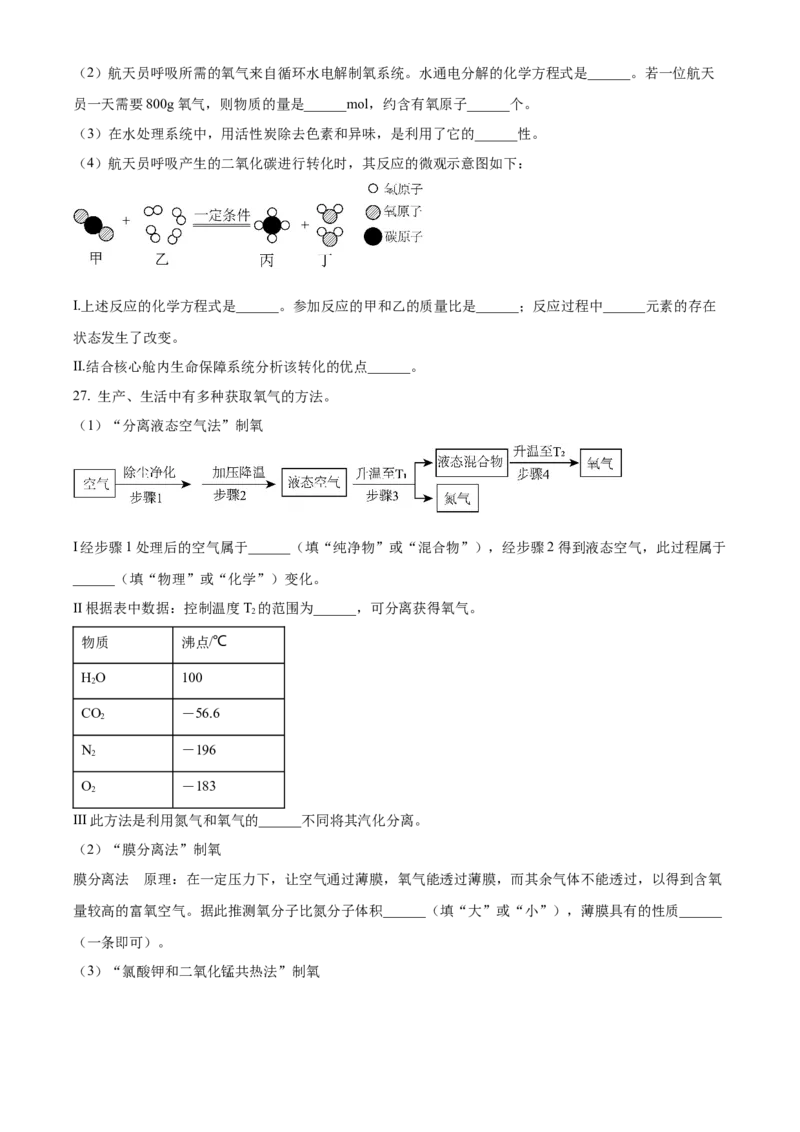
24. 向一定量的稀盐酸中逐滴加入氢氧化钠溶液至过量,测得水的质量、氯化钠的质量随氢氧化钠溶液质
量的变化如图所示。说法正确的是
A. 乙表示的物质为水 B. a→b,所得溶液的酸性逐渐减弱
C. b→c,所得溶液中氯化钠的质量没有变化 D. 0→c,所得溶液中NaOH的质量不断增加
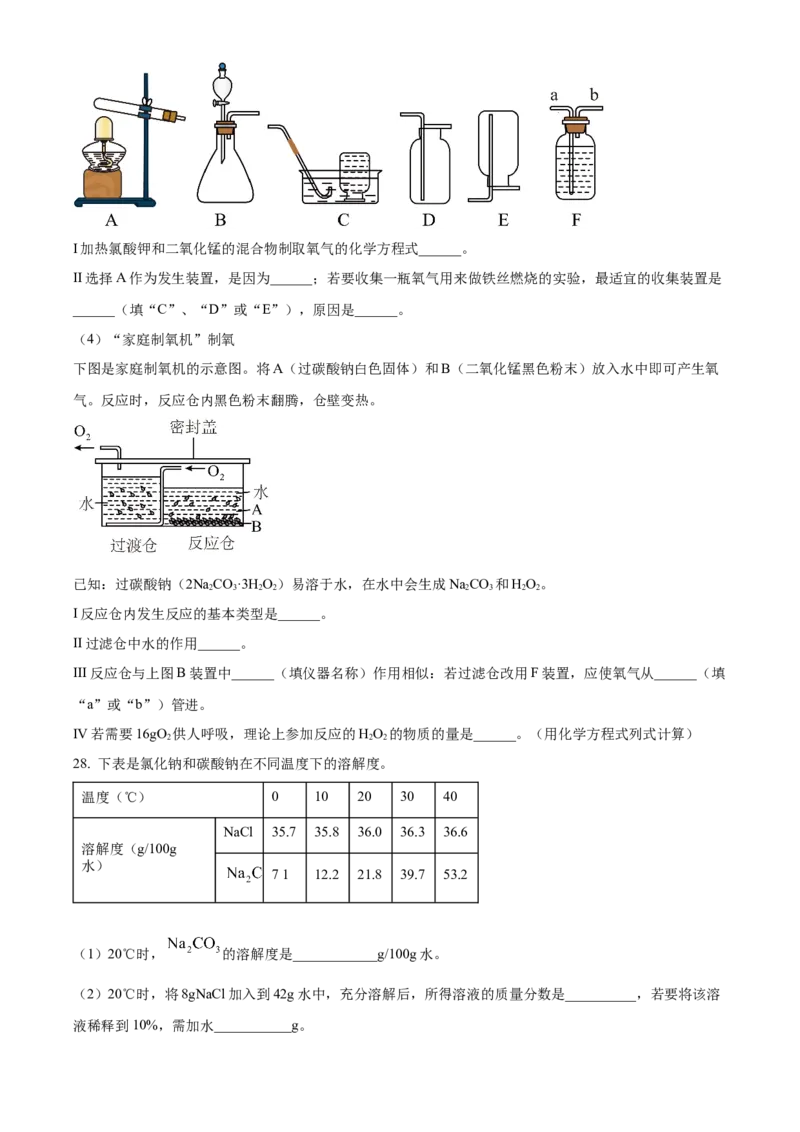
25. 利用如图所示装置探究CO的化学性质,说法错误的是
A. 甲、丙两处澄清石灰水作对比,说明CO与CuO反应能生成二氧化碳
B. 乙、丙、丁三处的实验现象都能说明CO能与CuO发生化学反应
C. 丁处燃烧,说明CO有毒
D. 省略甲处澄清石灰水也能达到实验目的
二、填空题(本大题共3小题,共38分)
26. 神舟十七号载人飞船于2023年10月26日成功对接空间站。核心舱内生命保障系统包括电解制氧、水
处理、二氧化碳去除等子系统。
(1)发送飞船的运载火箭使用的燃料中有液氢,氢气作燃料的优点是______(一条即可)。(2)航天员呼吸所需的氧气来自循环水电解制氧系统。水通电分解的化学方程式是______。若一位航天
员一天需要800g氧气,则物质的量是______mol,约含有氧原子______个。
(3)在水处理系统中,用活性炭除去色素和异味,是利用了它的______性。
(4)航天员呼吸产生的二氧化碳进行转化时,其反应的微观示意图如下:
I.上述反应的化学方程式是______。参加反应的甲和乙的质量比是______;反应过程中______元素的存在
状态发生了改变。
II.结合核心舱内生命保障系统分析该转化的优点______。
27. 生产、生活中有多种获取氧气的方法。
(1)“分离液态空气法”制氧
I经步骤1处理后的空气属于______(填“纯净物”或“混合物”),经步骤2得到液态空气,此过程属于
______(填“物理”或“化学”)变化。
II根据表中数据:控制温度T 的范围为______,可分离获得氧气。
2
物质 沸点/℃
HO 100
2
CO -56.6
2
N -196
2
O -183
2
III此方法是利用氮气和氧气的______不同将其汽化分离。
(2)“膜分离法”制氧
膜分离法 的原理:在一定压力下,让空气通过薄膜,氧气能透过薄膜,而其余气体不能透过,以得到含氧
量较高的富氧空气。据此推测氧分子比氮分子体积______(填“大”或“小”),薄膜具有的性质______
(一条即可)。
(3)“氯酸钾和二氧化锰共热法”制氧I加热氯酸钾和二氧化锰的混合物制取氧气的化学方程式______。
II选择A作为发生装置,是因为______;若要收集一瓶氧气用来做铁丝燃烧的实验,最适宜的收集装置是
______(填“C”、“D”或“E”),原因是______。
(4)“家庭制氧机”制氧
下图是家庭制氧机的示意图。将A(过碳酸钠白色固体)和B(二氧化锰黑色粉末)放入水中即可产生氧
气。反应时,反应仓内黑色粉末翻腾,仓壁变热。
已知:过碳酸钠(2NaCO·3H O)易溶于水,在水中会生成NaCO 和HO。
2 3 2 2 2 3 2 2
I反应仓内发生反应的基本类型是______。
II过滤仓中水的作用______。
III反应仓与上图B装置中______(填仪器名称)作用相似:若过滤仓改用F装置,应使氧气从______(填
“a”或“b”)管进。
IV若需要16gO 供人呼吸,理论上参加反应的HO 的物质的量是______。(用化学方程式列式计算)
2 2 2
28. 下表是氯化钠和碳酸钠在不同温度下的溶解度。
温度(℃) 0 10 20 30 40
NaCl 35.7 35.8 36.0 36.3 36.6
溶解度(g/100g
.
水)
71 12.2 21.8 39.7 53.2
(1)20℃时, 的溶解度是____________g/100g水。
(2)20℃时,将8gNaCl加入到42g水中,充分溶解后,所得溶液的质量分数是__________,若要将该溶
液稀释到10%,需加水___________g。(3)我国很多的盐碱湖中溶有NaCl和 。“夏天晒盐”是人们利用__________(填“蒸发结晶”
或“降温结晶”)的方法获得粗盐,粗盐中的主要成分是____________(填“NaCl”或“ ”);
盐碱湖中 的质量分数较大的季节___________(填“夏季”或“冬季”)。分析表中数据,说明
冬天能“捞碱”的原因__________________。
(4)利用氯化钠和碳酸钠的溶解性差异,设计实验验证某白色固体是氯化钠还是碳酸钠。
_________________
三、简答题(本大题共4小题,共32分)
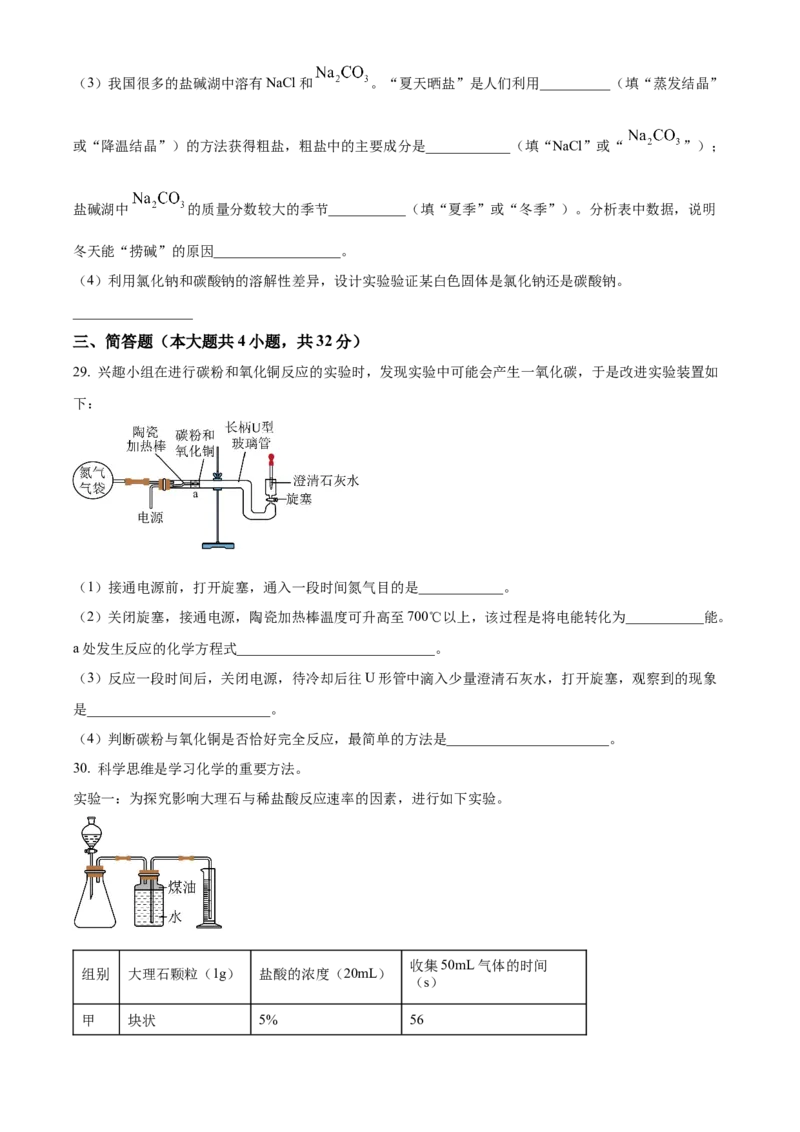
29. 兴趣小组在进行碳粉和氧化铜反应的实验时,发现实验中可能会产生一氧化碳,于是改进实验装置如
下:
(1)接通电源前,打开旋塞,通入一段时间氮气目的是____________。
(2)关闭旋塞,接通电源,陶瓷加热棒温度可升高至700℃以上,该过程是将电能转化为___________能。
a处发生反应的化学方程式____________________________。
(3)反应一段时间后,关闭电源,待冷却后往U形管中滴入少量澄清石灰水,打开旋塞,观察到的现象
是__________________________。
(4)判断碳粉与氧化铜是否恰好完全反应,最简单的方法是_______________________。
30. 科学思维是学习化学的重要方法。
实验一:为探究影响大理石与稀盐酸反应速率的因素,进行如下实验。
收集50mL气体的时间
组别 大理石颗粒(1g) 盐酸的浓度(20mL)
(s)
甲 块状 5% 56乙 块状 10% 31
丙 粉末状 10% M
(1)大理石与稀盐酸反应的化学方程式____________________________。
(2)为达成实验目的,装置中分液漏斗的作用是____________________________。
(3)甲乙组对比得出的实验结论是_______________________________。
(4)验证大理石颗粒大小对速率的影响,可选择_________组别作对比。
(5)上表中M的数据合理的是_________(填“ ”、“ ”或“ ”)。
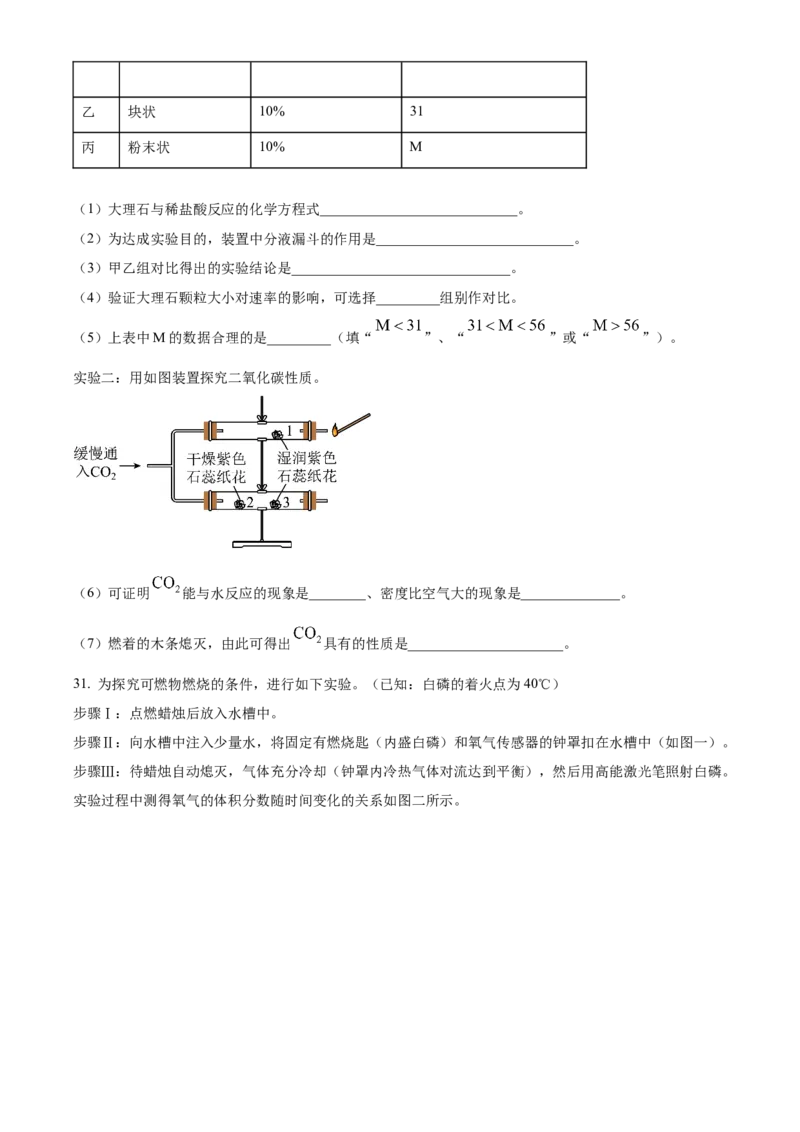
实验二:用如图装置探究二氧化碳性质。
(6)可证明 能与水反应的现象是________、密度比空气大的现象是______________。
(7)燃着的木条熄灭,由此可得出 具有的性质是______________________。
31. 为探究可燃物燃烧的条件,进行如下实验。(已知:白磷的着火点为40℃)
步骤Ⅰ:点燃蜡烛后放入水槽中。
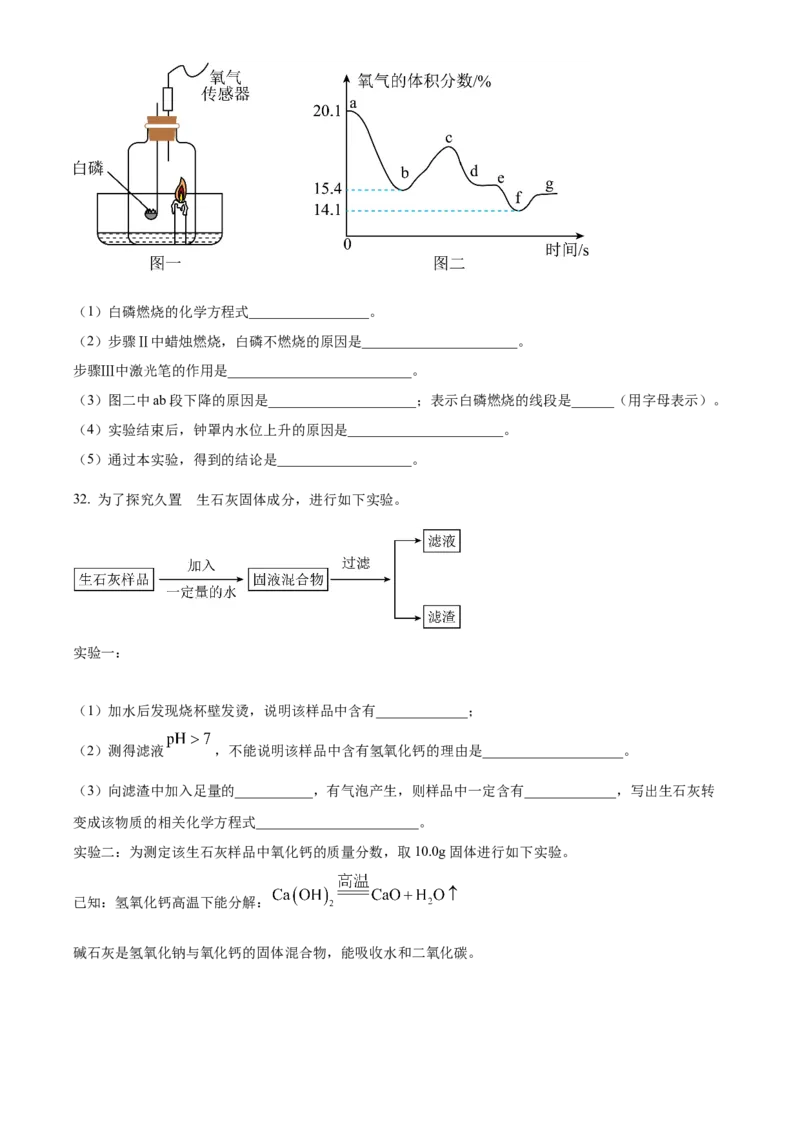
步骤Ⅱ:向水槽中注入少量水,将固定有燃烧匙(内盛白磷)和氧气传感器的钟罩扣在水槽中(如图一)。
步骤Ⅲ:待蜡烛自动熄灭,气体充分冷却(钟罩内冷热气体对流达到平衡),然后用高能激光笔照射白磷。
实验过程中测得氧气的体积分数随时间变化的关系如图二所示。(1)白磷燃烧的化学方程式_________________。
(2)步骤Ⅱ中蜡烛燃烧,白磷不燃烧的原因是______________________。
步骤Ⅲ中激光笔的作用是__________________________。
(3)图二中ab段下降的原因是_____________________;表示白磷燃烧的线段是______(用字母表示)。
(4)实验结束后,钟罩内水位上升的原因是______________________。
(5)通过本实验,得到的结论是___________________。
的
32. 为了探究久置 生石灰固体成分,进行如下实验。
实验一:
(1)加水后发现烧杯壁发烫,说明该样品中含有_____________;
(2)测得滤液 ,不能说明该样品中含有氢氧化钙的理由是____________________。
(3)向滤渣中加入足量的___________,有气泡产生,则样品中一定含有_____________,写出生石灰转
变成该物质的相关化学方程式_______________________。
实验二:为测定该生石灰样品中氧化钙的质量分数,取10.0g固体进行如下实验。
已知:氢氧化钙高温下能分解:
碱石灰是氢氧化钠与氧化钙的固体混合物,能吸收水和二氧化碳。连接装置,通一会儿空气,观察到C、D的质量不变时,点燃酒精喷灯,反应至C、D的质量不再增加,
继续通空气至装置冷却。测得C增重0.9g,D增重1.1g。
(4)实验前通入空气的目的是__________________________。
(5)通过___________________现象,说明生石灰样品中含有氢氧化钙。
(6)根据实验数据计算,该生石灰样品中氧化钙的质量分数为_____________。