文档内容
押新高考卷第 7-8 题
元素化合物的转化、物质的检验与鉴别、物质结构
与性质的应用和推理
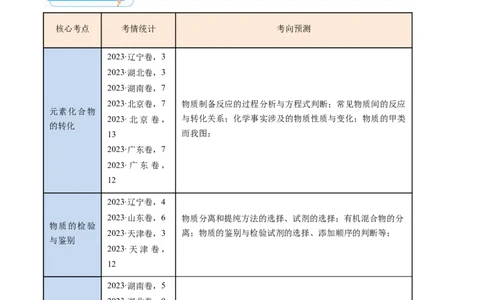
核心考点 考情统计 考向预测
2023·辽宁卷,3
2023·湖北卷,3
2023·湖南卷,7
2023·北京卷,7 物质制备反应的过程分析与方程式判断;常见物质间的反应
元素化合物
2023·北京卷, 与转化关系;化学事实涉及的物质性质与变化;物质的甲类
的转化
13 而我图;
2023·广东卷,7
2023·广东卷,
12
2023·辽宁卷,4
2023·山东卷,6 物质分离和提纯方法的选择、试剂的选择;有机混合物的分
物质的检验
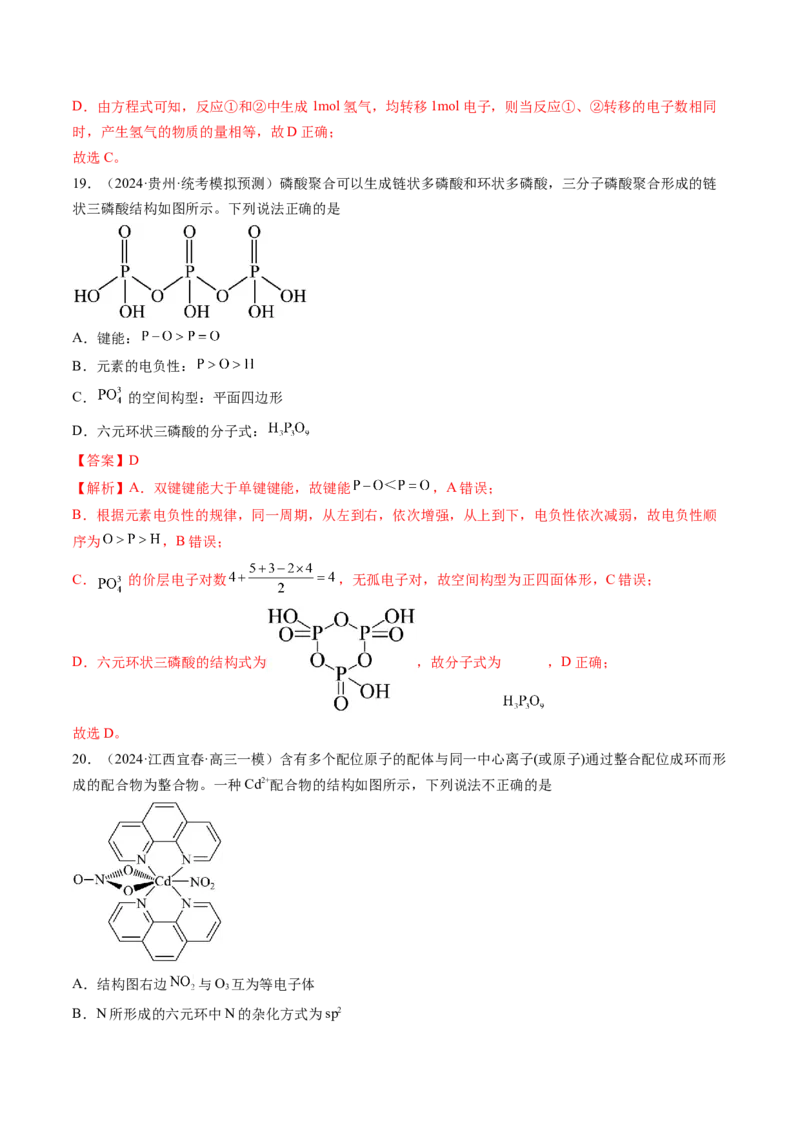
2023·天津卷,3 离;物质的鉴别与检验试剂的选择、添加顺序的判断等;
与鉴别
2023·天津卷,
12
2023·湖南卷,5
2023·湖北卷,9
物质结构与 2023·北京卷, “两大理论”与微粒构型;分子性质与微粒间作用;手性碳
性质的应用 10 原子
和推理 2023·重庆卷,6
2023·河北卷,7
2023·天津卷,6考点一 元素化合物的转化
1.(2023·江苏卷)氮及其化合物的转化具有重要应用。下列说法不正确的是
A.实验室探究稀硝酸与铜反应的气态产物:
B.工业制硝酸过程中的物质转化:
C.汽车尾气催化转化器中发生的主要反应:
D.实验室制备少量 的原理:
【答案】B
【解析】A.Cu与稀硝酸的反应产物之一为NO,NO与氧气发生反应 生成NO ,A正
2
确;
B.氮气与氧气在高温条件下生成NO,但NO无法与水发生化学反应,B错误;
C.汽车尾气催化转化器主要将污染气体NO、CO转化为无污染的气体,故该反应方程式为
,C正确;
D.实验室利用熟石灰和氯化铵制备少量 ,化学方程式为
,D正确。
故选B。
2.(2023·辽宁卷)下列有关物质的工业制备反应错误的是
A.合成氨:N+3H 2NH B.制HCl:H+Cl 2HCl
2 2 3 2 2
C.制粗硅:SiO+2C Si+2CO D.冶炼镁:2MgO(熔融) 2Mg+O↑
2 2
【答案】D
【解析】A.工业合成氨是利用氮气和氢气在催化剂的条件下反应生成的,反应方程式为N+3H
2 2
2NH ,A正确;
3
B.工业制氯化氢是利用氢气和氯气反应生成的,反应方程式为H+Cl 2HCl,B正确;
2 2C.工业制粗硅是将SiO 与C在高温下反应生成粗硅,反应方程式为SiO+2C Si+2CO,C正确;
2 2
D.冶炼金属镁是电解熔融氯化镁,反应方程式为MgCl (熔融) Mg+Cl ↑,D错误;
2 2
故答案选D。
3.(2023·广东卷)部分含 或含 物质的分类与相应化合价关系如图所示。下列推断不合理的是
A.可存在c→d→e的转化 B.能与 反应生成c的物质只有b
C.新制的d可用于检验葡萄糖中的醛基 D.若b能与 反应生成 ,则b中含共价键
【答案】B
【解析】由图可知a、b、c对应物质分别为:钠、氧化钠(过氧化钠)、氢氧化钠或a、b、e 、d对应物
质分别为:铜、氧化亚铜、氧化铜、氢氧化铜。
A.由分析可知氢氧化钠和硫酸铜反应生成氢氧化铜,氢氧化铜受热分解生成氧化铜所以存在c→d→e的
转化,A合理;
B.钠和氧化钠(过氧化钠)都能与 反应都能生成氢氧化钠,B不合理;
C.新制氢氧化铜可用于检验葡萄糖中的醛基,C合理;
D.若b能与 反应生成 ,则b为过氧化钠,结构中含共价键和离子键,D合理;
故选B。
考点二 物质的检验与鉴别
4.(2023·辽宁卷)下列鉴别或检验不能达到实验目的的是
A.用石灰水鉴别NaCO 与NaHCO
2 3 3
B.用KSCN溶液检验FeSO 是否变质
4
C.用盐酸酸化的BaCl 溶液检验NaSO 是否被氧化
2 2 3
D.加热条件下用银氨溶液检验乙醇中是否混有乙醛
【答案】A
【解析】A.石灰水的主要成分为Ca(OH) 能与碳酸钠和碳酸氢钠反应生成碳酸钙,二者均生成白色沉
2
淀,不能达到鉴别的目的,A错误;
B.Fe2+变质后会生成Fe3+,可以利用KSCN溶液鉴别,现象为溶液变成血红色,可以达到检验的目的,B
正确;
C.NaSO 被氧化后会变成NaSO ,加入盐酸酸化的BaCl 后可以产生白色沉淀,可以用来检验NaSO 是
2 3 2 4 2 2 3否被氧化,C正确;
D.含有醛基的物质可以与银氨溶液反应生成银单质,可以用来检验乙醇中混有的乙醛,D正确;
故答案选A。
5.(2023·天津卷)下列方法(试剂)中,无法鉴别 和 两种物质的是
A.焰色试验 B. 试纸 C.稀氨水 D.
【答案】C
【解析】A.钠元素、钡元素的焰色不同,可以用焰色试验鉴别碳酸钠和氯化钡,A不符合;
B.NaCO 溶液显碱性,BaCl 溶液显中性,故可以用pH试纸检验NaCO 和BaCl ,B不符合;
2 3 2 2 3 2
C.NaCO 溶液和BaCl 溶液与氨水都不反应,都无现象,C符合;
2 3 2
D.NaCO 溶液与NaSO 溶液不反应,BaCl 溶液与NaSO 反应生成白色沉淀硫酸钡, D不符合;
2 3 2 4 2 2 4
故答案为:C。
考点三 物质结构与性质的应用和推理
6.(2023·湖北卷)价层电子对互斥理论可以预测某些微粒的空间结构。下列说法正确的是
A. 和 的VSEPR模型均为四面体
B. 和 的空间构型均为平面三角形
C. 和 均为非极性分子
D. 与 的键角相等
【答案】A
【解析】A.甲烷分子的中心原子的价层电子对为4,水分子的中心原子价层电子对也为4,所以他们的
VSEPR模型都是四面体,A正确;
B.SO 的孤电子对为1,CO 的孤电子对为0,所以SO 的空间构型为三角锥形,CO 的空间构型为
平面三角形,B错误,
C.CH 为正四面体结构,为非极性分子,SF 中心原子有孤电子对,为极性分子,C错误;
4 4
D.XeF 和XeO 分子中,孤电子对不相等,孤电子对越多,排斥力越大,所以键角不等,D错误;
2 2
故选A。
7.(2023·湖北卷)物质结构决定物质性质。下列性质差异与结构因素匹配错误的是
选项 性质差异 结构因素
A 沸点:正戊烷(36.1℃)高于新戊烷(9.5℃) 分子间作用力
B 熔点: (1040℃)远高于 (178℃升华) 晶体类型
C 酸性: ( )远强于 ( ) 羟基极性
D 溶解度(20℃): (29g)大于 (8g) 阴离子电荷【答案】D
【解析】A.正戊烷和新戊烷形成的晶体都是分子晶体,由于新戊烷支链多,对称性好,分子间作用力
小,所以沸点较低,故A正确;
B.AlF 为离子化合物,形成的晶体为离子晶体,熔点较高,AlCl 为共价化合物,形成的晶体为分子晶
3 3
体,熔点较低,则 熔点远高于 ,故B正确;
C.由于电负性F>H,C-F键极性大于C-H键,使得羧基上的羟基极性增强,氢原子更容易电离,酸性增
强,故C正确;
D.碳酸氢钠在水中的溶解度比碳酸钠小的原因是碳酸氢钠晶体中HCO 间存在氢键,与晶格能大小无
关,即与阴离子电荷无关,故D错误;
答案选D。
8.(2022·天津卷)嫦娥5号月球探测器带回的月壤样品的元素分析结果如图,下列有关含量前六位元素
的说法正确的是
A.原子半径:Al<Si B.第一电离能:Mg<Ca
C.Fe位于元素周期表的p区 D.这六种元素中,电负性最大的是O
【答案】D
【解析】A.Al、Si同周期,Al的核电荷数小于Si,原子半径:Al>Si,故A错误;
B.Mg、Ca同主族,同主族从上到下第一电离能减小,故B错误;
C.Fe位于元素周期表的d区,故C错误;
D.同周期元素从左到右电负性增大,同主族元素从上到下电负性减弱,则由此可知六种元素中电负性最
大的为O,故D正确;
故选:D。
9.(2022·天津卷)利用反应 可制备N2H4。下列叙述正确的是
A.NH 分子有孤电子对,可做配体
3
B.NaCl晶体可以导电
C.一个NH 分子中有4个σ键
2 4
D.NaClO和NaCl均为离子化合物,他们所含的化学键类型相同
【答案】A
【解析】A.NH 中N原子的孤电子对数= =1,可以提供1对孤电子对,可以做配体,A正确;
3B.导电需要物质中有可自由移动的离子或电子,NaCl晶体中没有自由移动的电子或者离子,故不能导
电,B错误;
C.单键属于σ键,双键中含有1个σ键和1个π键,三键中含有1个σ键和2个π键;NH 的结构式为
2 4
,分子中含有5个σ键,C错误;
D.NaClO含有离子键和共价键,NaCl只含有离子键,都是离子化合物,但所含的化学键类型不同,D错
误;
故选A。
10.(2022·辽宁卷)理论化学模拟得到一种 离子,结构如图。下列关于该离子的说法错误的是
A.所有原子均满足8电子结构 B.N原子的杂化方式有2种
C.空间结构为四面体形 D.常温下不稳定
【答案】B
【解析】A.由 的结构式可知,所有N原子均满足8电子稳定结构,A正确;
B.中心N原子为 杂化,与中心N原子直接相连的N原子为 杂化,与端位N原子直接相连的N原子
为 杂化,端位N原子为 杂化,则N原子的杂化方式有3种,B错误;
C.中心N原子为 杂化,则其空间结构为四面体形,C正确;
D. 中含叠氮结构( ),常温下不稳定,D正确;
故答案选B。
一、掌握常见物质检验与鉴别的方法
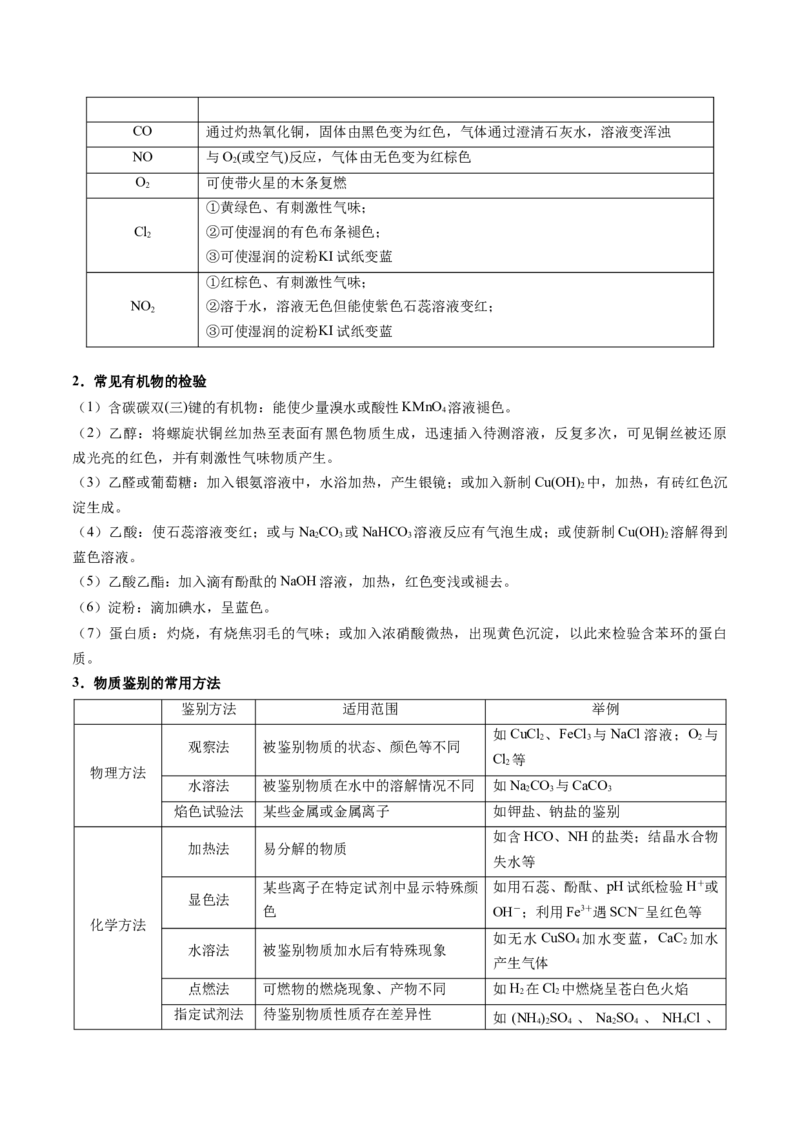
1.常见气体的检验
CO 无色无味气体通入澄清石灰水,澄清石灰水变浑浊
2
SO 通入品红溶液,红色褪去,再加热又变红色
2
①可使湿润的蓝色石蕊试纸(或湿润的pH试纸)变红;
HCl ②可使蘸有浓氨水的玻璃棒产生白烟;
③通入用硝酸酸化的硝酸银溶液产生白色沉淀
NH ①可使蘸有浓盐酸的玻璃棒产生白烟;
3
(碱性气体) ②可使湿润的红色石蕊试纸变蓝。
H 通过灼热氧化铜,固体由黑色变为红色,气体通过无水硫酸铜,粉末变蓝
2CO 通过灼热氧化铜,固体由黑色变为红色,气体通过澄清石灰水,溶液变浑浊
NO 与O(或空气)反应,气体由无色变为红棕色
2
O 可使带火星的木条复燃
2
①黄绿色、有刺激性气味;
Cl ②可使湿润的有色布条褪色;
2
③可使湿润的淀粉KI试纸变蓝
①红棕色、有刺激性气味;
NO ②溶于水,溶液无色但能使紫色石蕊溶液变红;
2
③可使湿润的淀粉KI试纸变蓝
2.常见有机物的检验
(1)含碳碳双(三)键的有机物:能使少量溴水或酸性KMnO 溶液褪色。
4
(2)乙醇:将螺旋状铜丝加热至表面有黑色物质生成,迅速插入待测溶液,反复多次,可见铜丝被还原
成光亮的红色,并有刺激性气味物质产生。
(3)乙醛或葡萄糖:加入银氨溶液中,水浴加热,产生银镜;或加入新制Cu(OH) 中,加热,有砖红色沉
2
淀生成。
(4)乙酸:使石蕊溶液变红;或与NaCO 或NaHCO 溶液反应有气泡生成;或使新制Cu(OH) 溶解得到
2 3 3 2
蓝色溶液。
(5)乙酸乙酯:加入滴有酚酞的NaOH溶液,加热,红色变浅或褪去。
(6)淀粉:滴加碘水,呈蓝色。
(7)蛋白质:灼烧,有烧焦羽毛的气味;或加入浓硝酸微热,出现黄色沉淀,以此来检验含苯环的蛋白
质。
3.物质鉴别的常用方法
鉴别方法 适用范围 举例
如CuCl 、FeCl 与NaCl溶液;O 与
2 3 2
观察法 被鉴别物质的状态、颜色等不同
Cl 等
2
物理方法
水溶法 被鉴别物质在水中的溶解情况不同 如NaCO 与CaCO
2 3 3
焰色试验法 某些金属或金属离子 如钾盐、钠盐的鉴别
如含HCO、NH的盐类;结晶水合物
加热法 易分解的物质
失水等
某些离子在特定试剂中显示特殊颜 如用石蕊、酚酞、pH试纸检验H+或
显色法
色 OH-;利用Fe3+遇SCN-呈红色等
化学方法
如无水CuSO 加水变蓝,CaC 加水
4 2
水溶法 被鉴别物质加水后有特殊现象
产生气体
点燃法 可燃物的燃烧现象、产物不同 如H 在Cl 中燃烧呈苍白色火焰
2 2
指定试剂法 待鉴别物质性质存在差异性 如 (NH )SO 、 NaSO 、 NH Cl 、
4 2 4 2 4 4NaCl四种无色溶液,可选择Ba(OH)
2
来鉴别
限用一种试剂的物质鉴别方法:
(1)先分析被鉴别物质的水溶性、密度、溶液的酸碱性,确定能否选用水或指示剂进行鉴别。
(2)在鉴别多种酸、碱、盐的溶液时,可依据“相反原理”确定试剂进行鉴别。即被鉴别的溶液多数
呈酸性时,可选用碱或水解呈碱性的盐溶液作试剂;若被鉴别的溶液多数呈碱性时,可选用酸或水解呈
酸性的盐溶液作试剂。
(3)常用溴水、新制氢氧化铜等作试剂鉴别多种有机物。
不另加试剂鉴别物质的一般分析思路:
(1)先依据外观特征,鉴别出其中的一种或几种。
(2)若均无明显外观特征,可考虑能否用加热或焰色试验的方法区别开来。
(3)若以上两种方法都不能鉴别时,可考虑两两混合或相互滴加,记录混合后的反应现象,分析确
定。
(4)若被鉴别物质两两滴加时,可考虑因试剂加入的顺序不同、现象不同而进行鉴别。如 Al3+与OH
-,CO与H+等。
(5)若采用上述方法鉴别出一种物质后,可用它作试剂鉴别余下的其他物质。
(6)若两液体互不相溶,可利用密度不同确定两液体。
【易错提醒】阳离子检验的注意事项
NaOH溶液可以同时鉴别出若干种阳离子,包括Al3+、Fe3+、Fe2+、Cu2+、NH、Mg2+等多种离子,在阳离子
鉴别中,NaOH溶液是一种应用较广的试剂。若先使用NaOH溶液(必要时可加热)检验出几种离子,再用
其他方法鉴别用NaOH溶液鉴别不出来的离子,整个问题可以较快解决。
阴离子检验的注意事项
①AgNO 溶液与稀硝酸、BaCl 溶液与稀盐酸这两组试剂,可以鉴别出若干种阴离子,是阴离子鉴别最常用
3 2
的试剂组合。一般说来,若待检的若干种离子中有 SO,最好先用BaCl 溶液和盐酸这组试剂,检出包括
2
SO在内的一些离子,其他离子再用AgNO 溶液与稀硝酸等去鉴别。
3
②为了检验某盐中含SO或CO,可以直接加酸(非氧化性酸,如盐酸),根据放出气体的气味等特征现象判
断气体是CO 或SO ,进而确定物质中含CO或SO。
2 2
③灵活运用阴离子检验的知识,有时可以解决某些阳离子的鉴别问题。例如,在一定条件下,可考虑用卤
素离子(如Cl-)检出Ag+,用SO检出Ba2+。
二、利用物质结构理论判断问题
1.根据价层电子对互斥模型判断分子或离子的空间结构
(1)方法I
根据上述方法I计算出σ键电子对数和中心原子上的孤电子对数,在确定了σ键电子对数和中心原子上的
孤电子对数后,可以依据下面的方法确定相应的较稳定的分子或离子的空间结构:
σ键电子对数+孤电子对数=价层电子对数⃗价层电子对相互排斥VSEPR模型⃗略去孤电子对分子的空间结构
以CO、NH +、NF 为例:
2 4 3①CO :中心C原子的价电子为4,配位原子为氧原子,配位原子数为2,即有2对σ键电子对数,中心C
2
原子上的孤电子对数=[4-2x(8-6)]/2=0,即中心C原子无孤电子对,VSEPR模型就是分子的实际构型,价层
电子对数为2的VSEPR模型为直线形,则CO 的实际构型为直线形。
2
②NH +:中心N原子的价电子为5,配位原子为氢原子,配位原子数为4,NH +带1个正电荷,中心N原
4 4
子上的孤电子对数=[5-1-4x(2-1)]/2=0,即中心N原子无孤电子对,VSEPR模型就是分子的实际构型,价层
电子对数为4的VSEPR模型为正面体形,则NH +的实际构型为正四面体形。
4
③NF :中心N原子的价电子为5,配位原子为氟原子,配位原子数为3,不带电荷,中心N原子上的孤电
3
子对数=[5-3x(8-7)]/2=1,即中心N原子有1孤电子对,VSEPR模型略去1孤电子对才是分子的实际构型,
价层电子对数为4的VSEPR模型为正面体形,则NF 的实际构型为三角锥形。
3
(2)方法II
根据上述方法II计算出价层电子对总数和中心原子上的孤电子对数,根据价层电子对总数得出VSEPR模
型,由VSEPR模型略去孤电子对就可以得出分子的实际构型。
价层电子对数⃗价层电子对相互排斥VSEPR模型⃗略去孤电子对分子的空间结构
以CO、NH +、NF 为例:
2 4 3
①CO :中心C原子的价电子为4,配位原子为氧原子,不计算配位原子数,中心C原子的价层电子对数
2
=4/2=2,中心碳原子与两个氧原子结合,故CO 中C原子孤电子对数=2-2=0,即中心C原子无孤电子对,
2
VSEPR模型就是分子的实际构型,价层电子对数为2的VSEPR模型为直线形,则CO 的实际构型为直线
2
形。
②NH +:中心N原子的价电子为5,配位原子为氢原子,配位原子数为4,NH +带1个正电荷,中心N原
4 4
子的价层电子对数=(5+4-1)/2=4,中心N原子与4个氢原子结合,故NH +中N原子孤电子对数=4-4=0,即
4
中心N原子无孤电子对,VSEPR模型就是分子的实际构型,价层电子对数为4的VSEPR模型为正面体
形,则NH +的实际构型为正四面体形。
4
③NF :中心N原子的价电子为5,配位原子为氟原子,配位原子数为3,不带电荷,中心N原子的价层电
3
子对数=(5+3)/2=4,中心N原子与3个氟原子结合,故NF 中N原子孤电子对数=4-3=1,即中心N原子有1
3
孤电子对,VSEPR模型略去1孤电子对才是分子的实际构型,价层电子对数为4的VSEPR模型为正面体
形,则NF 的实际构型为三角锥形。
3
2.杂化轨道类型的判断方法
(1)根据价层电子对互斥模型判断中心原子的杂化类型、空间结构
在确定了分子或离子的中心原子上的成键电子对数和孤电子对数后,可以依据下面的方法确定其中心原子
{
2→sp
的杂化轨道类型:σ键电子对数(成键电子对数)+孤电子对数=价电子对数=杂化轨道数
3→sp2
4→sp3
根据杂化类型及孤电子对数即可判断分子或离子的空间结构,列表如下:
价层电子对 杂化轨道类 成键电子对 孤电子对 杂化轨道 分子空间结 实例
数 型 数 数 数 构
2 sp 2 0 2 直线形 BeCl 、CO、HCN
2 23 0 平面三角形 BF、SO 、CO2—
3 3 3
3 sp2 3
2 1 V形 SnBr 、SO 、NO —
2 2 2
CHCl 、 SiCl 、
3 4
4 0 四面体形
PO 3—
4
4 sp3 4
3 1 三角锥形 NH 、PCl 、SO 2—
3 3 3
2 2 V形 OF 、HO、NH —
2 2 2
(2)根据杂化轨道间的夹角判断
杂化轨道间的夹角 杂化轨道类型
109º28´ sp3
120º sp2
180º sp
(3)根据分子或离子的空间结构判断
分子或离子的空间结构 杂化轨道类型
正四面体形 sp3
平面三角形 sp2
直线形 sp
(4)根据共价键类型判断
由杂化轨道理论可知,原子之间成键时,未参与杂化的轨道用于形成 π键,杂化轨道用于形成σ键或用来
容纳未参与成键的孤电子对。对于能明确结构式的分子、离子,其中心原子的杂化轨道数 n=中心原子形成
的σ键数+中心原子上的孤电子对数,即可将结构式和电子式相结合,从而判断中心原子形成的σ键数和中
心原子上的孤电子对数,进而判断杂化轨道数。例如:
①在SiF 分子中,基态硅原子有4个价电子,与4个氟原子形成4个σ键,没有孤电子对,n=4,则SiF 分子
4 4
中硅原子采用sp3杂化。
②在HCHO分子中,基态碳原子有4个价电子,与2个氢原子形成2个σ键,与氧原子形成C=O,C=O中有
1个σ键、1个π键,没有孤电子对,n=3,则HCHO分子中碳原子采用sp2杂化。
(5)以碳原子为中心原子的分子中碳原子的杂化类型
①没有形成π键,为sp3杂化:CH、CCl 、
4 4
②形成一个π键,为sp2杂化:CH=CH 、苯(大π键)、 、
2 2
③形成两个π键,为sp杂化:CH≡CH、O=C=O(CO )、S=C=S(CS )
2 2
考点一 元素化合物的转化1.(2024·山东济南一模)关于非金属含氧酸及其盐的性质,下列说法正确的是
A.Cu与浓硝酸反应比与稀硝酸反应快,所以实验室通常用浓硝酸洗涤附着在试管内壁上的银镜
B.加热浓硫酸与NaCl固体的混合物可制备HCl,说明浓硫酸酸性强于HCl
C.将CO 通入Ba(NO ):溶液无明显现象,则将SO 通入Ba(NO ) 溶液也无明显现象
2 3 2 3 2
D.向NaClO溶液中滴加酚酞试剂,先变红后褪色,证明NaClO在溶液中发生了水解反应
【答案】D
【解析】A.实验室通常用稀硝酸清洗银镜,稀硝酸成本更低,故A错误;
B.加热浓硫酸与NaCl固体反应方程式为: ,反应能发生,是由于HCl
为挥发性酸,不断离开反应体系,使得平衡正向移动,反应得以进行,与浓硫酸和HCl的酸性大小无关,
故B错误;
C.SO 通入Ba(NO ) 溶液中,SO 被氧化为硫酸根,会生成BaSO 白色沉淀,故C错误;
2 3 2 2 4
D.向NaClO溶液中滴加酚酞试剂,先变红后褪色,是由于次氯酸根水解: ,
使溶液呈碱性,由于生成的次氯酸具有漂白性,使得溶液变红后褪色,故D正确;
故选D。
2.(2024·山东淄博一模)实验室中使用钠盐或 溶液时,对应关系错误的是
A.饱和 溶液:除去 中的 B.饱和 溶液:除去 中
C. 水溶液:油脂的皂化反应 D. 醇溶液: 的消去反应
【答案】B
【解析】A.Cl 能溶于水,在饱和NaCl溶液中溶解度会变小,A正确;
2
B.NaCO 溶液既能与HCl反应,也能与CO 反应,应该用饱和碳酸氢钠溶液除去CO 中的HCl气体,B
2 3 2 2
错误。
C.油脂在碱性条件下水解为甘油和高级脂肪酸钠的反应称为皂化反应,C正确;
D.CHCHBr在NaOH醇溶液中反生消去反应生成乙烯,D正确;
3 2
故选B。
3.(2024·山东泰安一模)取一定体积的下列两种试剂(浓度均为 )进行反应,改变两种试剂的滴
加顺序,反应产生的现象相同的是
A. 溶液、稀盐酸 B. 溶液、氨水
C. 溶液、溴水 D. 溶液、酸性 溶液
【答案】B
【解析】A.向 溶液中滴加稀盐酸,刚开始没有气泡,然后才产生气泡,向稀盐酸中滴加
溶液直接产生气泡,故A不符合题意;
B. 溶液和氨水无论滴加顺序怎样,都会生成氢氧化铝沉淀,故B符合题意;
C.向 溶液中滴加溴水,溴水中的HCl和 反应生成二氧化碳气体,溴水过量时溶液变为橙黄色,向溴水中滴加 溶液,溴水中的HCl和 反应生成二氧化碳气体,溶液由橙黄色变
为无色,故C不符合题意;
D.向 溶液中滴加酸性 溶液,溶液由无色变为红色,向酸性 溶液中滴加 溶
液,溶液由红色变为无色,故D不符合题意;
故选B。
4.(2023·陕西渭南·统考一模)类比思想是化学学习的重要思想,下列各项中由客观事实类比得到的结论
正确的是
A.(干冰)CO 是分子晶体,(石英)SiO 也是分子晶体
2 2
B. 可以表示为 可以表示为
C. 通入到 溶液中不产生沉淀, 通入到 溶液中也无沉淀
D. 可作净水剂, 也可作净水剂
【答案】D
【解析】A. 是分子晶体,但 是原子晶体(或共价晶体),A错误;
B. 中Fe的化合价可以认为是+2、+3,则表示为 ,但是Pb常见的化合价为+2、+4,则
应表示为 ,B错误;
C.因酸性:HSO N>C>H>Cd
【答案】A
【解析】A. 与O 原子数相同,价电子为16和18,不互为等电子体,A错误;
3
B.邻二氮菲为平面结构,所以N原子的杂化方式都为sp2,且只有1种,B正确;
C.整合物是一种环状配合物,“螯”指螃蟹的大钳,在螯合物结构中,一定有多个多齿配体提供多对电
子与中心原子形成配位键,邻二氮菲为双齿配体,Cd2+的配位数为7,C正确;
D.元素非金属性越强,电负性越强,得电子能力越强,则图中所涉及元素的电负性由大到小顺序为:
O>N>C>H>Cd,D正确;
故选A。
21.(2024·黑龙江·高三一模)下列关于物质结构或性质及解释存在错误的是
选
物质结构或性质 解释
项
CO 中C原子为sp杂化,为直线形分子;CH 中C原子为sp3杂化,
2 4
A 键角:
为正四面体形分子
B 稳定性: 分子间可以形成氢键, 没有氢键
BF 与NH 形成[H N→BF ] 中的 有空轨道接受 中 的孤电子对
3 3 3 3
冠醚能加快KMnO 与环己烯 冠醚上不同大小的空穴适配不同大小的碱金属离子,冠醚通过与
4
D
的反应速率 K+结合将 带入有机相,起到催化剂的作用
【答案】B
【解析】A.CO 中C原子为sp杂化,为直线形分子,键角为180°,CH 中C原子为sp3杂化,为正四面体
2 4
形分子,键角为109°28’,因此键角: CO>CH ,A正确;
2 4
B.非金属性越强,气态氢化物越稳定,非金属性:F>Cl,因此稳定性:HF>HCl,气态氢化物的稳定性与
氢键无关,B错误;
C.BF 中的B有空轨道,NH 中N有孤电子对,因此BF3中的B与NH3中N可形成配位键,BF 与NH
3 3 3 3
形成[H N → BF ],C正确;
3 3
D.冠醚上不同大小的空穴适配不同大小的碱金属离子,冠醚通过与K结合将 带入有机相,起到催
化剂的作用,因此冠醚能加快 KMnO 与环己烯的反应速率,D正确;
4
故选B。
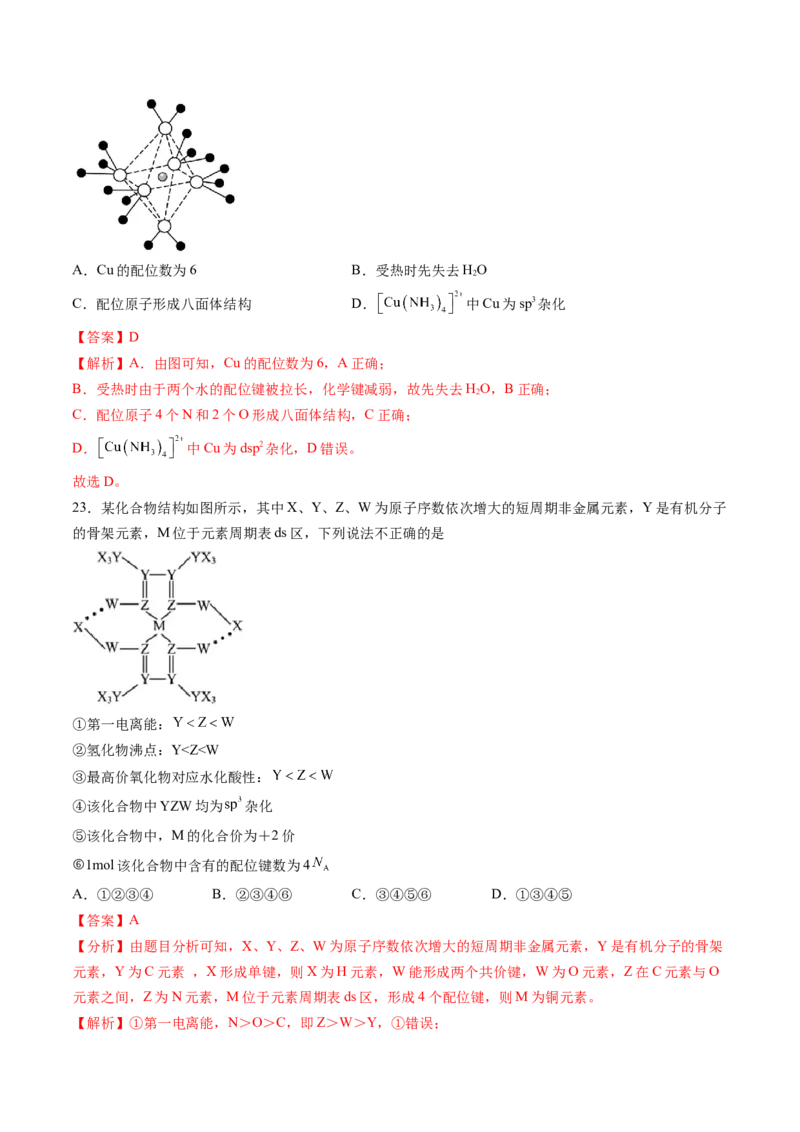
22.(2024·安徽·高三一模)四氨合铜离子一般写作 实际上应该是 结
构如图所示。由于姜泰勒(Jahn—Teller)效应的缘故,使其中的两个水的配位键被拉长。下列有关该离子的
说法错误的是A.Cu的配位数为6 B.受热时先失去HO
2
C.配位原子形成八面体结构 D. 中Cu为sp3杂化
【答案】D
【解析】A.由图可知,Cu的配位数为6,A正确;
B.受热时由于两个水的配位键被拉长,化学键减弱,故先失去HO,B正确;
2
C.配位原子4个N和2个O形成八面体结构,C正确;
D. 中Cu为dsp2杂化,D错误。
故选D。
23.某化合物结构如图所示,其中X、Y、Z、W为原子序数依次增大的短周期非金属元素,Y是有机分子
的骨架元素,M位于元素周期表ds区,下列说法不正确的是
①第一电离能:
②氢化物沸点:Y