文档内容
易错专题 05 金属元素及其化合物
聚焦易错点:
►易错点一 金属元素及其化合物的性质
►易错点二 金属元素及其化合物的转化
典例精讲
易错点一 金属元素及其化合物的性质
【易错典例】
例1为探究铜与稀硝酸反应的产物及影响反应速率的主要因素,进行如下实验。
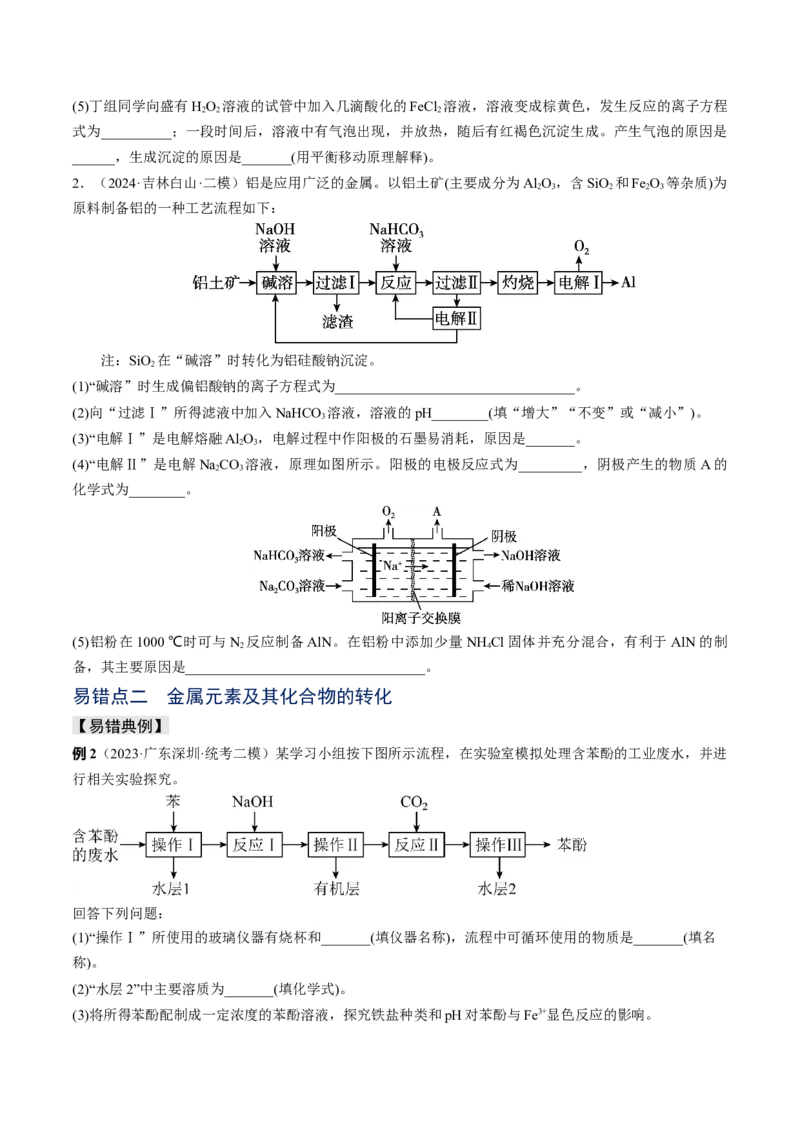
【实验一】探究铜和稀硝酸反应的产物。实验装置如图所示,气密性已检查。
已知:FeSO +NO===[Fe(NO)]SO 该反应较慢,待生成一定量[Fe(NO)]2+时,突显明显棕色。
4 4
(1)实验开始时先将Y形试管向盛有碳酸钙的支管倾斜,然后向其中缓慢滴入稀硝酸,该实验操作的目的是
________________________________。
(2)铜片和稀硝酸反应的化学方程式为_________________________________。
(3)若Y形试管中产生的气体有NO ,B中的实验现象为________________;若Y形试管中产生的气体只有
2
NO,B中的实验现象是____________________。
【实验二】 探究铜和稀硝酸反应速率先慢后快的原因。经过实验一,测得硝酸的浓度小于6 mol·L-1时,
只有NO生成。当铜片与5 mol·L-1硝酸反应,开始时反应非常缓慢,一段时间后反应速率明显加快。为探
究此反应的反应速率先慢后快的原因,进行如下探究。
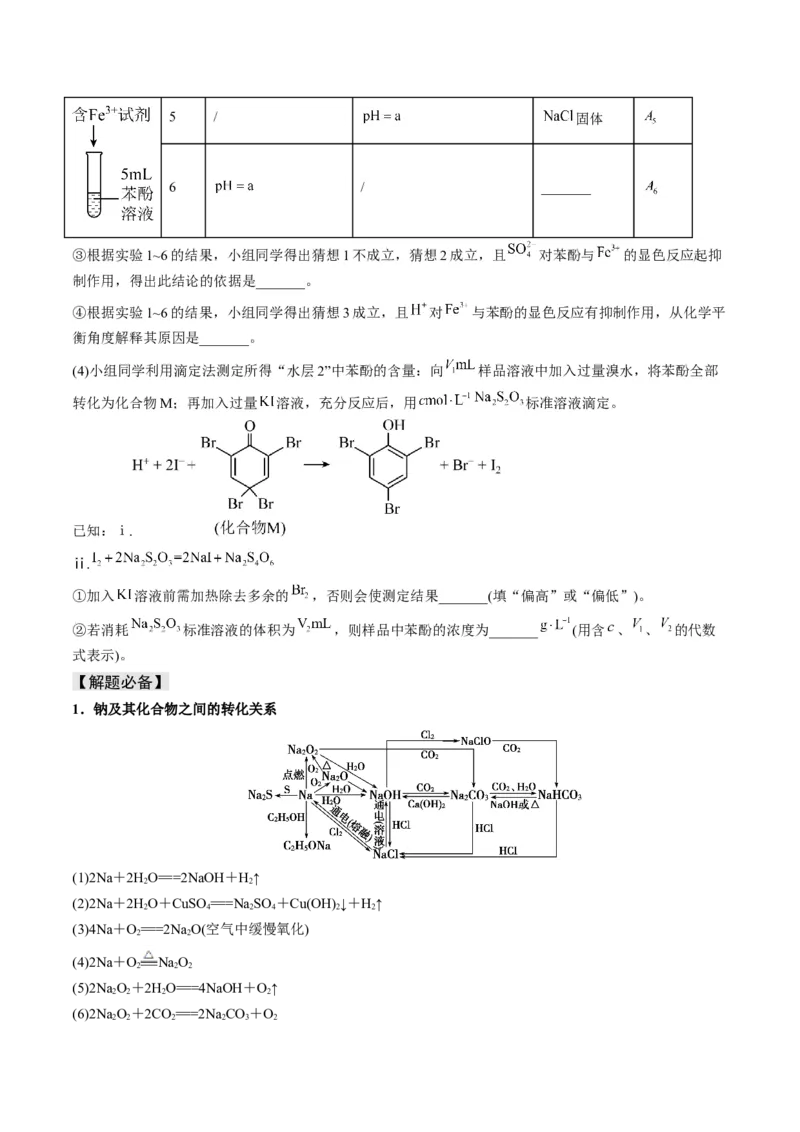
探究一:研究反应过程中温度变化对反应速率的影响,实验所得现象记录如表所示。
时间/min 现象
0~15 铜表面出现气泡,但速度很慢
25 溶液有很浅的蓝色,气泡生成速度加快
30 气泡生成速度较快,均匀冒出
45 洗气瓶中可见少量淡棕色的物质
50 溶液中蓝色明显变深,洗气瓶中突显明显棕色铜和稀硝酸的反应温度与时间的关系曲线
(4)分析上述图表信息可得到的结论是_______________________。
探究二:研究化学反应产物对反应速率的影响
某同学设计了如下实验,利用实验一的装置测定溶液突显明显棕色的时间。
序号 温度/ ℃ 铜片/g 硝酸/mL 硝酸铜/g
1 25 ① ② ③
2 25 5 20 0.5
3 25 5 20 1.0
(5)请将表中的实验条件填写完整:①________;②________;③________。
(6)通过实验发现实验 1、2、3的反应速率并无明显变化,为达到实验目的还需要继续进行的实验是
______________________________________________。
【解题必备】
1.钠和盐溶液反应,不能置换出盐中的金属,而是先与HO反应生成NaOH,然后生成
2
的NaOH溶液再与盐溶液反应,钠与HO、酸反应的实质都是与H+反应,所以钠与酸溶
2
液反应更为剧烈。钠与熔融的盐反应才可能置换出盐中的金属。
2.无论Na与O 反应生成NaO或NaO ,只要参与反应的Na质量相等,则转移电子的
2 2 2 2
物质的量一定相等。Li和O 反应只生成LiO。
2 2
钠及其化合物
3.Na及其化合物发生焰色反应时火焰颜色均为黄色,鉴别Na、K利用焰色反应。焰色反
应是大多金属元素的性质,属于物理变化。
4.NaO 具有强氧化性,能将具有还原性的物质氧化,每摩 NaO 得2 mol电子,1 mol
2 2 2 2
NaO 参与反应转移电子的物质的量为1 mol。
2 2
1.铝是活泼金属,但铝抗腐性相当强,因为铝表面生成一层致密的氧化物薄膜。
2.铝热反应不仅仅是单质铝与Fe O 反应,还包含制取其他难熔金属的反应,并不是 Al
2 3
与所有金属氧化物均能组成铝热剂,该金属氧化物对应的金属活泼性应比铝弱。
铝及其化合物 3.Al O 、Al(OH) 与NaOH溶液的反应常用于物质的分离提纯。Al(OH) 不溶于氨水,所
2 3 3 3
以实验室常用铝盐和氨水来制备Al(OH) 。Al(OH) 可用作抗酸药。
3 3
4.泡沫灭火器所用试剂为Al (SO ) 溶液和NaHCO 溶液。
2 4 3 3
1.Fe与O 、HO(g)反应的产物都是Fe O 而不是Fe O ,Fe与Cl 反应时生成FeCl ,与S
2 2 3 4 2 3 2 3
反应时生成FeS, Fe、Al在冷的浓硫酸和浓硝酸中发生钝化,但加热后继续反应。
2.FeCl 溶液与NaOH溶液在空气中反应的现象变化,常用于物质推断。向Fe2+溶液中加
2
入硝酸、KMnO 溶液、氯水等具有氧化性的物质时,溶液会出现浅绿色→棕色的颜色变
4
化,该现象可用于Fe2+的初步检验。Fe3+的检验方法较多,如观察溶液颜色法(棕黄色)、
NaOH溶液法(生成红褐色沉淀)、KSCN溶液法(生成血红色溶液),前面两种方法需溶液中
铁及其化合物
Fe3+浓度较大时才适用,最好也最灵敏的方法是KSCN溶液法。
3.配制FeCl 溶液既要防氧化(加入Fe粉),又要防水解(加入盐酸);配制FeCl 溶液要加
2 3
入浓盐酸防止水解。
4.Fe3+必须在酸性条件下才能大量存在,当pH=7时,Fe3+几乎完全水解生成Fe(OH) 沉
3淀。除去酸性溶液ZnCl 中的FeCl ,应先通入Cl 或加入HO ,再加入ZnO,使Fe3+水解
2 2 2 2 2
生成沉淀过滤除去。
5.制备Fe(OH) 的方法很多,原则有两点,一是溶液中的溶解氧必须提前除去,二是反
2
应过程中必须与O 隔绝。
2
6.铁元素在周期表中的位置,铁、铁离子、亚铁离子的电子排布式、轨道表示式,离子的
稳定性与洪特规则,配合物的中心离子、配体。
1.铜在潮湿的空气中最终不是生成CuO,而是铜绿[Cu (OH) CO]。
2 2 3
2.常用灼热的铜粉除去N 中的O,灼热的CuO除去CO 中的CO。
2 2 2
铜及其化合物 3.新制Cu(OH) 悬浊液常用来检验醛基。
2
4.Cu和一定量的浓HNO 反应,产生的是NO 和NO的混合气体,当Cu有剩余,再加入
3 2
稀HSO ,Cu继续溶解。
2 4
5.四水合铜离子与四氨合铜离子的中心离子、配体、配位能力、空间构型
1.金属的冶炼方法与金属活动性顺序表有密切的关系:
2.钠、镁的冶炼是电解熔融的NaCl、MgCl ,铝的冶炼是电解加了冰晶石的熔融Al O ,
2 2 3
金属冶炼
不是电解熔融AlCl ,因为AlCl 是共价化合物,熔融态不导电。
3 3
3.热还原法中使用的还原剂通常为碳、一氧化碳和氢气等。在金属活动性顺序表中,虽
然前面的金属能够将后面的金属从其化合物中置换出来,但不一定是从其盐溶液中置换,
例如Na由于活泼性太强,不能从CuCl 溶液中置换出Cu,但是可以在其熔融状态下置换
2
出铜。在高炉炼铁中,加入的还原剂是焦炭,但真正作还原剂的是CO。
【变式突破】
1.(2023年福建福州市高三期末) 某班同学用如下实验探究Fe2+、Fe3+的性质。回答下列问题:
(1)分别取一定量氯化铁、氯化亚铁固体,均配制成 0.1 mol·L-1的溶液。在FeCl 溶液中需加入少量铁屑,
2
其目的是____________________________________________________。
(2)甲组同学取2 mL FeCl 溶液,加入几滴氯水,再加入1滴KSCN溶液,溶液变红,说明Cl 可将Fe2+氧
2 2
化。FeCl 溶液与氯水反应的离子方程式为________________________。
2
(3)乙组同学认为甲组的实验不够严谨,该组同学在2 mL FeCl 溶液中先加入0.5 mL 煤油,再于液面下依
2
次加入几滴氯水和1滴KSCN溶液,溶液变红,煤油的作用是__________。
(4)丙组同学取10 mL 0.1 mol·L-1KI溶液,加入6 mL 0.1 mol·L-1 FeCl 溶液混合。分别取 2 mL 此溶液于3
3
支试管中进行如下实验:
①第一支试管中加入1 mL CCl 充分振荡、静置,CCl 层显紫色;
4 4
②第二支试管中加入1滴K[Fe(CN) ]溶液,生成蓝色沉淀;
3 6
③第三支试管中加入1滴KSCN溶液,溶液变红。
实验②检验的离子是________(填离子符号);实验①和③说明:在 I-过量的情况下,溶液中仍含有
________(填离子符号),由此可以证明该氧化还原反应为________。(5)丁组同学向盛有HO 溶液的试管中加入几滴酸化的FeCl 溶液,溶液变成棕黄色,发生反应的离子方程
2 2 2
式为__________;一段时间后,溶液中有气泡出现,并放热,随后有红褐色沉淀生成。产生气泡的原因是
______,生成沉淀的原因是_______(用平衡移动原理解释)。
2.(2024·吉林白山·二模)铝是应用广泛的金属。以铝土矿(主要成分为Al O ,含SiO 和Fe O 等杂质)为
2 3 2 2 3
原料制备铝的一种工艺流程如下:
注:SiO 在“碱溶”时转化为铝硅酸钠沉淀。
2
(1)“碱溶”时生成偏铝酸钠的离子方程式为__________________________________。
(2)向“过滤Ⅰ”所得滤液中加入NaHCO 溶液,溶液的pH________(填“增大”“不变”或“减小”)。
3
(3)“电解Ⅰ”是电解熔融Al O,电解过程中作阳极的石墨易消耗,原因是_______。
2 3
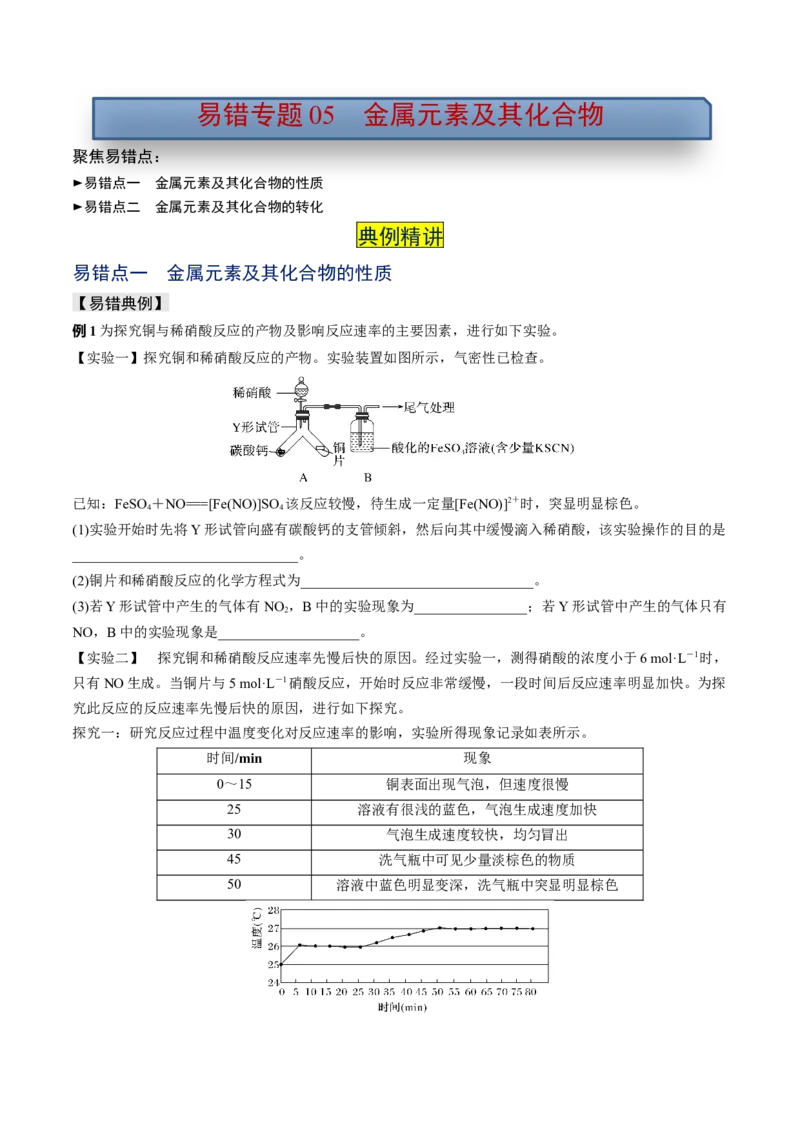
(4)“电解Ⅱ”是电解NaCO 溶液,原理如图所示。阳极的电极反应式为_________,阴极产生的物质A的
2 3
化学式为________。
(5)铝粉在1000 ℃时可与N 反应制备AlN。在铝粉中添加少量NH Cl固体并充分混合,有利于AlN的制
2 4
备,其主要原因是__________________________________。
易错点二 金属元素及其化合物的转化
【易错典例】
例2(2023·广东深圳·统考二模)某学习小组按下图所示流程,在实验室模拟处理含苯酚的工业废水,并进
行相关实验探究。
回答下列问题:
(1)“操作Ⅰ”所使用的玻璃仪器有烧杯和_______(填仪器名称),流程中可循环使用的物质是_______(填名
称)。
(2)“水层2”中主要溶质为_______(填化学式)。
(3)将所得苯酚配制成一定浓度的苯酚溶液,探究铁盐种类和pH对苯酚与Fe3+显色反应的影响。查阅资料
ⅰ. 为紫色;
ⅱ. 对苯酚与 的显色反应无影响;
ⅲ. 对特定波长光的吸收程度(用吸光度A表示)与 的浓度在一定范围内成正
比。
提出猜想:
猜想1: 对苯酚与 的显色反应有影响
猜想2: 对苯酚与 的显色反应有影响。
猜想3: 对苯酚与 的显色反应有影响。
进行实验:
常温下,用盐酸调节pH配制得到pH分别为a和b的 溶液( ),用硫酸调节pH配制得
到pH分别为a和b的 溶液。取 苯酚溶液于试管中,按实验1~4分别再加入
含 的试剂,显色 后用紫外-可见分光光度计测定该溶液的吸光度(本实验条件下,pH改变
对 水解程度的影响可忽略)。
含 的试剂
序号 吸光度
溶
溶液
液
1 /
2 /
3 /
4 /
结果讨论 实验结果为 。
①根据实验结果,小组同学认为此结果不足以证明猜想3成立的理由是_______。
②为进一步验证猜想,小组同学设计了实验5和6,补充下表中相关内容。(限选试剂: 溶液、
溶液、 固体、 固体)
含 的试剂
序 再加入的试
吸光度
号 剂
溶液 溶液5 / 固体
6 / _______
③根据实验1~6的结果,小组同学得出猜想1不成立,猜想2成立,且 对苯酚与 的显色反应起抑
制作用,得出此结论的依据是_______。
④根据实验1~6的结果,小组同学得出猜想3成立,且 对 与苯酚的显色反应有抑制作用,从化学平
衡角度解释其原因是_______。
(4)小组同学利用滴定法测定所得“水层2”中苯酚的含量:向 样品溶液中加入过量溴水,将苯酚全部
转化为化合物M;再加入过量 溶液,充分反应后,用 标准溶液滴定。
已知:ⅰ.
ⅱ.
①加入 溶液前需加热除去多余的 ,否则会使测定结果_______(填“偏高”或“偏低”)。
②若消耗 标准溶液的体积为 ,则样品中苯酚的浓度为_______ (用含 、 、 的代数
式表示)。
【解题必备】
1.钠及其化合物之间的转化关系
(1)2Na+2HO===2NaOH+H↑
2 2
(2)2Na+2HO+CuSO ===Na SO +Cu(OH) ↓+H↑
2 4 2 4 2 2
(3)4Na+O===2Na O(空气中缓慢氧化)
2 2
(4)2Na+O NaO
2 2 2
(5)2Na O+2HO===4NaOH+O↑
2 2 2 2
(6)2Na O+2CO===2Na CO+O
2 2 2 2 3 2(7)Na CO+2HCl(过量)===2NaCl+CO↑+HO
2 3 2 2
(8)Na CO+HCl(不足)===NaCl+NaHCO
2 3 3
(9)Na CO+CO+HO===2NaHCO
2 3 2 2 3
(10)Na CO+Ca(OH) ===CaCO ↓+2NaOH
2 3 2 3
(11)NaHCO +HCl===NaCl+CO↑+HO
3 2 2
(12)NaHCO +NaOH===Na CO+HO
3 2 3 2
(13)2NaHCO +Ca(OH) (不足)===Na CO+CaCO ↓+2HO
3 2 2 3 3 2
(14)NaHCO +Ca(OH) (过量)===CaCO ↓+NaOH+HO
3 2 3 2
(15)CO +2NaOH(过量)===Na CO+HO
2 2 3 2
(16)CO (过量)+NaOH===NaHCO
2 3
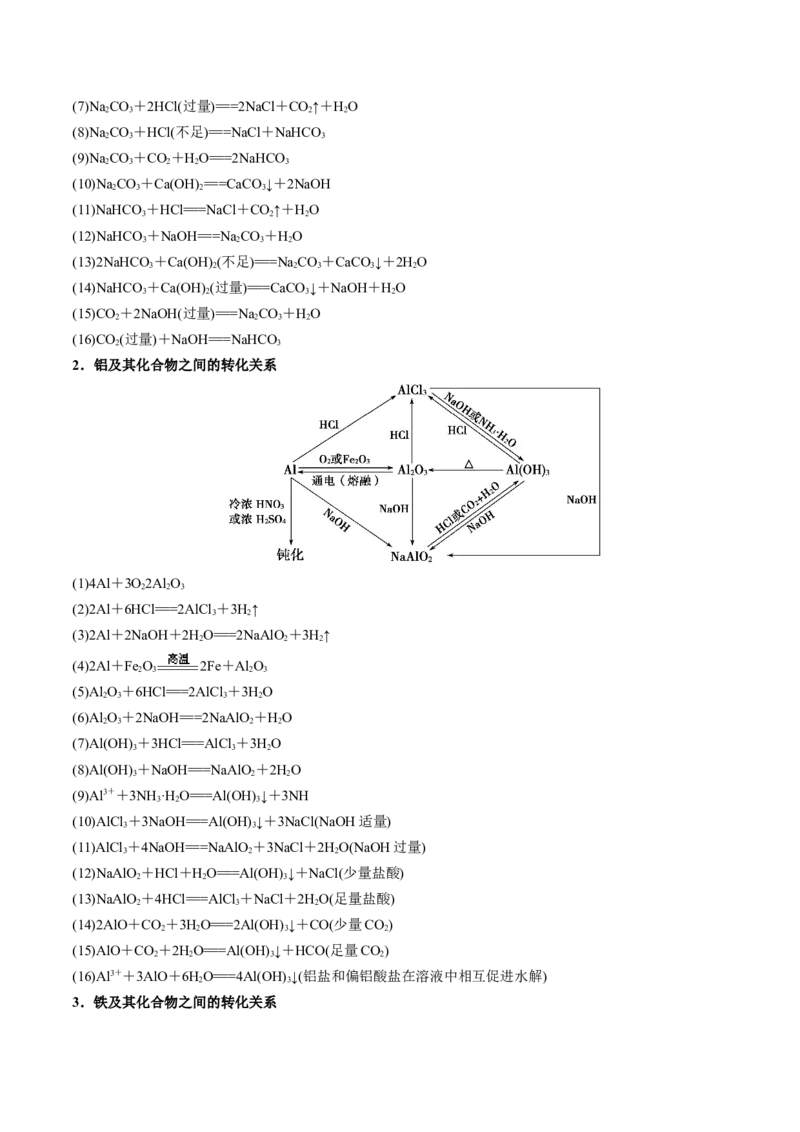
2.铝及其化合物之间的转化关系
(1)4Al+3O2Al O
2 2 3
(2)2Al+6HCl===2AlCl +3H↑
3 2
(3)2Al+2NaOH+2HO===2NaAlO+3H↑
2 2 2
(4)2Al+Fe O 2Fe+Al O
2 3 2 3
(5)AlO+6HCl===2AlCl +3HO
2 3 3 2
(6)AlO+2NaOH===2NaAlO+HO
2 3 2 2
(7)Al(OH) +3HCl===AlCl +3HO
3 3 2
(8)Al(OH) +NaOH===NaAlO+2HO
3 2 2
(9)Al3++3NH ·H O===Al(OH) ↓+3NH
3 2 3
(10)AlCl +3NaOH===Al(OH) ↓+3NaCl(NaOH适量)
3 3
(11)AlCl +4NaOH===NaAlO+3NaCl+2HO(NaOH过量)
3 2 2
(12)NaAlO +HCl+HO===Al(OH) ↓+NaCl(少量盐酸)
2 2 3
(13)NaAlO +4HCl===AlCl +NaCl+2HO(足量盐酸)
2 3 2
(14)2AlO+CO+3HO===2Al(OH) ↓+CO(少量CO)
2 2 3 2
(15)AlO+CO+2HO===Al(OH) ↓+HCO(足量CO)
2 2 3 2
(16)Al3++3AlO+6HO===4Al(OH) ↓(铝盐和偏铝酸盐在溶液中相互促进水解)
2 3
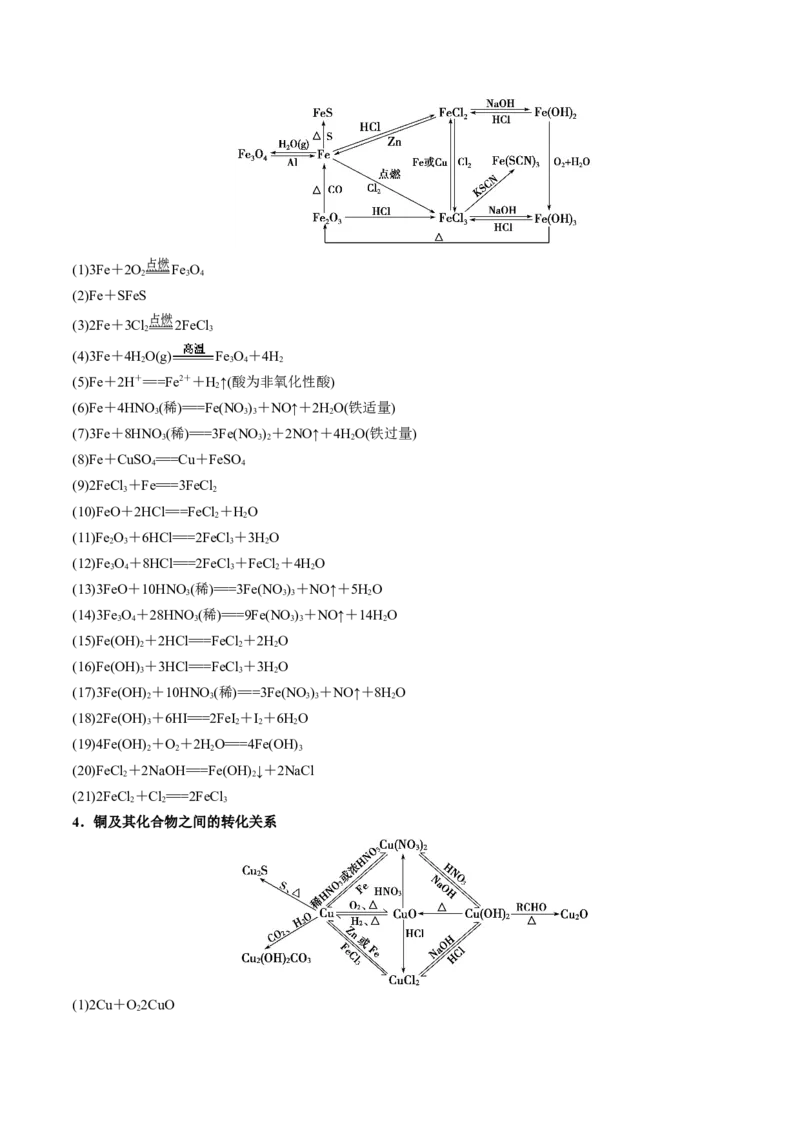
3.铁及其化合物之间的转化关系点燃
(1)3Fe+2O Fe O
2 3 4
(2)Fe+SFeS
点燃
(3)2Fe+3Cl 2FeCl
2 3
(4)3Fe+4HO(g) Fe O+4H
2 3 4 2
(5)Fe+2H+===Fe2++H↑(酸为非氧化性酸)
2
(6)Fe+4HNO(稀)===Fe(NO)+NO↑+2HO(铁适量)
3 3 3 2
(7)3Fe+8HNO(稀)===3Fe(NO)+2NO↑+4HO(铁过量)
3 3 2 2
(8)Fe+CuSO ===Cu+FeSO
4 4
(9)2FeCl +Fe===3FeCl
3 2
(10)FeO+2HCl===FeCl +HO
2 2
(11)Fe O+6HCl===2FeCl +3HO
2 3 3 2
(12)Fe O+8HCl===2FeCl +FeCl +4HO
3 4 3 2 2
(13)3FeO+10HNO(稀)===3Fe(NO)+NO↑+5HO
3 3 3 2
(14)3Fe O+28HNO(稀)===9Fe(NO)+NO↑+14HO
3 4 3 3 3 2
(15)Fe(OH) +2HCl===FeCl +2HO
2 2 2
(16)Fe(OH) +3HCl===FeCl +3HO
3 3 2
(17)3Fe(OH) +10HNO(稀)===3Fe(NO)+NO↑+8HO
2 3 3 3 2
(18)2Fe(OH) +6HI===2FeI +I+6HO
3 2 2 2
(19)4Fe(OH) +O+2HO===4Fe(OH)
2 2 2 3
(20)FeCl +2NaOH===Fe(OH) ↓+2NaCl
2 2
(21)2FeCl +Cl===2FeCl
2 2 3
4.铜及其化合物之间的转化关系
(1)2Cu+O2CuO
2(2)2Cu+SCu S
2
点燃
(3)Cu+Cl CuCl
2 2
(4)Cu+2FeCl ===CuCl +2FeCl
3 2 2
(5)2Cu+O+CO+HO===Cu (OH) CO
2 2 2 2 2 3
(6) Cu + 2H SO ( 浓 )CuSO + SO ↑ + 2H O、
2 4 4 2 2
(7)3Cu + 8HNO ( 稀 ) == =3Cu(NO ) + 2NO ↑ + 4H O
3 3 2 2
(8)2CuSO +2HO 2Cu+O↑+2HSO
4 2 2 2 4
【变式突破】
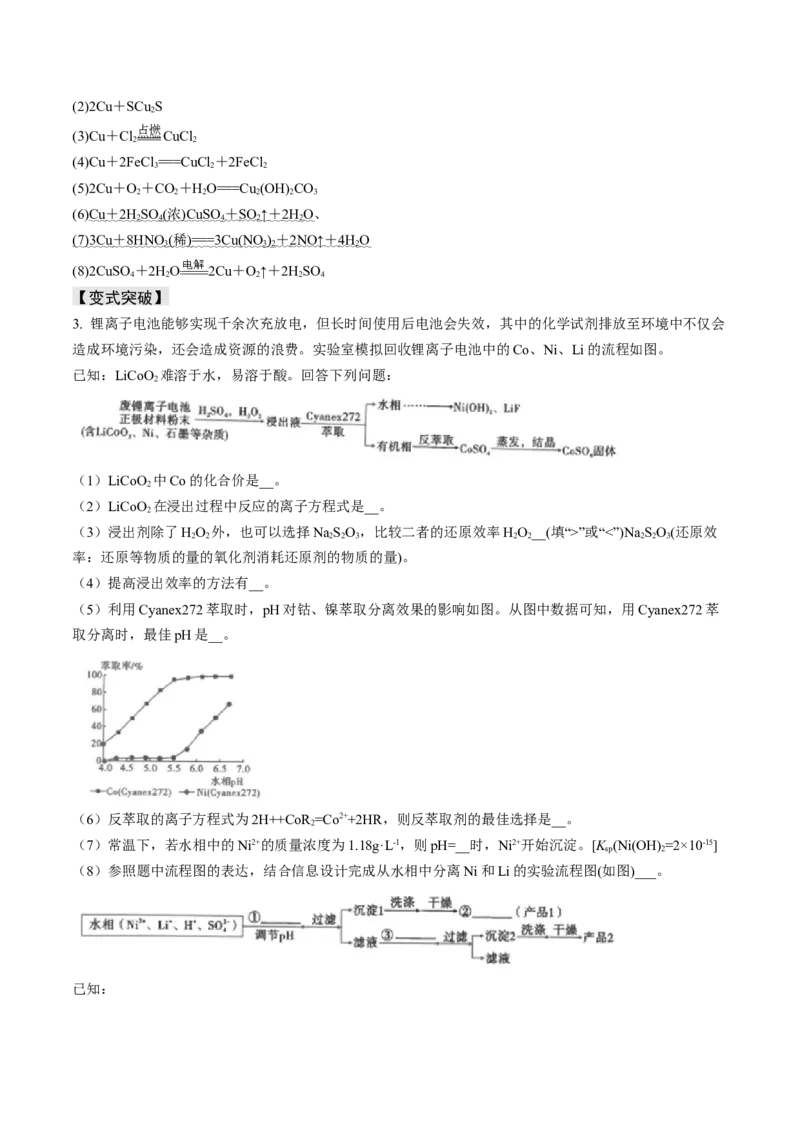
3. 锂离子电池能够实现千余次充放电,但长时间使用后电池会失效,其中的化学试剂排放至环境中不仅会
造成环境污染,还会造成资源的浪费。实验室模拟回收锂离子电池中的Co、Ni、Li的流程如图。
已知:LiCoO 难溶于水,易溶于酸。回答下列问题:
2
(1)LiCoO 中Co的化合价是__。
2
(2)LiCoO 在浸出过程中反应的离子方程式是__。
2
(3)浸出剂除了HO 外,也可以选择NaSO,比较二者的还原效率HO__(填“>”或“<”)Na SO(还原效
2 2 2 2 3 2 2 2 2 3
率:还原等物质的量的氧化剂消耗还原剂的物质的量)。
(4)提高浸出效率的方法有__。
(5)利用Cyanex272萃取时,pH对钴、镍萃取分离效果的影响如图。从图中数据可知,用Cyanex272萃
取分离时,最佳pH是__。
(6)反萃取的离子方程式为2H++CoR =Co2++2HR,则反萃取剂的最佳选择是__。
2
(7)常温下,若水相中的Ni2+的质量浓度为1.18g·L-1,则pH=__时,Ni2+开始沉淀。[K (Ni(OH) =2×10-15]
sp 2
(8)参照题中流程图的表达,结合信息设计完成从水相中分离Ni和Li的实验流程图(如图)___。
已知:提供的无机试剂:NaOH、NaCO、NaF。
2 3
4. 聚合硫酸铁(PFS)是一种性能优异的无机高分子絮凝剂,其化学式通常表示为[Fe (OH) (SO ) ]。某化
2 2a 4 3-a b
工厂制备PFS并用其处理废水。
I.用硫酸铜废液制备PFS
(1)试剂A为___。
(2)“控温氧化”发生反应的离子方程式为__。
(3)测定PFS样品中的n(OH-):取ag样品,溶解于VmLc mol∙L−1HCl溶液中,用KF溶液掩蔽Fe3+(使
1 1
Fe3+不能与OH-反应),滴入酚酞溶液,再用c mol∙L−1NaOH溶液滴定,到达滴定终点时消耗NaOH溶液体
2
积为VmL。agPFS样品中的n(OH-)=__mol。
2
II.用石灰乳-PFS法处理含砷废水
已知:
i.常温下,Ca (AsO) CaHAsO 的K 均大于FeAsO 的K ,Fe (HAsO ) 可溶;
3 4 2、 4 sp 4 sp 2 4 3
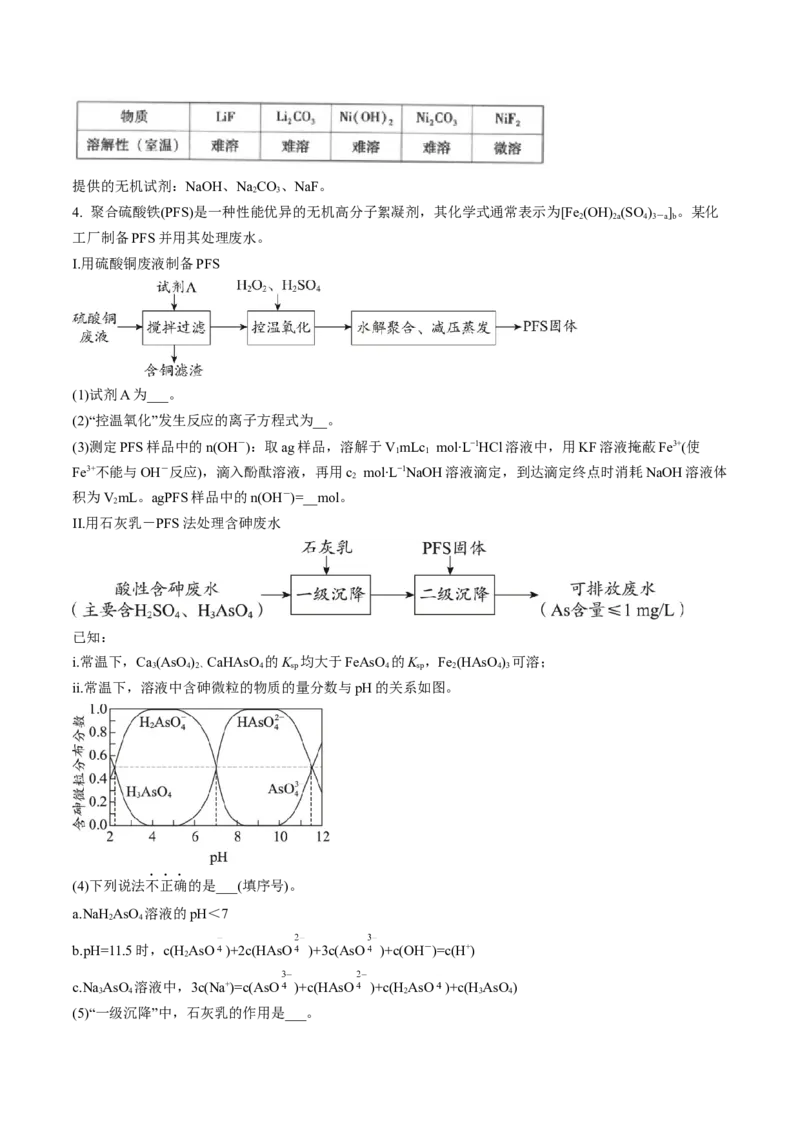
ii.常温下,溶液中含砷微粒的物质的量分数与pH的关系如图。
(4)下列说法不正确的是___(填序号)。
a.NaH AsO 溶液的pH<7
2 4
b.pH=11.5时,c(HAsO )+2c(HAsO )+3c(AsO )+c(OH-)=c(H+)
2
c.Na AsO 溶液中,3c(Na+)=c(AsO )+c(HAsO )+c(H AsO )+c(H AsO )
3 4 2 3 4
(5)“一级沉降”中,石灰乳的作用是___。(6)“二级沉降”中,溶液的pH在8~10之间,PFS形成的Fe(OH) 胶体粒子可以通过沉淀反应进一步减少溶
3
液中的As含量,反应的离子方程式为___。
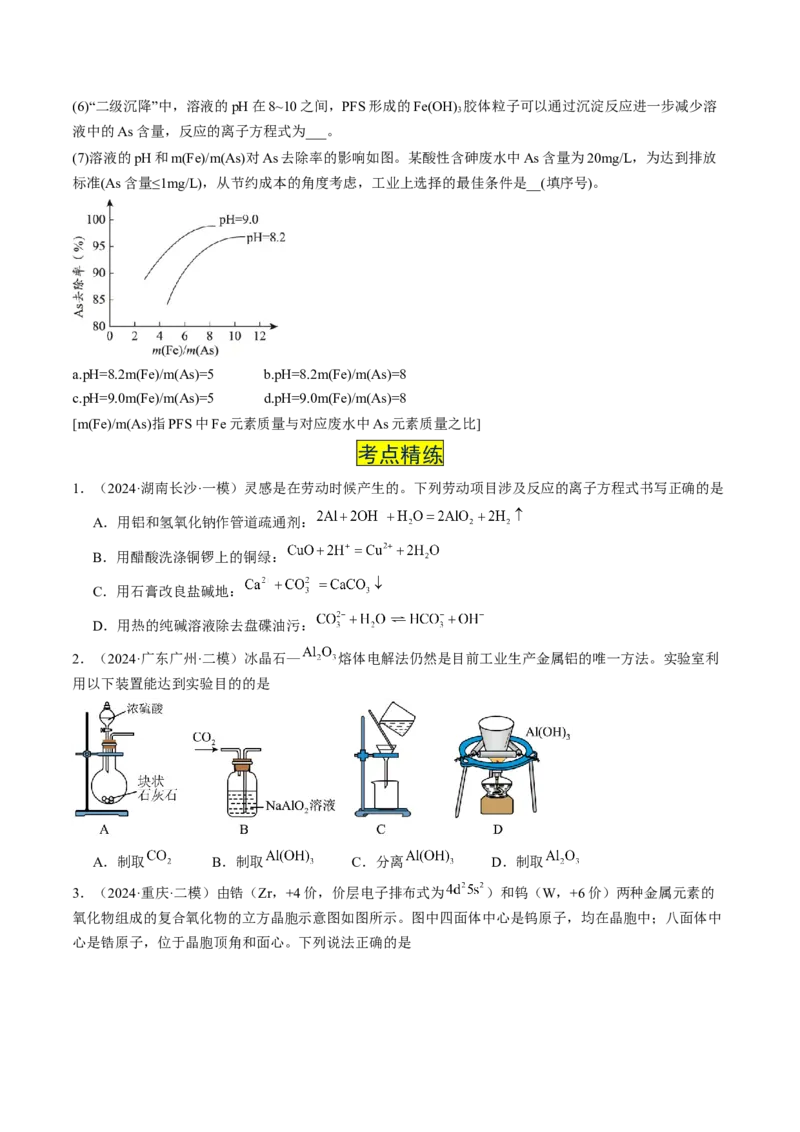
(7)溶液的pH和m(Fe)/m(As)对As去除率的影响如图。某酸性含砷废水中As含量为20mg/L,为达到排放
标准(As含量≤1mg/L),从节约成本的角度考虑,工业上选择的最佳条件是__(填序号)。
a.pH=8.2m(Fe)/m(As)=5 b.pH=8.2m(Fe)/m(As)=8
c.pH=9.0m(Fe)/m(As)=5 d.pH=9.0m(Fe)/m(As)=8
[m(Fe)/m(As)指PFS中Fe元素质量与对应废水中As元素质量之比]
考点精练
1.(2024·湖南长沙·一模)灵感是在劳动时候产生的。下列劳动项目涉及反应的离子方程式书写正确的是
A.用铝和氢氧化钠作管道疏通剂:
B.用醋酸洗涤铜锣上的铜绿:
C.用石膏改良盐碱地:
D.用热的纯碱溶液除去盘碟油污:
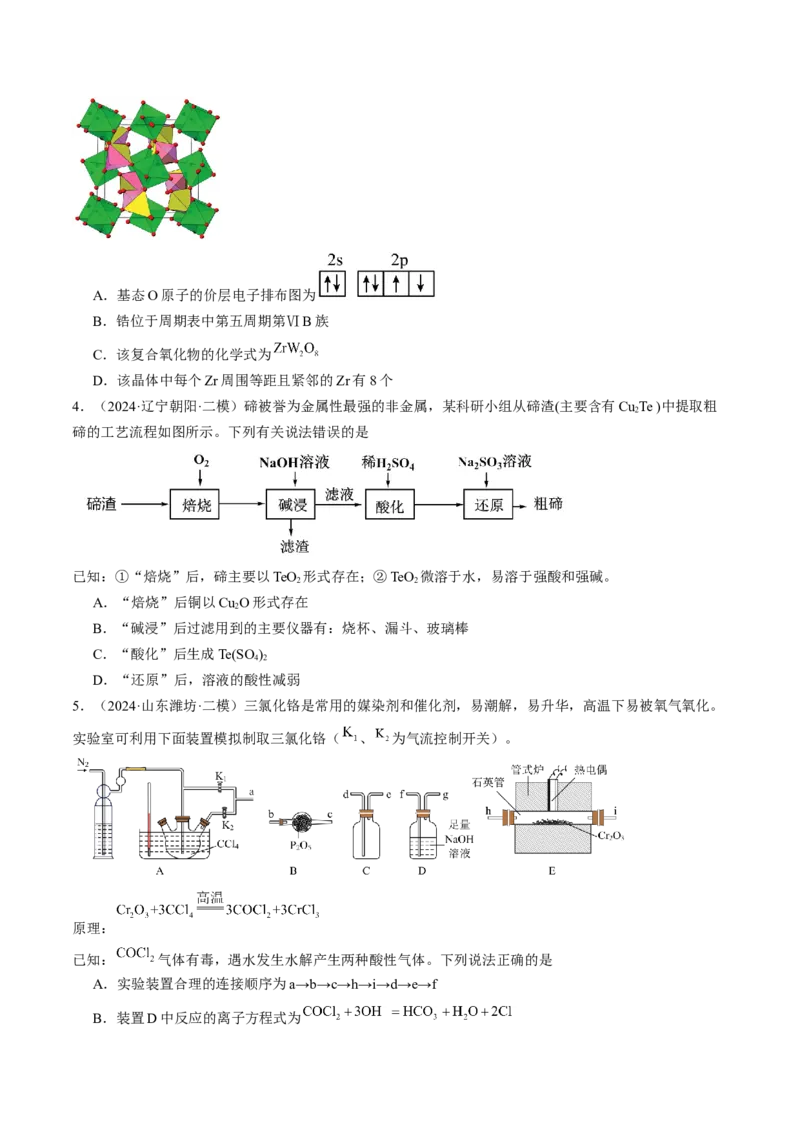
2.(2024·广东广州·二模)冰晶石— 熔体电解法仍然是目前工业生产金属铝的唯一方法。实验室利
用以下装置能达到实验目的的是
A.制取 B.制取 C.分离 D.制取
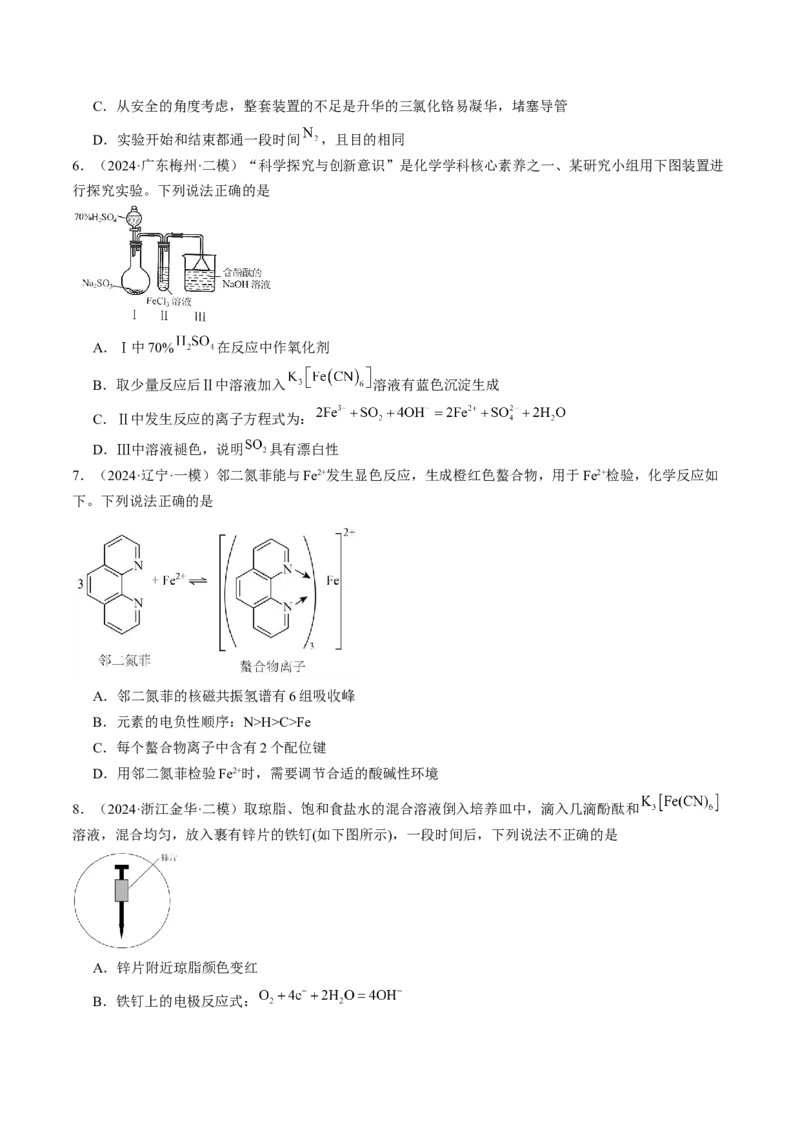
3.(2024·重庆·二模)由锆(Zr,+4价,价层电子排布式为 )和钨(W,+6价)两种金属元素的
氧化物组成的复合氧化物的立方晶胞示意图如图所示。图中四面体中心是钨原子,均在晶胞中;八面体中
心是锆原子,位于晶胞顶角和面心。下列说法正确的是A.基态O原子的价层电子排布图为
B.锆位于周期表中第五周期第ⅥB族
C.该复合氧化物的化学式为
D.该晶体中每个Zr周围等距且紧邻的Zr有8个
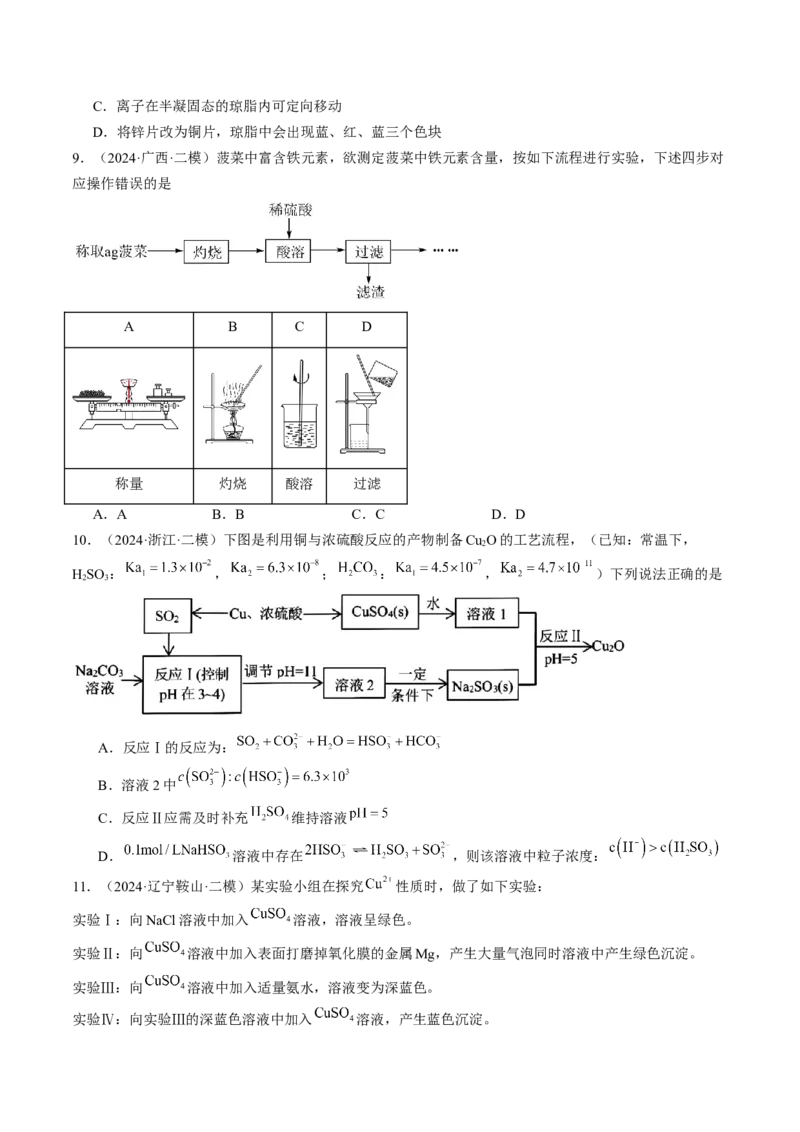
4.(2024·辽宁朝阳·二模)碲被誉为金属性最强的非金属,某科研小组从碲渣(主要含有Cu Te )中提取粗
2
碲的工艺流程如图所示。下列有关说法错误的是
已知:①“焙烧”后,碲主要以TeO 形式存在;②TeO 微溶于水,易溶于强酸和强碱。
2 2
A.“焙烧”后铜以Cu O形式存在
2
B.“碱浸”后过滤用到的主要仪器有:烧杯、漏斗、玻璃棒
C.“酸化”后生成Te(SO )
4 2
D.“还原”后,溶液的酸性减弱
5.(2024·山东潍坊·二模)三氯化铬是常用的媒染剂和催化剂,易潮解,易升华,高温下易被氧气氧化。
实验室可利用下面装置模拟制取三氯化铬( 、 为气流控制开关)。
原理:
已知: 气体有毒,遇水发生水解产生两种酸性气体。下列说法正确的是
A.实验装置合理的连接顺序为a→b→c→h→i→d→e→f
B.装置D中反应的离子方程式为C.从安全的角度考虑,整套装置的不足是升华的三氯化铬易凝华,堵塞导管
D.实验开始和结束都通一段时间 ,且目的相同
6.(2024·广东梅州·二模)“科学探究与创新意识”是化学学科核心素养之一、某研究小组用下图装置进
行探究实验。下列说法正确的是
A.Ⅰ中70% 在反应中作氧化剂
B.取少量反应后Ⅱ中溶液加入 溶液有蓝色沉淀生成
C.Ⅱ中发生反应的离子方程式为:
D.Ⅲ中溶液褪色,说明 具有漂白性
7.(2024·辽宁·一模)邻二氮菲能与Fe2+发生显色反应,生成橙红色螯合物,用于Fe2+检验,化学反应如
下。下列说法正确的是
A.邻二氮菲的核磁共振氢谱有6组吸收峰
B.元素的电负性顺序:N>H>C>Fe
C.每个螯合物离子中含有2个配位键
D.用邻二氮菲检验Fe2+时,需要调节合适的酸碱性环境
8.(2024·浙江金华·二模)取琼脂、饱和食盐水的混合溶液倒入培养皿中,滴入几滴酚酞和
溶液,混合均匀,放入裹有锌片的铁钉(如下图所示),一段时间后,下列说法不正确的是
A.锌片附近琼脂颜色变红
B.铁钉上的电极反应式:C.离子在半凝固态的琼脂内可定向移动
D.将锌片改为铜片,琼脂中会出现蓝、红、蓝三个色块
9.(2024·广西·二模)菠菜中富含铁元素,欲测定菠菜中铁元素含量,按如下流程进行实验,下述四步对
应操作错误的是
A B C D
称量 灼烧 酸溶 过滤
A.A B.B C.C D.D
10.(2024·浙江·二模)下图是利用铜与浓硫酸反应的产物制备Cu O的工艺流程,(已知:常温下,
2
HSO : , ; : , )下列说法正确的是
2 3
A.反应Ⅰ的反应为:
B.溶液2中
C.反应Ⅱ应需及时补充 维持溶液
D. 溶液中存在 ,则该溶液中粒子浓度:
11.(2024·辽宁鞍山·二模)某实验小组在探究 性质时,做了如下实验:
实验Ⅰ:向NaCl溶液中加入 溶液,溶液呈绿色。
实验Ⅱ:向 溶液中加入表面打磨掉氧化膜的金属Mg,产生大量气泡同时溶液中产生绿色沉淀。
实验Ⅲ:向 溶液中加入适量氨水,溶液变为深蓝色。
实验Ⅳ:向实验Ⅲ的深蓝色溶液中加入 溶液,产生蓝色沉淀。资料显示: 为黄色, 为绿色不溶物。
下列说法错误的是
A.实验Ⅰ: 在NaCl溶液中部分转化为
B.实验Ⅱ:Mg消耗了溶液中的 从而产生了
C.实验Ⅲ:有 生成
D.实验Ⅳ:获得的蓝色沉淀为
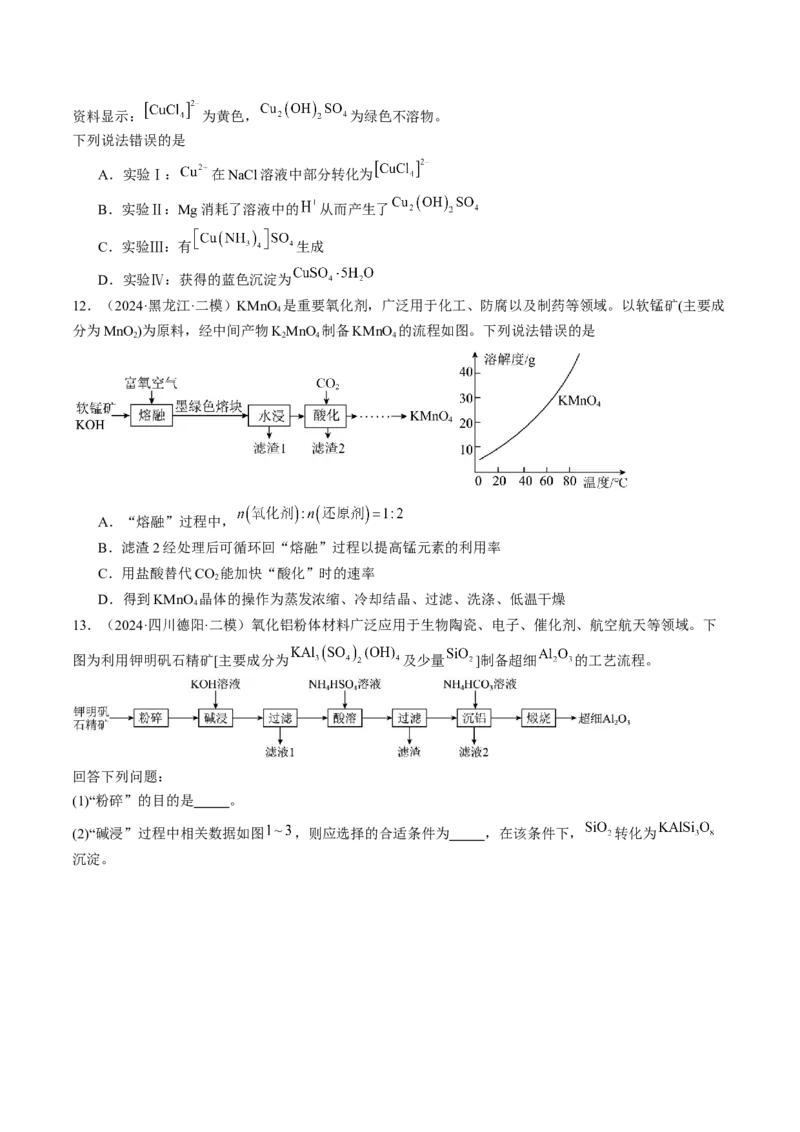
12.(2024·黑龙江·二模)KMnO 是重要氧化剂,广泛用于化工、防腐以及制药等领域。以软锰矿(主要成
4
分为MnO )为原料,经中间产物KMnO 制备KMnO 的流程如图。下列说法错误的是
2 2 4 4
A.“熔融”过程中,
B.滤渣2经处理后可循环回“熔融”过程以提高锰元素的利用率
C.用盐酸替代CO 能加快“酸化”时的速率
2
D.得到KMnO 晶体的操作为蒸发浓缩、冷却结晶、过滤、洗涤、低温干燥
4
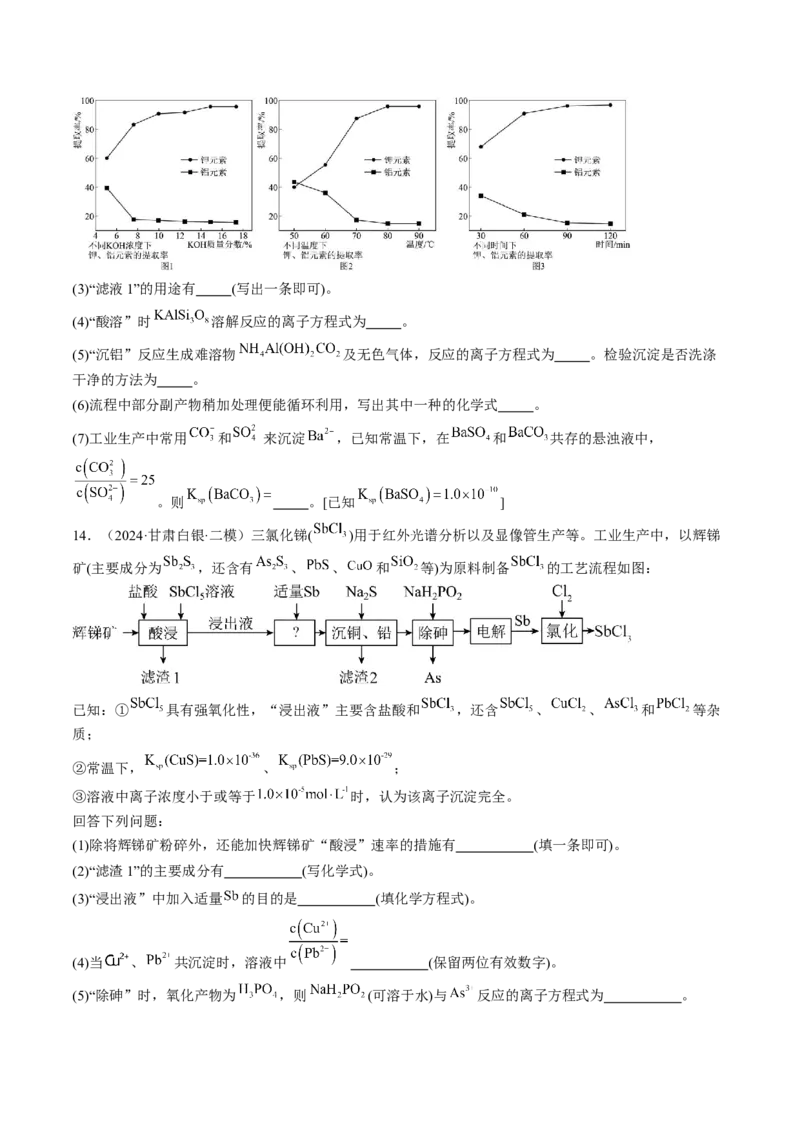
13.(2024·四川德阳·二模)氧化铝粉体材料广泛应用于生物陶瓷、电子、催化剂、航空航天等领域。下
图为利用钾明矾石精矿[主要成分为 及少量 ]制备超细 的工艺流程。
回答下列问题:
(1)“粉碎”的目的是 。
(2)“碱浸”过程中相关数据如图 ,则应选择的合适条件为 ,在该条件下, 转化为
沉淀。(3)“滤液1”的用途有 (写出一条即可)。
(4)“酸溶”时 溶解反应的离子方程式为 。
(5)“沉铝”反应生成难溶物 及无色气体,反应的离子方程式为 。检验沉淀是否洗涤
干净的方法为 。
(6)流程中部分副产物稍加处理便能循环利用,写出其中一种的化学式 。
(7)工业生产中常用 和 来沉淀 ,已知常温下,在 和 共存的悬浊液中,
。则 。[已知 ]
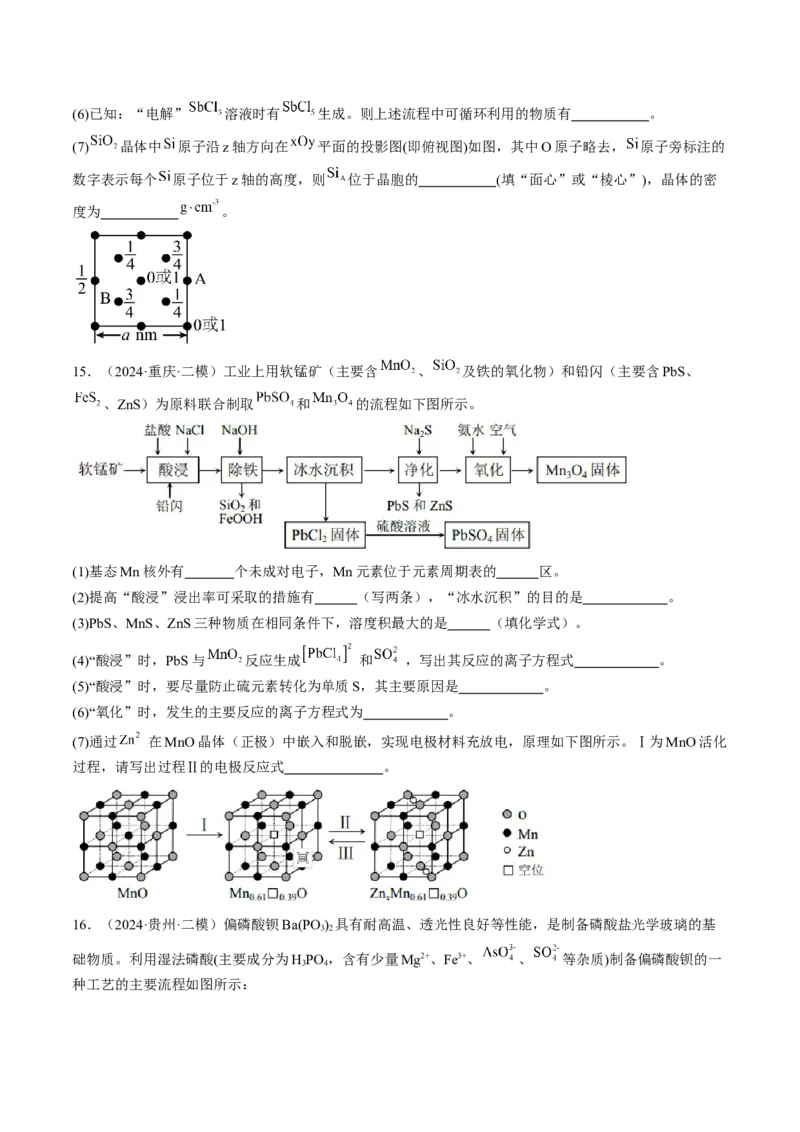
14.(2024·甘肃白银·二模)三氯化锑( )用于红外光谱分析以及显像管生产等。工业生产中,以辉锑
矿(主要成分为 ,还含有 、 、 和 等)为原料制备 的工艺流程如图:
已知:① 具有强氧化性,“浸出液”主要含盐酸和 ,还含 、 、 和 等杂
质;
②常温下, 、 ;
③溶液中离子浓度小于或等于 时,认为该离子沉淀完全。
回答下列问题:
(1)除将辉锑矿粉碎外,还能加快辉锑矿“酸浸”速率的措施有 (填一条即可)。
(2)“滤渣1”的主要成分有 (写化学式)。
(3)“浸出液”中加入适量 的目的是 (填化学方程式)。
(4)当 、 共沉淀时,溶液中 (保留两位有效数字)。
(5)“除砷”时,氧化产物为 ,则 (可溶于水)与 反应的离子方程式为 。(6)已知:“电解” 溶液时有 生成。则上述流程中可循环利用的物质有 。
(7) 晶体中 原子沿z轴方向在 平面的投影图(即俯视图)如图,其中O原子略去, 原子旁标注的
数字表示每个 原子位于z轴的高度,则 位于晶胞的 (填“面心”或“棱心”),晶体的密
度为 。
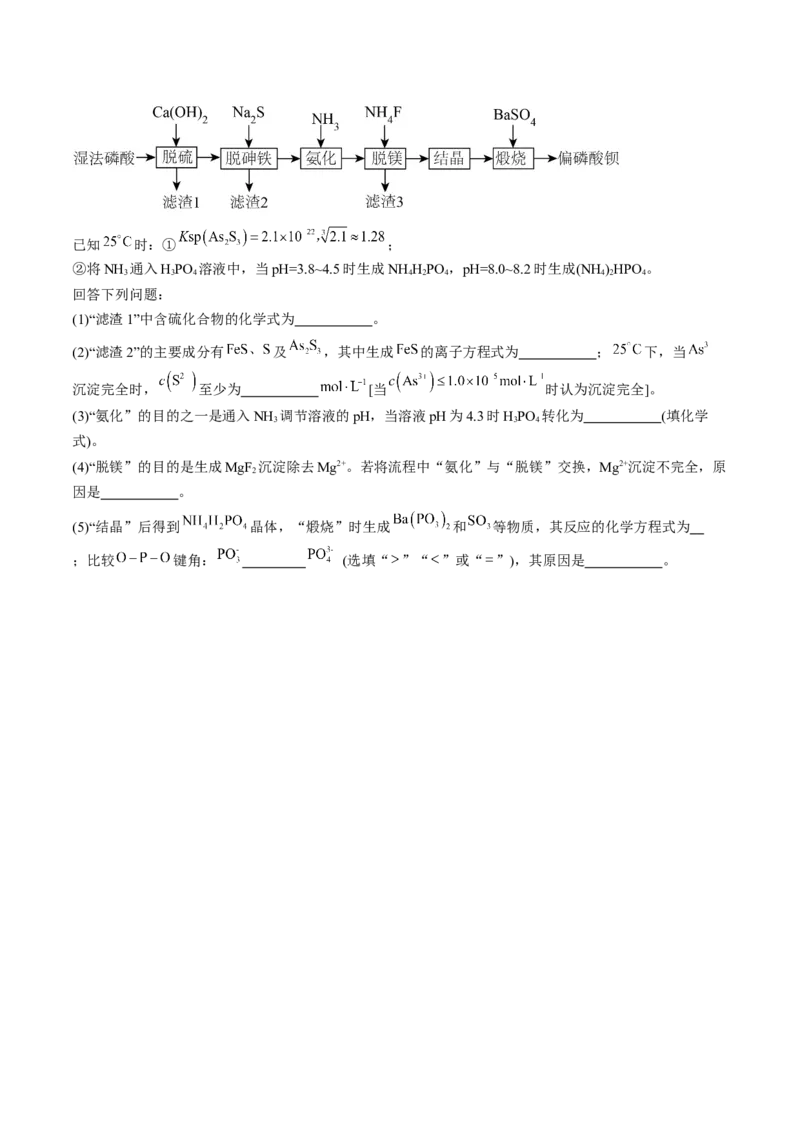
15.(2024·重庆·二模)工业上用软锰矿(主要含 、 及铁的氧化物)和铅闪(主要含PbS、
、ZnS)为原料联合制取 和 的流程如下图所示。
(1)基态Mn核外有 个未成对电子,Mn元素位于元素周期表的 区。
(2)提高“酸浸”浸出率可采取的措施有 (写两条),“冰水沉积”的目的是 。
(3)PbS、MnS、ZnS三种物质在相同条件下,溶度积最大的是 (填化学式)。
(4)“酸浸”时,PbS与 反应生成 和 ,写出其反应的离子方程式 。
(5)“酸浸”时,要尽量防止硫元素转化为单质S,其主要原因是 。
(6)“氧化”时,发生的主要反应的离子方程式为 。
(7)通过 在MnO晶体(正极)中嵌入和脱嵌,实现电极材料充放电,原理如下图所示。Ⅰ为MnO活化
过程,请写出过程Ⅱ的电极反应式 。
16.(2024·贵州·二模)偏磷酸钡Ba(PO) 具有耐高温、透光性良好等性能,是制备磷酸盐光学玻璃的基
3 2
础物质。利用湿法磷酸(主要成分为HPO ,含有少量Mg2+、Fe3+、 、 等杂质)制备偏磷酸钡的一
3 4
种工艺的主要流程如图所示:已知 时:① ;
②将NH 通入HPO 溶液中,当pH=3.8~4.5时生成NH HPO ,pH=8.0~8.2时生成(NH )HPO 。
3 3 4 4 2 4 4 2 4
回答下列问题:
(1)“滤渣1”中含硫化合物的化学式为 。
(2)“滤渣2”的主要成分有 及 ,其中生成 的离子方程式为 ; 下,当
沉淀完全时, 至少为 [当 时认为沉淀完全]。
(3)“氨化”的目的之一是通入NH 调节溶液的pH,当溶液pH为4.3时HPO 转化为 (填化学
3 3 4
式)。
(4)“脱镁”的目的是生成MgF 沉淀除去Mg2+。若将流程中“氨化”与“脱镁”交换,Mg2+沉淀不完全,原
2
因是 。
(5)“结晶”后得到 晶体,“煅烧”时生成 和 等物质,其反应的化学方程式为
;比较 键角: (选填“ ”“ ”或“ ”),其原因是 。