文档内容
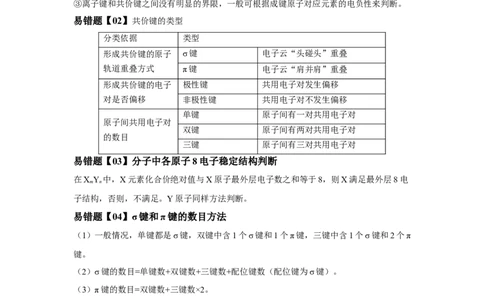
易错点 15 化学键
易错题【01】离子键和共价键
①由活泼金属与活泼非金属形成的化学键不一定都是离子键,如AlCl 中Al—Cl键为共价
3
键。
②非金属元素的两个原子之间一定形成共价键,但多个原子间也可能形成离子键,如
NH Cl等。
4
③离子键和共价键之间没有明显的界限,一般可根据成键原子对应元素的电负性来判断。
易错题【02】共价键的类型
分类依据 类型
形成共价键的原子 σ键 电子云“头碰头”重叠
轨道重叠方式 π键 电子云“肩并肩”重叠
形成共价键的电子 极性键 共用电子对发生偏移
对是否偏移 非极性键 共用电子对不发生偏移
单键 原子间有一对共用电子对
原子间共用电子对
双键 原子间有两对共用电子对
的数目
三键 原子间有三对共用电子对
易错题【03】分子中各原子8电子稳定结构判断
在X Y 中,X元素化合价绝对值与X原子最外层电子数之和等于8,则X满足最外层8电
m n
子结构,否则,不满足。Y原子同样方法判断。
易错题【04】σ键和π键的数目方法
(1)一般情况,单键都是σ键,双键中含1个σ键和1个π键,三键中含1个σ键和2个π
键。
(2)σ键的数目=单键数+双键数+三键数+配位键数(配位键为σ键)。
(3)π键的数目=双键数+三键数×2。
易错题【05】配位键
(1)判断配位数:配位数就是在配位体中与中心原子(或离子)成键的配位原子的总数。
若是由单齿配体(1个配体提供1个配位原子)形成的配合物,中心原子(或离子)的配
位数=配位体的数目。若是由双齿配体(1个配体提供2个配位原子)形成的配合物,中心
原子(或离子)的配位数=配位体的数目×2。
(2)判断配位键的稳定性:一般情况,与同种金属原子(或离子)形成配位键时,配位原
子的电负性越小,形成配位键就越稳定。例如,电负性:N<O,则配离子的稳定性:[Cu(NH )]2+>[Cu(H O) ]2+。
3 4 2 4
典例分析
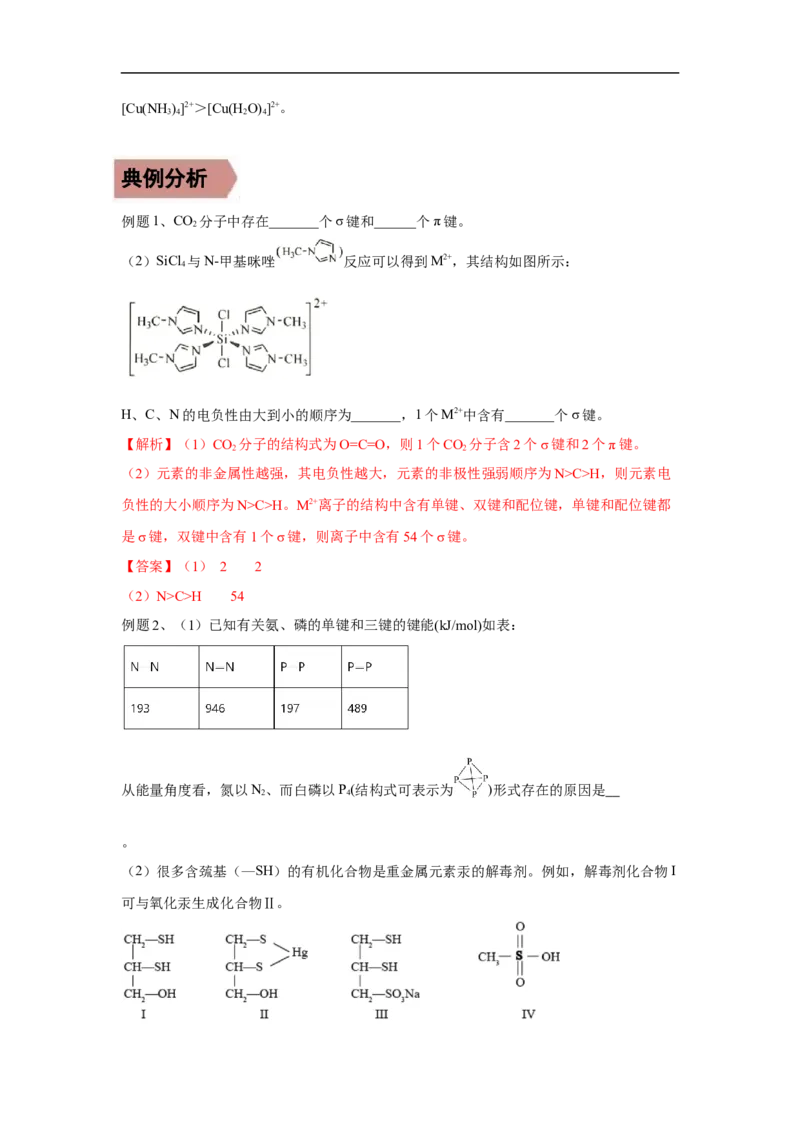
例题1、CO 分子中存在_______个σ键和______个π键。
2
(2)SiCl 与N-甲基咪唑 反应可以得到M2+,其结构如图所示:
4
H、C、N的电负性由大到小的顺序为_______,1个M2+中含有_______个σ键。
【解析】(1)CO 分子的结构式为O=C=O,则1个CO 分子含2个σ键和2个π键。
2 2
(2)元素的非金属性越强,其电负性越大,元素的非极性强弱顺序为N>C>H,则元素电
负性的大小顺序为N>C>H。M2+离子的结构中含有单键、双键和配位键,单键和配位键都
是σ键,双键中含有1个σ键,则离子中含有54个σ键。
【答案】(1) 2 2
(2)N>C>H 54
例题2、(1)已知有关氨、磷的单键和三键的键能(kJ/mol)如表:
从能量角度看,氮以N、而白磷以P(结构式可表示为 )形式存在的原因是
2 4
。
(2)很多含巯基(—SH)的有机化合物是重金属元素汞的解毒剂。例如,解毒剂化合物I
可与氧化汞生成化合物Ⅱ。化合物Ⅲ也是一种汞解毒剂。化合物Ⅳ是一种强酸。下列说法正确的有________。
A. 在I中S原子采取sp3杂化
B. 在Ⅱ中S元素的电负性最大
C. 在Ⅲ中C—C—C键角是180°
D. 在Ⅲ中存在离子键与共价键
E. 在Ⅳ中硫氧键的键能均相等
【解析】(1)根据表中的相关共价键的键能可知,若6mol N形成类似白磷分子结构的N
4
分子,可以释放出的能量为193kJ6=1158kJ;若6mol N形成N 分子,则可释放的能量为
2
946kJ2=1892kJ,显然,形成N 分子放出的能量更多,故在N数目相同的条件下,N 具有
2 2
更低的能量,能量越低越稳定。同理,若6mol P形成P 分子,可以释放出的能量为
4
197kJ6=1182kJ;若6mol P形成P 分子,则可释放的能量为489kJ2=978kJ,显然,形成
2
P 分子放出的能量更多,故在P数目相同的条件下,P 具有更低的能量,能量越低越稳定。
4 4
(2)I中S原子形成2个σ键,且有2对孤电子对,则S原子采取sp3杂化,A正确;II中
元素电负性:O>S>C>H>Hg,电负性最大的是O,B错误;III中C原子采取sp3杂化,
故C—C—C键角小于180°,C错误;III是一种钠盐,含有离子键和共价键,D正确;IV
中S—O键和S=O键的键长不同,则其键角不同,E错误。
【答案】(1)在原子数目相同的条件下,N 比N 具有更低的能量,而P 比P 具有更低的
2 4 4 2
能量,能量越低越稳定
(2)AD
例题3、(1)三价铬离子能形成多种配位化合物。[Cr(NH )(H O) Cl]2+
3 3 2 2
中提供电子对形成配位键的原子是_______,中心离子的配位数为_______。
(2)NH BH 分子中,N—B化学键称为 键,其电子对由 提供。
3 3
(3) [Fe(H O) ]2+中与Fe2+配位的原子是 (填元素符号)。
2 6
(4)含有多个配位原子的配体与同一中心离子(或原子)通过螯合配位成环而形成的配合物
为螯合物。一种Cd2+配合物的结构如图所示,1 mol该配合物中通过螯合作用形成的配位键
有 mol。
【解析】(1)[Cr(NH )(H O) Cl]2+中心离子是Cr3+,配位体为NH 、HO和Cl—,故中心离
3 3 2 2 3 2
子的配位数为3+2+1=6;提供电子对形成配位键的原子是N、O、Cl。
(2)NH BH 分子中,N原子提供孤电子对,B原子提供空轨道,形成配位键(N→B)。
3 3
(3)[Fe(H O) ]2+中,HO是配位体,O原子提供孤电子对与Fe2+配位。
2 6 2(4)Cd2+配合物中, 提供2个N原子,左侧NO —提供2个O原子,均与Cd2+通
3
过螯合作用形成配位键,右侧—NO 中N原子与Cd形成共价键,故1mol该配合物形成的
2
配位键有6 mol。
【答案】(1)N、O、Cl 6
(2)配位 N(或氮)
(3)O (4)6
1.(2022·辽宁·高考真题)理论化学模拟得到一种 离子,结构如图。下列关于该离子
的说法错误的是
A.所有原子均满足8电子结构 B.N原子的杂化方式有2种
C.空间结构为四面体形 D.常温下不稳定
2.(2021·江苏·高考真题)反应Cl+2NaOH=NaClO+NaCl+H O可用于制备含氯消毒剂。
2 2
下列说法正确的是
A.Cl 是极性分子
2
B.NaOH的电子式为
C.NaClO既含离子键又含共价键
D.Cl-与Na+具有相同的电子层结构
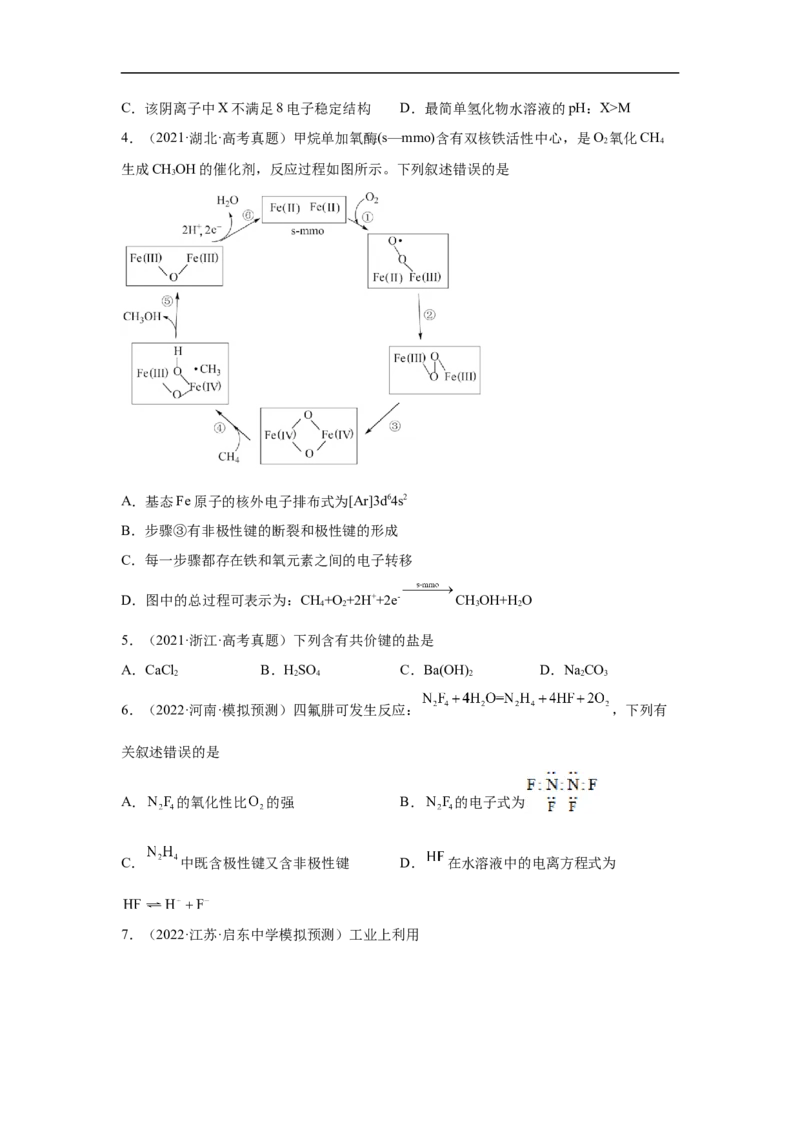
3.(2021·湖北·高考真题)某离子液体的阴离子的结构如图所示,其中W、X、Y、Z、M
为原子序数依次增大的短周期非金属元素,W是有机分子的骨架元素。下列说法正确的是
A.Z元素的最高价态为+7 B.基态原子未成对电子数:W>YC.该阴离子中X不满足8电子稳定结构 D.最简单氢化物水溶液的pH:X>M
4.(2021·湖北·高考真题)甲烷单加氧酶(s—mmo)含有双核铁活性中心,是O 氧化CH
2 4
生成CHOH的催化剂,反应过程如图所示。下列叙述错误的是
3
A.基态Fe原子的核外电子排布式为[Ar]3d64s2
B.步骤③有非极性键的断裂和极性键的形成
C.每一步骤都存在铁和氧元素之间的电子转移
D.图中的总过程可表示为:CH+O +2H++2e- CHOH+H O
4 2 3 2
5.(2021·浙江·高考真题)下列含有共价键的盐是
A.CaCl B.HSO C.Ba(OH) D.NaCO
2 2 4 2 2 3
6.(2022·河南·模拟预测)四氟肼可发生反应: ,下列有
关叙述错误的是
A. 的氧化性比 的强 B. 的电子式为
C. 中既含极性键又含非极性键 D. 在水溶液中的电离方程式为
7.(2022·江苏·启东中学模拟预测)工业上利用制备无水 。下列说法正确的是
A. 为非极性分子
B. 中既含离子键又含共价键
C. 的电子式为
D.基态O原子的价电子排布式为
8.(2022·上海金山·二模)NaI晶体中两核间距约0.28 nm,呈共价键;激光脉冲照射NaI
时,Na+和I—两核间距为1.0~1.5 nm,呈离子键。下列说法正确的是
A.离子化合物中不可能含共价键
B.共价键和离子键之间没有明显界线
C.NaI晶体中既有离子键又有共价键
D.NaI晶体是离子化合物和共价化合物的混合物
9.(2022·江苏淮安·模拟预测)工业上利用MgCl •6H O+6SOCl MgCl +6SO↑+12HCl↑
2 2 2 2 2
制备无水MgCl 。下列说法正确的是
2
A.SO 为非极性分子 B.MgCl 中既含离子键又含共价键
2 2
C.HO的电子式为 D.基态O原子的电子排布式为1s22s22p4
2
10.(2022·北京·杨镇第一中学模拟预测)硼氢化钠(NaBH )与水在催化剂作用下获得氢气
4
的微观过程如下图所示。下列说法正确的是
A.NaBH 中含有离子键和非极性共价键
4B.BH 中 B—H 键键长小于 HO 中 O—H 键键长
3 2
C.整个过程中涉及的含硼微粒有 6 种
D.每产生 1mol H 转移 2mol 电子
2
11.(2022·北京·101中学三模)NH Cl的晶胞为立方体,其结构如下。下列说法不正确的
4
是
A.NH Cl晶体属于离子晶体
4
B.NH Cl晶胞中H-N-H键角为90°
4
C.NH Cl晶体中既有离子键又有共价键
4
D.每个Cl-周围与它最近且等距离的 的数目为8
12.(2022·湖北·襄阳五中模拟预测)复兴号高铁车体材质用到Mn、Co等元素。Mn的一
种配合物化学式为 ,下列说法错误的是
A.Mn原子的配位数为6
B. 与Mn原子配位时,提供孤电子对的是N原子
C. 中C原子的杂化类型为 、
D. 中σ键和π键数目之比为5∶2
13.(2022·河南开封·模拟预测)固体电解质的化学式为WXY Z,其中W、X、Y、Z为
6 5
原子序数依次增大的短周期主族元素,w为金属,且最外层电子数是次外层的一半,X、
Y、Z为第三周期的非金属元素。下列说法正确的是
A.单质W不能与水反应
B.X的单质有多种同素异形体
C.简单离子半径:X”或“<”)。
(5)元素e在周期表中的位置是___区;e的一种常见氯化物中的化学键具有明显的共价性,
蒸汽状态下以双聚分子存在,结构式为 ,请补写e的元素符号并用
“→”表示出其中的配位键___。
17.(2022南靖县第一中学一模)A、B、C、D、E是元素周期表前四周期中的常见元素,
原子序数依次增大,相关信息如下:
元素 相关信息
A 基态原子的价电子排布式为nSnnPn
B 元素原子的核外p电子数比s电子数少1个
C 最外层电子数是电子层数的3倍
D 简单离子是第三周期元素中离子半径最小的
E 价电子层中的未成对电子数为4
请回答下列问题:
(1)写出下列元素的名称:A______, B_______, C________,D__________
(2)写出C元素在周期表的位置_________,E2+价电子的轨道表示式________________,B
元素能量最高的电子为_____轨道上的电子,其轨道呈_______形.
(3)按原子轨道的重叠方式,1molA与C形成的最高价化合物中σ键有______个,π键有
______个。
(4)B、C、D的简单离子的半径由大到小的顺序为_____________(用离子符号表示)。
(5)写出C的核外有18个电子的氢化物的电子式_____________。
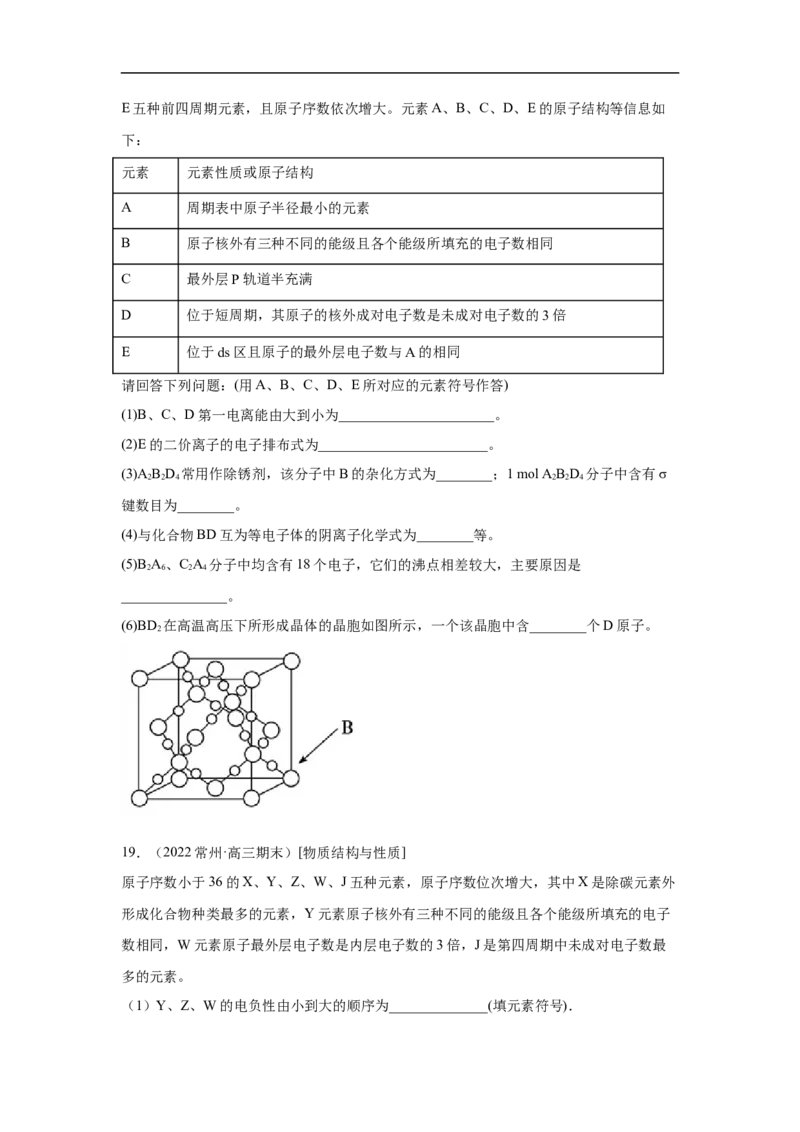
18.(2022西藏日喀则·高三期末)我国从国外进口某原料经测定主要含有A、B、C、D、E五种前四周期元素,且原子序数依次增大。元素A、B、C、D、E的原子结构等信息如
下:
元素 元素性质或原子结构
A 周期表中原子半径最小的元素
B 原子核外有三种不同的能级且各个能级所填充的电子数相同
C 最外层P轨道半充满
D 位于短周期,其原子的核外成对电子数是未成对电子数的3倍
E 位于ds区且原子的最外层电子数与A的相同
请回答下列问题:(用A、B、C、D、E所对应的元素符号作答)
(1)B、C、D第一电离能由大到小为______________________。
(2)E的二价离子的电子排布式为________________________。
(3)A B D 常用作除锈剂,该分子中B的杂化方式为________;1 mol AB D 分子中含有σ
2 2 4 2 2 4
键数目为________。
(4)与化合物BD互为等电子体的阴离子化学式为________等。
(5)B A、C A 分子中均含有18个电子,它们的沸点相差较大,主要原因是
2 6 2 4
_______________。
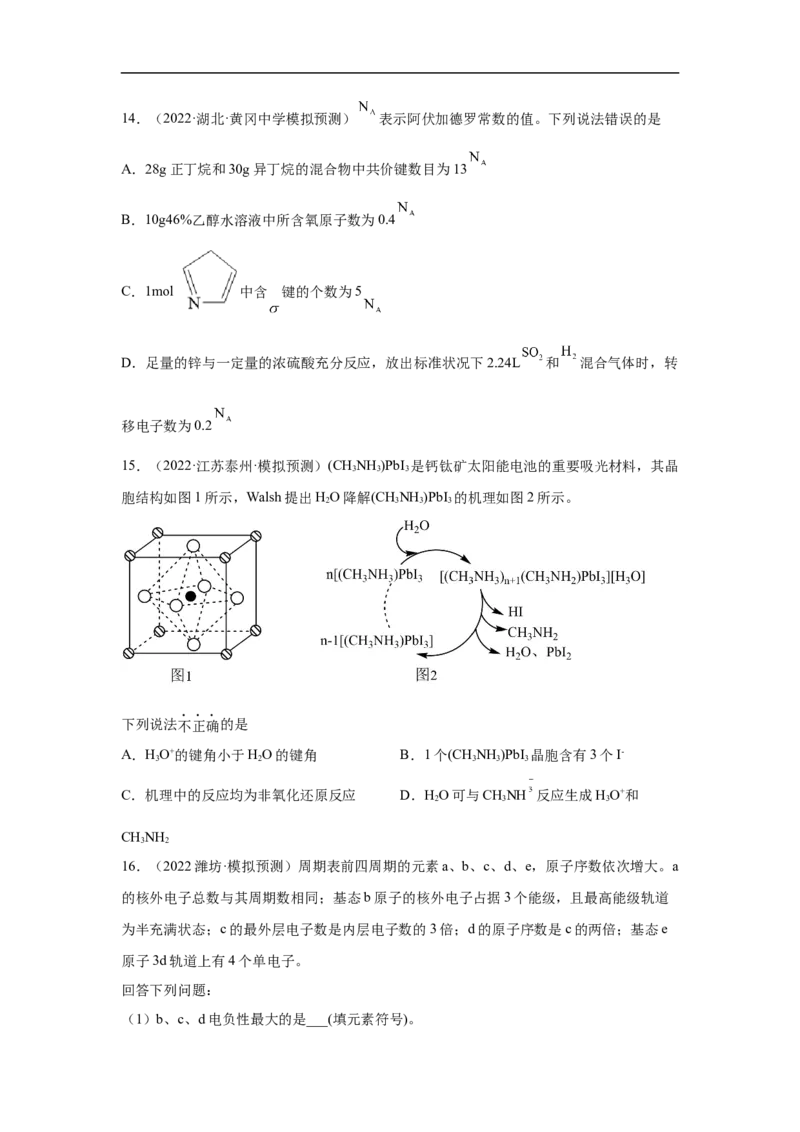
(6)BD 在高温高压下所形成晶体的晶胞如图所示,一个该晶胞中含________个D原子。
2
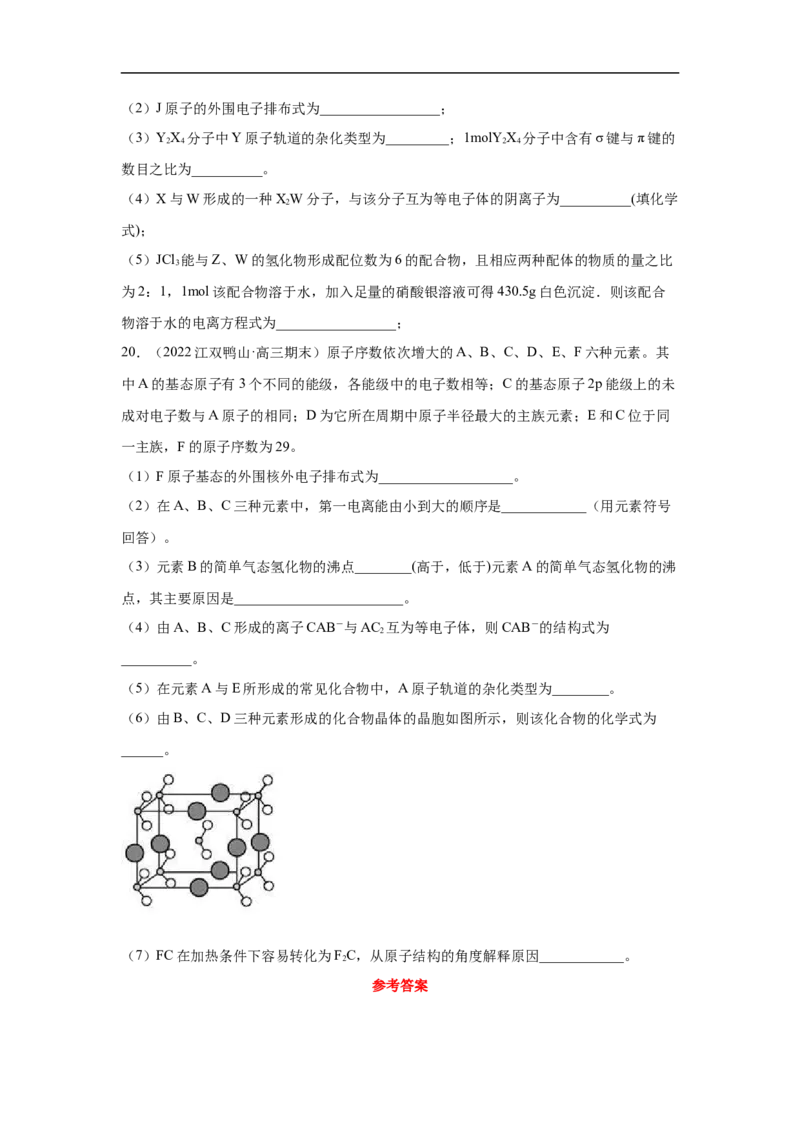
19.(2022常州·高三期末)[物质结构与性质]
原子序数小于36的X、Y、Z、W、J五种元素,原子序数位次增大,其中X是除碳元素外
形成化合物种类最多的元素,Y元素原子核外有三种不同的能级且各个能级所填充的电子
数相同,W元素原子最外层电子数是内层电子数的3倍,J是第四周期中未成对电子数最
多的元素。
(1)Y、Z、W的电负性由小到大的顺序为______________(填元素符号).(2)J原子的外围电子排布式为_________________;
(3)YX 分子中Y原子轨道的杂化类型为_________;1molY X 分子中含有σ键与π键的
2 4 2 4
数目之比为__________。
(4)X与W形成的一种XW分子,与该分子互为等电子体的阴离子为__________(填化学
2
式);
(5)JCl 能与Z、W的氢化物形成配位数为6的配合物,且相应两种配体的物质的量之比
3
为2:1,1mol该配合物溶于水,加入足量的硝酸银溶液可得430.5g白色沉淀.则该配合
物溶于水的电离方程式为_________________;
20.(2022江双鸭山·高三期末)原子序数依次增大的A、B、C、D、E、F六种元素。其
中A的基态原子有3个不同的能级,各能级中的电子数相等;C的基态原子2p能级上的未
成对电子数与A原子的相同;D为它所在周期中原子半径最大的主族元素;E和C位于同
一主族,F的原子序数为29。
(1)F原子基态的外围核外电子排布式为___________________。
(2)在A、B、C三种元素中,第一电离能由小到大的顺序是____________(用元素符号
回答)。
(3)元素B的简单气态氢化物的沸点________(高于,低于)元素A的简单气态氢化物的沸
点,其主要原因是________________________。
(4)由A、B、C形成的离子CAB-与AC 互为等电子体,则CAB-的结构式为
2
__________。
(5)在元素A与E所形成的常见化合物中,A原子轨道的杂化类型为________。
(6)由B、C、D三种元素形成的化合物晶体的晶胞如图所示,则该化合物的化学式为
______。
(7)FC在加热条件下容易转化为FC,从原子结构的角度解释原因____________。
2
参考答案1.B【详解】A.由 的结构式可知,所有N原子均满足8电子稳定结构,A正确;
B.中心N原子为 杂化,与中心N原子直接相连的N原子为 杂化,与端位N原子直
接相连的N原子为 杂化,端位N原子为 杂化,则N原子的杂化方式有3种,B错误;
C.中心N原子为 杂化,则其空间结构为四面体形,C正确;
D. 中含叠氨结构( ),常温下不稳定,D正确;
故答案选B。
2.C【详解】A.氯气分子结构对称,正负电荷中心重合,为非极性分子,A错误;
B.NaOH为离子化合物,电子式为 ,B错误;
C.NaClO含有钠离子和次氯酸根形成的离子键,含有O原子和Cl原子形成的共价键,C
正确;
D.Cl-有3层电子,Na+有2层电子,D错误;
综上所述答案为C。
3.D【详解】根据W是有机分子的骨架元素,知W为C元素:由图可如,Y形成1个双
键,则其最外层有6个电子,结合原子序数关系知,Y为O元素,则X为N元素;Z形成
1个单键,则Z为F元素;M的成键总数为6,则M为S元素。以此解答。
【详解】A.根据上述分析可知:Z为F元素,无正化合价,故A错误;
B.根据上述分析可知:W为C元素,Y为O元素。C原子的电子排布式为 ,未
成对电子数为2,O原子的电子排布式为 ,未成对电子数也为2,故B错误;
C.根据上述分析可知:X为N元素,该阴离子中N形成2个单键,有2对孤对电子,满足
8电子稳定结构,故C错误:
D.根据上述分析可知:X为N元素, 最简单氢化物 , 的水溶液星碱性;M为S元
素, 最简单氢化物 , 的水溶液呈酸性,故水溶液的 ,故D正确;
故答案:D。4.C【详解】A.基态Fe原子核外有26个电子,其核外电子排布式为 ,A项正确;
B.步骤③中断裂 非极性键,形成 (Ⅳ)极性键,B项正确;
C.步骤④中电子转移发生在Fe和C元素之间,C项错误;
D.根据图示,总过程的反应为: ,D项正确;
故选C。
5.D【详解】A.CaCl 由Ca2+和Cl-构成,只含有离子键不含有共价键,A不符合题意;
2
B.HSO 由分子构成,只含有共价键不含有离子键,B不符合题意;
2 4
C.Ba(OH) 由Ba2+和OH-构成,属于碱,不属于盐,C不符合题意;
2
D.NaCO 有Na+和CO 构成,含有离子键,CO 内部C与O原子之间还含有共价键,D
2 3
符合题意;
故答案选D。
6.B【详解】A.反应中 作氧化剂,氧气是氧化产物,所以 的氧化性比 的强,
正确;
B. 中氟原子周用应满足 结构,电子式为 ,B错误。
C. 的电子式为 ,其中既含极性键又含非极性键,C正确;
D. 是一元弱酸,在水溶液中的电离方程式为 ,D正确;
答案选B。
7.D【详解】A.利用AB 型分子极性的判断方法可知,中心硫原子化合价的绝对值不等
n
于最外层电子数, 为极性分子,A错误;
B. 中Mg2+分别于两个Cl-形成离子键,两个Cl-之间无化学键,则 中只含离
子键,B错误;
C. 为共价化合物,其电子式为 ,C错误;D.O为8号元素,基态O原子的价电子排布式为 ,D正确;
故选D。
8.B【详解】A.离子化合物中可能含共价键,如过氧化钠是含有离子键和共价键的离子
化合物,故A错误;
B.由题给信息可知,碘化钠晶体中核间距发生变化时,化学键的类型发生变化,所以共
价键和离子键之间没有明显界线,故B正确;
C.由题给信息可知,晶体中核间距发生变化时,化学键的类型发生变化,则在状态相同
时,两种原子组成的晶体中不可能同时存在离子键和共价键,故C错误;
D.由碘化钠晶体的组成可知,晶体是由同种物质形成的纯净物,故D错误;
故选B。
9.D【详解】A.二氧化硫是极性分子,是sp2杂化,二氧化硫分子并不是直线形的,它是
V形分子,硫氧键的极性不能互相抵消,所以是极性分子,A项错误;
B.MgCl 中只有镁离子、氯离子形成的离子键,B项错误;
2
C.HO的电子式为 ,C项错误;
2
D.基态O原子的电子排布式为1s22s22p4,D项正确;
答案选D。
10.C【详解】硼氢化钠(NaBH )与水在催化剂作用下获得氢气的总反应方程式为:
4
。
【详解】A.NaBH 为离子化合物,阳离子和阴离子之间为离子键,B-H之间为极性共价
4
键,A错误;
B.B原子半径大于O原子,半径越大,键长越长,键能越小,故BH 中 B—H 键键长大
3
于 HO 中 O—H 键键长,B错误;
2
C.整个过程中涉及的含硼微粒有 ,共6
种,C正确;
D.根据总反应方程式可知,每生成1mol H 转移 1mol 电子,D错误;
2
故选C。11.B【详解】A.氯化铵由铵根离子和氯离子构成,为离子晶体,A正确;
B.铵根离子中N原子杂化方式为sp3杂化,键角为109。28',B错误;
C.NH Cl晶体中铵根和氯离子之间为离子键,氮原子和氢原子之间为共价键,C正确;
4
D.根据晶胞结构可知每个Cl-周围与它最近且等距离的铵根离子的数目为8,在周围八个
立方体体心位置,D正确;
故选B。
12.C【详解】A.由化学式可知,配合物中锰原子为中心原子,一氧化碳和 为配
体,配位数为6,故A正确;
B. 的结构简式为CHC≡N,与锰原子配位时,提供孤电子对的是形成碳氮三键的
3
氮原子,故B正确;
C. 的结构简式为CHC≡N,分子中单键碳原子为sp3杂化、三键碳原子为sp杂化,
3
故C错误;
D. 的结构简式为CHC≡N,分子中单键为σ键,三键中含有1个σ键和2个π键,
3
σ键和π键数目之比为5∶2,故D正确;
故选C。
13.B【详解】W、X、Y、Z为原子序数依次增大的短周期主族元素,w为金属,且最外
层电子数是次外层的一半,W是Li元素;X、Y、Z为第三周期的非金属元素,根据
LiXY Z元素化合价代数和等于0,可知X是P元素、Y是S元素、Z是Cl元素。
6 5
A.W是Li,单质Li能与水反应生成LiOH和H,故A错误;
2
B.X是P元素,有白磷、红磷等多种同素异形体,故B正确;
C.电子层数相同,质子数越多半径越小,简单离子半径:Cl-III 、V>VI ,第一电离能大小顺序是
A A A A
N>O>C;
(3)B的氢化物是NH ,A的简单氢化物是CH,NH 分子之间存在氢键,而CH 分子间的
3 4 3 4
作用是范德华力,氢键比范德华力更强;
(4)CAB-的化学式为OCN-,AC 的化学式为CO,两者为等电子体,它们的结构相似,因
2 2
此OCN-的结构式为:[N=C=O]−;
(5)形成的化合物是CS,结构式为S=C=S,杂化轨道数等于价层电子对数,即C的杂化类
2型为sp;
(6)根据半径大小,大黑球是Na,大黑球位于晶胞的棱上,因此真正属于晶胞的个数为8×
=2,大白球为N,小白球为O,两者形成离子是NO -,其位于顶点和体心,真正的个数
2
为8× +1=2,因此化学式为NaNO ;
2
(7)FC为CuO,FC为Cu O,Cu的核外电子排布式1s22s22p63s23p63d104s1,Cu2+的电子排布
2 2
式为1s22s22p63s23p63d9,Cu+的电子排布式为1s22s22p63s23p63d10,根据洪特规则,处于半满、
全满、全空,相对稳定,原因是Cu+外围电子3d10轨道全充满稳定,Cu2+外围电子3d9轨道
电子非全充满状态不稳定。