文档内容
素养说明:固体溶解度的概念属于初中知识体系,气体的溶解度属于知识拓展内
容,与之有关的溶度积属于高中知识,本素养属于知识衔接部分。设计本素养,可
以进一步强化学生学习化学的科学方法,真正做到“从生活到化学,从化学到社
会”,所以通过图表,让学生进一步得到物质溶解度的变化规律,从而培养学生识
图能力,阅读查找数据能力和比较分析能力。
1.溶解度
在一定温度下,某固体物质在100 g溶剂(通常是水)里达到饱和状态时所溶解的
质量,叫做这种物质在该溶剂里的溶解度,其单位为“g”。
固体物质溶解度(饱和溶液)S=×100 g。
影响溶解度大小的因素
(1)内因:物质本身的性质(由结构决定)。
(2)外因:
①溶剂的影响(如NaCl易溶于水不易溶于汽油)。
②温度的影响:升温,大多数固体物质的溶解度增大,少数物质却相反,如
Ca(OH) ;温度对NaCl的溶解度影响不大。
2
2.溶解度曲线
(1)定义:溶解度曲线是同种物质在不同温度下的溶解度绘制出来的曲线,一般随
着温度的升高而升高,但是少部分物质会随着温度的升高而降低。由于固体物质
的溶解度随温度变化而变化,该变化可以用溶解度曲线来表示;用纵坐标表示溶
解度,横坐标表示温度,绘出固体物质的溶解度随温度变化的曲线就叫做溶解度
曲线。
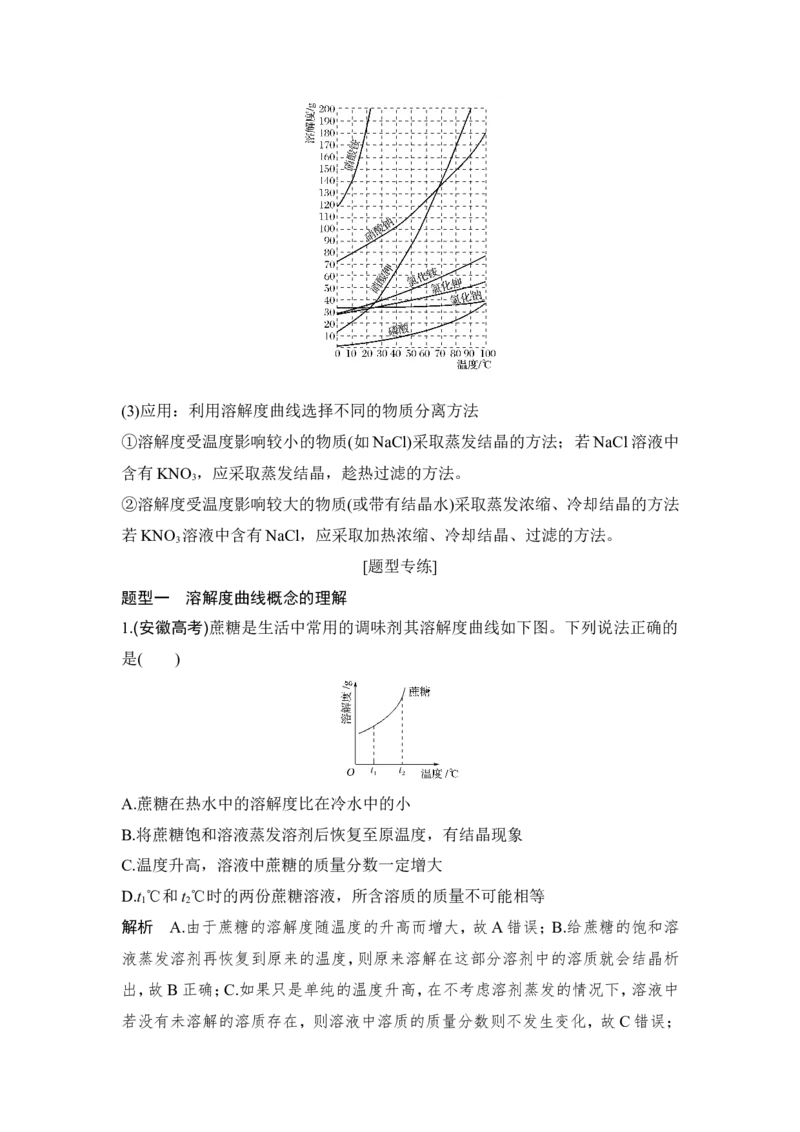
(2)曲线举例(3)应用:利用溶解度曲线选择不同的物质分离方法
①溶解度受温度影响较小的物质(如NaCl)采取蒸发结晶的方法;若NaCl溶液中
含有KNO ,应采取蒸发结晶,趁热过滤的方法。
3
②溶解度受温度影响较大的物质(或带有结晶水)采取蒸发浓缩、冷却结晶的方法
若KNO 溶液中含有NaCl,应采取加热浓缩、冷却结晶、过滤的方法。
3
[题型专练]
题型一 溶解度曲线概念的理解
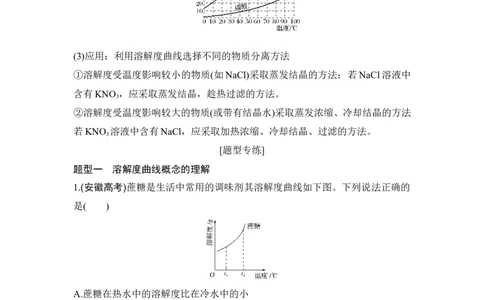
1.(安徽高考)蔗糖是生活中常用的调味剂其溶解度曲线如下图。下列说法正确的
是( )
A.蔗糖在热水中的溶解度比在冷水中的小
B.将蔗糖饱和溶液蒸发溶剂后恢复至原温度,有结晶现象
C.温度升高,溶液中蔗糖的质量分数一定增大
D.t ℃和t ℃时的两份蔗糖溶液,所含溶质的质量不可能相等
1 2
解析 A.由于蔗糖的溶解度随温度的升高而增大,故A错误;B.给蔗糖的饱和溶
液蒸发溶剂再恢复到原来的温度,则原来溶解在这部分溶剂中的溶质就会结晶析
出,故B正确;C.如果只是单纯的温度升高,在不考虑溶剂蒸发的情况下,溶液中
若没有未溶解的溶质存在,则溶液中溶质的质量分数则不发生变化,故C错误;D.由于温度越高溶解度越大,只能说这两个温度下的饱和溶液中溶质的质量分数
不可能相等,但溶液所含溶质的质量可能相等,故D错误。
答案 B
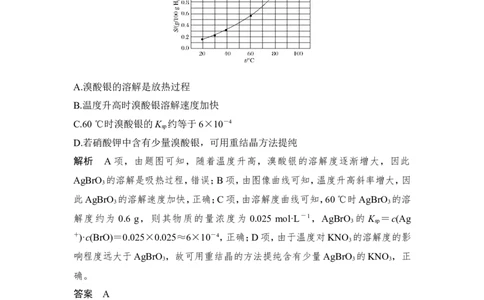
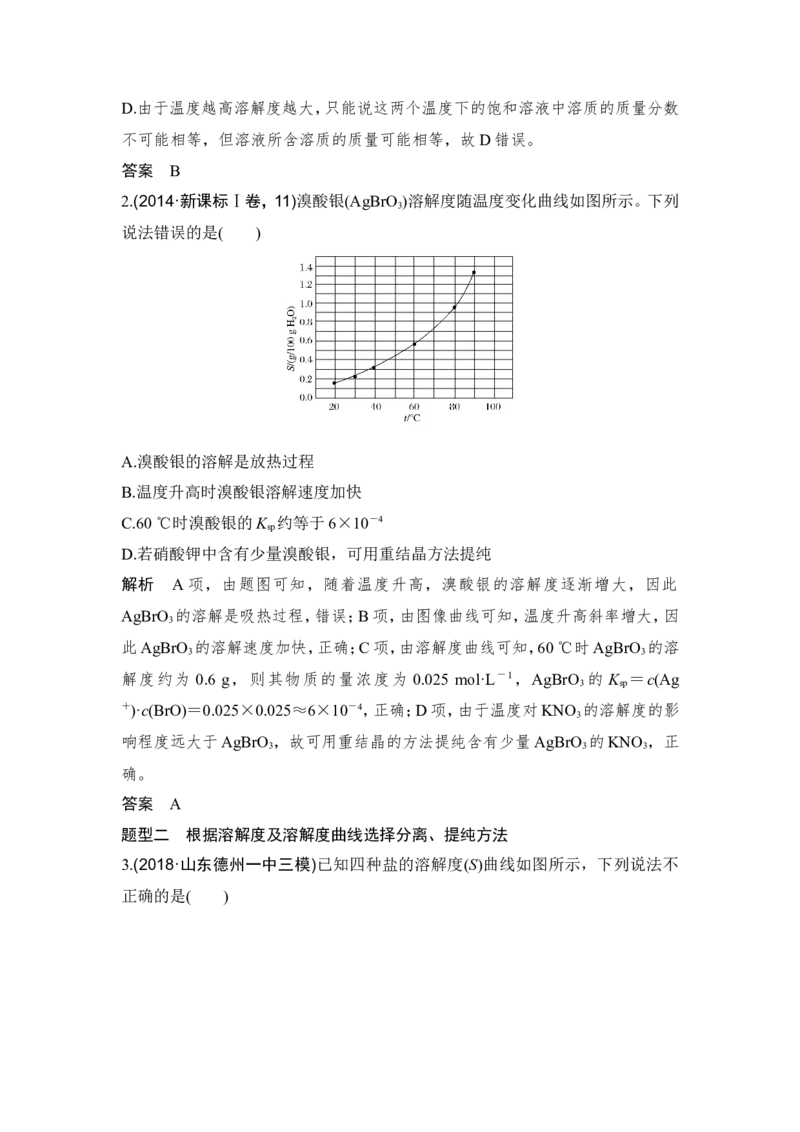
2.(2014·新课标Ⅰ卷,11)溴酸银(AgBrO )溶解度随温度变化曲线如图所示。下列
3
说法错误的是( )
A.溴酸银的溶解是放热过程
B.温度升高时溴酸银溶解速度加快
C.60 ℃时溴酸银的K 约等于6×10-4
sp
D.若硝酸钾中含有少量溴酸银,可用重结晶方法提纯
解析 A项,由题图可知,随着温度升高,溴酸银的溶解度逐渐增大,因此
AgBrO 的溶解是吸热过程,错误;B项,由图像曲线可知,温度升高斜率增大,因
3
此AgBrO 的溶解速度加快,正确;C项,由溶解度曲线可知,60 ℃时AgBrO 的溶
3 3
解度约为 0.6 g,则其物质的量浓度为 0.025 mol·L-1,AgBrO 的 K =c(Ag
3 sp
+)·c(BrO)=0.025×0.025≈6×10-4,正确;D项,由于温度对KNO 的溶解度的影
3
响程度远大于AgBrO ,故可用重结晶的方法提纯含有少量AgBrO 的KNO ,正
3 3 3
确。
答案 A
题型二 根据溶解度及溶解度曲线选择分离、提纯方法
3.(2018·山东德州一中三模)已知四种盐的溶解度(S)曲线如图所示,下列说法不
正确的是( )A.将NaCl溶液蒸干可得NaCl固体
B.将MgCl 溶液蒸干可得MgCl 固体
2 2
C.Mg(ClO ) 中混有少量NaCl杂质,可用重结晶法提纯
3 2
D.可用MgCl 和NaClO 制备Mg(ClO )
2 3 3 2
解析 因NaCl的溶解度受温度的影响不大,所以将NaCl溶液蒸干可得NaCl固
体,故A正确;因MgCl 能够水解,水解产生了氢氧化镁和氯化氢,加热水解平衡
2
正向移动,氯化氢易挥发,所以将MgCl 溶液蒸干得到的固体为氢氧化镁,故B
2
错误;因Mg(ClO ) 的溶解度随温度升高而增大且受温度影响变化较大,NaCl的
3 2
溶解度受温度影响较小,所以Mg(ClO ) 中混有少量NaCl杂质,可用重结晶法提
3 2
纯,故C正确;反应MgCl +2NaClO ===Mg(ClO ) +2NaCl类似于侯德榜制碱法
2 3 3 2
生成 NaHCO 的原理,因为 NaCl 溶解度小而从溶液中析出,使反应向生成
3
Mg(ClO ) 的方向进行,故D正确。
3 2
答案 B
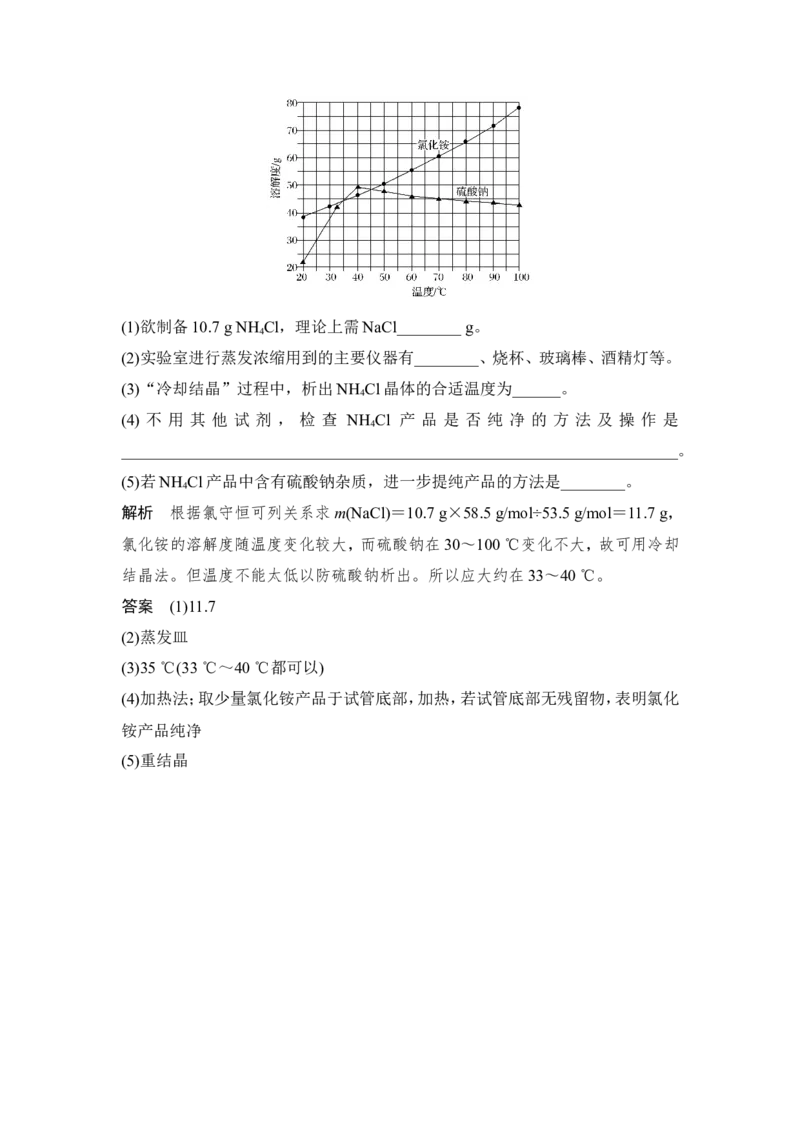
4.(广东化学)以氯化钠和硫酸铵为原料制备氯化铵及副产品硫酸钠,工艺流程如
下:
氯化铵和硫酸钠的溶解度随温度变化如下图所示。回答下列问题:(1)欲制备10.7 g NH Cl,理论上需NaCl________ g。
4
(2)实验室进行蒸发浓缩用到的主要仪器有________、烧杯、玻璃棒、酒精灯等。
(3)“冷却结晶”过程中,析出NH Cl晶体的合适温度为______。
4
(4) 不 用 其 他 试 剂 , 检 查 NH Cl 产 品 是 否 纯 净 的 方 法 及 操 作 是
4
_____________________________________________________________________。
(5)若NH Cl产品中含有硫酸钠杂质,进一步提纯产品的方法是________。
4
解析 根据氯守恒可列关系求m(NaCl)=10.7 g×58.5 g/mol÷53.5 g/mol=11.7 g,
氯化铵的溶解度随温度变化较大,而硫酸钠在30~100 ℃变化不大,故可用冷却
结晶法。但温度不能太低以防硫酸钠析出。所以应大约在33~40 ℃。
答案 (1)11.7
(2)蒸发皿
(3)35 ℃(33 ℃~40 ℃都可以)
(4)加热法;取少量氯化铵产品于试管底部,加热,若试管底部无残留物,表明氯化
铵产品纯净
(5)重结晶