文档内容
模板 02 化学平衡的计算
本节导航
识·题型解读 考情分析+命题预测/技巧解读
明 ·模板构建 答题模板 + 技巧点拨
技法01 速率方程与速率常数 技法02 平衡常数及应用
技法03 常见化学平衡分析模型
通·模板运用 真题示例+模板答题+变式训练
练 ·模板演练 最新模拟、预测考向
化学平衡的计算以非选择题考查为主,重点结合图像中的曲线变化规律考查温度、压强(物种分压变
化)、投料比、催化剂对化学平衡即转化率(或产率)的影响,结合数据考查平衡常数、转化率的计
算,目的是考查考生提取信息并分析和解决问题的能力。考查计算时,侧重有惰性气体参与或多反应
体系的复杂计算,创新考查压强平衡常数和物质的量分数等,以新信息的形式呈现。
模型1 “三段式”计算模型
第一步 书写方程式
第二步 标价始、转、平
mA(g) + nB(g) pC(g) + qD(g)
起始量/mol a b 0 0
转化量/mol mx nx px qx
平衡量/mol a-mx b-nx px qx
第三步 找关系计算
①n (平)=(a-mx+b-nx+px+qx)mol
总
②平衡浓度c (A) = mol·L-1
平
③平衡分压p (A) = p kPa
平 0
④平衡转化率α (A) = ×100%
平⑤平衡体积分数ψ(A) = ×100%
⑥ = (恒温恒容)
⑦K = 用平衡分压代替平衡浓度可以得到K =
c p
模型2 “差量法”计算模型
第一步 书写方程式及差量
xA(g) + yB(g) pC(g) + qD(g) Δ= p+q-(x+y)≠0
第二步 标记转化量 n n
转 变
第三步 找关系计算 =
模型3 “原子守恒法”计算模型
第一步 析物质
①分析起始体系中投入的物质及其物质的量;
②分析平衡体系中的物质及物质的量(部分物质可能已经给出物质的量)。
第二步 列守恒、巧计算
列出不同种类原子的原子守恒关系式,解方程组,计算平衡时未知物质的物质的量。
第三步 找关系计算
代入公式求转化率、平衡常数等。
三种模型中,“三段式法”适用于几乎所有的平衡计算问题;对于反应前后分子数发生变化的单平衡
体系,可以使用“差量法”,计算过程比“三段式法”更简便;对于多平衡体系,可使用“原子守恒法”,
只需要考虑起始时和平衡时体系中的物质,忽略中间的转化过程,比“三段式法”更简便。
技法01 速率方程与速率常数
1.速率方程与速率常数
(1)速率方程:对于基元反应:aA(g)+bB(g)gG(g)+hH(g),则v正 =k
正
ca(A)·cb(B)(其中k
正
为正反应
的速率常数),v逆 =k 逆 cg(G)·ch(H)(其中k 逆 为逆反应的速率常数)。如:2NO 2 (g)2NO(g)+O 2 (g) v逆 =k
·c2(NO)·c(O )
逆 2
(2)速率常数(k)影响因素
速率常数k表示单位浓度下的化学反应速率,与浓度无关,但受温度、催化剂、固体表面积等因素的
影响,通常反应速率常数越大,反应进行得越快。不同反应有不同的速率常数。
2.速率常数与平衡常数的关系
对于基元反应aA(g)+bB(g)cC(g)+dD(g),v正 =k
正
·ca(A)·cb(B),v逆 =k
逆
·cc(C)·cd(D),平衡常数K
==,反应达到平衡时,v正 =v逆 ,故K=。
技法02 平衡常数及应用
1.高考常考的4种化学平衡常数
以aA(g)+bB(g)cC(g)+dD(g)为例
(1)浓度平衡常数(K):K=。
c c(2)压强平衡常数(K ):K =。
p p
(3)物质的量分数平衡常数(K):K=。
x x
(4)标准平衡常数(Kθ)
对于反应dD(g)+eE(g)gG(g)+hH(g),Kθ=,其中pθ=100 kPa,p 、p 、p 、p 为各组分的平衡分
G H D E
压。
2.平衡常数的应用
(1)判断、比较可逆反应进行的程度
一般来说,一定温度下的一个具体的可逆反应:
K值 正反应进行的程度 平衡时生成物浓度 平衡时反应物浓度 反应物转化率
越大 越大 越大 越小 越高
越小 越小 越小 越大 越低
(2)判断正在进行的可逆反应的方向以及反应是否达到平衡
Q=K 体系处于平衡状态,v =v
c 正 逆
Qv
c 正 逆
Qc+d时,A与B的转化率均增大,A与B的体积分数均减小,C与D的体积分数均增大。
a+b=c+d时,A与B的转化率均不变,A、B、C、D的体积分数均不变。
a+b”“<”或“=”)
a a a a
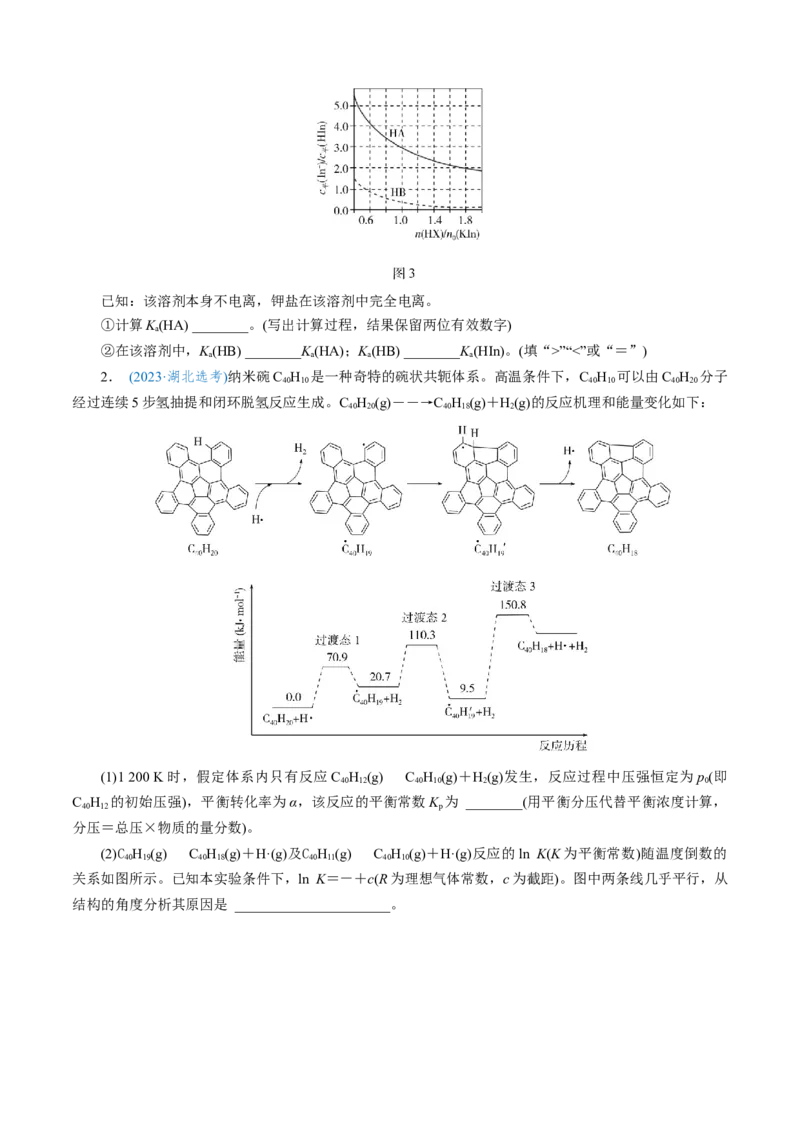
2. (2023·湖北选考)纳米碗C H 是一种奇特的碗状共轭体系。高温条件下,C H 可以由C H 分子
40 10 40 10 40 20
经过连续5步氢抽提和闭环脱氢反应生成。C H (g)――→C H (g)+H(g)的反应机理和能量变化如下:
40 20 40 18 2
(1)1 200 K时,假定体系内只有反应C H (g)C H (g)+H(g)发生,反应过程中压强恒定为p(即
40 12 40 10 2 0
C H 的初始压强),平衡转化率为α,该反应的平衡常数K 为 ________(用平衡分压代替平衡浓度计算,
40 12 p
分压=总压×物质的量分数)。
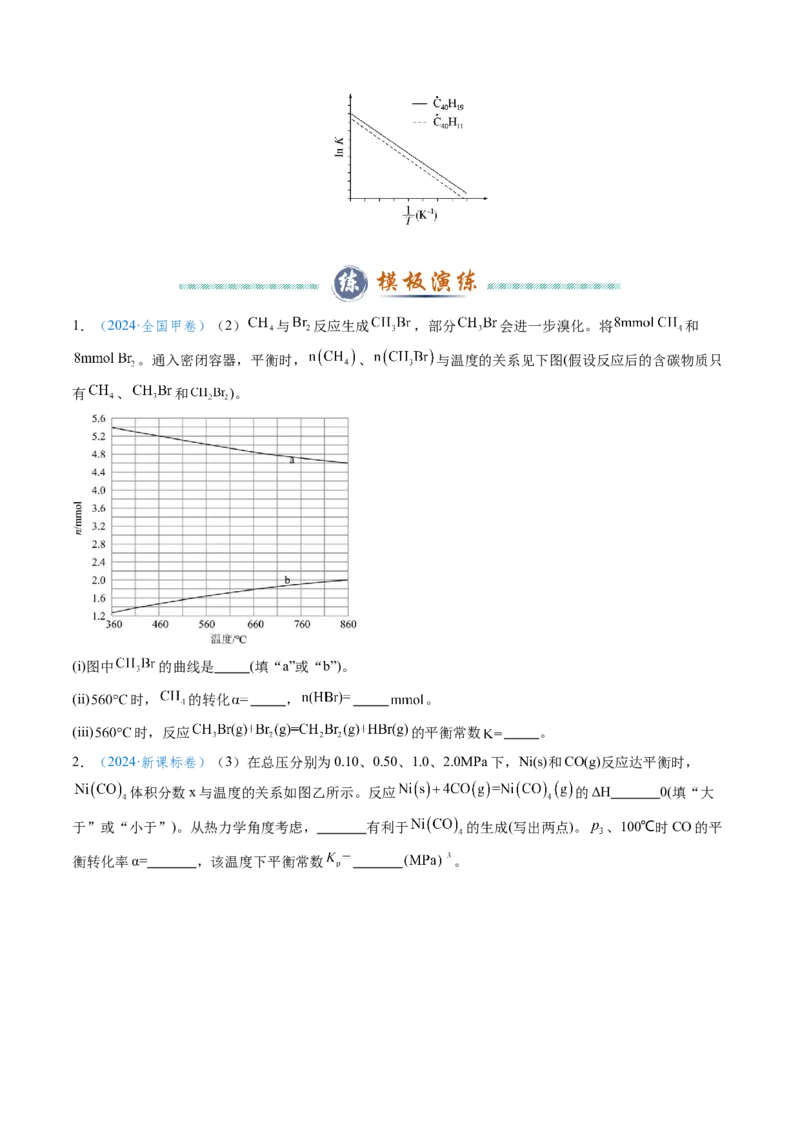
(2)C H (g)C H (g)+H·(g)及C H (g)C H (g)+H·(g)反应的ln K(K为平衡常数)随温度倒数的
40 19 40 18 40 11 40 10
关系如图所示。已知本实验条件下,ln K=-+c(R为理想气体常数,c为截距)。图中两条线几乎平行,从
结构的角度分析其原因是 ______________________。1.(2024·全国甲卷)(2) 与 反应生成 ,部分 会进一步溴化。将 和
。通入密闭容器,平衡时, 、 与温度的关系见下图(假设反应后的含碳物质只
有 、 和 )。
(i)图中 的曲线是 (填“a”或“b”)。
(ii) 时, 的转化 , 。
(iii) 时,反应 的平衡常数 。
2.(2024·新课标卷)(3)在总压分别为0.10、0.50、1.0、2.0MPa下,Ni(s)和CO(g)反应达平衡时,
体积分数x与温度的关系如图乙所示。反应 的ΔH 0(填“大
于”或“小于”)。从热力学角度考虑, 有利于 的生成(写出两点)。 、100℃时CO的平
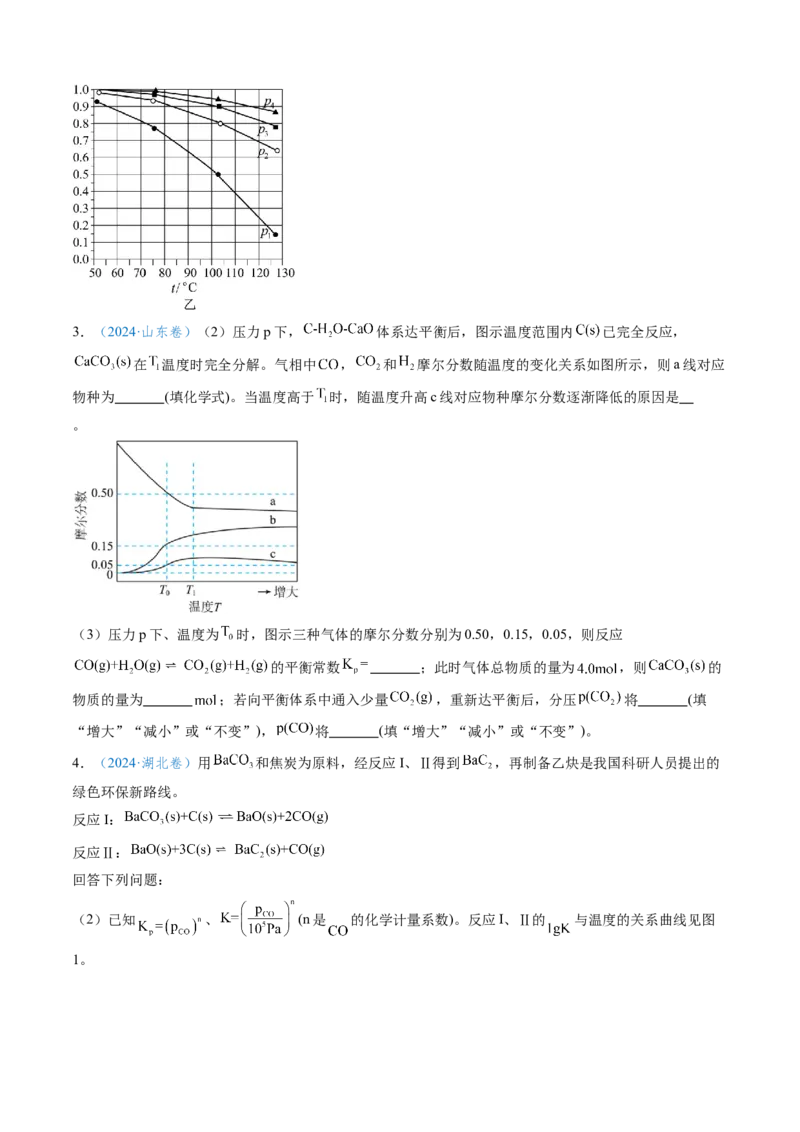
衡转化率α= ,该温度下平衡常数 。3.(2024·山东卷)(2)压力p下, 体系达平衡后,图示温度范围内 已完全反应,
在 温度时完全分解。气相中 , 和 摩尔分数随温度的变化关系如图所示,则a线对应
物种为 (填化学式)。当温度高于 时,随温度升高c线对应物种摩尔分数逐渐降低的原因是
。
(3)压力p下、温度为 时,图示三种气体的摩尔分数分别为0.50,0.15,0.05,则反应
的平衡常数 ;此时气体总物质的量为 ,则 的
物质的量为 ;若向平衡体系中通入少量 ,重新达平衡后,分压 将 (填
“增大”“减小”或“不变”), 将 (填“增大”“减小”或“不变”)。
4.(2024·湖北卷)用 和焦炭为原料,经反应I、Ⅱ得到 ,再制备乙炔是我国科研人员提出的
绿色环保新路线。
反应I:
反应Ⅱ:
回答下列问题:
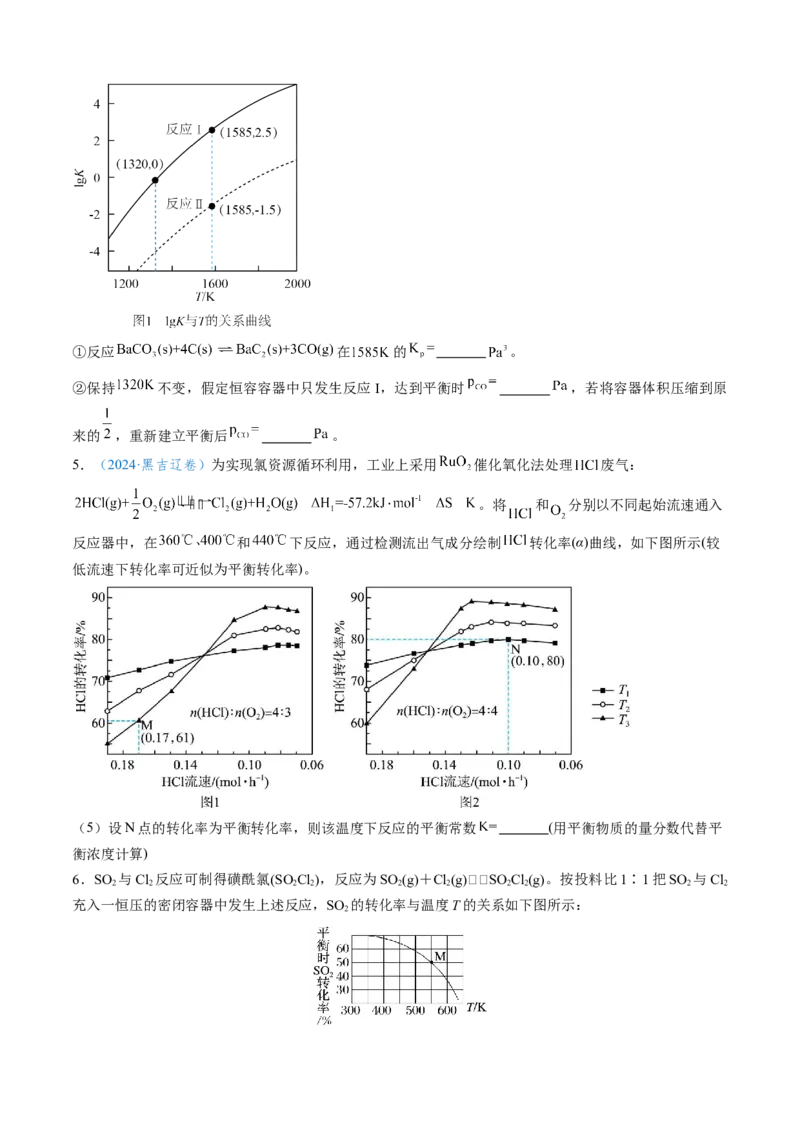
(2)已知 、 (n是 的化学计量系数)。反应I、Ⅱ的 与温度的关系曲线见图
1。①反应 在 的 。
②保持 不变,假定恒容容器中只发生反应I,达到平衡时 ,若将容器体积压缩到原
来的 ,重新建立平衡后 。
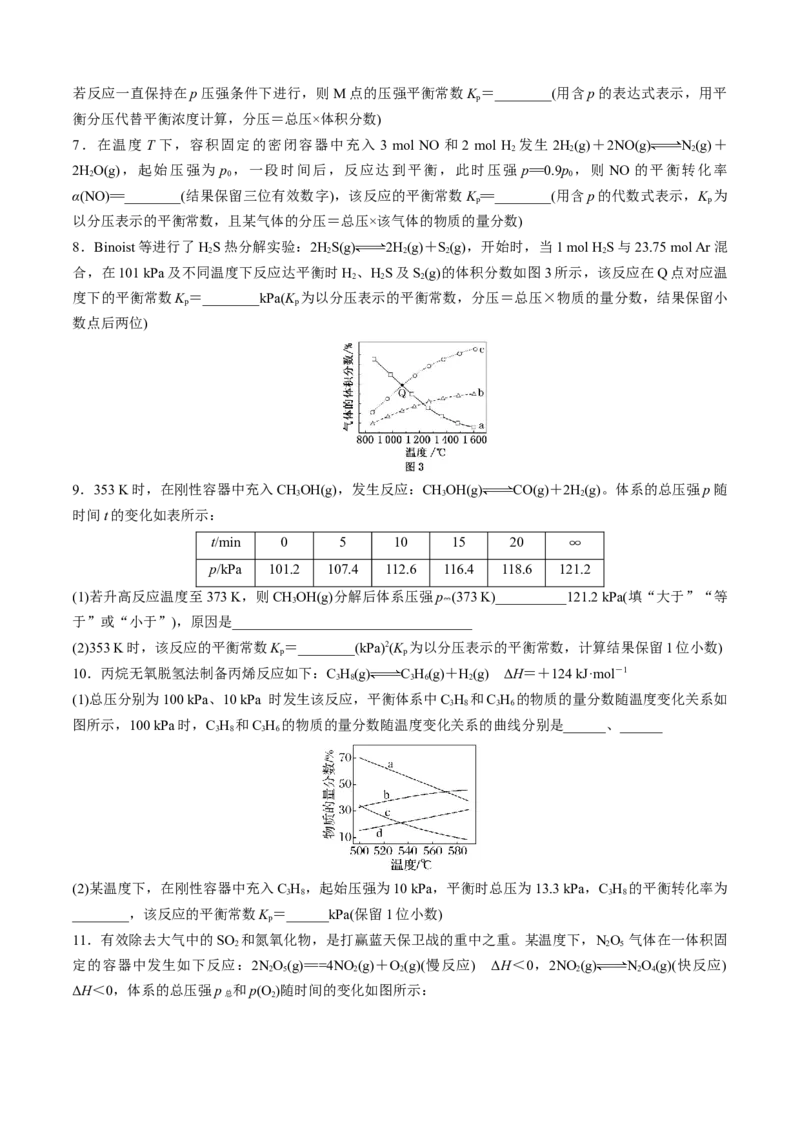
5.(2024·黑吉辽卷)为实现氯资源循环利用,工业上采用 催化氧化法处理 废气:
。将 和 分别以不同起始流速通入
反应器中,在 和 下反应,通过检测流出气成分绘制 转化率(α)曲线,如下图所示(较
低流速下转化率可近似为平衡转化率)。
(5)设N点的转化率为平衡转化率,则该温度下反应的平衡常数 (用平衡物质的量分数代替平
衡浓度计算)
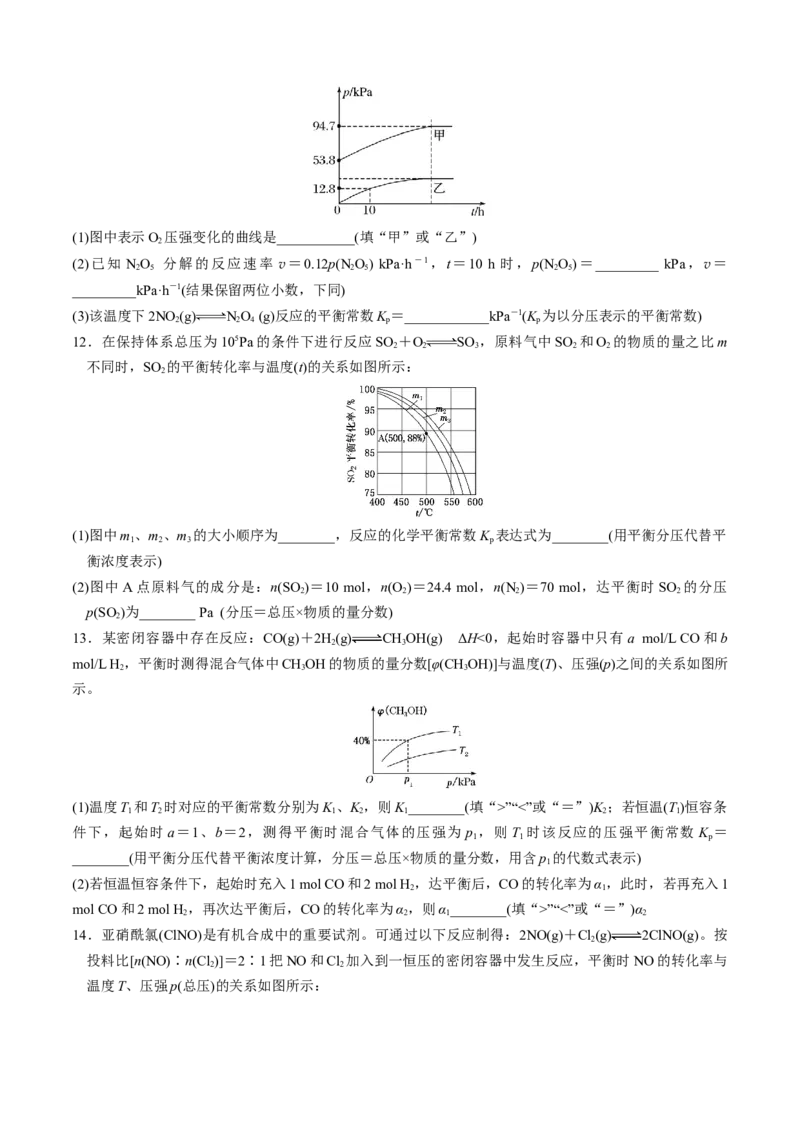
6.SO 与Cl 反应可制得磺酰氯(SO Cl),反应为SO (g)+Cl(g)SO Cl(g)。按投料比1∶1把SO 与Cl
2 2 2 2 2 2 2 2 2 2
充入一恒压的密闭容器中发生上述反应,SO 的转化率与温度T的关系如下图所示:
2若反应一直保持在p压强条件下进行,则M点的压强平衡常数K =________(用含p的表达式表示,用平
p
衡分压代替平衡浓度计算,分压=总压×体积分数)
7.在温度 T 下,容积固定的密闭容器中充入 3 mol NO 和 2 mol H 发生 2H(g)+2NO(g) N(g)+
2 2 2
2HO(g),起始压强为 p ,一段时间后,反应达到平衡,此时压强 p==0.9p ,则 NO 的平衡转化率
2 0 0
α(NO)==________(结果保留三位有效数字),该反应的平衡常数K ==________(用含p的代数式表示,K 为
p p
以分压表示的平衡常数,且某气体的分压=总压×该气体的物质的量分数)
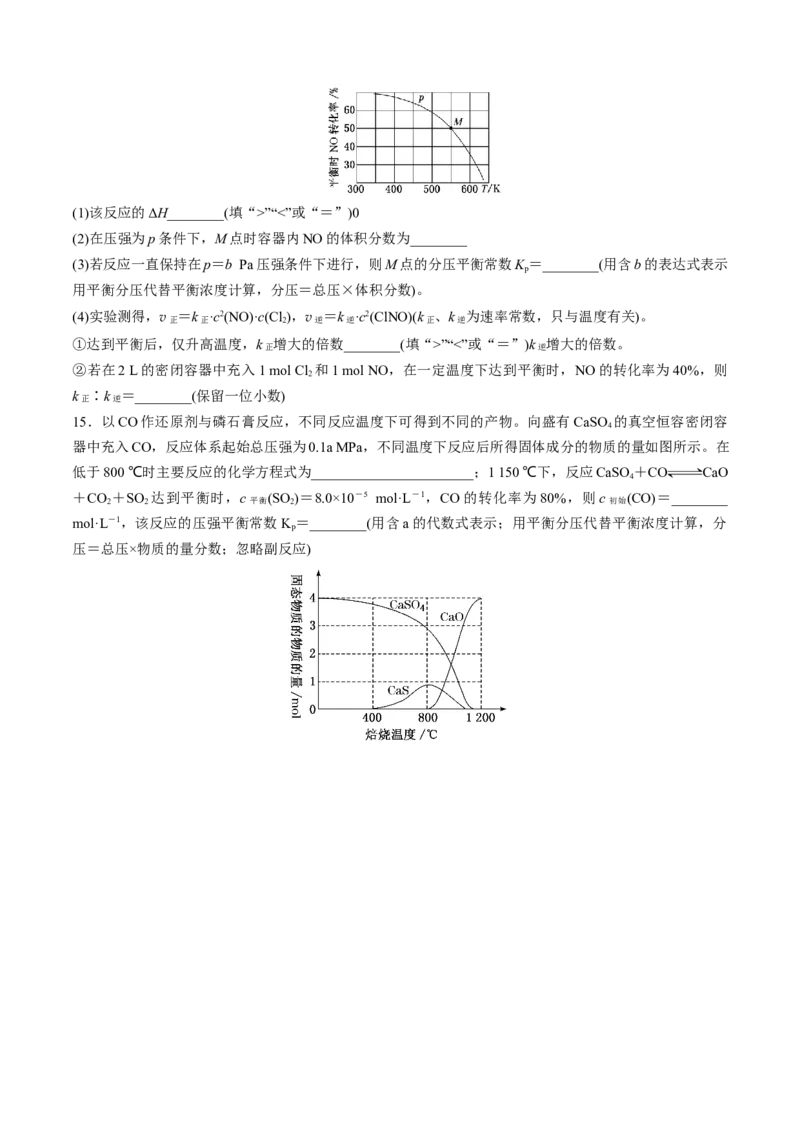
8.Binoist等进行了HS热分解实验:2HS(g) 2H(g)+S(g),开始时,当1 mol H S与23.75 mol Ar混
2 2 2 2 2
合,在101 kPa及不同温度下反应达平衡时H 、HS及S(g)的体积分数如图3所示,该反应在Q点对应温
2 2 2
度下的平衡常数K =________kPa(K 为以分压表示的平衡常数,分压=总压×物质的量分数,结果保留小
p p
数点后两位)
9.353 K时,在刚性容器中充入CHOH(g),发生反应:CHOH(g) CO(g)+2H(g)。体系的总压强p随
3 3 2
时间t的变化如表所示:
t/min 0 5 10 15 20 ∞
p/kPa 101.2 107.4 112.6 116.4 118.6 121.2
(1)若升高反应温度至373 K,则CHOH(g)分解后体系压强p (373 K)__________121.2 kPa(填“大于”“等
3 ∞
于”或“小于”),原因是__________________________________
(2)353 K时,该反应的平衡常数K =________(kPa)2(K 为以分压表示的平衡常数,计算结果保留1位小数)
p p
10.丙烷无氧脱氢法制备丙烯反应如下:C H(g) C H(g)+H(g) ΔH=+124 kJ·mol-1
3 8 3 6 2
(1)总压分别为100 kPa、10 kPa 时发生该反应,平衡体系中C H 和C H 的物质的量分数随温度变化关系如
3 8 3 6
图所示,100 kPa时,C H 和C H 的物质的量分数随温度变化关系的曲线分别是______、______
3 8 3 6
(2)某温度下,在刚性容器中充入C H ,起始压强为10 kPa,平衡时总压为13.3 kPa,C H 的平衡转化率为
3 8 3 8
________,该反应的平衡常数K =______kPa(保留1位小数)
p
11.有效除去大气中的SO 和氮氧化物,是打赢蓝天保卫战的重中之重。某温度下,NO 气体在一体积固
2 2 5
定的容器中发生如下反应:2NO(g)===4NO (g)+O(g)(慢反应) ΔH<0,2NO (g) NO(g)(快反应)
2 5 2 2 2 2 4
ΔH<0,体系的总压强p 和p(O )随时间的变化如图所示:
总 2(1)图中表示O 压强变化的曲线是___________(填“甲”或“乙”)
2
(2)已知 NO 分解的反应速率 v=0.12p(N O) kPa·h-1,t=10 h 时,p(N O)=_________ kPa,v=
2 5 2 5 2 5
_________kPa·h-1(结果保留两位小数,下同)
(3)该温度下2NO (g) NO (g)反应的平衡常数K =____________kPa-1(K 为以分压表示的平衡常数)
2 2 4 p p
12.在保持体系总压为105Pa的条件下进行反应SO +O SO ,原料气中SO 和O 的物质的量之比m
2 2 3 2 2
不同时,SO 的平衡转化率与温度(t)的关系如图所示:
2
(1)图中m 、m 、m 的大小顺序为________,反应的化学平衡常数K 表达式为________(用平衡分压代替平
1 2 3 p
衡浓度表示)
(2)图中A点原料气的成分是:n(SO )=10 mol,n(O )=24.4 mol,n(N )=70 mol,达平衡时SO 的分压
2 2 2 2
p(SO )为________ Pa (分压=总压×物质的量分数)
2
13.某密闭容器中存在反应:CO(g)+2H(g) CHOH(g) ΔH<0,起始时容器中只有a mol/L CO和b
2 3
mol/L H ,平衡时测得混合气体中CHOH的物质的量分数[φ(CHOH)]与温度(T)、压强(p)之间的关系如图所
2 3 3
示。
(1)温度T 和T 时对应的平衡常数分别为K 、K ,则K ________(填“>”“<”或“=”)K ;若恒温(T)恒容条
1 2 1 2 1 2 1
件下,起始时 a=1、b=2,测得平衡时混合气体的压强为 p ,则 T 时该反应的压强平衡常数 K =
1 1 p
________(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数,用含p 的代数式表示)
1
(2)若恒温恒容条件下,起始时充入1 mol CO和2 mol H,达平衡后,CO的转化率为α,此时,若再充入1
2 1
mol CO和2 mol H ,再次达平衡后,CO的转化率为α,则α________(填“>”“<”或“=”)α
2 2 1 2
14.亚硝酰氯(ClNO)是有机合成中的重要试剂。可通过以下反应制得:2NO(g)+Cl(g) 2ClNO(g)。按
2
投料比[n(NO)∶n(Cl )]=2∶1把NO和Cl 加入到一恒压的密闭容器中发生反应,平衡时NO的转化率与
2 2
温度T、压强p(总压)的关系如图所示:(1)该反应的ΔH________(填“>”“<”或“=”)0
(2)在压强为p条件下,M点时容器内NO的体积分数为________
(3)若反应一直保持在p=b Pa压强条件下进行,则M点的分压平衡常数K=________(用含b的表达式表示
p
用平衡分压代替平衡浓度计算,分压=总压×体积分数)。
(4)实验测得,v正 =k
正
·c2(NO)·c(Cl
2
),v逆 =k
逆
·c2(ClNO)(k
正
、k
逆
为速率常数,只与温度有关)。
①达到平衡后,仅升高温度,k 增大的倍数________(填“>”“<”或“=”)k 增大的倍数。
正 逆
②若在2 L的密闭容器中充入1 mol Cl 和1 mol NO,在一定温度下达到平衡时,NO的转化率为40%,则
2
k ∶k =________(保留一位小数)
正 逆
15.以CO作还原剂与磷石膏反应,不同反应温度下可得到不同的产物。向盛有CaSO 的真空恒容密闭容
4
器中充入CO,反应体系起始总压强为0.1a MPa,不同温度下反应后所得固体成分的物质的量如图所示。在
低于800 ℃时主要反应的化学方程式为_______________________;1 150 ℃下,反应CaSO+CO CaO
4
+CO +SO 达到平衡时,c (SO )=8.0×10-5 mol·L-1,CO的转化率为80%,则c (CO)=________
2 2 平衡 2 初始
mol·L-1,该反应的压强平衡常数K =________(用含a的代数式表示;用平衡分压代替平衡浓度计算,分
p
压=总压×物质的量分数;忽略副反应)