文档内容
2023年普通高等学校全国统一模拟招生考试
新未来9月联考化学
可能用到的相对原子质量:H 1 C 12 N 14 O 16 Mg 24 Al 27 P 31 S 32 Fe 56 Zn 65
一、选择题:本题共14小题,每小题3分,共42分.在每小题给出的四个选项中,只有一项符合题目要求.
1.化学与科技、生产、生活密切相关.下列有关说法错误的是( )
A.量子通信材料螺旋碳纳米管与石墨互为同素异形体
B.硅橡胶密封材料既耐低温又耐高温,在中国空间站上得到广泛应用
C.在汽车尾气排放系统中安装催化转化器可有效地减少空气污染
D.为促进社会可持续发展,需加快化石燃料的开采与使用
2.设 为阿伏加德罗常数的值,下列说法正确的是( )
A.2.0 g 和 的混合物中含有的中子数为
B.标准状况下,22.4 L 参加反应,转移的电子数一定为
C.100 g溶质质量分数为46%的 水溶液中含有的氧原子数为
D.足量 与含4 mol HCl的热的浓盐酸充分反应,转移电子数为
3.常温下,下列各组离子在指定溶液中能大量共存的是( )
A.醋酸溶液中: 、 、 、
B.20%的 溶液中: 、 、 、
C.透明酸性溶液中: 、 、 、
D.能使甲基橙变红的溶液中: 、 、 、
4.利用下列装置和试剂进行实验,不能达到实验目的的是( )
B.验证非金属性:
A.制备并收集NO气体 C.除去 中的HCl并 D.量取9.5 mL液体
S>C>Si
干燥
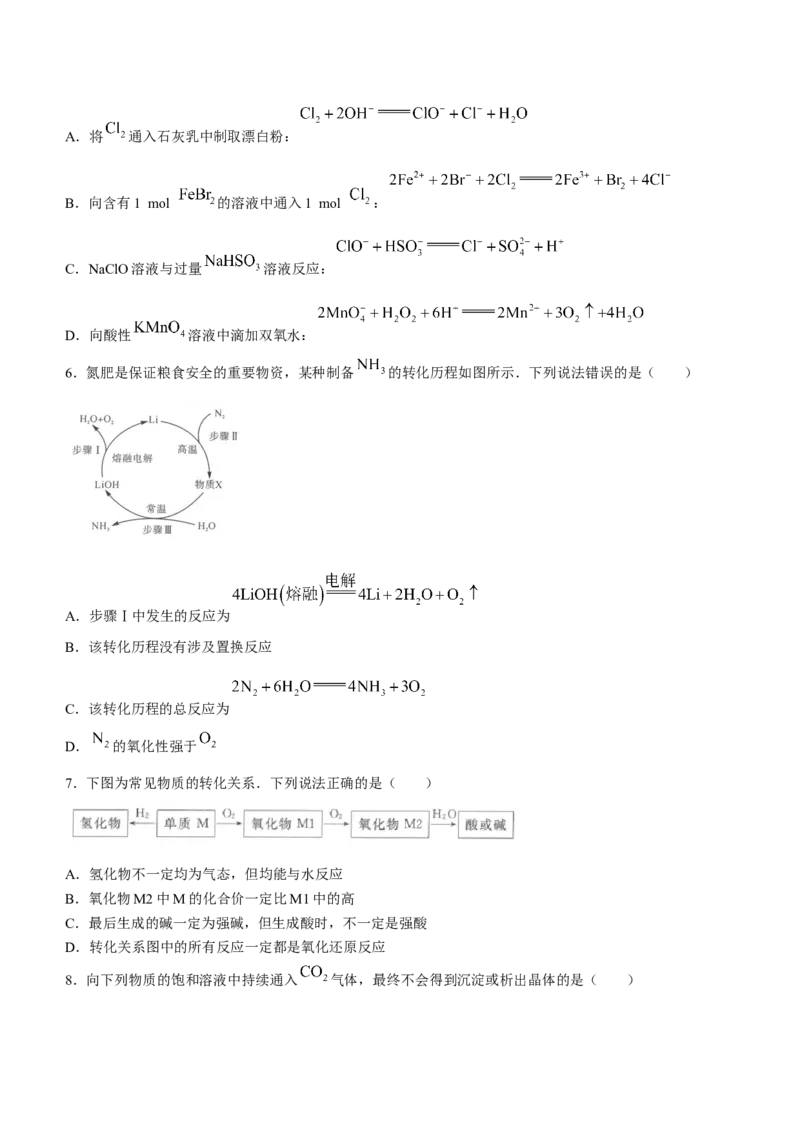
5.下列过程中的化学反应,相应的离子方程式正确的是( )A.将 通入石灰乳中制取漂白粉:
B.向含有1 mol 的溶液中通入1 mol :
C.NaClO溶液与过量 溶液反应:
D.向酸性 溶液中滴加双氧水:
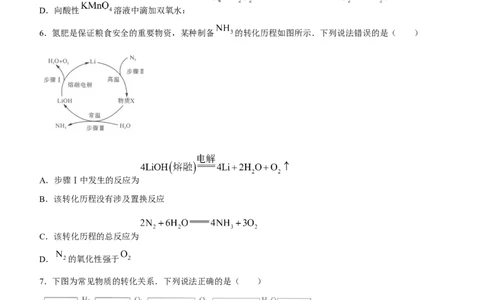
6.氮肥是保证粮食安全的重要物资,某种制备 的转化历程如图所示.下列说法错误的是( )
A.步骤Ⅰ中发生的反应为
B.该转化历程没有涉及置换反应
C.该转化历程的总反应为
D. 的氧化性强于
7.下图为常见物质的转化关系.下列说法正确的是( )
A.氢化物不一定均为气态,但均能与水反应
B.氧化物M2中M的化合价一定比M1中的高
C.最后生成的碱一定为强碱,但生成酸时,不一定是强酸
D.转化关系图中的所有反应一定都是氧化还原反应
8.向下列物质的饱和溶液中持续通入 气体,最终不会得到沉淀或析出晶体的是( )A. B. 和NaCl C. D.
9.25℃、101kPa条件下,相同体积的两个密闭容器甲和乙,甲中充满 ,乙中充满 和 的混合气体.
下列说法错误的是( )
A.两容器中气体的质量不相同 B.两容器中气体的分子数目相同
C.两容器中气体的氧原子数目不相同 D.两容器中气体的密度相同
10.向13.6 g Fe和 的混合物中加入150 mL足量的稀硫酸,搅拌,使其充分反应,收集到1.12 L
(标准状况),向反应后的溶液中滴加KSCN溶液不变红.为中和过量的稀硫酸,并使铁元素全部转化
为 沉淀,恰好消耗了200 mL NaOH溶液.则该稀硫酸的物质的量浓度为( )
A. B. C. D.
11.如图是工业上利用菱镁矿 (含杂质 、 )制取镁的工艺流程.下列说法错误的是(
)
A.为了提高酸浸速率,菱镁矿送入酸浸池前需要粉碎
B.氧化池中通入氯气的目的是将 氧化成
C.“沉淀混合物”为 、
D.工业上常用热还原法制取金属镁
12.部分含铜物质的分类与相应化合价的关系如图所示.下列叙述错误的是( )
A.d的代表物质 具有强氧化性B.将c的溶液与氢氧化钠溶液混合可制得不溶性碱
C.将b投入稀硫酸中,溶液变蓝
D.铜生锈的条件是铜和氧气、水同时发生接触
13.下列根据实验操作和现象所得到的结论错误的是( )
选项 实验操作和现象 结论
A
向 中滴加浓盐酸,出现黄绿色气体 具有氧化性
B
向溶有 的 溶液中通入气体X,出现白色沉淀
气体X一定具有强氧化性
C
向少量 溶液中滴加维生素C溶液,溶液变为浅绿色
维生素C具有还原性
D
向KI溶液中滴加几滴 溶液,再滴加淀粉溶液后变蓝色 的氧化性比 的强
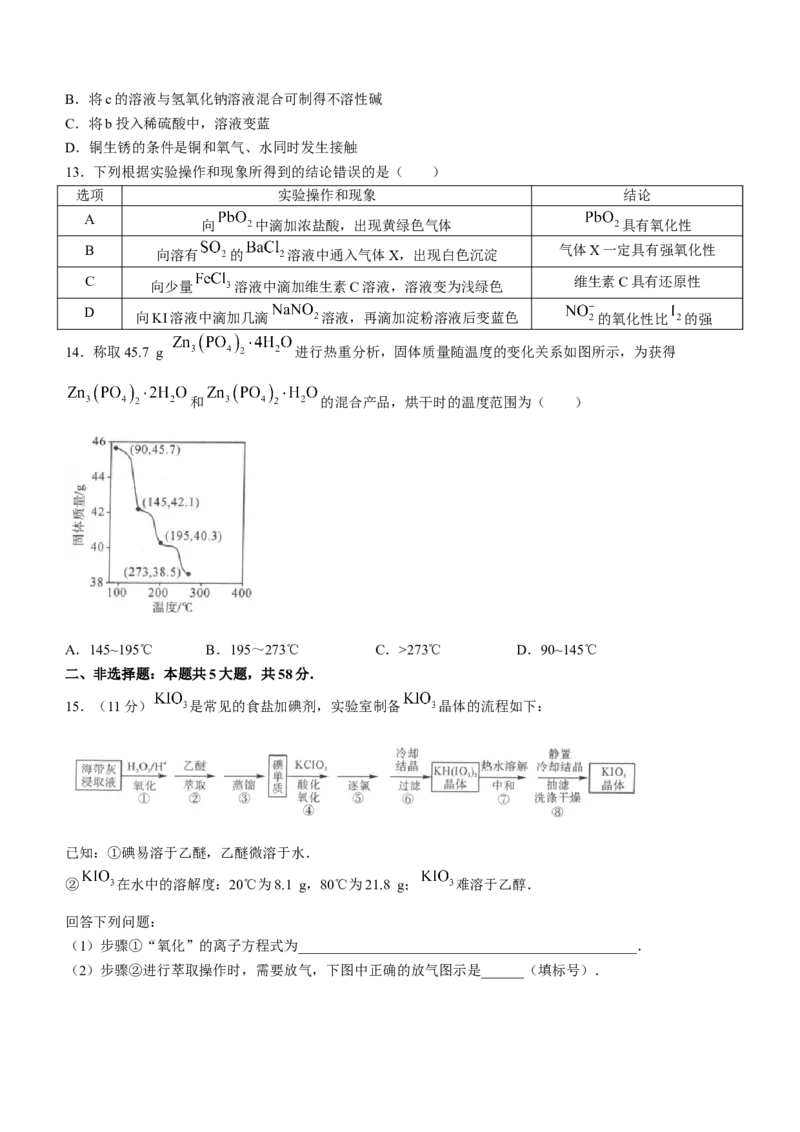
14.称取45.7 g 进行热重分析,固体质量随温度的变化关系如图所示,为获得
和 的混合产品,烘干时的温度范围为( )
A.145~195℃ B.195~273℃ C.>273℃ D.90~145℃
二、非选择题:本题共5大题,共58分.
15.(11分) 是常见的食盐加碘剂,实验室制备 晶体的流程如下:
已知:①碘易溶于乙醚,乙醚微溶于水.
② 在水中的溶解度:20℃为8.1 g,80℃为21.8 g; 难溶于乙醇.
回答下列问题:
(1)步骤①“氧化”的离子方程式为________________________________________________.
(2)步骤②进行萃取操作时,需要放气,下图中正确的放气图示是______(填标号).(3)步骤④中,每1 mol碘单质被氧化,转移______mol电子.
(4)步骤⑦“中和”的化学方程式为__________________________________________.
(5)步骤③中“洗涤”时,最好选用______作为洗涤剂.
(6)我们食用的加碘盐中的碘以 形式存在.已知在溶液中 和 可发生反应:
.根据该反应,可用试纸和一些生活中常见的物质进行实验,证明食盐中
存在 .可供选用的物质有:淀粉、蒸馏水、食糖、食醋、白酒、蓝色石蕊试纸、红色石蕊试纸、碘化钾
淀粉试纸.进行上述实验时必须使用的物质是__________________.
16.(12分)工业上以硫铁矿烧渣(主要成分为 、 ,含少量难溶性杂质)为主要原料制备
的步骤如下.
(1)酸浸:用足量硫酸溶液浸取烧渣中的铁元素.能提高铁元素的浸出率的措施有__________________(写
出两条措施).
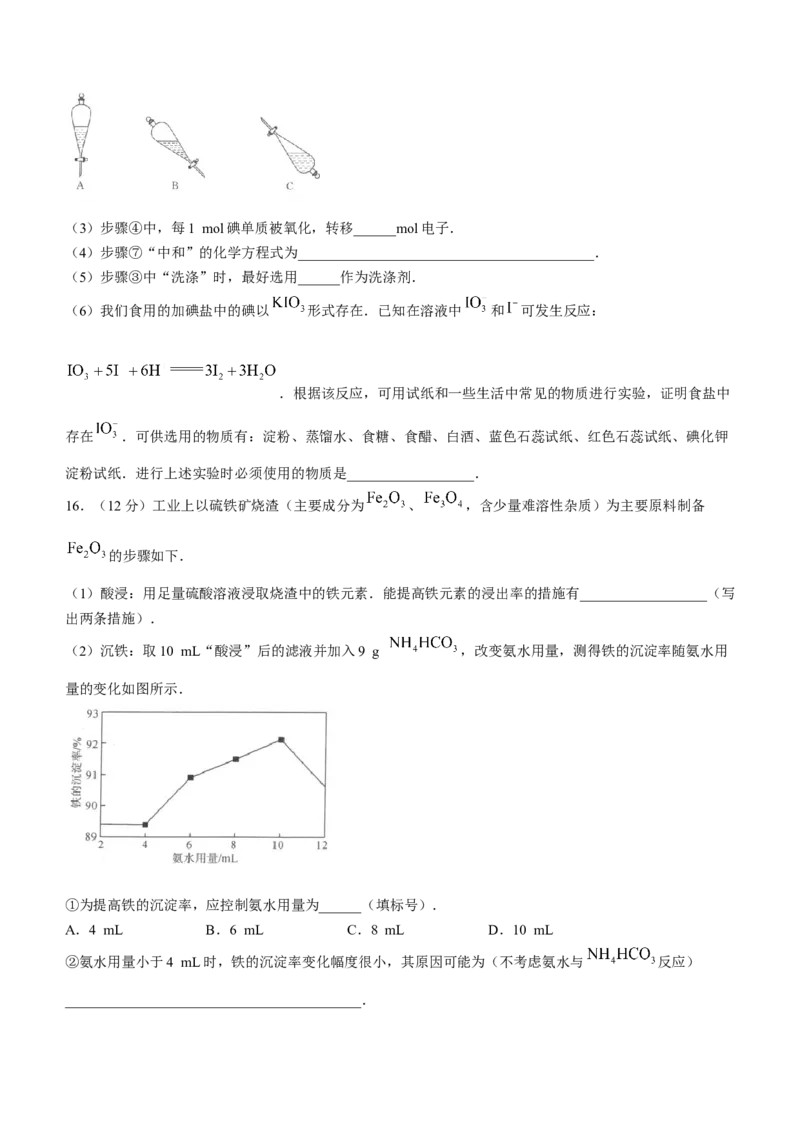
(2)沉铁:取10 mL“酸浸”后的滤液并加入9 g ,改变氨水用量,测得铁的沉淀率随氨水用
量的变化如图所示.
①为提高铁的沉淀率,应控制氨水用量为______(填标号).
A.4 mL B.6 mL C.8 mL D.10 mL
②氨水用量小于4 mL时,铁的沉淀率变化幅度很小,其原因可能为(不考虑氨水与 反应)
__________________________________________.(3)过滤:“沉铁”后过滤,滤渣中含有FeOOH和 ,滤液中浓度最大的阳离子是______(填化学
式).
(4)焙烧:FeOOH和 在空气中高温熔烧后均可得到 ,反应的化学方程式分别为
__________________________________________、__________________________________________.
17.(13分)某化学兴趣小组对仅含下表中某些离子的工业废水进行研究,该废水呈无色,废水中各种离子
的物质的量浓度相等,均为 (忽略水的电离、离子的水解).
阳离子
、 、 、 、 、 、 、
阴离子
、 、 、 、
甲同学欲探究废水的组成,进行了如下实验:
Ⅰ.取废水5 mL,滴加几滴稀氨水有沉淀生成,且溶液中离子种类增加.
Ⅱ.用铂丝蘸取废水,在火焰上灼烧,透过蓝色钴玻璃观察,无紫色火焰.
Ⅲ.另取废水少许,加入过量盐酸,有无色气体生成,该无色气体遇空气变成红棕色.
Ⅳ.将Ⅲ中所得溶液分成两份,一份滴入KSCN溶液,溶液不变红;另一份加入 溶液,有白色沉淀生
成.
回答下列问题:
(1)该废水中一定存在的阳离子是______,一定存在的阴离子是______.
(2)该废水与过量的NaOH溶液反应,产生的沉淀是______(填化学式).
(3)Ⅲ中加入盐酸生成无色气体的离子方程式是____________________________________.
(4)若向Ⅲ中所得的溶液中加入过量 溶液,充分反应后过滤;然后向所得滤液中加入 溶
液,观察到有白色沉淀生成.
①该白色沉淀是______(填化学式).
②仅根据此实验现象,______(填“能”或“不能”)说明该废水中一定存在该白色沉淀中的阴离子,其原
因是__________________________________________.
(5)乙同学取200 mL该工业废水,向其中加入足量的氨水,充分反应后过滤、洗涤、灼烧沉淀至恒重,得
到的固体质量为______g(保留2位小数).
18.(10分)几种中学化学常见的单质及其化合物相互转化的关系图如下:
已知:
①甲、乙、丙、丁为单质,乙中元素在地壳中的含量占第三位,丙为红色固体,其余为化合物.②A由X和Y两种元素组成,其原子个数比为1:2,元素质量之比为7:8.
③B气体是引起酸雨的主要物质,H常温下为无色、无味的液体,E常用作油漆、涂料的红色颜料.
回答下列问题:
(1)高温下,A和甲反应生成B和E的化学方程式为____________________________________,每反应1
mol A,转移______mol电子.
(2)F的水溶液与丁单质反应也可以生成G,反应的离子方程式为______________________________.
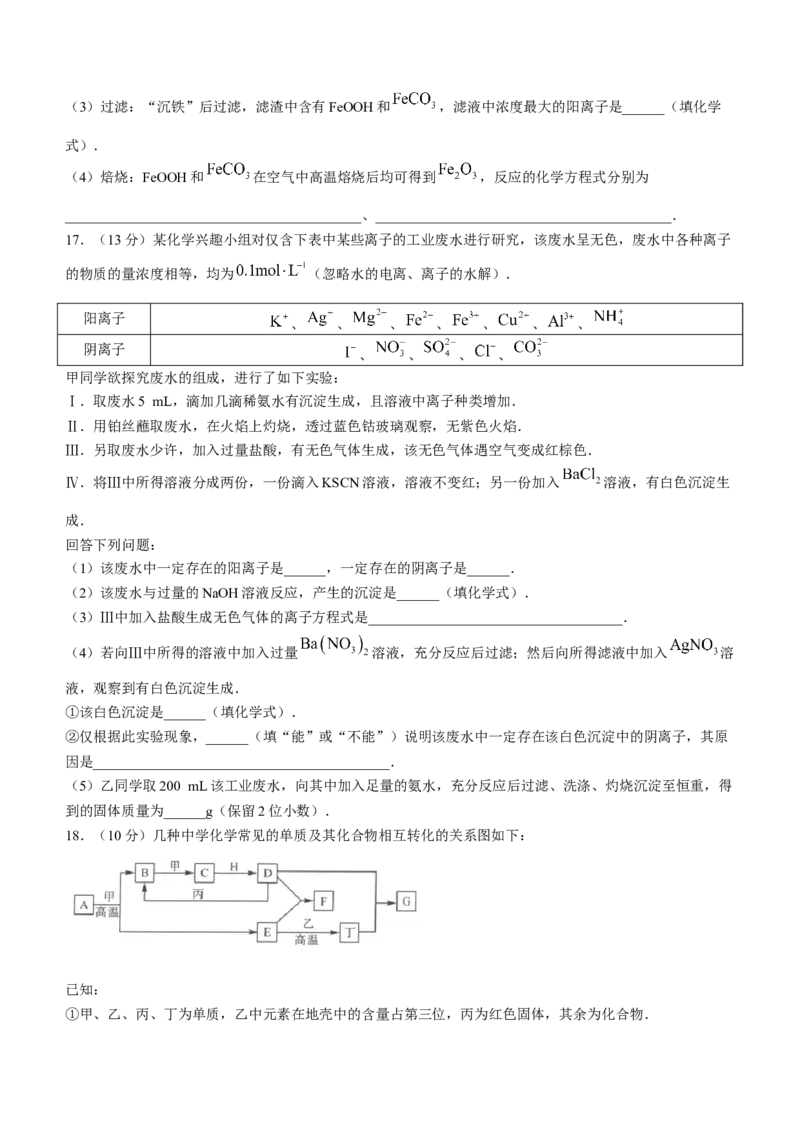
(3)少量F的饱和溶液分别滴加到下列物质中,得到三种分散系①、②、③.
得到的三种分散系①、②、③的名称分别为______、______、______(填“胶体”“悬浊液”“乳浊液”或
“溶液”).
(4)一定条件下,丙和D反应生成B的化学方程式为____________________________________.
19.(12分)亚硝基硫酸( )是染料工艺中重要的原料.回答下列问题:
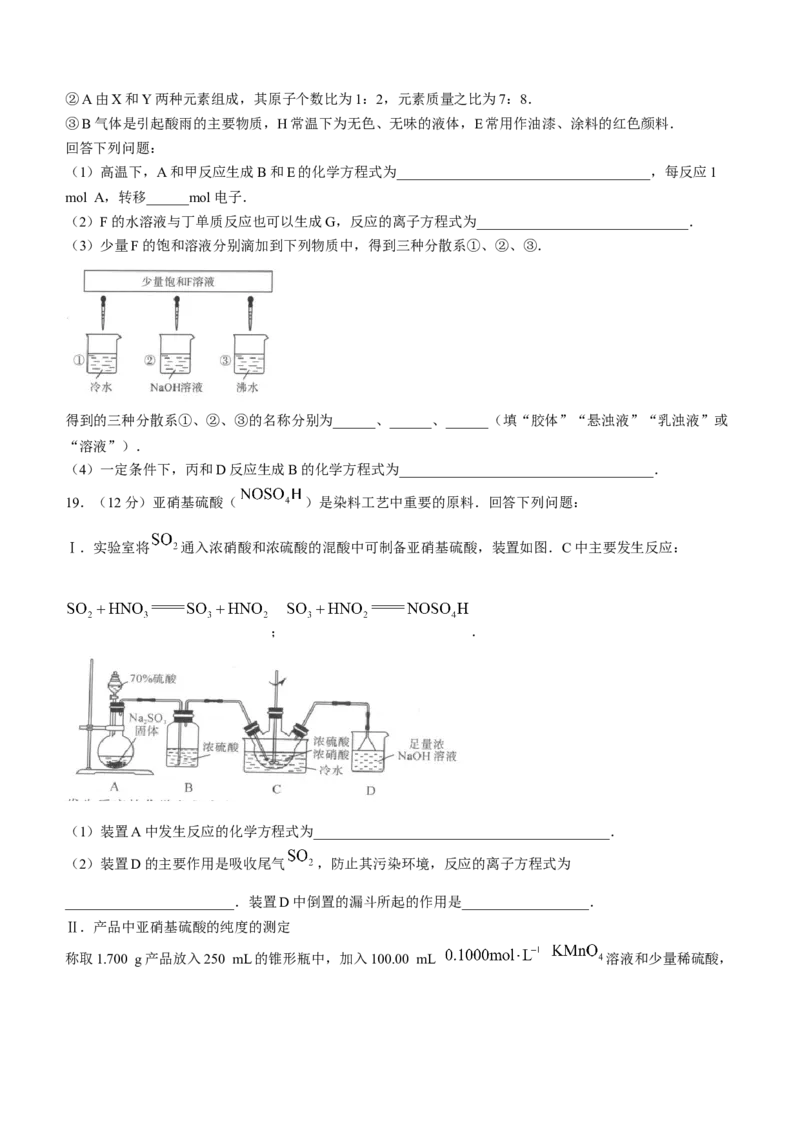
Ⅰ.实验室将 通入浓硝酸和浓硫酸的混酸中可制备亚硝基硫酸,装置如图.C中主要发生反应:
; .
(1)装置A中发生反应的化学方程式为__________________________________________.
(2)装置D的主要作用是吸收尾气 ,防止其污染环境,反应的离子方程式为
________________________.装置D中倒置的漏斗所起的作用是__________________.
Ⅱ.产品中亚硝基硫酸的纯度的测定
称取1.700 g产品放入250 mL的锥形瓶中,加入100.00 mL 溶液和少量稀硫酸,发生反应: ,产品中其他杂
质不与 反应.反应完全后,用 标准溶液滴定过量的 ,发生反应:
,消耗 标准溶液30.00 mL.
(1)配制100 mL 溶液所需要的玻璃仪器有量筒、烧杯、玻璃棒、____________.
(2)滴定到终点时的实验现象是__________________________________________.
(3)产品中亚硝基硫酸的纯度为______%(保留1位小数).
2023年普通高等学校全国统一模拟招生考试
新未来9月联考·化学参考答案、提示及评分细则
1.【答案】D
【解析】量子通信材料螺旋碳纳米管与石墨均为由碳元素组成的单质,两者互为同素异形体,A正确;硅橡
胶具有空间网状结构,具有耐磨、耐高温、耐低温等性能,硅橡胶是目前最好的既耐高温又耐低温的橡胶,
广泛应用于航天航空工业,B正确;在汽车尾气排放系统中安装催化转化器,可以将尾气中的氮氧化物、一
氧化碳等气体转化为氮气、二氧化碳等无毒气体,减少空气污染,C正确;加快化石燃料的开采与使用会增
加污染物的排放,不利于环境保护,D错误.
2.【答案】A
【解析】2.0 g 的物质的量为0.1 mol,含有的中子数为 ,2.0 g 的物质的量为0.1 mol,含
有的中子数也为 ,2.0 g 和 的混合物中含有的中子数为 ,A正确;氯气参加反应,表现
性质不同,转移电子数不同,若 与冷的稀NaOH溶液反应生成NaCl和NaClO,1 mol 参加反应,转
移电子数为 ;若 与热的浓NaOH溶液反应,化学方程式为
,1 mol 参加反应,转移电子数为 ;若 与金属
或氢气反应,则 全部做氧化剂,1 mol 参加反应,转移电子数为 ,B错误;100 g质量分数为
46%的 水溶液中含有46 g(即1 mol)溶质 ,46 g 中含有 个氧原子,还含有54 g(即3 mol)溶剂 ,54 g 中含有 个氧原子,C错误; 与浓盐酸反应的化学方
程式为 ,随着反应的进行,盐酸浓度下降,变成稀盐酸时
反应停止,故足量 与含4 mol HCl的热的浓盐酸充分反应,实际参加反应的HCl小于4 mol,转移电
子数小于 ,D错误.
3.【答案】C
【解析】 在酸性溶液中不能大量共存,A错误; 能氧化 ,B错误;在透明酸性溶液中,
、 、 、 能大量共存,C正确;能使甲基橙变红的溶液显酸性, 可与 反应生成
沉淀和气体,D错误.
4.【答案】D
【解析】用稀硝酸与铜反应制备NO,NO不溶于水,用排水法收集,A能达到实验目的;用稀硫酸制备 ,
与硅酸钠反应生成硅酸沉淀,说明酸性: ,故非金属性:S>C>Si,B能达
到实验目的;饱和食盐水中含有大量的氯离子,可以抑制氯气的溶解,而食盐水中的水可以吸收HCl,洗气
后再用浓硫酸干燥,C能达到实验目的;量取9.5 mL液体,应该用规格为10 mL的量筒,100 mL量筒的精
确度是1 mL,无法量取9.5 mL液体,D不能达到实验目的.
5.【答案】B
【解析】 微溶于水,将 通入石灰乳(属于悬浊液)中制取漂白粉,在离子方程式中,
应写化学式,不能写成离子形式,正确的离子方程式为
,A错误;1 mol 中含有1 mol 和2 mol
,因为还原性: ,故通入1 mol ,转移2 mol电子,有1 mol 和1 mol 被氧化,
反应的离子方程式为 ,B正确;NaClO溶液与 溶液
反应产生的 会继续和剩余的 反应生成 和 ,离子方程式为,C错误;向酸性 溶液中滴加双氧水,双氧水被氧
化成氧气,其反应的离子方程式为 ,D错误.
6.【答案】D
【解析】步骤Ⅰ中发生反应为 ,A正确;步骤Ⅰ中发生的反应属于
分解反应,步骤Ⅱ中发生的反应为 ,属于化合反应,步骤Ⅲ中发生的反应为
,属于复分解反应,该转化历程没有涉及置换反应,B正确;三步反应
加起来可得总反应为 ,C正确;元素的非金属性越强,单质得电子能力越强,
其单质的氧化性就越强,因非金属性:O>N,则 的氧化性强于 ,D错误.
7.【答案】C
【解析】由转换关系图可知,单质M可以是金属Na,也可以是非金属单质C、N、S.氢化物为NaH(s)、
、 、 ,其中 、 与水不反应,A错误;M2为 、 、 、
,M1为 、CO、 、NO, 与 中Na的化合价均为+1价,B错误;最后生成的碱
为NaOH,NaOH为强碱,生成的 是弱酸,生成的 、 均为强酸,C正确; 和
反应、 和 反应均不属于氧化还原反应,D错误.
8.【答案】A
【解析】过量的 与 反应: ,最终不会得到沉淀,A符
合题意;通入 与 和NaCl反应生成氯化铵和碳酸氢钠,碳酸氢钠的溶解度较小,则最终析出碳酸氢
钠晶体,B不符合题意;碳酸的酸性比硅酸的强,过量的 与 溶液反应:,产生硅酸沉淀,C不符合题意;碳酸的酸性比氢氧
化铝的强,过量的 与 溶液反应: ,产生
氢氧化铝沉淀,D不符合题意.
9.【答案】D
【解析】同温、同压、同体积的两个密闭容器中,气体的分子数相同(即气体的物质的量相同).由于两个
容器中气体的摩尔质量不相同,故两容器中气体的质量也不相同,A、B均正确;容器甲中,1 mol气体含有
2 mol氧原子,容器乙中,1 mol气体含有氧原子的物质的量为2~3 mol之间,所以两容器中气体的氧原子数
目不相同,C正确;同温、同压条件下,气体的密度与气体的摩尔质量成正比,由于两个容器中气体的摩尔
质量不相同,所以两容器中气体的密度也不相同,D错误.
10.【答案】A
【解析】根据题干信息可知,涉及的反应有: 、
、 、
、 ,即铁元素完全
沉淀后,溶液中的溶质只有 一种,根据 和 守恒可得: ,即
,则 ,解得 ,A
正确.
11.【答案】D
【解析】固体颗粒越小,总表面积就越大,固体和液体的接触就越多,反应速率就越快,为了提高酸浸速率,
菱镁矿送入酸浸池前需要粉碎,A正确;氧化池中通入氯气的目的是将 氧化成 ,B正确;加入的
MgO与 反应,溶液的pH增大,使 和 转化为氢氧化物沉淀,故“沉淀混合物”为 、
,C正确;工业上常用电解熔融氯化镁的方法制取金属镁,D错误.
12.【答案】D
【解析】由图可知,d的代表物质 中的铜元素具有最高价,化合价容易降低,具有强氧化性,A正确;c为正二价的铜盐,将铜盐溶液与氢氧化钠溶液混合可制得氢氧化铜沉淀,B正确;氧化铜遇到稀硫酸发生反
应: ,溶液变蓝,C正确;铜生锈的条件是铜和氧气、水、二氧化碳同时发生
接触,生成铜绿 ,D错误.
13.【答案】B
【解析】向 中滴加浓盐酸,出现黄绿色气体,该气体是 ,说明 具有氧化性,可以将HCl氧化
为 ,A正确;向溶有 的 溶液中通入气体X,出现白色沉淀,该白色沉淀可能是 ,也可
能是 .若沉淀为 ,说明气体X具有强氧化性,若沉淀为 ,则该气体可能是碱性气体
(例如 ,与 反应使溶液显碱性,反应产生 , 与 反应结合形成 沉淀,由此
说明气体X不一定具有强氧化性,B错误;向少量 溶液中滴加维生素C溶液,溶液变为浅绿色,说明
被还原成 ,维生素C具有还原性,C正确:向KI溶液中滴加几滴 溶液,再滴加淀粉溶液
后变蓝色,说明 被 溶液氧化产生 ,淀粉溶液遇 变为蓝色,故 的氧化性比 的强,D正
确.
14.【答案】A
【解析】由图可知当温度小于90℃时,固体为 ,此时固体的物质的量为
;当温度为145℃时,固体的质量为42.1 g,失去结晶水的物质的量为
,则产品为 ;同理可得,当温度为195℃时产品为
,当温度为273℃时产品为 .为获得 和
的混合产品,应控制温度范围为145~195℃,A正确.
15.【答案】
(1) (2分)
(2)C(2分)(3)10(2分)
(4) (2分)
(5)乙醇(1分)
(6)食醋、碘化钾淀粉试纸(2分)
【解析】(1)步骤①“氧化”的离子方程式为 .
(2)步骤②进行萃取操作时,需要放气,放气时应将分液漏斗的下端倾斜朝上,打开活塞,就可放气.
(3)步骤④中,碘单质( )被氧化为 ,每1 mol碘单质被氧化,转移10 mol电子.
(4)步骤⑦“中和”的化学方程式为 .
(5) 溶于水,难溶于乙醇,为减少产品损失,步骤③中“洗涤”时,最好选用乙醇作为洗涤剂.
(6)证明食盐中存在 ,检验时应在酸性条件下发生反应 ,淀粉遇到
生成的单质碘变蓝色,故可选用食醋、碘化钾淀粉试纸.
16.【答案】
(1)将烧渣粉碎、升高温度、搅拌、增大硫酸浓度等(写出其中的两条即可)(2分)
(2)①D(2分)
②氨水与过量的硫酸发生中和反应(2分)
(3) (2分)
(4) (2分) (2分)
【解析】(1)能提高铁元素的浸出率的措施有升高温度、搅拌、增大硫酸浓度等.
(2)①由图可知,为提高铁的沉淀率,应控制氨水用量为10 mL.
②酸浸步骤中,硫酸过量.氨水用量小于4 mL时,铁的沉淀率变化幅度很小,其原因可能为氨水与过量的
硫酸发生中和反应.
(3)“沉铁”后过滤,滤液中浓度最大的阳离子是 .
(4)FeOOH和 在空气中高温焙烧后均可得到 ,反应的化学方程式分别为
、 .17.【答案】
(1) 、 (2分)、 、 、 、 (2分)
(2) (1分)
(3) (2分)
(4)①AgCl(1分)
②不能(1分) Ⅲ中所得的溶液是加入过量盐酸后的溶液,溶液中一定含有 ,但不能说明该废水中就一
定含有 (2分)
(5)1.82(2分)
【解析】该废水呈无色,无色溶液中一定不存在 、 、 .取5 mL废水,滴加几滴稀氨水,有
沉淀生成,则 、 、 中至少含有一种,则 一定不存在,该反应有 生成,由于离子种
类增加,说明增加的是 ,所以该废水中一定不含有 .用铂丝蘸取废水,在火焰上灼烧,透过蓝色
钴玻璃观察,无紫色火焰,说明该废水中一定不含有 .另取废水少许,加入过量盐酸,有无色气体生成,
该无色气体遇空气变成红棕色,说明发生了反应: 和
,即该废水中一定含有 、 ,则一定不含有 .将Ⅲ中所得溶液分成两份,
一份中滴入KSCN溶液,溶液不变红;另一份中加入 溶液,有白色沉淀生成,说明该废水中一定不含
有 、 ,一定含有 .由此可知,该废水中一定存在的阴离子是 、 、 ,且各为
,该废水中一定存在的阳离子是 、 ,且各为 ,由电荷守恒可知该废水中还
存在 .该废水中一定不存在的阳离子是 、 、 、 、 、 ,该废水一定不存在的
阴离子是 .该废水与过量的NaOH溶液反应, 转变为可溶性的 , 转变为白色沉淀.若向Ⅲ中所得的溶液中加入过量 溶液,充分反应后过滤;然后向所得滤液
中加入 溶液,观察到的实验现象是:有白色沉淀生成,该白色沉淀是AgCl,仅根据此实验现象,不
能说明该废水中一定存在 ,其原因是:Ⅲ中所得的溶液是加入过量盐酸后的溶液,溶液中一定含有 ,
故不能说明该废水中一定含有 .乙同学取200 mL该工业废水,向其中加入足量的氨水,充分反应后生
成0.02 mol 沉淀和0.02 mol 沉淀,过滤、洗涤、灼烧沉淀至恒重,得到的固体是
0.02mol MgO和0.01 mol ,其质量为: .
18.【答案】
(1) (2分) 11(2分)
(2) (1分)
(3)溶液(1分) 悬浊液(1分) 胶体(1分)
(4) (2分)
【解析】根据题意可知,甲、乙、丙、丁分别为 、Al、Cu、Fe,A、B、C、D、E、F、G、H分别为
、 、 、 、 、 、 、 .
(1)高温下, 和 反应生成 和 的化学方程式为 ,每
反应1 mol ,转移11 mol电子.
(2) 的水溶液与Fe反应也可以生成 ,反应的离子方程式为 .
(3)少量 的饱和溶液分别滴加到下列物质中,得到三种分散系①、②、③,其中①为
溶液,②为 悬浊液,③为 胶体.(4)加热条件下,Cu和浓硫酸反应生成 的化学方程式为
.
19.【答案】
Ⅰ.(1) (2分)
(2) (2分) 防止溶液倒吸(1分)
Ⅱ.(1)100 mL容量瓶、胶头滴管(2分)
(2)当滴入最后半滴 标准溶液时,溶液恰好由浅紫色变为无色,且半分钟内不变色(2分)
(3)74.7(3分)
【解析】Ⅰ.(1)装置A中发生反应的化学方程式为 .
(2)装置D中发生反应的离子方程式为 .装置D中倒置的漏斗所起的作用
是防止溶液倒吸.
Ⅱ.(1)配制100 mL 溶液所需要的玻璃仪器有量筒、烧杯、玻璃棒、100 mL
容量瓶、胶头滴管.
(2)滴定到终点时的实验现象是:当滴入最后半滴 标准溶液时,溶液恰好由浅紫色变为无色,且
半分钟内不变色.
(3) 与 反应,过量的 用 标准溶液滴定,根据 的物质的量可
求出过量的 的物质的量,根据 的总量可求出与 反应的 的物质的量,进
而求出 的物质的量.
根据关系式: ,可得出
,与 反应的 的物质的量为.然后根据关系式:
,可得出
,产品中亚硝基硫酸的纯度
.下载最新免费模拟卷,到公众号:一枚试卷君