文档内容
热点 02 电离能、电负性与元素周期律
元素周期律是江苏高考的必考内容,属于热点问题,本题考查元素周期律的应用,进
行元素推断,判断元素及其化合物的性质,如第一电离能、电负性、微粒半径、化学键、
酸碱性等。高考对本讲内容的考查空间很大,知识面很广,主要考查原子结构中各种微粒
关系,结合原子结构图式进行分析判断和简单计算,对 1~20号元素原子结构的考查是重
点,注意规律和结论的应用。其次以元素化合物为载体,综合应用元素周期表和元素周期
律。另外高考对化学键的考查主要是围绕电子式正误判断、化学键与物质类别和性质的关
系两方面进行、题目基础性强,一般不独立命题。通常为选择题的一个选项和基础填空。
2023年高考仍然以短周期元素原子或离子结构特征及核外电子排布规律为背景,考查原子
结构、元素周期律和常见物质的相关性质;或者以“残缺的”元素周期表或元素性质的递
变规律为切入点,考查元素的“位-构-性”关系;结合元素化合物和化学反应原理等基础
知识,采用框图或文字叙述形式,考查元素推断、元素周期律的综合运用。
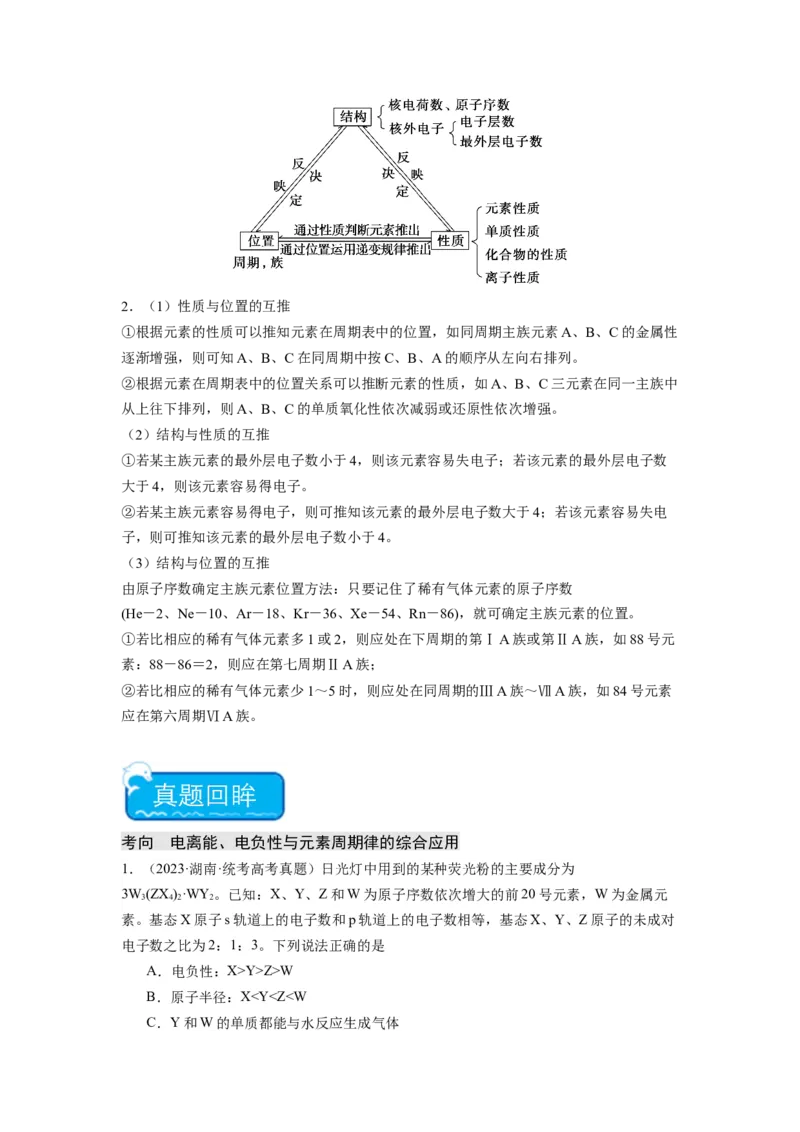
一、元素第一电离能变化规律及考点突破
1.每个周期的第一种元素的第一电离能最小,最后一种元素的第一电离能最大,即一般来
说,随着核电荷数的递增,元素的第一电离能呈增大趋势。
2.同一族,从上到下第一电离能逐渐减小。
3.电离能的应用
(1)根据电离能数据,确定元素原子核外电子的排布及元素的化合价。如 Li:I≪IⅢA,ⅤA>ⅥA。
二、电负性的考点突破
1.电负性的概念
(1)电负性:用来描述不同元素的原子对键合电子吸引力的大小。电负性越大的原子,对键
合电子的吸引力越大。
(2)键合电子:元素相互化合时,原子中用于形成化学键的电子称为键合电子。
(3)电负性大小的标准:以氟的电负性为4.0和锂的电负性为1.0作为相对标准。
2.电负性的递变规律
(1)同周期,自左到右,元素的电负性逐渐增大,元素的非金属性逐渐增强、金属性逐渐减
弱。
(2)同主族,自上到下,元素的电负性逐渐减小,元素的金属性逐渐增强、非金属性逐渐减
弱。
3.电负性的应用
(1)判断元素的金属性和非金属性强弱
①金属的电负性一般小于1.8,非金属的电负性一般大于1.8,而位于非金属三角区边界的
“类金属”(如锗、锑等)的电负性则在1.8左右,它们既有金属性,又有非金属性。
②金属元素的电负性越小,金属元素越活泼;非金属元素的电负性越大,非金属元素越活
泼。
(2)判断元素的化合价
①电负性数值小的元素在化合物中吸引电子的能力弱,元素的化合价为正值。
②电负性数值大的元素在化合物中吸引电子的能力强,元素的化合价为负值。
(3)判断化合物的类型
如H的电负性为2.1,Cl的电负性为3.0,Cl的电负性与H的电负性之差为3.0-2.1=
0.9<1.7,故HCl为共价化合物;如Al的电负性为1.5,Cl的电负性与Al的电负性之差为
3.0-1.5=1.5<1.7,因此AlCl 为共价化合物;同理,BeCl 也是共价化合物。
3 2
三、关注元素推断的突破口
1.掌握 “位—构—性”的转化应用2.(1)性质与位置的互推
①根据元素的性质可以推知元素在周期表中的位置,如同周期主族元素A、B、C的金属性
逐渐增强,则可知A、B、C在同周期中按C、B、A的顺序从左向右排列。
②根据元素在周期表中的位置关系可以推断元素的性质,如A、B、C三元素在同一主族中
从上往下排列,则A、B、C的单质氧化性依次减弱或还原性依次增强。
(2)结构与性质的互推
①若某主族元素的最外层电子数小于4,则该元素容易失电子;若该元素的最外层电子数
大于4,则该元素容易得电子。
②若某主族元素容易得电子,则可推知该元素的最外层电子数大于4;若该元素容易失电
子,则可推知该元素的最外层电子数小于4。
(3)结构与位置的互推
由原子序数确定主族元素位置方法:只要记住了稀有气体元素的原子序数
(He-2、Ne-10、Ar-18、Kr-36、Xe-54、Rn-86),就可确定主族元素的位置。
①若比相应的稀有气体元素多1或2,则应处在下周期的第ⅠA族或第ⅡA族,如88号元
素:88-86=2,则应在第七周期ⅡA族;
②若比相应的稀有气体元素少1~5时,则应处在同周期的ⅢA族~ⅦA族,如84号元素
应在第六周期ⅥA族。
考向 电离能、电负性与元素周期律的综合应用
1.(2023·湖南·统考高考真题)日光灯中用到的某种荧光粉的主要成分为
3W(ZX)·WY。已知:X、Y、Z和W为原子序数依次增大的前20号元素,W为金属元
3 4 2 2
素。基态X原子s轨道上的电子数和p轨道上的电子数相等,基态X、Y、Z原子的未成对
电子数之比为2:1:3。下列说法正确的是
A.电负性:X>Y>Z>W
B.原子半径:XX>Z>W,A错误;
B.同一周期原子半径从左到右依次减小,同一主族原子半径从上到下依次增大,故四种
原子的原子半径大小为:YX,A正确;
B.N最高正价为+5价,O无最高正价,最高正价N大于O,B错误;
C.Na和O形成的过氧化钠中含有非极性共价键,C正确;
D.非金属性越强,最高价氧化物对应水化物的酸性越强,非金属性N大于C,硝酸酸性
强于碳酸,D正确;
故选B。3.(2023·浙江·统考高考真题)X、Y、Z、W四种短周期主族元素,原子序数依次增大。
X、Y与Z位于同一周期,且只有X、 Y元素相邻。X基态原子核外有2个未成对电子,
W原子在同周期中原子半径最大。下列说法不正确的是
A.第一电离能:
B.电负性:
C.Z、W原子形成稀有气体电子构型的简单离子的半径:
D. 与水反应生成产物之一是非极性分子
【答案】A
【分析】X、Y、Z、W四种短周期主族元素,原子序数依次增大。X、Y与Z位于同一周
期,且只有X、 Y元素相邻。X基态原子核外有2个未成对电子,则X为C,Y为N,Z
为F,W原子在同周期中原子半径最大,则W为Na。
【解析】A.根据同周期从左到右第一电离能呈增大趋势,但第IIA族大于第IIIA族,第
VA族大于第VIA族,则第一电离能: ,故A错误;
B.根据同周期从左到右电负性逐渐增大,同主族从上到下电负性逐渐减小,则电负性:
,故B正确;
C.根据同电子层结构核多径小,则Z、W原子形成稀有气体电子构型的简单离子的半径:
,故C正确;
D. 与水反应生成产物之一为乙炔,乙炔是非极性分子,故D正确。
综上所述,答案为A。
4.(2023·湖北·统考高考真题)W、X、Y、Z为原子序数依次增加的同一短周期元素,其
中X、Y、Z相邻,W的核外电子数与X的价层电子数相等, 是氧化性最强的单质,4
种元素可形成离子化合物 。下列说法正确的是
A.分子的极性: B.第一电离能:XY>W>X
D.非金属性:Y>Z
【答案】B
【分析】由图可知,常温下,W和Z的最高价氧化物对应的水化物溶液(浓度均为
0.01mol·L-1)的pH为2,则W和Z的最高价氧化物对应的水化物为一元强酸,W原子序数
小于Z,则W为N,Z为Cl;常温下,Y的最高价氧化物对应的水化物溶液(浓度均为
0.01mol·L-1)的pH小于2,则Y的最高价氧化物对应的水化物为二元强酸,则Y为S;常温
下,X的最高价氧化物对应的水化物溶液(浓度均为0.01mol·L-1)的pH为12,则X的最高价
氧化物对应的水化物溶液为一元强碱,则X为Na。
【解析】A.X为Na,Y为S,化合物XY 为NaS,NaS 中含有离子键和非极性共价键,
2 2 2 2 2 2
A错误;
B.Y为S,W为N,N非金属性大于S,元素的非金属性越强,简单气态氢化物的稳定性
越强,则简单气态氢化物的热稳定性为YZ>W>X,C错误;
D.Y为S,Z为Cl,同周期元素从左往右,非金属性逐渐增强,则非金属性Y<Z,D错
误;
故选B。
3.(2024·四川成都·统考模拟预测)已知短周期主族元素R、W、X、Y、Z,其中R原子
最外层电子数是其电子层数的2倍,其两种常见简单氧化物均为酸性氧化物,W与Z同主
族,X单质与冷水反应剧烈且反应后溶液呈碱性,Y元素原子最外层电子数为m,次外层
电子数为n,Z元素原子L层电子数为m+n,M层电子数为 。下列叙述中一定正确的
是
A.简单氢化物的沸点:
B.简单离子半径:
C.含X、Y的化合物中无非极性键
D.相同温度下,W、Z的最高价含氧酸的钠盐溶液
【答案】D
【分析】已知短周期主族元素R、W、X、Y、Z,其中R元素所在的周期数是其族序数的
一半,且对应的两种常见氧化物均为酸性氧化物,R位于第三周期ⅣA族,则R为S元素;
X单质与冷水反应剧烈且反应后溶液呈碱性,则X为Na;Y元素原子最外层电子数为m,
次外层电子数为n,Z元素原子L层电子数为m+n,M层电子数为m−n,Z的L层含有电
子数m+n=8,Y的次外层电子数n=2,则m=8−2=6,所以Y为O,Z为Si元素;W元
素与Z元素在同一主族,则W为C元素,以此分析解答。
【解析】A.Y为O,R为S元素,则简单氢化物的沸点: ,A错误;
B.X为Na,Y为O,R为S,则简单离子半径: ,B错误;
C.X为Na,Y为O,NaO 中含有O-O非极性键,C错误;
2 2
D.W为C,Z为Si,最高价含氧酸酸性:W>Z,则最高价含氧酸的钠盐溶液 ,D
正确;
故选D。
4.(2024·四川资阳·统考二模)U、V、W、Z是原子序数依次增大的四种短周期元素。盐
X由U、V、Z三种元素组成,y为元素W的单质,物质a、b、c、d、e、f均为中学常见二
元化合物。各物质间能发生如图所示的转化关系(部分反应的产物及反应条件已略),相对
分子质量:c比b大16,f比e大16。已知:非金属性Z强于V,下列推断错误的是A.原子半径:Z>W>V B.物质沸点:aW;同一周期从左到右原子半径逐渐减小,所以原子半径:N>O即原子半径:V>W,
A错误;
B.a为HS,d为NH ,因为NH 分子间存在氢键,所以沸点:HS , D正确;
故答案为:A。
5.(2023上·湖南·高三湖南师大附中校联考阶段练习)X、Y、Z、W、R为原子序数依次
增大的前四周期元素,X元素的某种同位素可用于测定文物年代,Y原子中有7个运动状
态不同的电子,Z原子最外层电子数是内层的3倍,W在Z的下一周期,且其简单阴离子
半径是同周期主族元素中最小的,R的基态原子核外未成对电子数是前四周期中最多的。
下列说法正确的是
A.第一电离能:
B.简单氢化物的沸点:
C.含氧酸的酸性:
D.同周期元素的基态原子中,与R元素原子最外层电子排布式相同的元素有1种
【答案】A
【分析】X元素的某种同位素可用于测定文物年代,X为C;Y原子中有7个运动状态不同
的电子,Y为N;Z原子最外层电子数是内层的3倍,Z为O;W在Z的下一周期,且其简
单阴离子半径是同周期主族元素中最小的,W为Cl;R的基态原子核外未成对电子数是前四周期中最多的,R为Cr。
【解析】A.X为C,Y为N,Z为O,同周期从左往右第一电离能呈增大趋势,但N的2p
轨道半满,第一电离能大于O,故第一电离能:N>O>C,A正确;
B.Z为O,W为Cl,简单氢化物分别为HO和HCl,水分子间存在氢键,沸点
2
HO>HCl,B错误;
2
C.X为C,W为Cl,最高价含氧酸的酸性:HClO>H CO,C错误;
4 2 3
D.同周期元素的基态原子中,与Cr元素原子最外层电子排布式相同的元素有2种:K,
Cu,D错误;
故选A。
6.(2023上·湖南长沙·高三长郡中学校考阶段练习)原子序数依次增大的四种短周期主族
元素Q、X、Y、Z形成的一种化合物结构如图所示,其中只有X、Y同周期,X、Y基态
原子核外电子中均有2个未成对电子。下列说法正确的是
A.Q、X、Z分别与Y形成的二元化合物均不止一种
B.同周期主族元素中第一电离能比Y大的只有一种
C.Z的氧化物对应的水化物为二元强酸
D.X、Y、Z形成的简单氢化物稳定性:
【答案】A
【分析】Q、X、Y、Z是原子序数依次增大的短周期主族元素,Q只连接1个共价键,则
Q为H;X、Y基态原子核外电子中均有2个未成对电子,结合只有X、Y同周期说明价电
子排布分别为 或 ,可知X为C、Y为O,Z能形成6个共价键,则Z为S。
【解析】A.H、C、S均能与O形成一种以上的二元化合物,比如HO、HO,CO、
2 2 2
CO,SO 、SO ,A正确;
2 2 3
B.同一周期从左向右,第一电离能呈增大的趋势,但第ⅡA族、第ⅦA族的第一电离能
比相邻元素的大,N、F的第一电离能均比O大,B错误;
C.Z为S元素,未说明是最高价的氧化物对应的水化物,则该酸不一定是硫酸,若是亚硫
酸则为弱酸,C错误;
D.元素的非金属性越强,形成的简单氢化物越稳定,非金属性:O>S>C,则氢化物稳定
性:HO>HS>CO,D错误;
2 2 2
故选A。
7.(2023上·广东·高三广州市第一中学校联考阶段练习)化合物甲 是一
种常见的医药中间体,所含5种元素均为短周期主族元素,Z比W原子序数小且二者在元素周期表中左右相邻,X是宇宙中最丰富的元素,基态Y原子s轨道电子总数是p轨道的2
倍,R的原子半径在短周期元素中最大,基态Z原子价电子排布式为 。下列说法正
确的是
A.Y的多种同素异形体都是共价晶体 B.第一电离能:
C.简单离子半径: D. 和 的空间结构均为直线形
【答案】B
【分析】H是宇宙中最丰富的元素,X为H元素,基态Y原子s轨道电子数是p轨道的2
倍,核外电子排布式为 为C元素;R的原子半径在短周期元素中最大,R为
元素;基态Z原子价电子排布式为 ,即 为N元素;Z比W原子序数
小且在元素周期表中左右相邻,W为O元素。
【解析】A.C的同素异形体有金刚石、石墨、 等,金刚石是共价晶体,石墨是混合晶
体、 是分子晶体,A项错误;
B.基态N原子的 轨道为半充满状态,比较稳定,第一电离能较高,即第一电离能:
,B项正确;
C. 和 核外电子排布均相同,核电荷数越大,半径越小,离子半径:
,C项错误;
D. 的中心原子N是 即杂化,有一个孤电子对,空间结构为V形,D项错误。
故选B。
8.(2023上·河南洛阳·高三孟津县第一高级中学校考阶段练习)短周期主族元素X、Y、
Z、W的原子序数依次增大,其中X元素在地壳中含量最多,在短周期主族元素中Y原子
的半径最大,在上述四种元素中基态Z原子的核外电子排布中未成对电子数最多。下列说
法不正确的是
A.X与Y形成的化合物中可能存在非极性共价键
B.最简单氢化物的沸点:X>W
C.最高价氧化物对应水化物的酸性:Z S或Cl,B正确;
C.元素非金属性越强,其最高价氧化物对应水化物的酸性越强,非金属性PY>X
D.W、Z形成的化合物中一定不含非极性σ键
【答案】C
【分析】W元素原子的M层没有成对电子,则W为Na元素;X原子序数小于W,采取
即杂化时,杂化轨道上有4个未成对电子,则X为C元素;Y元素的第一电离能大于同
周期相邻元素的,结合原子序数关系,则Y为N元素;CZ分子与 分子的价电子总数相
同,则Z为O元素;Q元素为金属元素且+1价离子的价层电子处于全充满状态,Q的硫酸
盐可用于配制波尔多液,则Q为Cu元素;
【解析】A.Cu原子序数为29,核外电子排布: ,位于元素周期表ds
区,A错误;
B.氧元素形成的单质有 和 两种, 为极性分子,B错误;
C.同周期元素从左到右非金属性逐渐增强, ,C正确;
D.O、Na能够形成 , 中O—O键是非极性σ键,D错误;
答案选C。
10.(2024上·浙江绍兴·高三阶段练习)X、Y、Z、Q、T、W为前36号元素,原子序数
依次增大。其中仅X、Y、Z为短周期主族元素,且分占三个周期。基态Y元素原子价层p
轨道上的电子数比s轨道多,且第一电离能小于同周期的相邻元素;在同周期元素中,Z
的电负性最大;基态W元素原子的4p轨道半充满;Q和T既处于同一周期又位于同一族,
且原子序数T比Q多2。下列说法正确的是
A.基态Y原子核外电子有8种空间运动状态
B. 为非极性分子
C.与X形成的简单化合物沸点:
D. 有2个未成对电子
【答案】D【分析】X、Y、Z原子序数依次增大,且为短周期主族元素,分占三个周期,则X是H,
Y在第二周期,Z在第三周期。基态Y元素原子价层p轨道上的电子数比s轨道多,且第一
电离能小于同周期的相邻元素,则Y在第ⅥA族,Y是O。Z是第三周期电负性最大的元
素,Z是Cl;基态W元素原子的4p轨道半充满,W是As;Q和T既处于同一周期又位于
同一族,且原子序数T比Q多2,则Q、T在第四周期Ⅷ族,是Fe和Ni。综上,X、Y、
Z、Q、T、W分别为H、O、Cl、Fe、Ni、As。
【解析】A.基态O原子核外电子轨道表示式为 ,则氧原子的空间运
动状态有5种,故A错误;
B.WZ 为AsCl ,中心原子As有一个孤电子对,空间构型为三角锥形,为极性分子,故B
3 3
错误;
C.Y与X形成的简单化合物是HO,W与X形成的简单化合物是AsH ,水分子间有氢键,
2 3
沸点高于AsH ,故C错误;
3
D.Ni2+价层电子轨道表示式为 ,有2个未成对电子,故D正确;
答案选D。
11.(2024·全国·高三专题练习)X、Y、Z、W为原子序数依次增大的短周期主族元素,X
与W同主族,Y、Z同周期。四种元素组成的某化合物M的结构如图所示。下列叙述错误
的是
A.电负性:XX>W
B.M中属于p区的元素有4种
C.L形成的单质在X形成的单质中燃烧主要生成
D.M中L和Z元素最外层均不满足 结构
【答案】B
【分析】由题干信息可知,M的组成元素W、X、Y、Z、L均为短周期主族元素且原子半
径依次增大,基态L原子仅s能级上填充电子结合L为+1价离子,故L为Li,基态Y原子
s能级上的电子数是p能级上的2倍,且Y能形成4个共价键,半径比Li小,故Y为C,
原子半径大小在C和Li之间的元素为Be、B,且Z周围形成4个共价键,则Z为B,W的
简单氢化物的沸点高于同主族相邻元素且W的半径最小,则W为F,X可以形成2个共价
键,且半径在F和C之间,故X为O,综上分析可知,W、X、Y、Z、L分别为F、O、
C、B、Li,据此分析解题。
【解析】A.由分析可知,W为F、X为O、Y为C,根据同一周期元素第一电离能呈增大
趋势,ⅡA与ⅢA、ⅤA与ⅥA反常,故元素的第一电离能为F>O>C即W >X>Y,A错
误;
B.由分析可知,W、X、Y、Z、L分别为F、O、C、B、Li,故M中除Li属于s区,其余
4种元素属于p区,B正确;
C.由分析可知,X为O、L为Li,L形成的单质即Li在X形成的单质O 中燃烧只能生成
2
LiO即LX,得不到LiO 即 ,C错误;
2 2 2 2
D.由分析可知,L为Li,Z为B,由题干图示信息可知,Z周围形成4个共价键,即M中
L元素即Li+最外层不满足 结构,而Z元素即B最外层满足 结构,D错误;
故答案为:B。13.(2023上·山西·高三校联考阶段练习)已知短周期主族元素X、Y、Z、W可组成一种
含磷阻燃添加剂(结构如图所示),且原子序数依次增大,Z与Y位于同一周期。下列说法
正确的是
A.W的含氧酸是强酸
B.基态原子的第一电离能:Y>Z
C.W、Y、Z分别与X形成的化合物中均只含有极性键
D.Y形成的单质可能为共价晶体、分子晶体或混合型晶体
【答案】D
【分析】短周期主族元素X、Y、Z、W可组成一种含磷阻燃添加剂,结合结构可知W为
P,Z能形成两个共价键且Z的原子序数小于P则Z为O;Y、Z同周期,Y能形成四个共
价键Y为C;X能形成一个共价键,且原子序数小于Y为H。
【解析】A.W为P其含氧酸在水溶液中都不能完全电离属于弱酸,故A错误;
B.Z为O、Y为C,同周期元素第一电离能整体呈现增大趋势,第一电离能O>C,故B
错误;
C.Z为O,HO 中存在非极性共价键,故C错误;
2 2
D.Y为C,其单质中金刚石是共价晶体、C 属于分子晶体、石墨是混合晶体,故D正确;
60
故选D。
14.(2023·全国·高三专题练习)化合物[(YX ) W(TZ)·6X Z]是分析化学中重要的基准物
4 2 4 2 2
质,其中X、Y、Z、T分别位于三个短周期,原子序数依次增加,T与Z同主族;常温下
YZ 为气体,其分子的总电子数为奇数;W为常见的金属元素,在该化合物中W离子的价
2
层电子排布式为3d6在惰性气体氛围中该物质的热重曲线如图所示,下列说法错误的是
A.元素的第一电离能:Y>Z>T
B.W元素位于元素周期表的f区
C.580℃热分解后得到的固体化合物是WZ
2 3
D.简单气态氢化物的稳定性:Z>Y
【答案】B【分析】W为常见的金属元素,离子的价层电子排布式为3d6,则W为Fe元素;X、Y、
Z、T分别位于三个短周期,原子序数依次增加,则X为H元素;常温下YZ 为气体,其
2
分子的总电子数为奇数,则YZ 为二氧化氮、Y为N元素、Z为O元素;T与Z同主族,
2
则T为S元素。
【解析】A.同主族元素,从上到下第一电离能依次减小,同周期元素,从左到右第一电
离能呈增大趋势,氮原子的2p轨道为稳定的半充满结构,元素的第一电离能大于相邻元素,
则第一电离能由大到小的顺序为N>O>S,故A正确;
B.铁元素的原子序数为26,基态原子的价电子排布式为3d64s2,则铁元素位于元素周期表
的d区,故B错误;
C.由题意可知,化合物的化学式为(NH )Fe(SO )⋅6HO,相对分子质量为392,取1mol
4 2 4 2 2
该物质进行热重分析,由热重曲线可知,580℃热分解后得到固体的质量为392g×(100%
−9.2%−9.2%−9.2%−52.0%)≈80g,则固体化合物为0.5mol氧化铁,故C正确;
D.同周期元素,从左到右元素的非金属性依次增强,简单氢化物的稳定性依次增强,则
水分子的稳定性强于氨分子,故D正确;
故选B。
15.(2023上·河南洛阳·高三栾川县第一高级中学校考期末)W、X、Y、Z四种短周期元
素,它们在周期表中位置如图所示,下列说法不正确的是
A.Y的气态氢化物比X的稳定
B.Z、Y、W的最高价氧化物对应水化物的酸性依次降低
C.WH 与Z元素的单质在一定条件下可能发生化学反应
4
D.W的位置是第二周期、第ⅣA族
【答案】A
【分析】W、X、Y、Z四种短周期元素,它们在周期表中位置如表所示,Z位于第三周期
ⅦA族,为Cl元素,结合各元素的相对位置可知,Y为S元素,X为O元素,W为C元
素,以此分析解答。
【解析】A.由分析可知,X为O元素,Y为S元素,非金属性越强,气态氢化物越稳定,
非金属性SS>C,所以Z、Y、W的最高价氧化物对应水化物的
酸性依次降低,B项正确;
C.由分析可知, 为 ,Z为Cl元素, 与 在光照条件下可能发生取代反应,
C项正确;D.由分析可知,W为C元素,在周期表中位于第二周期第ⅣA族,D项正确;
故选A。
16.(2023上·福建福州·高三福建省福州第一中学校考阶段练习)某有机化合物由原子序
数依次增大的短周期主族元素W、X、Y、Z组成,Y、Z同主族且Z的原子序数是Y的2
倍,该化合物的质谱图如下,m/z为139时,其碎片离子组成为 。
下列叙述正确的是
A.电负性:
B.氢化物沸点:
C.化合物 、 、 均为直线型分子
D. 溶液与 溶液混合,无明显现象
【答案】A
【分析】某有机化合物由原子序数依次增大的短周期主族元素W、X、Y、Z组成,Y、Z
同主族且Z的原子序数是Y的2倍,Y为O元素、Z为S元素,有机物含C,则X为C,
W为H,碎片离子为C HOS+。
7 7
【解析】A.电负性:O>S>C>H,A正确;
B.C的氢化物有多种,C数越多沸点越高,B错误;
C.二氧化碳分子中碳原子的价层电子对数为2、孤对电子对数为0,则分子的空间结构为
直线形;二氧化硫分子中硫原子的价层电子对数都为2、孤对电子对数都为1,分子的空间
结构为V形;CS 分子中,以C为中心,价层电子对数为2、孤对电子对数为0,则分子的
2
空间结构为直线形,C错误;
D.过氧化氢溶液与氢硫酸溶液反应生成硫沉淀和水,则过氧化氢溶液与氢硫酸溶液混合
有明显实验现象,D错误;
故选A。
17.(2024上·黑龙江哈尔滨·高三哈尔滨三中校考期末)某化合物结构如图所示,其中
X、Y、Z、W为原子序数依次增大的短周期非金属元素,Y是有机分子的骨架元素,M位
于元素周期表ds区,下列说法不正确的是①第一电离能:
②氢化物沸点:YY>Z>R
C.R与Z形成的化合物中只含有离子键
D.Y、M的氧化物对应的水化物均为强酸
【答案】B
【分析】X、Y、Z、R、M为原子序数依次增大的五种短周期主族元素,且Y与Z可形成
一种红棕色有刺激性气味的气体,Y为N元素,Z为O元素;X的原子半径最小,X为H
元素;R与X同主族,R为Na元素;M原子最外层的电子数与Y的电子总数相同,M为Cl
元素,以此分析。【解析】A.X与Y可以形成NH 、NH 等多种二元化合物,A错误;
3 2 4
B.简单离子半径:Cl->N3->O2->Na+,B正确;
C.R与Z形成的化合物可以是NaO,既含有离子键,又含有共价键,C错误;
2 2
D.Y、M的氧化物对应的水化物可以为HNO、HClO,为弱酸,D错误;
2
故选B。
20.(2024上·海南省直辖县级单位·高三校考阶段练习)X、Y、Z、W、Q为原子序数依
次增大的短周期主族元素,X、Q为同主族元素且这两种元素能组成离子化合物M,Y元
素的气态氢化物是碱性气体。下列说法正确的是
A. 分子含有34个电子 B.简单离子半径:
C.元素最高正价: D.M溶于水后形成的溶液呈碱性
【答案】AD
【分析】X、Y、Z、W、Q为原子序数依次增大的短周期主族元素,X、Q为同主族元素且
这两种元素能组成离子化合物M,则X为H元素,Q为Na元素;Y元素的气态氢化物是
碱性气体,Y为N元素;则Z为O元素,W为F元素;以此解答。
【解析】A.NF 分子含有7+3×9=34个电子,故A正确;
3
B.Na+、F-、O2-的电子层结构相同,核电荷数越大,半径越小,则离子半径:
,故B错误;
C.W为F元素,没有正价,故C错误;
D.M为NaH溶于水后生成NaOH,溶液呈碱性,故D正确;
故选AD。