文档内容
热点专项 多平衡体系中最佳反应条件、选择性、转化率、
产率判断
目录
01考情透视·目标导航............................................................................................................................
02知识导图·思维引航............................................................................................................................
03核心精讲·题型突破............................................................................................................................
【真题研析】...........................................................................................................................................................
【核心精讲】...........................................................................................................................................................
1.多重平衡体系分类.............................................................................................................................................
2.有关多重平衡及选择性的问题.........................................................................................................................
3.连续反应的思维模型.........................................................................................................................................
4.竞争反应的思维模型.........................................................................................................................................
5.工业生产图像中转化率、产率变化分析思路.................................................................................................
【命题预测】...........................................................................................................................................................
考向1选择反应最佳条件.......................................................................................................................................
考向2解释曲线发生某种现象的原因...................................................................................................................
考向3多重化学平衡的计算...................................................................................................................................
考点要求 考题统计 考情分析
反应条件
2024·安徽卷,12,3分;2024·辽吉黑卷,10,3
的选择或 近几年高考对化学平衡相关
分;2024·江苏卷,13,3分;2023•江苏卷,
曲线原因 知识的考查中,经常出现同
13,3分;2022•江苏卷,13,3分;
分析 一体系中多平衡共存问题,
这类试题有固定的的设问、
答法或有确定的解题思路。
多重化学
2024·浙江6月卷,11,3分;2024·湖南卷,
预计2025年重点考查多重平
平衡的计 衡下化学平衡体系的分析、
14,3分;2023•湖南卷,16(2);
算 化学平衡常数的计算等。1.(2024·浙江6月卷,11,3分)二氧化碳氧化乙烷制备乙烯,主要发生如下两个反应:
I.C H(g)+CO(g) C H(g)+CO(g)+HO(g) ΔH >0
2 6 2 2 4 2 1
II.C H(g)+2CO(g) 4CO(g)+3H(g) ΔH >0
2 6 2 2 2
向容积为 的密闭容器中投入2 mol C H 和3 mol CO ,不同温度下,测得 时(反应均未平衡)的
2 6 2
相关数据见下表,下列说法不正确的是( )
温度( ) 400 500 600
乙烷转化率( ) 2.2 9.0 17.8
乙烯选择性( ) 92.6 80.0 61.8
注:乙烯选择性
A.反应活化能:I<II
B. 时,0~5 min反应I的平均速率为:v(C H)=2.88×10-3mol·L-1·min-1
2 4
C.其他条件不变,平衡后及时移除HO(g),可提高乙烯的产率
2
D.其他条件不变,增大投料比[n(C H)/ n(CO)]投料,平衡后可提高乙烷转化率
2 6 2
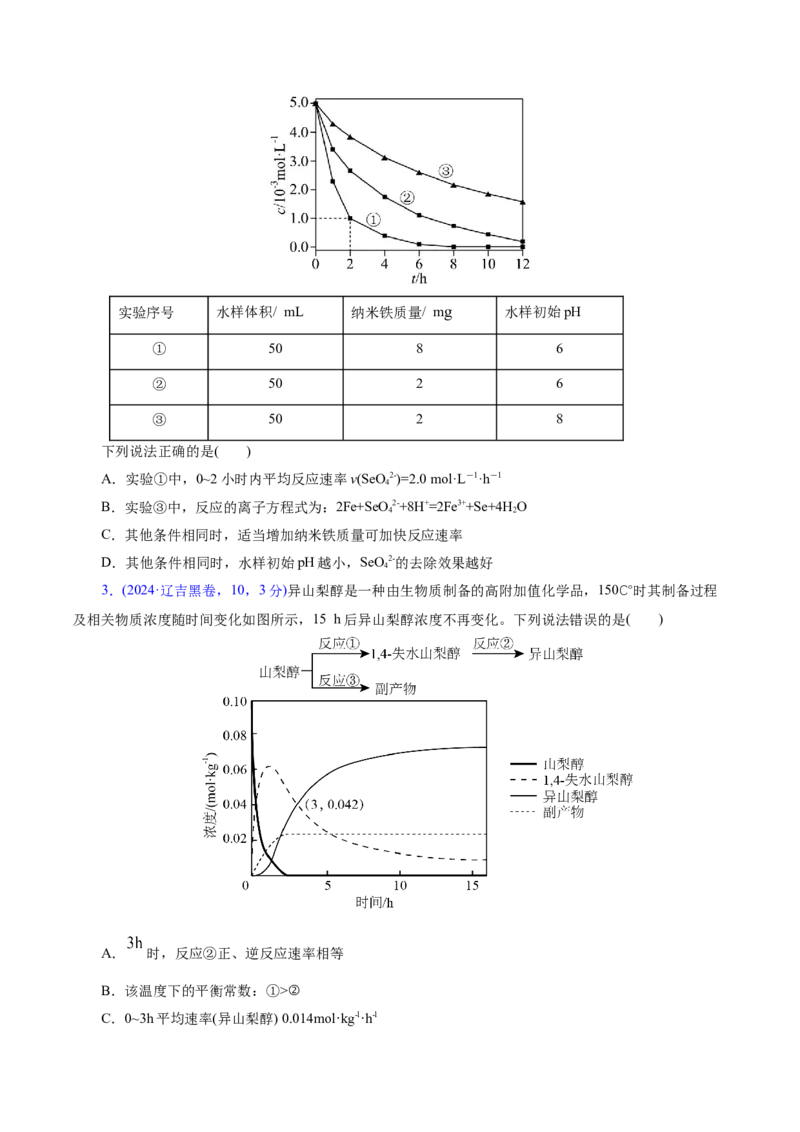
2.(2024·安徽卷,12,3分)室温下,为探究纳米铁去除水样中SeO2-的影响因素,测得不同条件下
4
SeO2-浓度随时间变化关系如下图。
4实验序号 水样体积/ mL 纳米铁质量/ mg 水样初始pH
① 50 8 6
② 50 2 6
③ 50 2 8
下列说法正确的是( )
A.实验①中,0~2小时内平均反应速率v(SeO 2-)=2.0mol·L-1·h-1
4
B.实验③中,反应的离子方程式为:2Fe+SeO2-+8H+=2Fe3++Se+4H O
4 2
C.其他条件相同时,适当增加纳米铁质量可加快反应速率
D.其他条件相同时,水样初始pH越小,SeO2-的去除效果越好
4
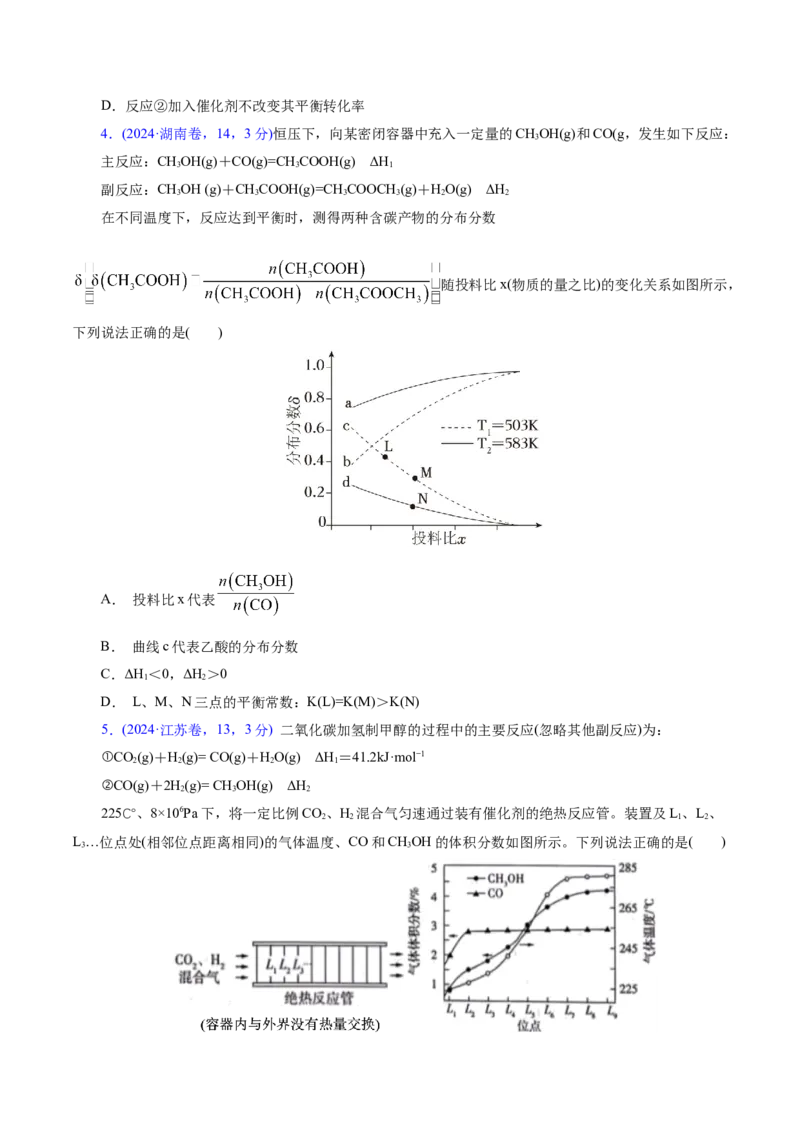
3.(2024·辽吉黑卷,10,3分)异山梨醇是一种由生物质制备的高附加值化学品,150℃时其制备过程
及相关物质浓度随时间变化如图所示,15 h后异山梨醇浓度不再变化。下列说法错误的是( )
A. 时,反应②正、逆反应速率相等
B.该温度下的平衡常数:①>②
C.0~3h平均速率(异山梨醇) 0.014mol·kg-l·h-lD.反应②加入催化剂不改变其平衡转化率
4.(2024·湖南卷,14,3分)恒压下,向某密闭容器中充入一定量的CHOH(g)和CO(g,发生如下反应:
3
主反应:CHOH(g)+CO(g)=CHCOOH(g) ΔH
3 3 1
副反应:CHOH (g)+CHCOOH(g)=CH COOCH (g)+HO(g) ΔH
3 3 3 3 2 2
在不同温度下,反应达到平衡时,测得两种含碳产物的分布分数
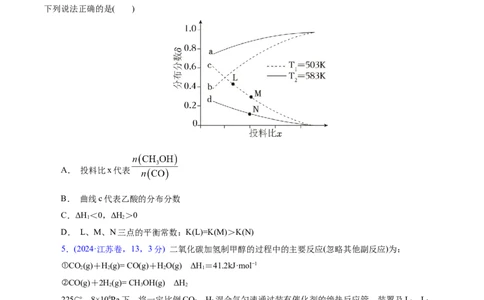
随投料比x(物质的量之比)的变化关系如图所示,
下列说法正确的是( )
A. 投料比x代表
B. 曲线c代表乙酸的分布分数
C.ΔH<0,ΔH>0
1 2
D. L、M、N三点的平衡常数:K(L)=K(M)>K(N)
5.(2024·江苏卷,13,3分) 二氧化碳加氢制甲醇的过程中的主要反应(忽略其他副反应)为:
①CO(g)+H(g)= CO(g)+HO(g) ΔH =41.2kJ·mol−1
2 2 2 1
②CO(g)+2H(g)= CH OH(g) ΔH
2 3 2
225℃、8×106Pa下,将一定比例CO、H 混合气匀速通过装有催化剂的绝热反应管。装置及L、L、
2 2 1 2
L…位点处(相邻位点距离相同)的气体温度、CO和CHOH的体积分数如图所示。下列说法正确的是( )
3 3A.L 处与L 处反应①的平衡常数K相等
4 5
B.反应②的焓变ΔH>0
2
C.L 处的HO的体积分数大于L 处
6 2 5
D.混合气从起始到通过L 处,CO的生成速率小于CHOH的生成速率
1 3
6.(2023•江苏卷,13,3分)二氧化碳加氢制甲烷过程中的主要反应为
CO(g)+4H(g)=CH (g)+2HO(g) ΔH=-164.7kJ·mol−1
2 2 4 2
CO(g)+H(g)=CO(g)+HO(g) ΔH=41.2kJ·mol−1
2 2 2
在密闭容器中, 、 时,CO 平衡转化率、在催化剂作用下
2
反应相同时间所测得的CO 实际转化率随温度的变化如题图所示。CH 的选择性可表示为
2 4
。下列说法正确的是( )
A.反应2CO(g)+2H(g)=CO (g)+CH(g)的焓变ΔH=-205.9kJ·mol−1
2 2 4
B.CH 的平衡选择性随着温度的升高而增加
4
C.用该催化剂催化二氧化碳反应的最佳温度范围约为480~530℃
D.450℃时,提高 的值或增大压强,均能使 平衡转化率达到X点的值
7.(2022•江苏卷,13)乙醇-水催化重整可获得H。其主要反应为
2C HOH(g)+3H O(g)= 2CO (g)+6H(g) ΔH =173.3kJ·mol−1
2 5 2 2 2 2
CO(g)+H(g)= CO(g)+HO(g) ΔH =41.2kJ·mol−1
2 2 2 2
在 、n (C HOH):n (HO)=1:3时,若仅考虑上述反应,平衡时CO 和CO的选择性及H
始 2 5 始 2 2 2
的产率随温度的变化如图所示。
CO的选择性 ,下列说法正确的是( )
A.图中曲线①表示平衡时H 产率随温度的变化
2
B.升高温度,平衡时CO的选择性增大
C.一定温度下,增大 可提高乙醇平衡转化率
D.一定温度下,加入CaO(s)或选用高效催化剂,均能提高平衡时H 产率
2
1.多重平衡问题的解题思路
2.多平衡体系中有关平衡常数的计算技巧
(1)有关多平衡体系平衡常数的计算,如何确定多个反应相关联物质在平衡时量的多少是解题的关键点。
若用常规的三段式计算,对反应过程分析要求高,容易出错。但无论多少个反应,反应进行的程度如何,
反应前后的原子总数是不变的,因而解答这类问题可用原子守恒法,可规避对反应过程的分析。
(2)原子守恒法解题基本思路。1 .多重平衡体系分类
多重平衡可分成两类:一种是竞争性的多重平衡,此类反应被称为平行反应或竞争反应。平行反应指
的是反应物相同,生成物不同的两个或多个反应(其中一个生成目标产物的反应是主反应,其余的是副反
应)。另一种是连续性的多重平衡,此类反应被称为连续反应或分步反应。
2 .有关多重平衡及选择性的问题
在多重平衡中,几个可逆反应是相互影响的。
(1)如果主反应的生成物又与主反应的某一反应物发生另一个可逆反应,那么该反应物的平衡转化率就
会增大。
(2)在一定温度下,特定的混合体系,多重平衡选择性为定值。因为平衡常数只与温度有关,且催化剂
不能改变某一物质的平衡转化率。
(3)如果在同一条件下,两个物质同时可以发生几个可逆反应,那么催化剂的选用就可以使其中某一反
应的选择性提高。
3 .连续反应的思维模型【易错提醒】
连续反应中只要有一个反应平衡发生移动,那么另一个反应平衡也会联动。
4 .竞争反应的思维模型
5 .工业生产图像中转化率、产率变化分析思路
【易错提醒】
多重平衡体系达到整体综合平衡后,每种平衡组分都只能有一个平衡浓度。
考向 1 选择反应最佳条件
1.(2025·四川省绵阳市阶段练习)二甲醚和水蒸气制氢气可作为燃料电池的氢能源,发生的主要反应
如下:
反应I:CHOCH (g)+HO(g) 2CHOH(g) ΔH >0
3 3 2 3 1
反应Ⅱ:CHOH(g)+HO(g)=CO(g)+3H(g) ΔH >0
3 2 2 2 2
反应Ⅲ:CO(g)+H(g) CO(g)+HO(g) ΔH >0
2 2 2 3
在恒压下,将一定比例的二甲醚和水蒸气混合后,以一定流速通过装有催化剂的反应器,反应相同时间测得的CHOCH 实际转化率、CO 实际选择性与CO 平衡选择性随温度的变化如图所示,CO 的选择性
3 3 2 2 2
。下列说法不正确的是( )
A.曲线b表示CO 实际选择性随温度的变化
2
B.适当增加HO的物质的量,可提高H 的产率
2 2
C. 时,反应Ⅱ的速率大于反应Ⅲ的速率
D.一定温度下,若增大压强,反应Ⅲ平衡不移动,CO的平衡产量不变
2.(2025·北京市北师大附中高三模拟)甲烷还原二氧化碳是实现“双碳”目标的有效途径之一,常压、
催化剂作用下,按照CO 和CH 的物质的量之比 投料。有关反应如下:
2 4
反应I:CH(g)+CO(g) 2CO(g)+2H(g) ΔH =+247kJ·mol−1
4 2 2 1
反应Ⅱ:CO(g)+H(g) CO(g)+HO(g) ΔH =+41kJ·mol−1
2 2 2 2
某一时段内,CH 和CO 的转化率随温度变化如下图所示。
4 2
已知:CO 的转化效率
2
下列分析不正确的是( )A.根据反应Ⅰ、Ⅱ,低压高温有利于提高CO 的平衡转化率
2
B. 时,CO 转化的R值为
2
C.由 升高到 ,含氢产物中水的占比增大
D.由 升高到 ,CO 的转化效率逐渐增大
2
3.(2025·江苏省南京师大附中高三质检)在CO 与H 反应制甲醇的反应体系中,主要反应的热化学方
2 2
程式为
反应I:CO(g)+3H(g) CHOH(g)+HO(g) ΔH =-49.5kJ·mol−1
2 2 3 2 1
反应Ⅱ:CO(g)+H(g) CO(g)+HO(g) ΔH =+40.9kJ·mol−1
2 2 2 2
向恒压密闭容器中通入1molCO 和3molH ,CO 的平衡转化率、CHOH的平衡产率随温度的变化如下
2 2 2 3
图所示。下列说法正确的是( )
A.反应I的平衡常数
B.1molCO (g)和1molH (g)充分反应,吸收热量40.9kJ
2 2
C.平衡时CHOH的体积分数可能大于0.5
3
D.曲线a代表的是CO 的平衡转化率
2
4.一定条件下,用Fe O 、NiO或Cr O 作催化剂对燃煤烟气回收。反应为 2CO(g)+SO (g)
2 3 2 3 2
2CO(g)+S(l) ΔH=-270 kJ·mol-1。
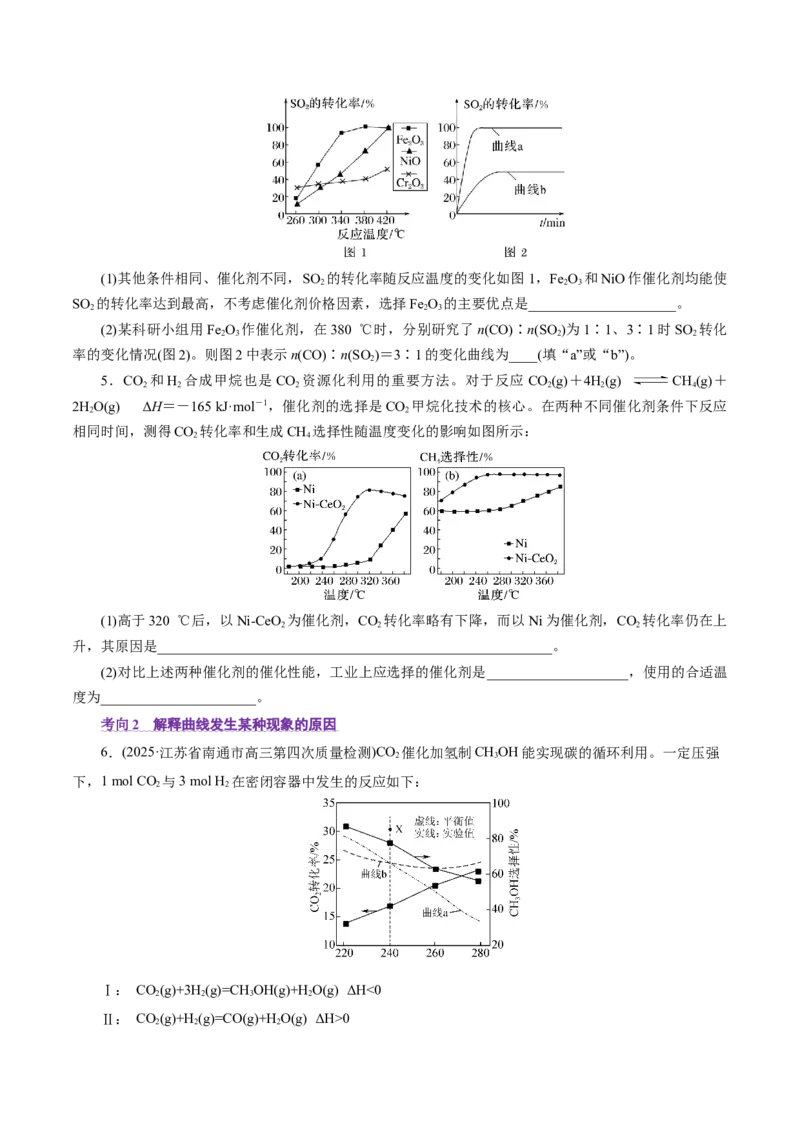
2(1)其他条件相同、催化剂不同,SO 的转化率随反应温度的变化如图1,Fe O 和NiO作催化剂均能使
2 2 3
SO 的转化率达到最高,不考虑催化剂价格因素,选择Fe O 的主要优点是_____________________。
2 2 3
(2)某科研小组用Fe O 作催化剂,在380 ℃时,分别研究了n(CO)∶n(SO )为1∶1、3∶1时SO 转化
2 3 2 2
率的变化情况(图2)。则图2中表示n(CO)∶n(SO )=3∶1的变化曲线为____(填“a”或“b”)。
2
5.CO 和H 合成甲烷也是CO 资源化利用的重要方法。对于反应 CO(g)+4H(g) CH(g)+
2 2 2 2 2 4
2HO(g) ΔH=-165 kJ·mol-1,催化剂的选择是CO 甲烷化技术的核心。在两种不同催化剂条件下反应
2 2
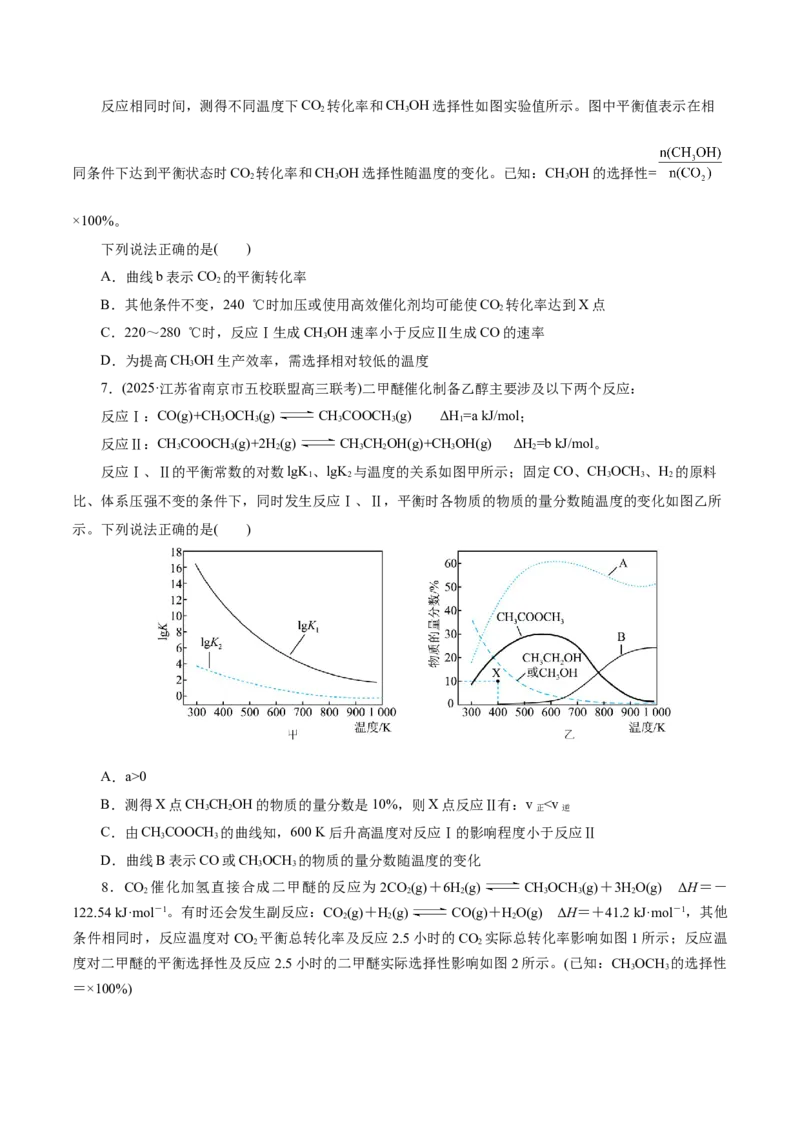
相同时间,测得CO 转化率和生成CH 选择性随温度变化的影响如图所示:
2 4
(1)高于320 ℃后,以Ni-CeO 为催化剂,CO 转化率略有下降,而以Ni为催化剂,CO 转化率仍在上
2 2 2
升,其原因是________________________________________________________。
(2)对比上述两种催化剂的催化性能,工业上应选择的催化剂是____________________,使用的合适温
度为______________________。
考向 2 解释曲线发生某种现象的原因
6.(2025·江苏省南通市高三第四次质量检测)CO 催化加氢制CHOH能实现碳的循环利用。一定压强
2 3
下,1 mol CO 与3 mol H 在密闭容器中发生的反应如下:
2 2
Ⅰ: CO(g)+3H(g)=CH OH(g)+H O(g) ΔH<0
2 2 3 2
Ⅱ: CO(g)+H(g)=CO(g)+HO(g) ΔH>0
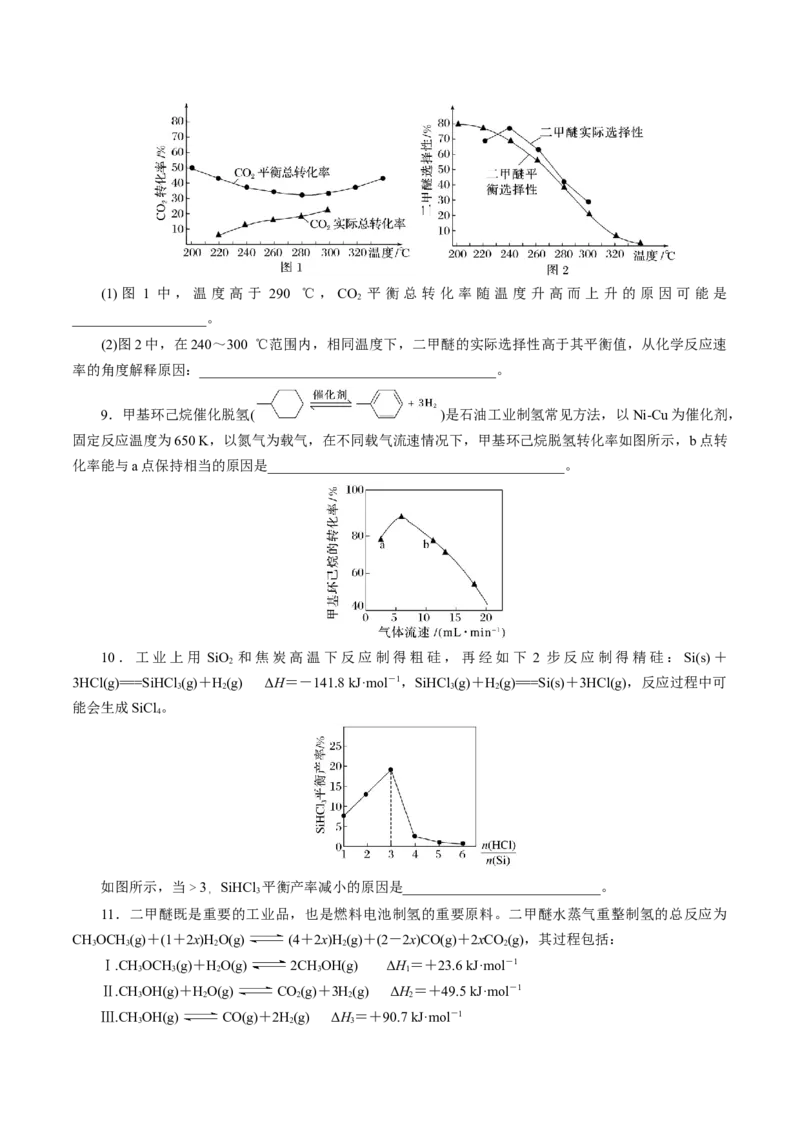
2 2 2反应相同时间,测得不同温度下CO 转化率和CHOH选择性如图实验值所示。图中平衡值表示在相
2 3
同条件下达到平衡状态时CO 转化率和CHOH选择性随温度的变化。已知:CHOH的选择性=
2 3 3
×100%。
下列说法正确的是( )
A.曲线b表示CO 的平衡转化率
2
B.其他条件不变,240 ℃时加压或使用高效催化剂均可能使CO 转化率达到X点
2
C.220~280 ℃时,反应Ⅰ生成CHOH速率小于反应Ⅱ生成CO的速率
3
D.为提高CHOH生产效率,需选择相对较低的温度
3
7.(2025·江苏省南京市五校联盟高三联考)二甲醚催化制备乙醇主要涉及以下两个反应:
反应Ⅰ:CO(g)+CHOCH (g) CHCOOCH (g) ΔH =a kJ/mol;
3 3 3 3 1
反应Ⅱ:CHCOOCH (g)+2H(g) CHCHOH(g)+CH OH(g) ΔH =b kJ/mol。
3 3 2 3 2 3 2
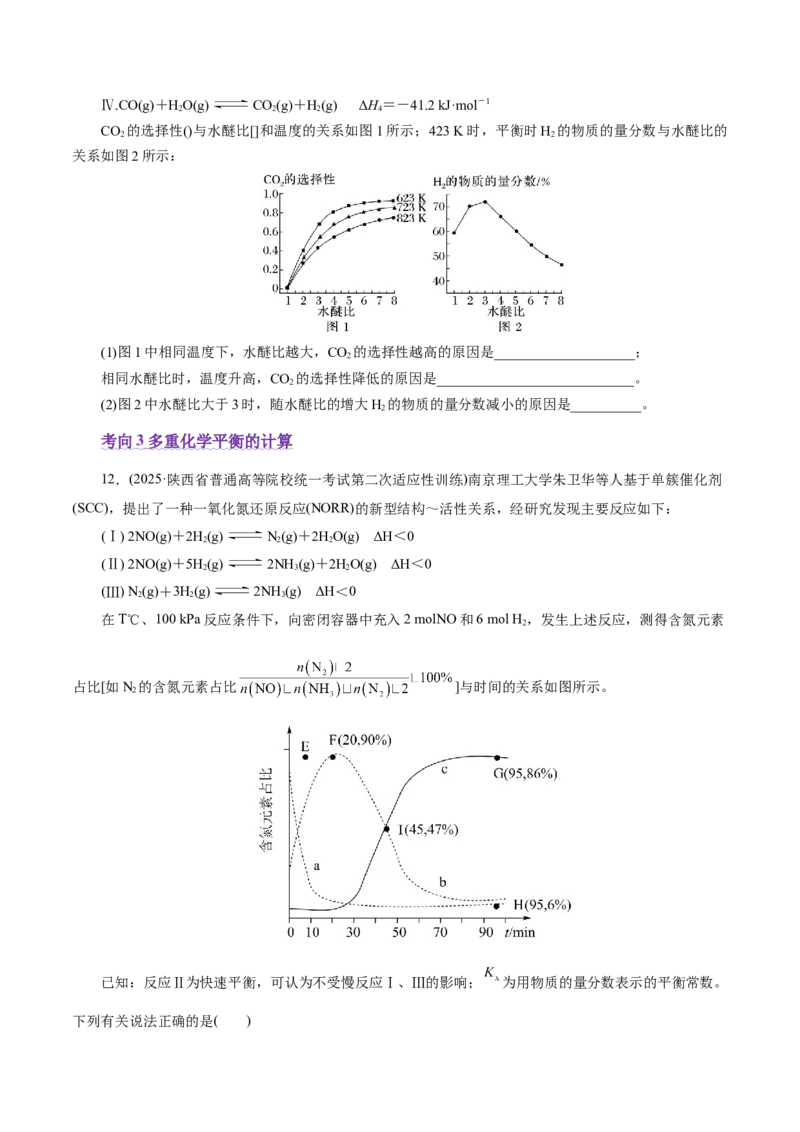
反应Ⅰ、Ⅱ的平衡常数的对数lgK 、lgK 与温度的关系如图甲所示;固定CO、CHOCH 、H 的原料
1 2 3 3 2
比、体系压强不变的条件下,同时发生反应Ⅰ、Ⅱ,平衡时各物质的物质的量分数随温度的变化如图乙所
示。下列说法正确的是( )
A.a>0
B.测得X点CHCHOH的物质的量分数是10%,则X点反应Ⅱ有:v