文档内容
热点强化练 3 高考试题中的铁及其化合物
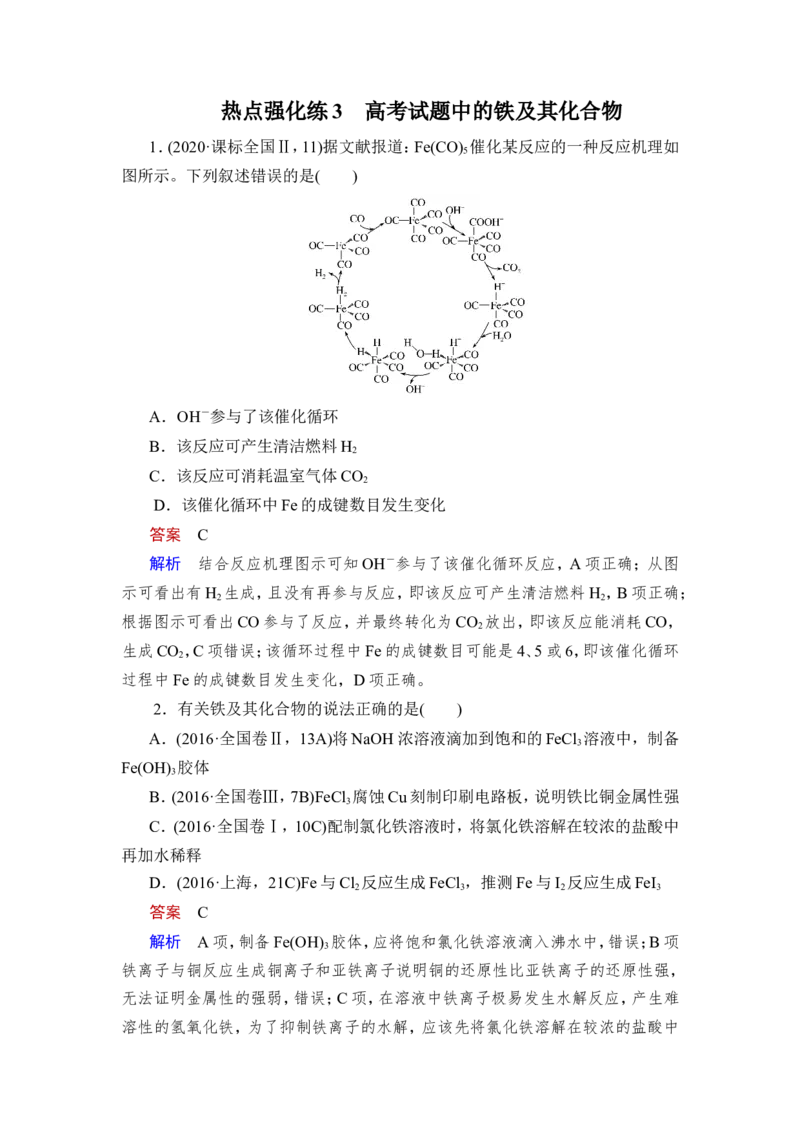
1.(2020·课标全国Ⅱ,11)据文献报道:Fe(CO) 催化某反应的一种反应机理如
5
图所示。下列叙述错误的是( )
A.OH-参与了该催化循环
B.该反应可产生清洁燃料H
2
C.该反应可消耗温室气体CO
2
D.该催化循环中Fe的成键数目发生变化
答案 C
解析 结合反应机理图示可知OH-参与了该催化循环反应,A项正确;从图
示可看出有H 生成,且没有再参与反应,即该反应可产生清洁燃料H ,B项正确;
2 2
根据图示可看出CO参与了反应,并最终转化为CO 放出,即该反应能消耗CO,
2
生成CO ,C项错误;该循环过程中Fe的成键数目可能是4、5或6,即该催化循环
2
过程中Fe的成键数目发生变化,D项正确。
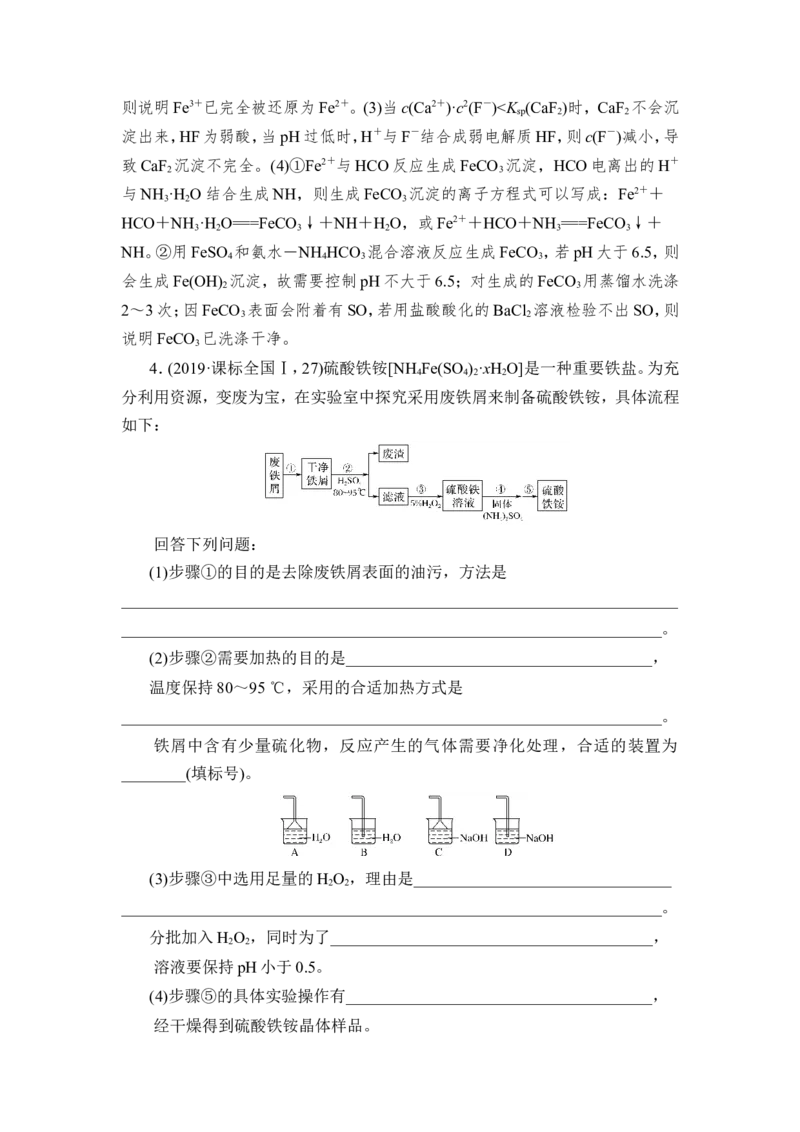
2.有关铁及其化合物的说法正确的是( )
A.(2016·全国卷Ⅱ,13A)将NaOH浓溶液滴加到饱和的FeCl 溶液中,制备
3
Fe(OH) 胶体
3
B.(2016·全国卷Ⅲ,7B)FeCl 腐蚀Cu刻制印刷电路板,说明铁比铜金属性强
3
C.(2016·全国卷Ⅰ,10C)配制氯化铁溶液时,将氯化铁溶解在较浓的盐酸中
再加水稀释
D.(2016·上海,21C)Fe与Cl 反应生成FeCl ,推测Fe与I 反应生成FeI
2 3 2 3
答案 C
解析 A项,制备Fe(OH) 胶体,应将饱和氯化铁溶液滴入沸水中,错误;B项
3
铁离子与铜反应生成铜离子和亚铁离子说明铜的还原性比亚铁离子的还原性强,
无法证明金属性的强弱,错误;C项,在溶液中铁离子极易发生水解反应,产生难
溶性的氢氧化铁,为了抑制铁离子的水解,应该先将氯化铁溶解在较浓的盐酸中然后再加水稀释到相应的浓度,正确;D项,因I 的氧化性较弱,故与铁反应生成
2
FeI ,错误。
2
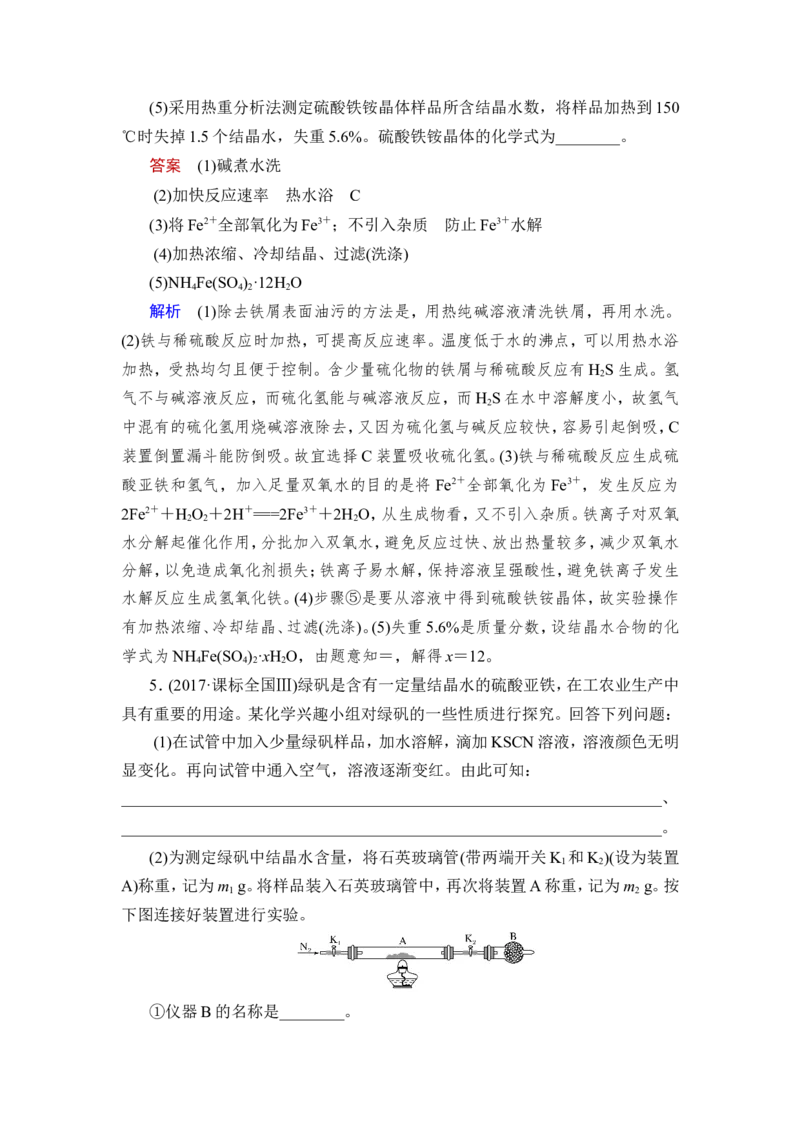
3.(2020·江苏卷)实验室由炼钢污泥(简称铁泥,主要成分为铁的氧化物)制备
软磁性材料αFe O 。其主要实验流程如下:
2 3
铁泥→→→→……→αFe O
2 3
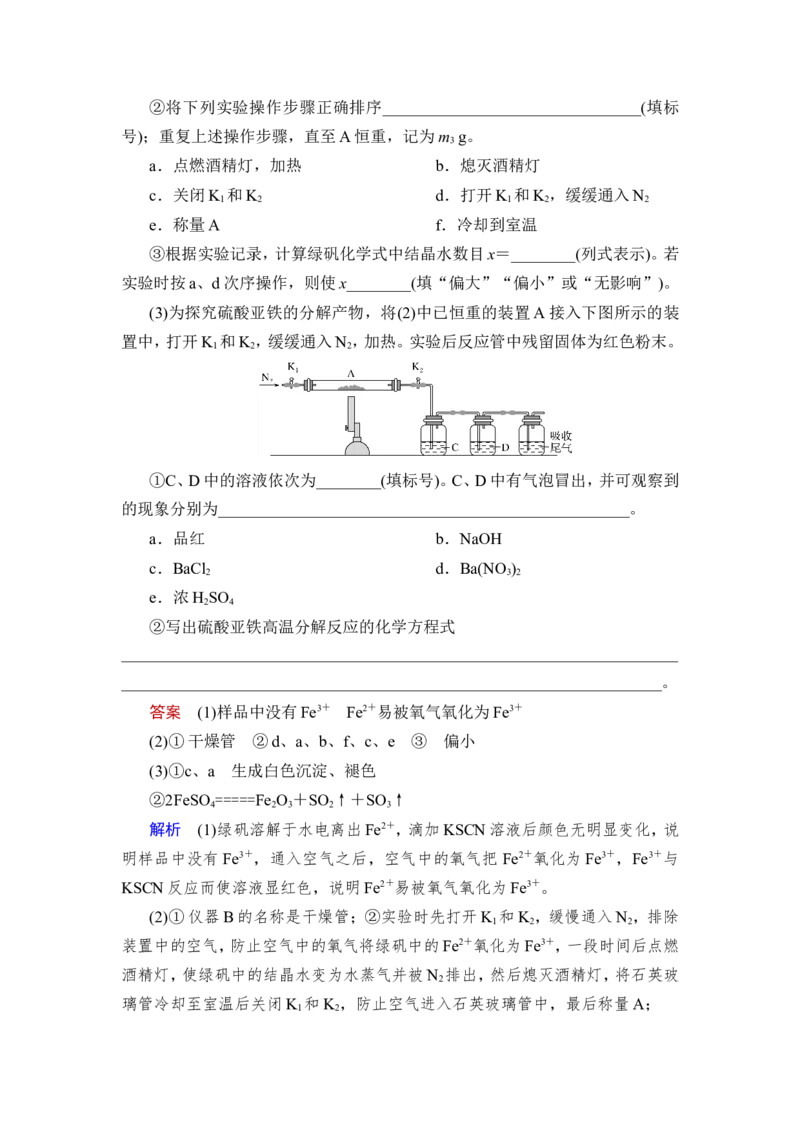
(1)酸浸。用一定浓度的H SO 溶液浸取铁泥中的铁元素。
2 4
(2)还原。向“酸浸”后的滤液中加入过量铁粉,使 Fe3+完全转化为 Fe2
+。“还原”过程中除生成Fe2+外,还会生成________(填化学式);检验Fe3+是否
还 原 完 全 的 实 验 操 作 是
__________________________________________________
___________________________________________________________________。
(3)除杂。向“还原”后的滤液中加入NH F溶液,使Ca2+转化为CaF 沉淀除
4 2
去 。 若 溶 液 的 pH 偏 低 , 将 会 导 致 CaF 沉 淀 不 完 全 , 其 原 因 是
2
____________________________________________________________________
_____________________________________________________________________
[K (CaF )=5.3×10-9,K (HF)=6.3×10-4]。
sp 2 a
(4)沉铁。将提纯后的 FeSO 溶液与氨水-NH HCO 混合溶液反应,生成
4 4 3
FeCO 沉淀。
3
①生成FeCO 沉淀的离子方程式为
3
_____________________________________________________________________
___________________________________________________________________。
②设计以FeSO 溶液、氨水-NH HCO 混合溶液为原料,制备FeCO 的实验
4 4 3 3
方案[FeCO 沉淀需“洗涤完全”,Fe(OH) 开始沉淀的pH=6.5]。
3 2
答案 (2)H 取少量清液,向其中滴加几滴KSCN溶液,观察溶液颜色是否
2
呈血红色 (3)pH偏低形成HF,导致溶液中F-浓度减小,CaF 沉淀不完全
2
(4)①Fe2++HCO+NH ·H O===FeCO ↓+NH+H O 或 Fe2++HCO+
3 2 3 2
NH ===FeCO ↓+NH
3 3
②在搅拌下向FeSO 溶液中缓慢加入氨水-NH HCO 混合溶液,控制溶液
4 4 3
pH不大于6.5;静置后过滤,所得沉淀用蒸馏水洗涤2~3次;取最后一次洗涤后
的滤液,滴加盐酸酸化的BaCl 溶液,不出现白色沉淀
2
解析 (2)“酸浸”时,H SO 过量,加入过量铁粉,除生成Fe2+外,还会产生
2 4
H 。Fe3+与KSCN反应所得溶液呈血红色,当加入KSCN溶液观察不到血红色,
2则说明Fe3+已完全被还原为Fe2+。(3)当c(Ca2+)·c2(F-)