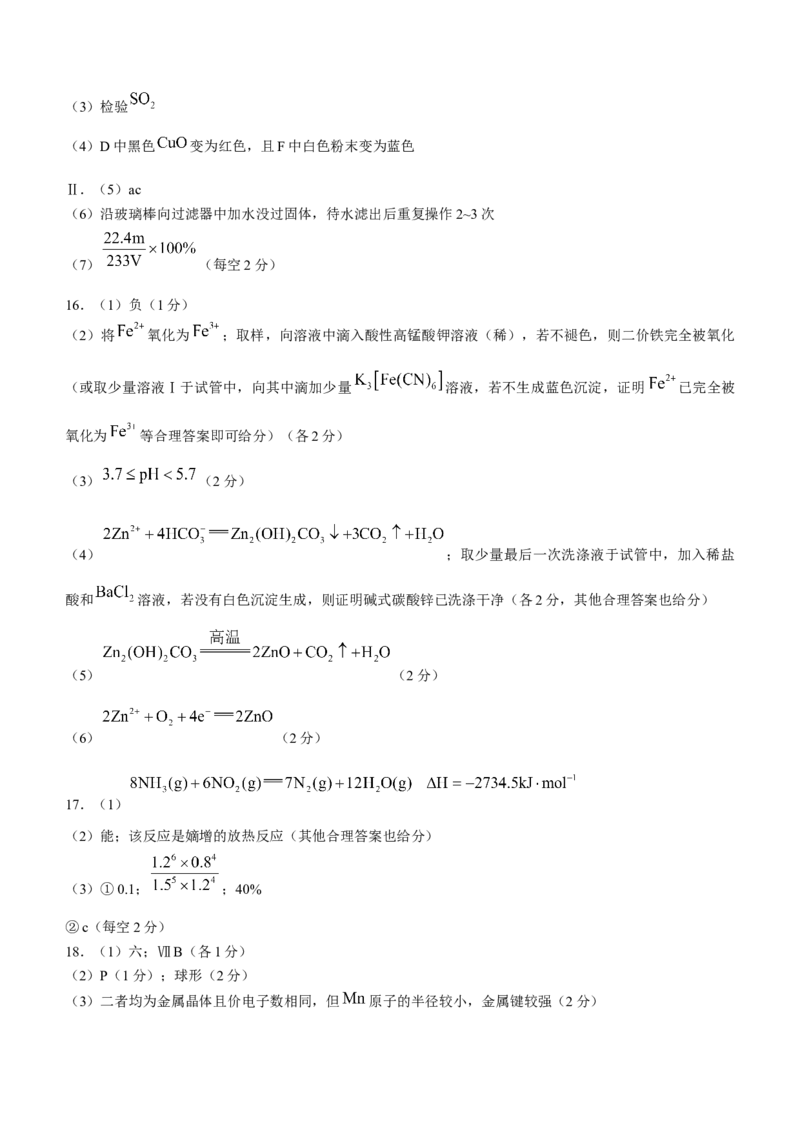文档内容
金昌市 2022-2023 学年高三上学期 9 月第一次模拟考试
化学
考生注意:
1.本试卷分选择题和非选择题两部分。满分100分,考试时间90分钟。
2.答题前,考生务必用直径0.5毫米黑色墨水签字笔将密封线内项目填写清楚。
3.考生作答时,请将答案答在答题卡上。选择题每小题选出答案后,用2B铅笔把答题卡上对
应题目的答案标号涂黑;非选择题请用直径 0.5毫米黑色墨水签字笔在答题卡上各题的答题区
域内作答,超出答题区域书写的答案无效,在试题卷、草稿纸上作答无效。
4.本试卷主要命题范围:高考范围。
5.可能用到的相对原子质量:H 1 C 12 O 16 S 32 Ba 137
一、选择题:本题共14小题,每小题3分,共计42分。在每小题列出的四个选项中,只有一
项是符合题目要求的。
1.化学与生活、环境密切相关。下列说法正确的是( )
A.烟花爆炸后产生的 污染空气 B.使用新能源汽车,有利于减少空气污染
C.厨房垃圾燃烧产物只有 和 D. 既能净化水又能软化硬水
2.已知有机物甲存在如图转化关系。下列说法正确的是( )
A.甲分子中所有原子共平面 B.乙、丙均能与 溶液反应
C. 甲最多能与 发生反应 D.丙存在与其具有相同官能团的芳香族同分异构体
3.下列说法正确的是( )
A.常温下,铝制品不能盛放任何含氧酸
B.电解、电离、电镀均需外加电源才能实现
C.氮、碳、硫的氧化物均是形成酸雨的物质
D.用 溶液可一次性鉴别出 和 四种溶液
4.关于下列仪器使用的说法正确的是( )A.滴定时用①盛放 溶液 B.②、③均可以直接加热
C.②、④可用于物质分离 D.③、⑤可用作反应容器
5.对下列粒子组在溶液中能否大量共存的判断和分析正确的是( )
选项 粒子组 判断和分析
不能大量共存,能发生反应:
A
B
不能大量共存,因发生反应:
C 能大量共存,粒子间不反应
D 能大量共存,粒子间不反应
A.A B.B C.C D.D
6. 为阿伏加德罗常数的值。下列说法中正确的是( )
A. 的 溶液中含 数目为
B. 溶液中, 的数目为
C. 中含极性键数目为
D. 由 与 组成的混合气体中氧原子数目为
7.下列气体的制备中,不能用启普发生器的是( )
选
化学试剂 制备的气体
项
A
(稀)
B
(浓)
C 石灰石 (稀)
D
锌粒 (稀)
A.A B.B C.C D.D
8.W、X、Y、Z为原子序数依次增大的短周期元素,W与X为同周期相邻元素,X与Z同主族,Y为地壳
中含量最丰富的金属元素,W与Z形成的一种气体化合物具有强氧化性,常用于自来水消毒。下列说法正确的是( )
A.常温下,W的氢化物为液态 B.X的最高价氧化物对应水化物为强酸
C.最简单氢化物的沸点: D.工业上常电解Y与Z形成的化合物制备金属Y
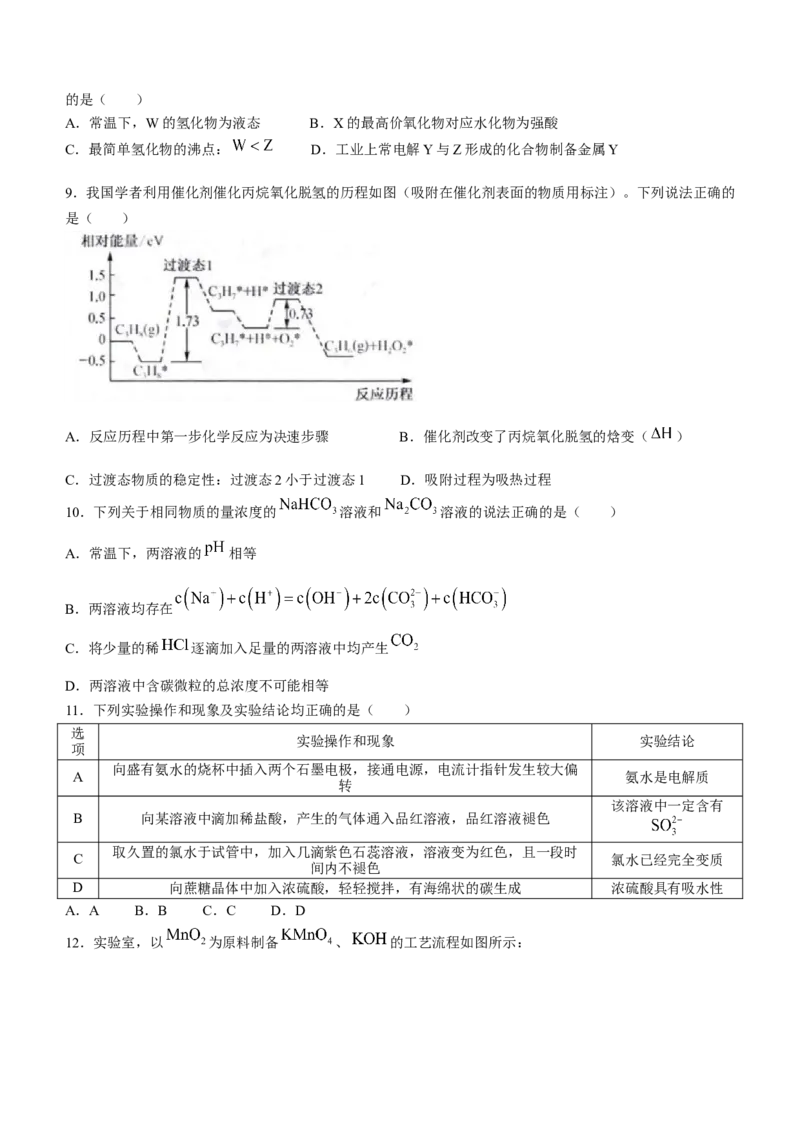
9.我国学者利用催化剂催化丙烷氧化脱氢的历程如图(吸附在催化剂表面的物质用标注)。下列说法正确的
是( )
A.反应历程中第一步化学反应为决速步骤 B.催化剂改变了丙烷氧化脱氢的焓变( )
C.过渡态物质的稳定性:过渡态2小于过渡态1 D.吸附过程为吸热过程
10.下列关于相同物质的量浓度的 溶液和 溶液的说法正确的是( )
A.常温下,两溶液的 相等
B.两溶液均存在
C.将少量的稀 逐滴加入足量的两溶液中均产生
D.两溶液中含碳微粒的总浓度不可能相等
11.下列实验操作和现象及实验结论均正确的是( )
选
实验操作和现象 实验结论
项
向盛有氨水的烧杯中插入两个石墨电极,接通电源,电流计指针发生较大偏
A 氨水是电解质
转
该溶液中一定含有
B 向某溶液中滴加稀盐酸,产生的气体通入品红溶液,品红溶液褪色
取久置的氯水于试管中,加入几滴紫色石蕊溶液,溶液变为红色,且一段时
C 氯水已经完全变质
间内不褪色
D 向蔗糖晶体中加入浓硫酸,轻轻搅拌,有海绵状的碳生成 浓硫酸具有吸水性
A.A B.B C.C D.D
12.实验室,以 为原料制备 、 的工艺流程如图所示:下列说法正确的是( )
A.步骤①用瓷坩埚作反应器 B.步骤②中 只体现还原性
C.步骤③用到的玻璃仪器有漏斗、烧杯,玻璃棒等 D.步骤④过程中有电子转移
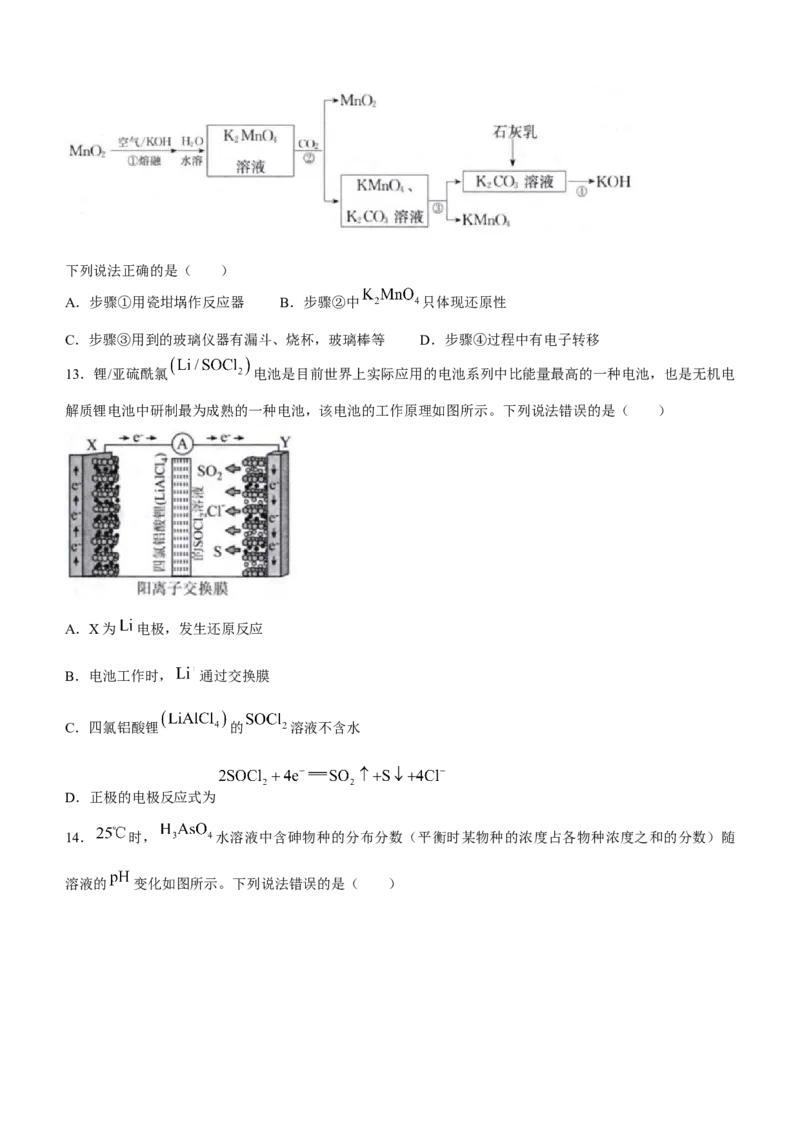
13.锂/亚硫酰氯 电池是目前世界上实际应用的电池系列中比能量最高的一种电池,也是无机电
解质锂电池中研制最为成熟的一种电池,该电池的工作原理如图所示。下列说法错误的是( )
A.X为 电极,发生还原反应
B.电池工作时, 通过交换膜
C.四氯铝酸锂 的 溶液不含水
D.正极的电极反应式为
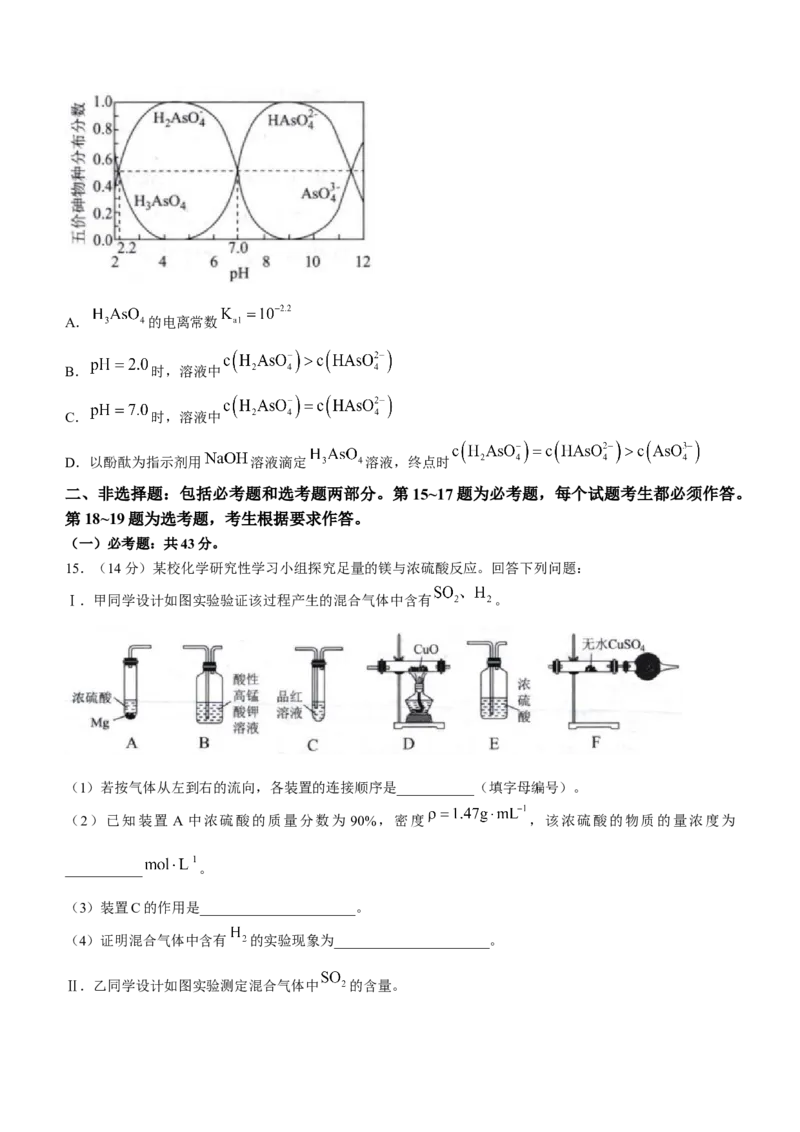
14. 时, 水溶液中含砷物种的分布分数(平衡时某物种的浓度占各物种浓度之和的分数)随
溶液的 变化如图所示。下列说法错误的是( )A. 的电离常数
B. 时,溶液中
C. 时,溶液中
D.以酚酞为指示剂用 溶液滴定 溶液,终点时
二、非选择题:包括必考题和选考题两部分。第15~17题为必考题,每个试题考生都必须作答。
第18~19题为选考题,考生根据要求作答。
(一)必考题:共43分。
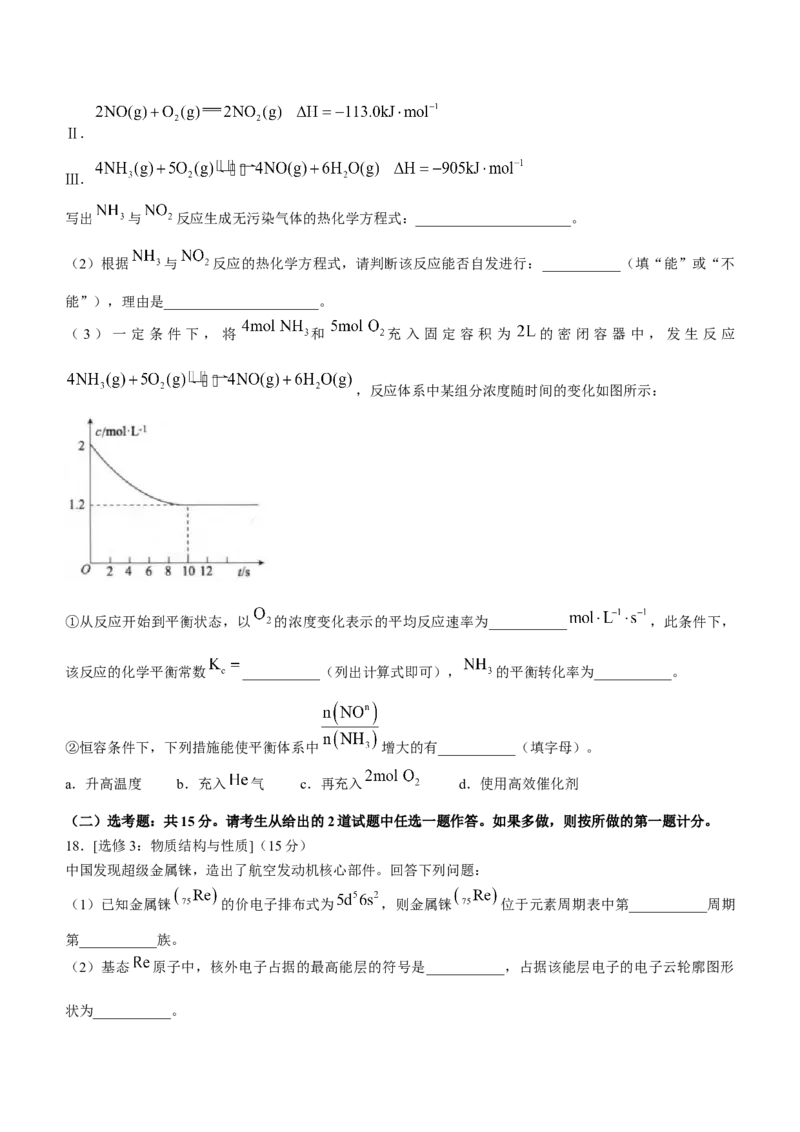
15.(14分)某校化学研究性学习小组探究足量的镁与浓硫酸反应。回答下列问题:
Ⅰ.甲同学设计如图实验验证该过程产生的混合气体中含有 。
(1)若按气体从左到右的流向,各装置的连接顺序是___________(填字母编号)。
(2)已知装置 A 中浓硫酸的质量分数为 90%,密度 ,该浓硫酸的物质的量浓度为
___________ 。
(3)装置C的作用是______________________。
(4)证明混合气体中含有 的实验现象为______________________。
Ⅱ.乙同学设计如图实验测定混合气体中 的含量。(5)W溶液可以是___________(填字母)。
a. 溶液 b.酸性 溶液(硫酸酸化) c.溴水
(6)步骤③中洗涤沉淀的操作为______________________。
(7)通过的混合气体体积为 (已换算成标准状况)时,该混合气体中 的含量(体积分数)为
___________(用V、m的代数式表示)。
16.(15分)氧化锌是一种常用的化学添加剂,广泛应用于合成橡胶、油漆涂料等产品的制作中。工业用废
旧电池中的锌皮(含杂质铁)生产氧化锌的工艺流程如图所示:
已知相关离子开始沉淀及完全沉淀的 如下表所示:
开始沉淀的 沉淀完全的
离子
6.4 8.4
2.7 3.7
5.7 9.0
回答下列问题:
(1)锌锰干电池中,锌作___________极。
(2)流程中,加入物质 A 的目的是 ___________,证明已达到目的的实验方法和现象为
______________________。
(3)加入 溶液调节 的范围为___________。
(4)滤液Ⅰ生成碱式碳酸锌 的离子方程式为______________________,洗涤碱式碳酸锌时,
证明已洗涤干净的方法为______________________。
(5)煅烧碱式碳酸锌的化学方程式为______________________。
(6)工业也可用阴极电沉积法制备氧化锌,基本原理是用锌的盐溶液作电解液,用溶液中溶解的氧气作为氧
化物合成的氧源,则阴极的电极反应式为______________________。
17.(14分)随着环境治理深入开展,大气污染治理已见成效。回答下列问题:
(1)已知:Ⅰ.Ⅱ.
Ⅲ.
写出 与 反应生成无污染气体的热化学方程式:______________________。
(2)根据 与 反应的热化学方程式,请判断该反应能否自发进行:___________(填“能”或“不
能”),理由是______________________。
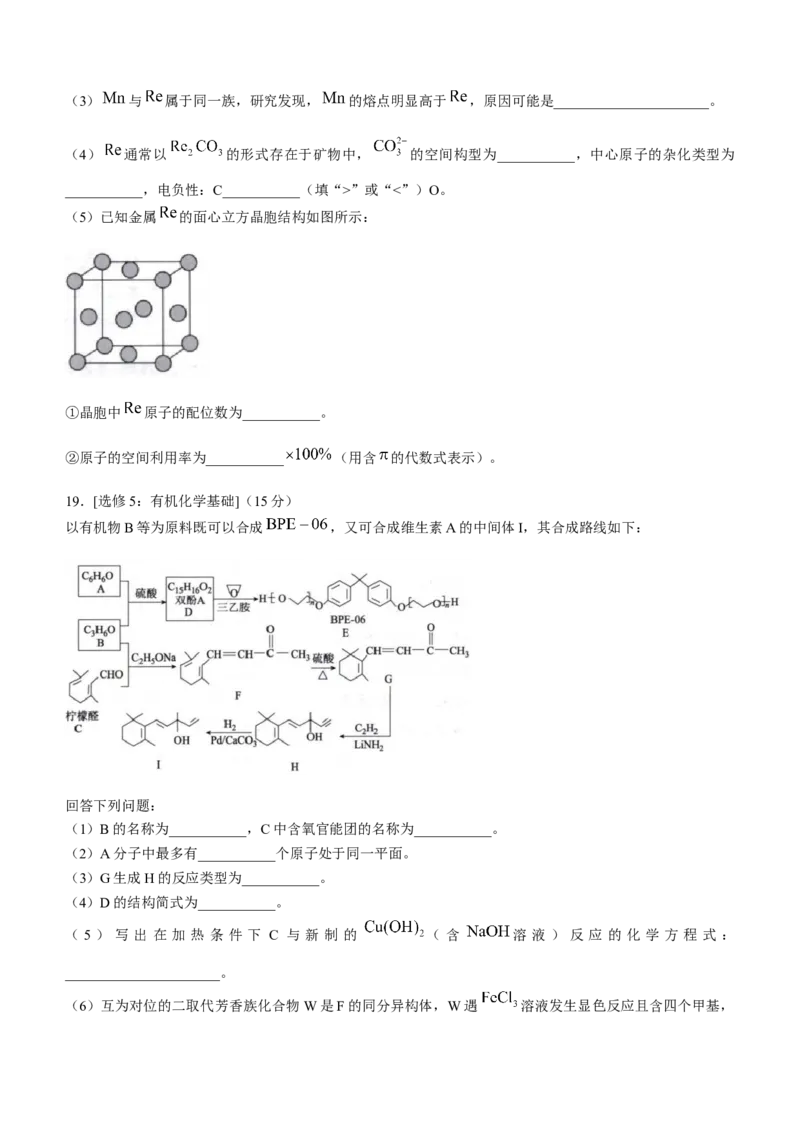
( 3 ) 一 定 条 件 下 , 将 和 充 入 固 定 容 积 为 的 密 闭 容 器 中 , 发 生 反 应
,反应体系中某组分浓度随时间的变化如图所示:
①从反应开始到平衡状态,以 的浓度变化表示的平均反应速率为___________ ,此条件下,
该反应的化学平衡常数 ___________(列出计算式即可), 的平衡转化率为___________。
②恒容条件下,下列措施能使平衡体系中 增大的有___________(填字母)。
a.升高温度 b.充入 气 c.再充入 d.使用高效催化剂
(二)选考题:共15分。请考生从给出的2道试题中任选一题作答。如果多做,则按所做的第一题计分。
18.[选修3:物质结构与性质](15分)
中国发现超级金属铼,造出了航空发动机核心部件。回答下列问题:
(1)已知金属铼 的价电子排布式为 ,则金属铼 位于元素周期表中第___________周期
第___________族。
(2)基态 原子中,核外电子占据的最高能层的符号是___________,占据该能层电子的电子云轮廓图形
状为___________。(3) 与 属于同一族,研究发现, 的熔点明显高于 ,原因可能是______________________。
(4) 通常以 的形式存在于矿物中, 的空间构型为___________,中心原子的杂化类型为
___________,电负性:C___________(填“>”或“<”)O。
(5)已知金属 的面心立方晶胞结构如图所示:
①晶胞中 原子的配位数为___________。
②原子的空间利用率为___________ (用含 的代数式表示)。
19.[选修5:有机化学基础](15分)
以有机物B等为原料既可以合成 ,又可合成维生素A的中间体I,其合成路线如下:
回答下列问题:
(1)B的名称为___________,C中含氧官能团的名称为___________。
(2)A分子中最多有___________个原子处于同一平面。
(3)G生成H的反应类型为___________。
(4)D的结构简式为___________。
( 5 ) 写 出 在 加 热 条 件 下 C 与 新 制 的 ( 含 溶 液 ) 反 应 的 化 学 方 程 式 :
______________________。
(6)互为对位的二取代芳香族化合物W是F的同分异构体,W遇 溶液发生显色反应且含四个甲基,则 W 的结构共有___________种(不考虑立体异构),其中核磁共振氢谱为 7 组峰,且峰面积之比为
1∶1∶2∶2∶2∶3∶9的结构简式为______________________。
高三化学参考答案、提示及评分细则
1.B 烟花爆炸能产生 ,A项错误;新能源汽车使用的是电能或氢能,无污染气体产生,B项正确;厨
房垃圾中含蛋白质,燃烧产生含氨物质,C项错误; 不能软化硬水,D项错误。
2.C 甲中含有饱和碳原子,A项错误;乙不与 溶液反应,B项错误;甲分子中有三个碳碳双键,可
与 反应,C项正确;苯环的不饱和度为4,而丙的不饱和度恰好为4,其芳香族同分异构体不可能
含有羧基,D项错误。
3.D 常温下,铝能盛放浓 ,A项错误;电离无需外加电源,B项错误;碳的氧化物不能形成酸雨,
C项错误;分别加入过量 溶液,可产生不同现象,D项正确。
4.C ①为酸式滴定管,A项错误;锥形瓶、蒸馏烧瓶不能直接加热,B项错误;蒸馏烧瓶,分液漏斗均可
用于物质分离,C项正确;容量瓶不可作为反应容器,D项错误。
5.B 之间发生反应 ,不能大量共存,A项错
误; 与 因发生反应: 而不能大量共存,B项正确; 与 不
共存,C项错误;在酸性条件下 能将 氧化为 ,不能大量共存,D项错误。
6.C 溶液体积未知,A项错误; 溶液中, 会发生水解反应, 的数目
小于 ,B项错误; 为 ,含 极性键,C项正确;未说明标准状况,且氧
原子数不可能为 ,D项错误。
7.B 制备 需要加热,故制备时不能用启普发生器,B项符合题意。
8.A 由题意知,W为O,X为F,Y为 ,Z为 。常温下, 、 均为液态,A项正确;F无
最高正价,B项错误;最简单氢化物的沸点: ,C项错误;工业上常电解 制备 ,D项错误。
9.A 化学反应的决速步骤是慢反应,而活化能越大,反应的速率越慢,由图可知能垒(活化能)最大的是
到过渡态I的能量,故第一步化学反应为决速步骤,A项正确;催化剂不能改反应的焓变( ),B
项错误;物质含的能量越低越稳定,故过渡态 2更稳定,C项错误;由图可知吸附过程为放热过程,D项错
误。
10.B 由于 的水解程度大于 ,故相同物质的量浓度时,两溶液 不等,A项错误;根据电离
守恒知,B项正确;少量稀盐酸与 反应无 产生,C项错误;两溶液含碳微粒的总浓度相等,D
项错误。
11.C 氨水是混合物,不属于电解质,A项错误;也可能含有 等,B项错误;石蕊不会褪色
说明氯水中已不含有 或 ,完全变质,C项正确;结论为浓硫酸具有脱水性,D项错误。
12.C 瓷埚中含 ,与 能反应,A项错误;②中 也体现氧化性,B项错误;③有过滤操
作,C项正确;④为复分解反应,D项错误。
13.A 根据电子流向可知,X为负极,Y为正极,故X为 电极,发生氧化反应,A项错误;负极的电极
反应式为 , 可透过离子交换膜向正极移动,B项正确; 的性质较活泼,易与水反应,
C 项 正 确 ; 由 装 置 图 可 知 , 正 极 有 生 成 , 故 电 极 反 应 式 为
,D项正确。
14 . D 由 图 可 知 , 时 , ,
,A 项正确;由图可知, 时,溶液中存在较多的
,几乎不存在 ,B项正确;由图可知, 时, ,C项
正确;酚酞试剂的变色范围为8.2~10.0,由图可知,此时 ,D项错误。
15.Ⅰ.(1)ACBEDF(其他合理答案也给分)
(2)13.5(3)检验
(4)D中黑色 变为红色,且F中白色粉末变为蓝色
Ⅱ.(5)ac
(6)沿玻璃棒向过滤器中加水没过固体,待水滤出后重复操作2~3次
(7) (每空2分)
16.(1)负(1分)
(2)将 氧化为 ;取样,向溶液中滴入酸性高锰酸钾溶液(稀),若不褪色,则二价铁完全被氧化
(或取少量溶液Ⅰ于试管中,向其中滴加少量 溶液,若不生成蓝色沉淀,证明 已完全被
氧化为 等合理答案即可给分)(各2分)
(3) (2分)
(4) ;取少量最后一次洗涤液于试管中,加入稀盐
酸和 溶液,若没有白色沉淀生成,则证明碱式碳酸锌已洗涤干净(各2分,其他合理答案也给分)
(5) (2分)
(6) (2分)
17.(1)
(2)能;该反应是嫡增的放热反应(其他合理答案也给分)
(3)①0.1; ;40%
②c(每空2分)
18.(1)六;ⅦB(各1分)
(2)P(1分);球形(2分)
(3)二者均为金属晶体且价电子数相同,但 原子的半径较小,金属键较强(2分)(4)平面三角形(2分); (1分);<(1分)
(5)①12(2分) ② (2分)
19.(1)丙酮;醛基(各1分)
(2)13(1分)
(3)加成反应(1分)
(4) (2分)
(5) (3分)
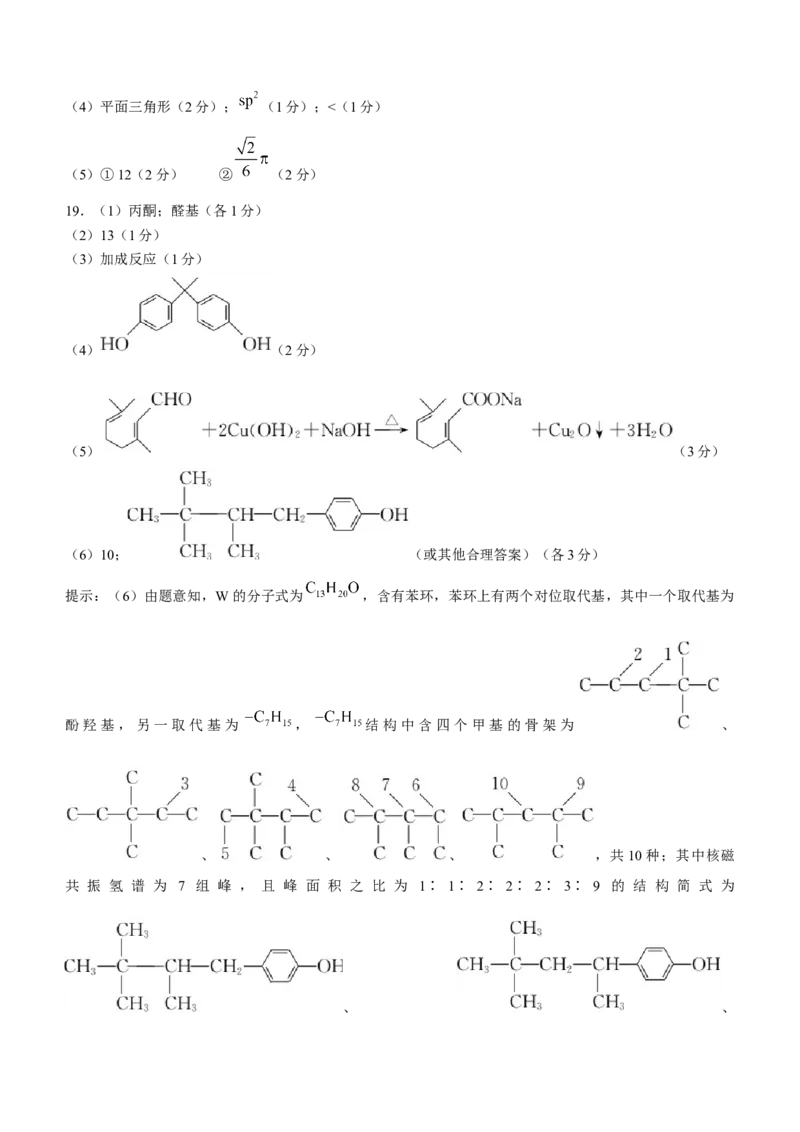
(6)10; (或其他合理答案)(各3分)
提示:(6)由题意知,W的分子式为 ,含有苯环,苯环上有两个对位取代基,其中一个取代基为
酚羟基,另一取代基为 , 结构中含四个甲基的骨架为 、
、 、 、 ,共10种;其中核磁
共 振 氢 谱 为 7 组 峰 , 且 峰 面 积 之 比 为 1∶ 1∶ 2∶ 2∶ 2∶ 3∶ 9 的 结 构 简 式 为
、 、。