文档内容
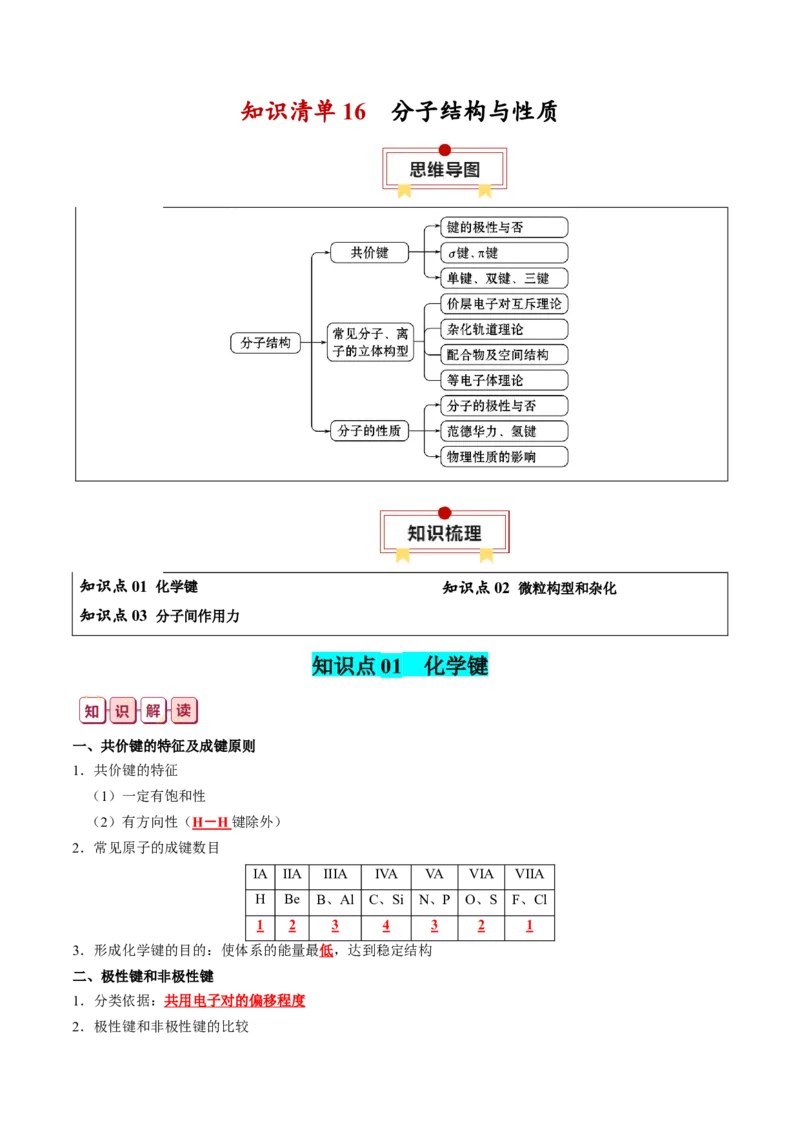
知识清单 16 分子结构与性质
知识点01 化学键 知识点02 微粒构型和杂化
知识点03 分子间作用力
知识点 01 化学键
一、共价键的特征及成键原则
1.共价键的特征
(1)一定有饱和性
(2)有方向性( H - H 键除外)
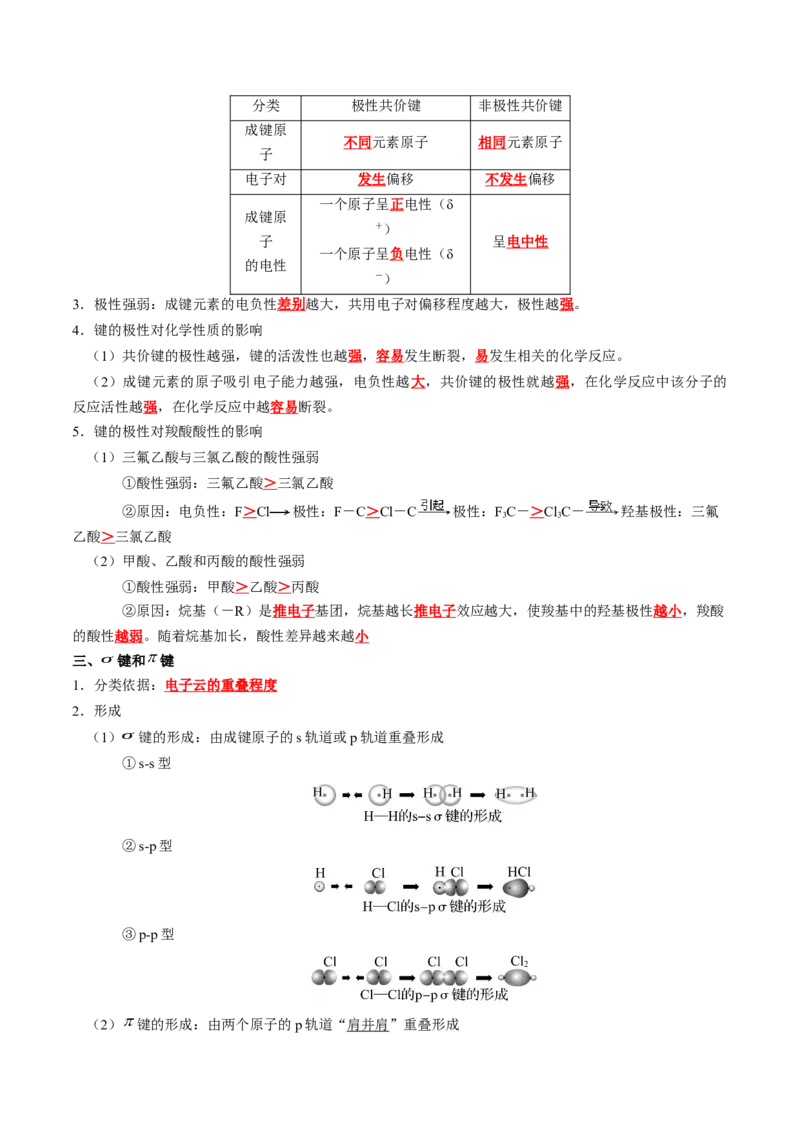
2.常见原子的成键数目
IA IIA IIIA IVA VA VIA VIIA
H Be B、Al C、Si N、P O、S F、Cl
1 2 3 4 3 2 1
3.形成化学键的目的:使体系的能量最低,达到稳定结构
二、极性键和非极性键
1.分类依据:共用电子对的偏移程度
2.极性键和非极性键的比较分类 极性共价键 非极性共价键
成键原
不同元素原子 相同元素原子
子
电子对 发生偏移 不发生偏移
一个原子呈正电性(δ
成键原
+)
子 呈电中性
一个原子呈负电性(δ
的电性
-)
3.极性强弱:成键元素的电负性差别越大,共用电子对偏移程度越大,极性越强。
4.键的极性对化学性质的影响
(1)共价键的极性越强,键的活泼性也越强,容易发生断裂,易发生相关的化学反应。
(2)成键元素的原子吸引电子能力越强,电负性越大,共价键的极性就越强,在化学反应中该分子的
反应活性越强,在化学反应中越容易断裂。
5.键的极性对羧酸酸性的影响
(1)三氟乙酸与三氯乙酸的酸性强弱
①酸性强弱:三氟乙酸>三氯乙酸
②原因:电负性:F>Cl 极性:F-C>Cl-C 极性:FC->ClC- 羟基极性:三氟
3 3
乙酸>三氯乙酸
(2)甲酸、乙酸和丙酸的酸性强弱
①酸性强弱:甲酸>乙酸>丙酸
②原因:烷基(-R)是推电子基团,烷基越长推电子效应越大,使羧基中的羟基极性越小,羧酸
的酸性越弱。随着烷基加长,酸性差异越来越小
三、σ 键和 键
1.分类依据:电子云的重叠程度
2.形成
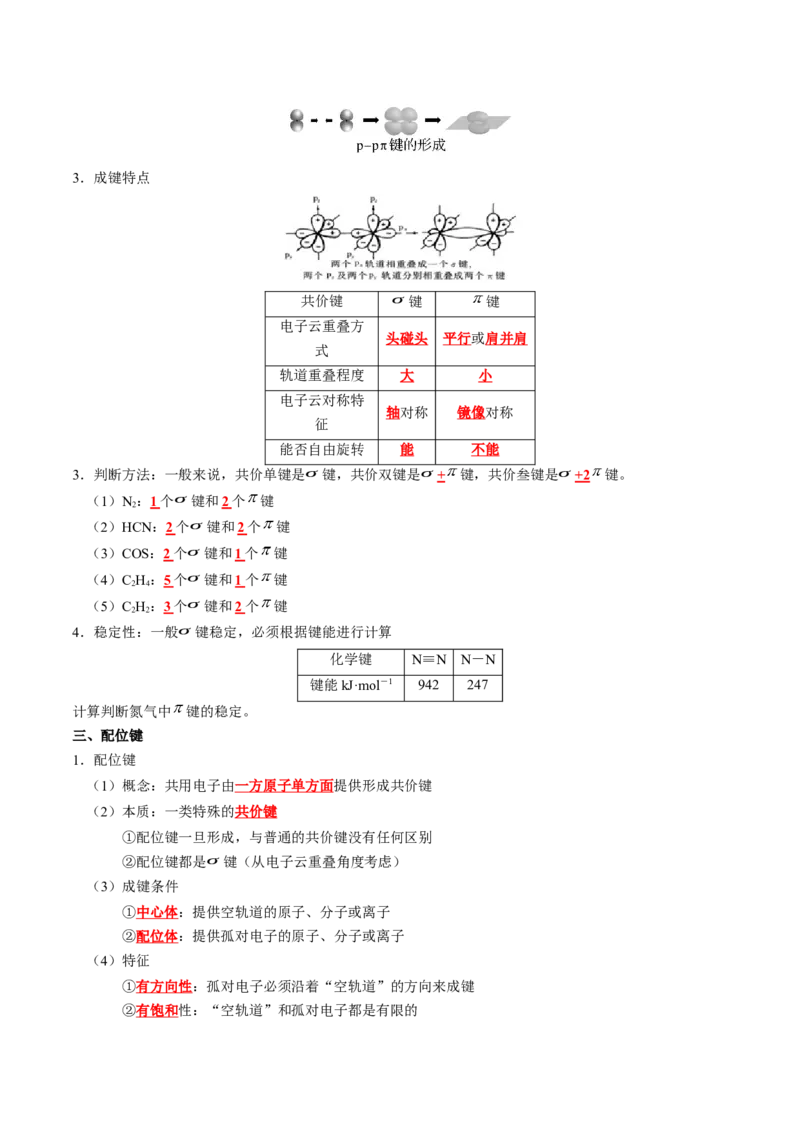
(1)σ 键的形成:由成键原子的s轨道或p轨道重叠形成
①s-s型
②s-p型
③p-p型
(2) 键的形成:由两个原子的p轨道“肩并肩”重叠形成3.成键特点
共价键 σ 键 键
电子云重叠方
头碰头 平行或肩并肩
式
轨道重叠程度 大 小
电子云对称特
轴对称 镜像对称
征
能否自由旋转 能 不能
3.判断方法:一般来说,共价单键是σ 键,共价双键是σ + 键,共价叁键是σ +2 键。
(1)N:1 个σ 键和2 个 键
2
(2)HCN:2 个σ 键和2 个 键
(3)COS:2 个σ 键和1 个 键
(4)C H:5 个σ 键和1 个 键
2 4
(5)C H:3 个σ 键和2 个 键
2 2
4.稳定性:一般σ 键稳定,必须根据键能进行计算
化学键 N≡N N-N
键能kJ·mol-1 942 247
计算判断氮气中 键的稳定。
三、配位键
1.配位键
(1)概念:共用电子由 一 方 原子单方面 提供形成共价键
(2)本质:一类特殊的共价键
①配位键一旦形成,与普通的共价键没有任何区别
②配位键都是σ 键(从电子云重叠角度考虑)
(3)成键条件
①中心体:提供空轨道的原子、分子或离子
②配位体:提供孤对电子的原子、分子或离子
(4)特征
①有方向性:孤对电子必须沿着“空轨道”的方向来成键
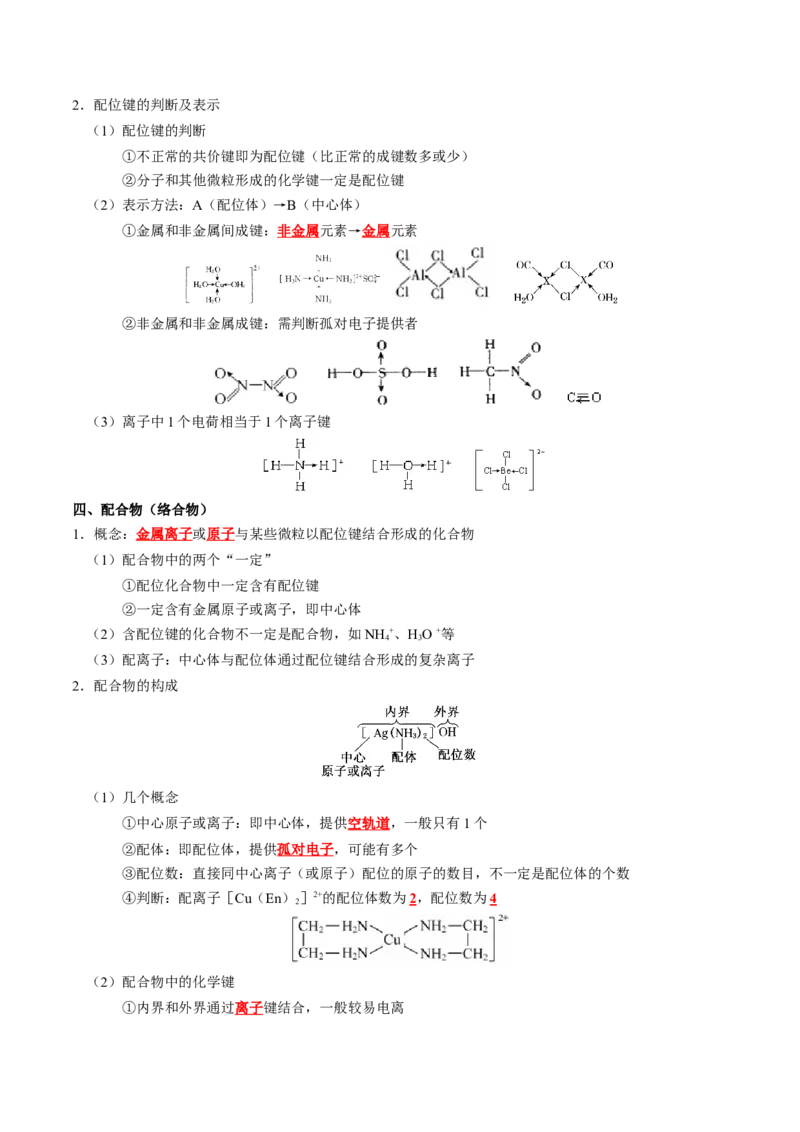
②有饱和性:“空轨道”和孤对电子都是有限的2.配位键的判断及表示
(1)配位键的判断
①不正常的共价键即为配位键(比正常的成键数多或少)
②分子和其他微粒形成的化学键一定是配位键
(2)表示方法:A(配位体)→B(中心体)
①金属和非金属间成键:非金属元素→金属元素
②非金属和非金属成键:需判断孤对电子提供者
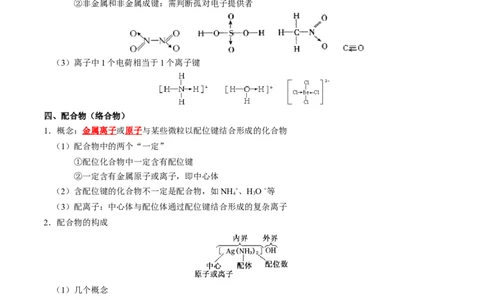
(3)离子中1个电荷相当于1个离子键
四、配合物(络合物)
1.概念:金属离子或原子与某些微粒以配位键结合形成的化合物
(1)配合物中的两个“一定”
①配位化合物中一定含有配位键
②一定含有金属原子或离子,即中心体
(2)含配位键的化合物不一定是配合物,如NH +、HO +等
4 3
(3)配离子:中心体与配位体通过配位键结合形成的复杂离子
2.配合物的构成
(1)几个概念
①中心原子或离子:即中心体,提供空轨道,一般只有1个
②配体:即配位体,提供孤对电子,可能有多个
③配位数:直接同中心离子(或原子)配位的原子的数目,不一定是配位体的个数
④判断:配离子[Cu(En)]2+的配位体数为2,配位数为4
2
(2)配合物中的化学键
①内界和外界通过离子键结合,一般较易电离②中心体和配位体通过配位键结合,一般很难电离
(3)配合物结构的确定
①1mol[CoCl (NH )]Cl--------------→1 mol AgCl
2 3 4
②1mol[CoCl(NH )]Cl--------------→2 mol AgCl
3 5 2
(4)特别提醒
①有的配合物没有外界。如五羰基合铁Fe(CO)、四羰基合镍Ni(CO)。
5 4
②有的配合物有多种配体。如[Cu(NH ) (HO) ] SO 、[Co(SO )(NH ) ]Br、[Co
3 2 2 2 4 4 3 5
(NH )Br]SO 。
3 5 4
3.配合物的稳定性:提供孤对电子和空轨道的能力越强,越稳定
(1)配位原子的半径越大,越易提供孤对电子
(2)过渡金属提供空轨道的能力强
(3)判断
①血红蛋白:Mb·O、Mb·CO、Mb·NO, Mb·C O 最稳定
2
②稳定性:[Mg(NH )]2+<[Cu(NH )]2+
3 4 3 4
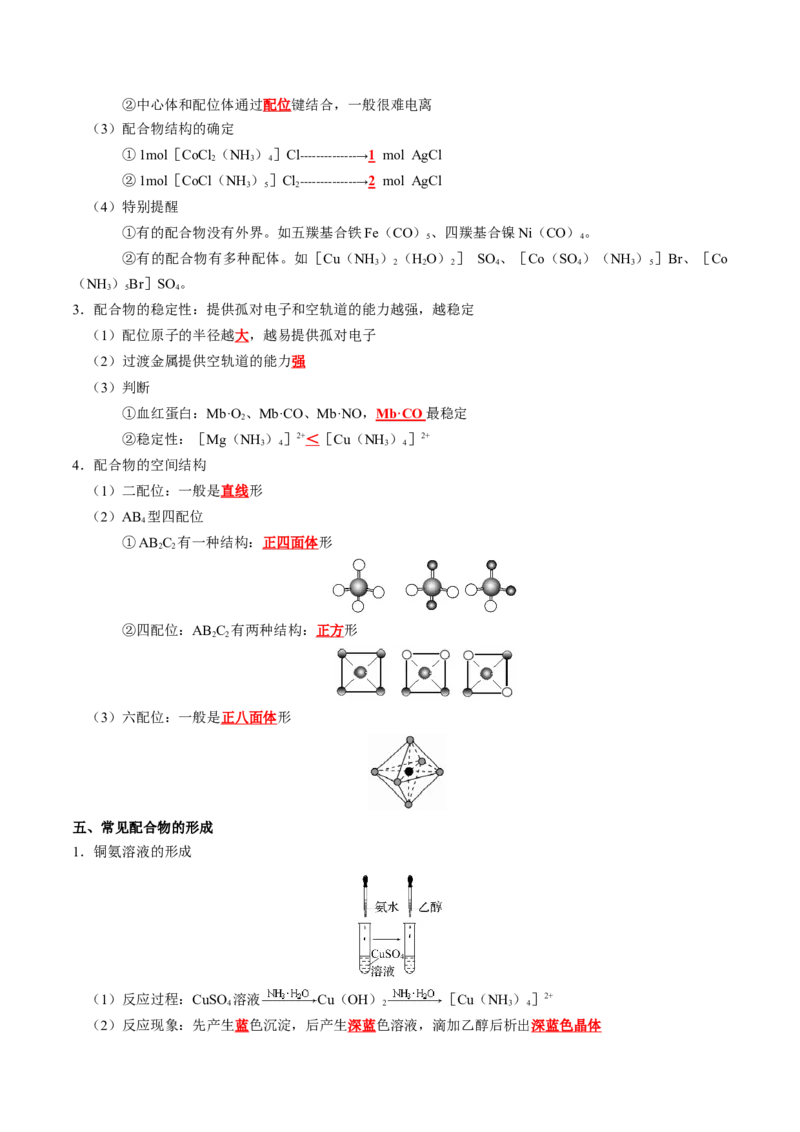
4.配合物的空间结构
(1)二配位:一般是直线形
(2)AB 型四配位
4
①AB C 有一种结构:正四面体形
2 2
②四配位:AB C 有两种结构:正方形
2 2
(3)六配位:一般是正八面体形
五、常见配合物的形成
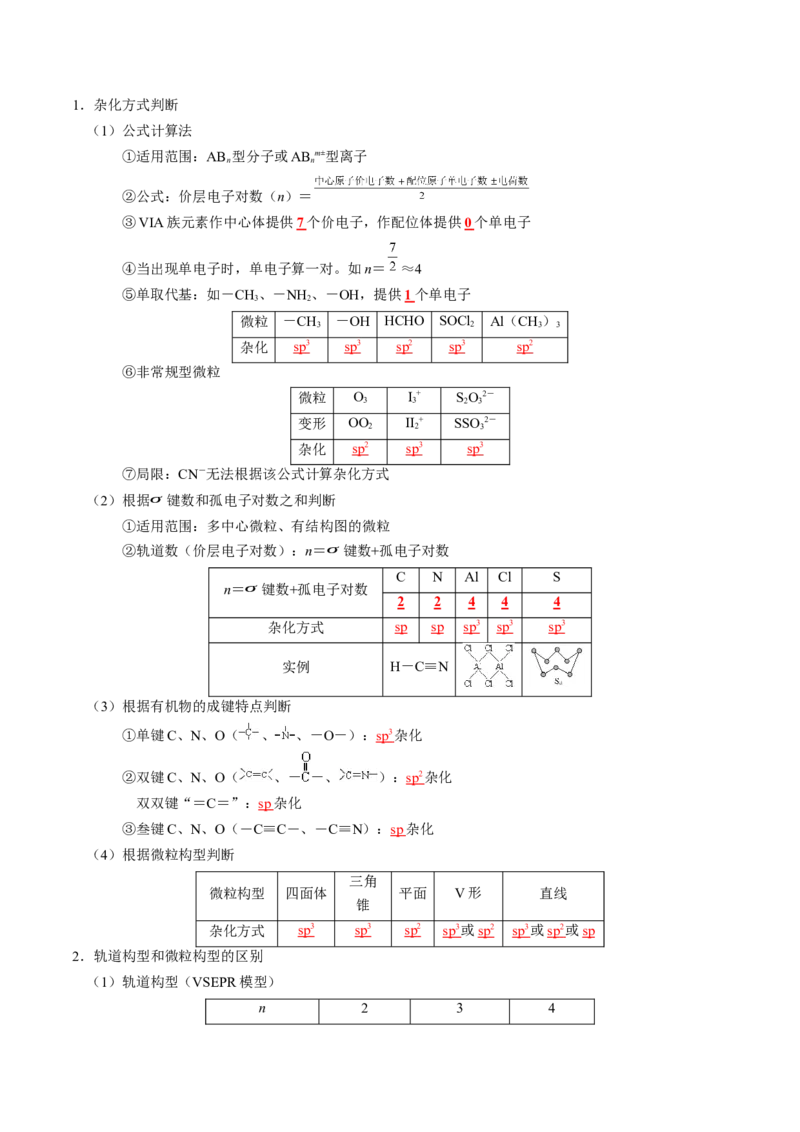
1.铜氨溶液的形成
(1)反应过程:CuSO 溶液 Cu(OH) [Cu(NH )]2+
4 2 3 4
(2)反应现象:先产生蓝色沉淀,后产生深蓝色溶液,滴加乙醇后析出深蓝色晶体(3)相关反应:
① Cu 2+ +2NH · H O Cu ( OH ) ↓ + 2 NH +
3 2 2 4
② Cu ( OH ) +4NH [ Cu ( NH ) ] 2 + +2OH -
2 3 3 4
③ [ Cu ( NH ) ] 2 + +SO 2 - +H O [ Cu ( NH ) ] SO · H O ↓
3 4 4 2 3 4 4 2
2.银氨溶液的形成
(1)反应过程:AgNO 溶液 AgOH [Ag(NH )]+
3 3 2
(2)反应现象:先产生白色沉淀,后产生无色溶液
(3)相关反应:
①AgNO +NH · H O AgOH ↓ +NH NO
3 3 2 4 3
②AgOH+2NH · H O [ A g ( NH ) ] OH+2H O
3 2 3 2 2
3.硫氰酸铁型溶液的形成
(1)反应过程:FeCl 溶液 [Fe(SCN) ]3-m
3 m
(2)反应现象:产生血红色溶液
(3)相关反应:
①m=1:FeCl + K SCN [ F e ( SCN ) ] C l + KCl
3 2
②m=2:FeCl + 2K SCN [ F e ( SCN ) ] C l + 2KC l
3 2
③m=3:FeCl + 3K SCN Fe ( SCN ) + 3KCl
3 3
④m=4:FeCl + 4K SCN K [ Fe ( SCN ) ] + 3KC l
3 4
⑤m=5:FeCl + 5K SCN K [ F e ( SCN ) ] + 3KC l
3 2 5
⑥m=6:FeCl + 6K SCN K [ F e ( SCN ) ] + 3KC l
3 3 6
4.四羟基合铝酸盐的形成
(1)反应过程:AlCl 溶液 Al(OH) [Al(OH)]-
3 3 4
(2)反应现象:先产生白色沉淀,后产生无色溶液
(3)相关反应:
① Al 3 + + 3OH - Al ( OH ) ↓
3
② Al ( OH ) + OH - [ A l ( OH ) ] -
3 4
易错点01 σ 键和 键易错知识点
(1)s轨道与s轨道重叠形成σ键时,电子不是只在两核间运动,而是在两核间出现的概率较大。(2)因s轨道是球形的,故s轨道和s轨道形成σ键时,无方向性。两个s轨道只能形成σ键,不能
形成π键。
(3)两个原子间可以只形成σ键,但不能只形成π键。
易错点02 配合物的易错知识点
(1)单核配体的确认要注意是否带有电荷,如F-、Cl-等,如配合物[CoCl(NH )]Cl ,中心离子为
3 5 2
Co3+,配体是Cl-和NH ,而不是氯原子。
3
(2)高考中常考有关配合物的结构示意图,不考虑空间结构,但要注意配体中的配位原子一定要与
中心原子或中心离子直接相连。如[Cu(NH )]2+中NH 中N原子为配位原子,所以N原子必须要与铜离子
3 4 3
直接相连。
【典例1】下列关于σ键和π键的理解不正确的是( )
A.含有π键的分子在进行化学反应时,分子中的π键比σ键活泼
B.在有些分子中,共价键可能只含有π键而没有σ键
C.有些原子在与其他原子形成分子时只能形成σ键,不能形成π键
D.当原子形成分子时,首先形成σ键,可能形成π键
【答案】B
【解析】同一分子中的π键不如σ键牢固,反应时比较容易断裂,A项正确;在共价单键中只含有σ键,
而含有π键的分子中一定含有σ键,B项错误、D项正确;氢原子、氯原子等跟其他原子形成分子时只能
形成σ键,C项正确。
【典例2】向盛有硫酸铜水溶液的试管里加入氨水,首先形成难溶物,继续添加氨水,难溶物溶解得到深
蓝色的透明溶液。下列对此现象的说法正确的是( )
A.沉淀溶解后,生成深蓝色的配合离子[Cu(NH )]2+
3 4
B.[Cu(H O) ]2+比[Cu(NH )]2+中的配位键稳定
2 4 3 4
C.用硝酸铜溶液代替硫酸铜溶液进行实验,不能观察到同样的现象
D.在[Cu(NH )]2+中,Cu2+给出孤电子对,NH 提供空轨道
3 4 3
【答案】A
【解析】从实验现象分析可知,Cu2+与NH ·H O反应生成Cu(OH) 沉淀。继续添加氨水,由于Cu2+更易与
3 2 2
NH 结合,生成更稳定的[Cu(NH )]2+。上述现象是Cu2+的性质,与SO无关,故换用Cu(NO ) 溶液仍可观
3 3 4 3 2
察到同样的现象,C项错误;在[Cu(NH )]2+中,Cu2+提供空轨道,NH 给出孤电子对,属于配位体,D项
3 4 3
错误。
知识点 02 微粒构型和杂化
一、价层电子对互斥理论1.杂化方式判断
(1)公式计算法
①适用范围:AB 型分子或AB m±型离子
n n
②公式:价层电子对数(n)=
③VIA族元素作中心体提供7 个价电子,作配位体提供0 个单电子
④当出现单电子时,单电子算一对。如n= ≈4
⑤单取代基:如-CH、-NH、-OH,提供1 个单电子
3 2
微粒 -CH -OH HCHO SOCl Al(CH)
3 2 3 3
杂化 sp 3 sp 3 sp 2 sp 3 s p 2
⑥非常规型微粒
微粒 O I+ SO2-
3 3 2 3
变形 OO II+ SSO 2-
2 2 3
杂化 sp 2 sp 3 sp 3
⑦局限:CN-无法根据该公式计算杂化方式
(2)根据σ 键数和孤电子对数之和判断
①适用范围:多中心微粒、有结构图的微粒
②轨道数(价层电子对数):n=σ 键数+孤电子对数
C N Al Cl S
n=σ 键数+孤电子对数
2 2 4 4 4
杂化方式 sp sp sp 3 sp 3 sp 3
实例 H-C≡N
(3)根据有机物的成键特点判断
①单键C、N、O( 、 、-O-): sp 3 杂化
②双键C、N、O( 、- -、 ): sp 2 杂化
双双键“=C=”:sp 杂化
③叁键C、N、O(―C≡C―、―C≡N):sp 杂化
(4)根据微粒构型判断
三角
微粒构型 四面体 平面 V形 直线
锥
杂化方式 sp 3 sp 3 s p 2 sp 3 或 s p 2 sp 3 或 s p 2 或 s p
2.轨道构型和微粒构型的区别
(1)轨道构型(VSEPR模型)
n 2 3 4杂化方式 sp sp2 sp3
轨道构型
(理想化模型)
直线形 平面正三角形 正四面体形
轨道夹角 180° 120° 109°28′
(2)轨道构型和微粒构型的关系
微粒 杂化方式 VSEPR模型 微粒构型 分子极性
SO sp 2 正四面体形 三角锥形 极性分子
2
SO sp 2 正四面体形 平面正三角形 非极性分子
3
NO
2
sp 2 平面正三角形 三角锥形
-
NO
3
sp 2 平面正三角形 平面正三角形
-
NO+ sp 直线形 直线形
2
二、分子的极性
1.化学键极性和分子极性的关系
2.分子极性的判断方法
(1)根据键的极性判断
①只含有非极性键的双原子分子或多原子分子是非极性分子。如O、H、P、C 。
2 2 4 60
②含有极性键的双原子分子都是极性分子。如HCl、HF、HBr。
③含有极性键的多原子分子,空间结构对称的是非极性分子;空间结构不对称的是极性分子。
(2)判断AB 型分子极性的经验规律
n
①中心原子A的化合价的绝对值等于该元素所在的主族序数,则为非极性分子;若不等,则为极
性分子。
②中心原子有孤电子对,则为极性分子;若无孤电子对,则为非极性分子。
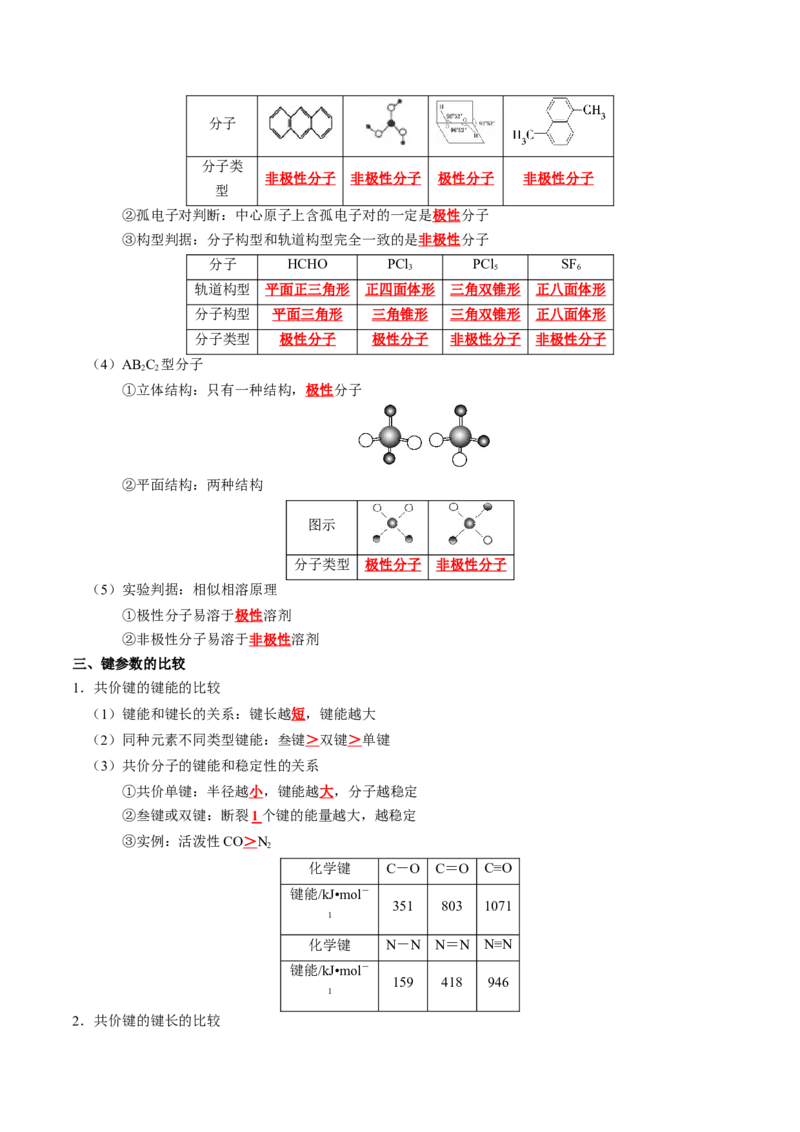
(3)结构判断
①对称性判断:高度对称的是非极性分子分子
分子类
非极性分子 非极性分子 极性分子 非极性分子
型
②孤电子对判断:中心原子上含孤电子对的一定是极性分子
③构型判据:分子构型和轨道构型完全一致的是非极性分子
分子 HCHO PCl PCl SF
3 5 6
轨道构型 平面正三角形 正四面体形 三角双锥形 正八面体形
分子构型 平面三角形 三角锥形 三角双锥形 正八面体形
分子类型 极性分子 极性分子 非极性分子 非极性分子
(4)AB C 型分子
2 2
①立体结构:只有一种结构,极性分子
②平面结构:两种结构
图示
分子类型 极性分子 非极性分子
(5)实验判据:相似相溶原理
①极性分子易溶于极性溶剂
②非极性分子易溶于非极性溶剂
三、键参数的比较
1.共价键的键能的比较
(1)键能和键长的关系:键长越短,键能越大
(2)同种元素不同类型键能:叁键>双键>单键
(3)共价分子的键能和稳定性的关系
①共价单键:半径越小,键能越大,分子越稳定
②叁键或双键:断裂1 个键的能量越大,越稳定
③实例:活泼性CO>N
2
化学键 C-O C=O C≡O
键能/kJ•mol-
351 803 1071
1
化学键 N-N N=N N≡N
键能/kJ•mol-
159 418 946
1
2.共价键的键长的比较(1)看有成键原子上是否都有孤对电子
①无孤对电子:只看成键原子的半径之和
②有孤对电子:还要看孤对电子之间的排斥作用
③键长比较
微粒组 键长长短
NH 和PH N-H<P-H
3 3
金刚石和晶体硅 C-C<Si-Si
稳定性:HO<NH<CHCH O-O>N-N>C-C
2 2 2 4 3 3
O、O-、O+、O2- 氧氧键:O2->O->O>O+
2 2 2 2 2 2 2 2
(2)看能否形成 键:形成 键使键长变短
①乙烷、苯和乙烯:C-C>特殊键>C=C
②金刚石和石墨中的碳碳键:金刚石<石墨
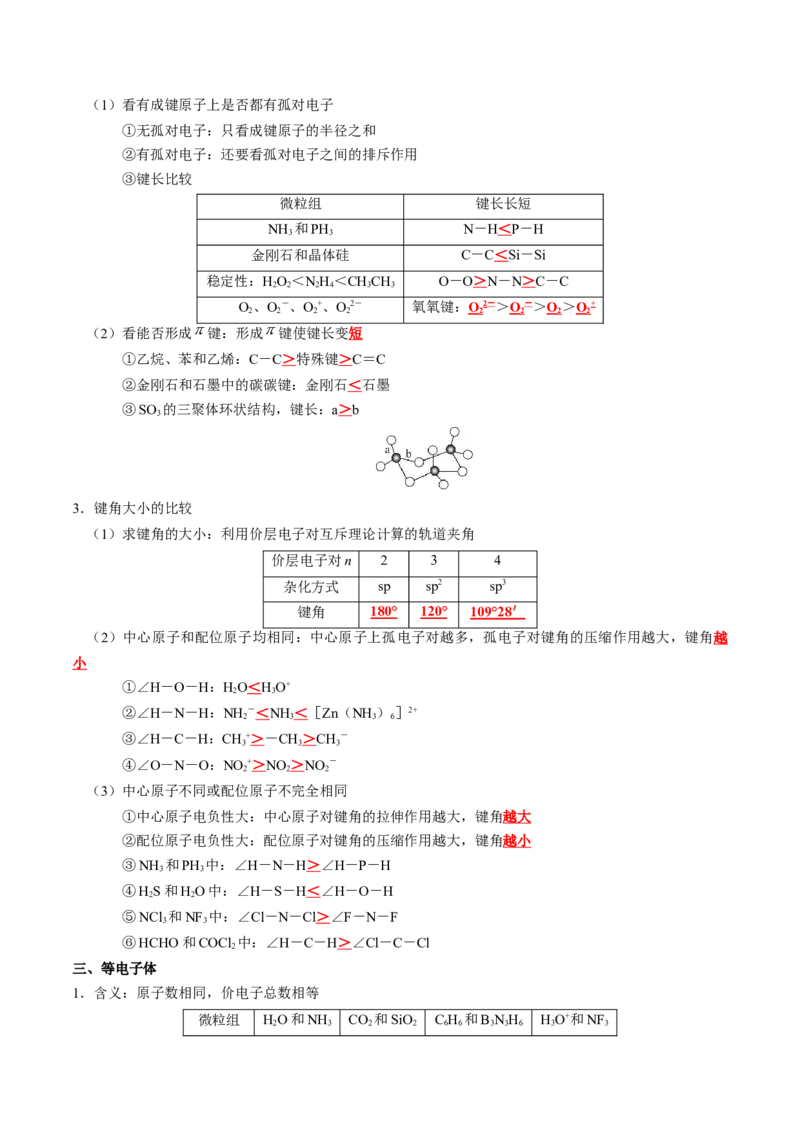
③SO 的三聚体环状结构,键长:a>b
3
3.键角大小的比较
(1)求键角的大小:利用价层电子对互斥理论计算的轨道夹角
价层电子对n 2 3 4
杂化方式 sp sp2 sp3
键角 1 8 0 ° 120 ° 109°28 ′
(2)中心原子和配位原子均相同:中心原子上孤电子对越多,孤电子对键角的压缩作用越大,键角越
小
①∠H-O-H:HO<HO+
2 3
②∠H-N-H:NH -<NH <[Zn(NH )]2+
2 3 3 6
③∠H-C-H:CH+>-CH>CH-
3 3 3
④∠O-N-O:NO +>NO >NO -
2 2 2
(3)中心原子不同或配位原子不完全相同
①中心原子电负性大:中心原子对键角的拉伸作用越大,键角越大
②配位原子电负性大:配位原子对键角的压缩作用越大,键角越小
③NH 和PH 中:∠H-N-H>∠H-P-H
3 3
④HS和HO中:∠H-S-H<∠H-O-H
2 2
⑤NCl 和NF 中:∠Cl-N-Cl>∠F-N-F
3 3
⑥HCHO和COCl 中:∠H-C-H>∠Cl-C-Cl
2
三、等电子体
1.含义:原子数相同,价电子总数相等
微粒组 HO和NH CO 和SiO C H 和B NH HO+和NF
2 3 2 2 6 6 3 3 6 3 3是否为
等电子 否 否 是 否
体
2.结构:立体结构、化学键类型相同,键角不一定相等
3.寻找方法
(1)同族元素上下换
(2)相邻元素左右移
(3)电子电荷可互换
4.常见的等电子体
(1)三原子8电子
①结构:sp3杂化,角型或V型
②典例:HO、HF+、NH -
2 2 2
(2)两原子10电子
①结构:sp杂化,直线形
②典例:N、CO、CN-、C 2-、O2+、NO+
2 2 2
(3)两原子11电子
①结构:sp杂化,直线形
②典例:NO、O+
2
(4)三原子16电子
①结构:sp杂化,直线形
②典例:CO、CS、NO、SCN-、NO +、N-、BeCl 、CNO-、AlO-、BeO2-
2 2 2 2 3 2 2 2
(5)三原子18电子
①结构:sp2杂化,角型或V型
②典例:SO 、O、NO -
2 3 2
(6)四原子24电子
①结构:sp2杂化,平面正三角形
②典例:BO3-、CO2-、NO -、SiO2-、SO 、BF、BCl 、AlCl
3 3 3 3 3 3 3 3
(7)四原子26电子
①结构:sp3杂化,三角锥型
②典例:PO 3-、SO 2-、ClO -
3 3 3
(8)五原子32电子
①结构:sp3杂化,正四面体形
②典例:ClO-、SO 2-、PO 3-、SiO4-、BF-、SiF、CCl 、CF、SiCl
4 4 4 4 4 4 4 4 4
(9)五原子8电子
①结构:sp3杂化,正四面体形
②典例:CH、NH +
4 4易错点01 分子空间构型易错知识点
(1)价层电子对的空间结构与分子的空间结构不一定一致,分子的空间结构指的是成键电子对的空间结
构,不包括孤电子对(未用于形成共价键的电子对)。两者是否一致取决于中心原子上有无孤电子对,当中
心原子上无孤电子对时,两者的空间结构一致;当中心原子上有孤电子对时,两者的空间结构不一致。
(2)四原子分子不是都为平面三角形或三角锥形。如 HO 分子的构型类似于一本打开的书,两个氧原子
2 2
在两页书的交接处,两个H原子分别在翻开的书的两页上,如图1所示:
再如白磷(P )分子为正四面体形,如图2所示。
4
(3)五原子分子不都是正四面体结构,如CHCl、CHCl 、CHCl 等,虽为四面体结构,但由于碳原子所
3 2 2 3
连的四个原子不相同,四个原子电子云的排斥力不同,使四个键的键角不全相等,所以并不是正四面体结
构。
易错点02 用价层电子对互斥模型推测分子或离子的空间结构时的常见错误
()计算阴、阳离子的中心原子的价层电子对数时未考虑离子所带电荷而计算错误。
()由电子式或路易斯结构式判断中心原子价层电子对数时未将双键或三键当作一对价层电子对计算。
()不能准确区分和判断孤电子对和成键电子对。判断 AB 型分子中孤电子对数的简单方法为孤电子对
n
数=价层电子对数-n。
()误将VSEPR模型当作分子或离子的空间结构。
()错误地利用相似性规律判断分子或离子的空间结构。
【典例1】下列说法正确的是( )
A.分子中键能越大,键长越长,则分子越稳定
B.元素周期表中第ⅠA族(除H外)和第ⅦA族元素间不能形成共价键
C.NH 、HO、CCl 和C H 四种分子中共价键的键角最小的为NH
3 2 4 2 2 3
D.H—O键的键能为463 kJ·mol-1,即18 g HO分解成H 和O 时,消耗的能量为926 kJ
2 2 2
【答案】B
【解析】分子中键能越大,键长越短,则分子越稳定,A项错误;第ⅠA族元素(除H外)的电负性都很小,
第ⅦA族元素的电负性都很大,不符合共价键的形成条件,B项正确;NH 、HO、CCl 和C H 四种分子
3 2 4 2 2
中共价键的键角依次为107°、105°、109°28′和180°,所以键角最小的为HO,C项错误;D项混淆了键能
2
和反应热的概念,反应热等于反应物中化学键的键能之和与生成物中化学键的键能之和的差,D项错误。【典例2】用价层电子对互斥理论(VSEPR)可以预测许多分子或离子的空间构型,有时也能用来推测键角
大小,下列判断正确的是
A.CS 是V形的分子
2
B.BF 键角为120°,HO键角大于120°
3 2
C.CHO、 都是平面三角形的分子
2
D.PCl 、PCl 都是三角锥形的分子
3 5
【答案】C
【解析】CS 的结构式为S=C=S,C原子价层电子对个数为2+ =2+0=2,无孤电子对,根据价层电子
2
对互斥理论判断CS 的空间构型为直线形,A错误; BF 分子中中,B原子价层电子对个数为3+
2 3
=3+0=3,无孤对电子,根据价层电子对互斥理论判断BF 的空间构型为平面正三角形,键角为120°;HO
3 2
分子中,O原子价层电子对个数为2+ =2+2=4,且含2个孤电子对,所以O原子采用sp3杂化,HO
2
的空间构型为V形,键角小于120°;B错误; CHO分子中,C原子形成3个σ键,C原子采用sp2杂化,
2
CHO的空间构型为平面三角形; 中,N原子形成3个σ键,孤对电子数为 =0,N原子采用
2
sp2杂化, 的空间构型为平面三角形;C正确; PCl 分子中,P原子价层电子对个数为3+
3
=3+1=4,含有一个孤电子对,根据价层电子对互斥理论判断PCl 的空间构型三角锥形;PCl 分子中,P原
3 5
子价层电子对个数为5+ =5+0=5,不含孤电子对,根据价层电子对互斥理论判断PCl 的空间构型为三
5
角双锥形;D错误;故选C。
知识点 03 分子间作用力
一、分子间作用力
1.概念:分子间存在的相互作用力
(1)实质:电性作用
(2)存在:分子和分子之间或稀有气体原子之间
2.分类
(1)范德华力:普通的分子间作用力
(2)氢键:特殊的分子间作用力
3.特点(1)作用范围很小,一般认为气体分子中无分子间作用力
(2)比化学键弱得多
4.外界条件对分子间作用力的影响
(1)压强:增大压强,分子间作用力增大
(2)温度:升高温度,分子间作用力减小
二、范德华力与物质性质
1.特点:无方向性,无饱和性
2.影响因素
(1)分子的极性越大,范德华力越大
(2)组成和结构相似的物质,相对分子质量越大,范德华力越大
3.作用效果
(1)组成和结构相似的分子,相对分子质量越大,熔沸点越高
(2)由分子构成的晶体熔点低、挥发性强、硬度小
4.范德华力与化学键作用效果的区别
(1)范德华力主要影响物质的物理性质,如物质的熔、沸点等
(2)化学键主要影响物质的化学性质,如热稳定性等
三、氢键与物质性质
1.氢键的实质:电性作用(介于范德华力和共价键之间)
2.氢键的表示方法: X - H … Y
(1)“-”表示共价键,“…”表示氢键
(2)氢键形成的一般条件
①分子中必须有氢原子
②氢原子两边有电负性大、半径小、具有孤对电子的元素(F、O、N)
③-NH +中的N原子能否形成氢键:不能
3
④-CHO中的H原子能否形成氢键:不能
3.氢键的特点
(1)有方向性:沿着孤对电子的伸展方向成键
(2)有饱和性:氢原子与孤电子对相对应
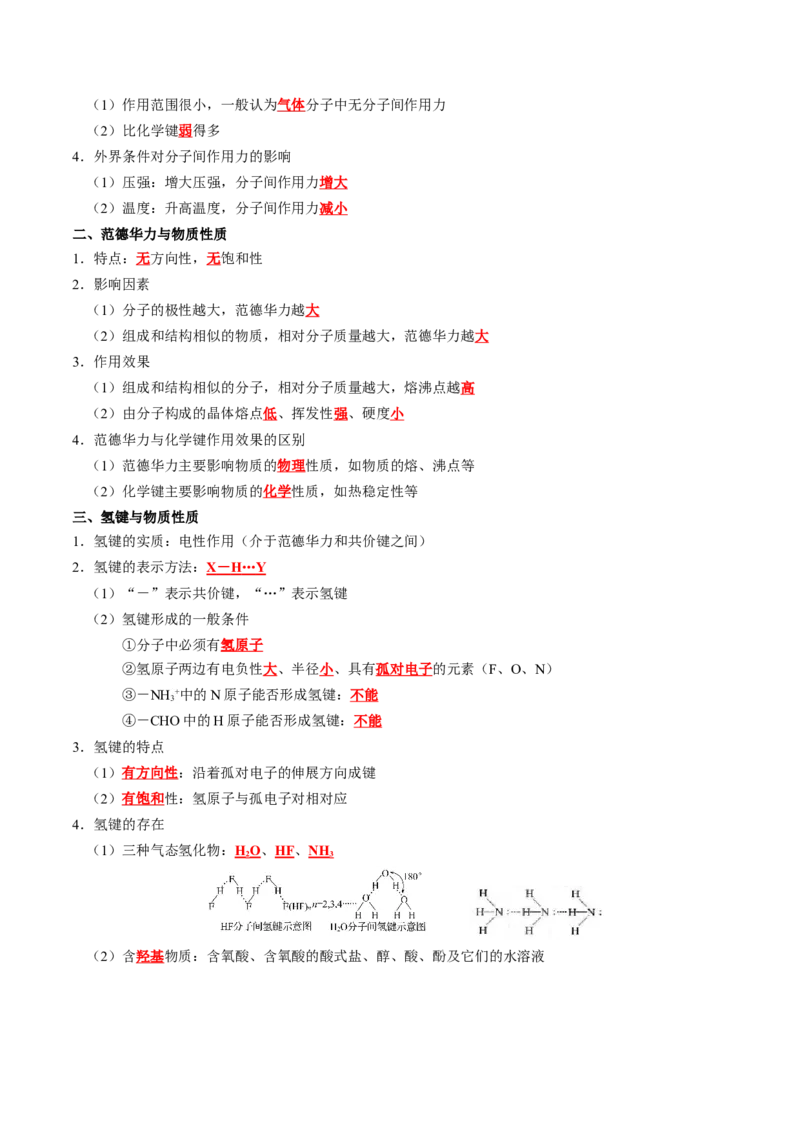
4.氢键的存在
(1)三种气态氢化物:HO、HF、NH
2 3
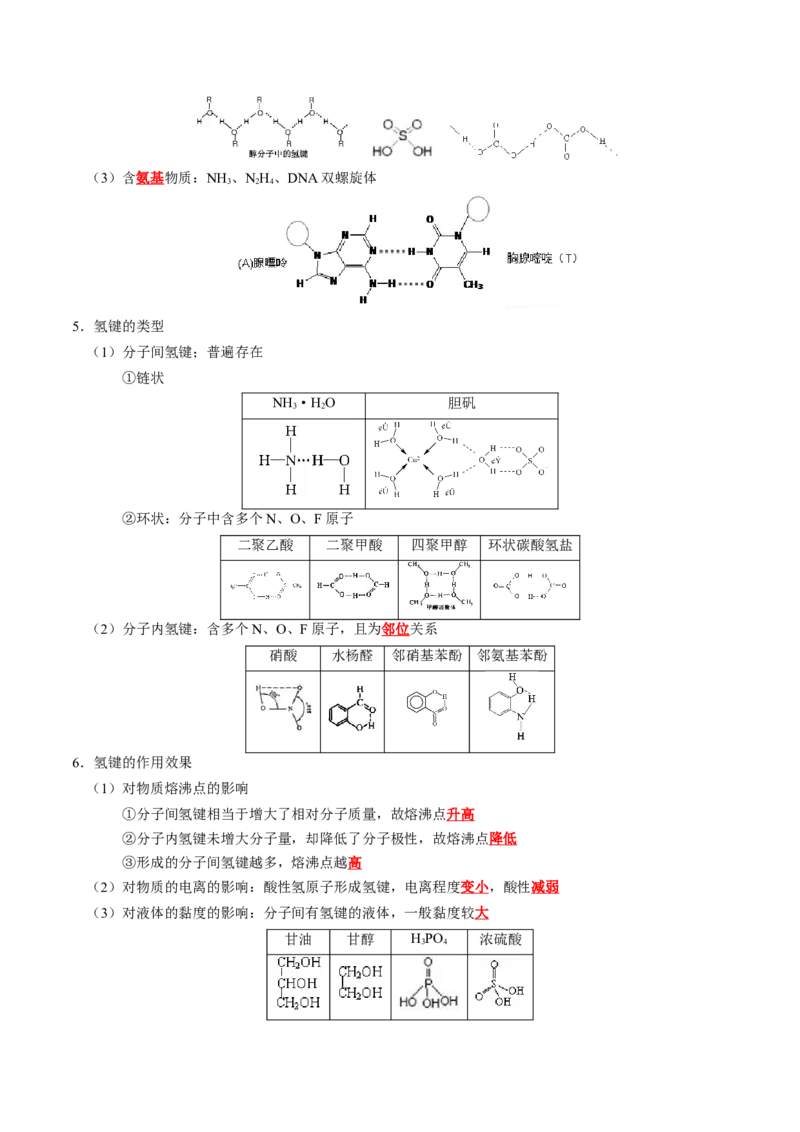
(2)含羟基物质:含氧酸、含氧酸的酸式盐、醇、酸、酚及它们的水溶液(3)含氨基物质:NH 、NH、DNA双螺旋体
3 2 4
5.氢键的类型
(1)分子间氢键;普遍存在
①链状
NH ·HO 胆矾
3 2
②环状:分子中含多个N、O、F原子
二聚乙酸 二聚甲酸 四聚甲醇 环状碳酸氢盐
(2)分子内氢键:含多个N、O、F原子,且为邻位关系
硝酸 水杨醛 邻硝基苯酚 邻氨基苯酚
6.氢键的作用效果
(1)对物质熔沸点的影响
①分子间氢键相当于增大了相对分子质量,故熔沸点升高
②分子内氢键未增大分子量,却降低了分子极性,故熔沸点降低
③形成的分子间氢键越多,熔沸点越高
(2)对物质的电离的影响:酸性氢原子形成氢键,电离程度变小,酸性减弱
(3)对液体的黏度的影响:分子间有氢键的液体,一般黏度较大
甘油 甘醇 HPO 浓硫酸
3 4(4)冰的密度:结冰时水中的氢键增多,水分子间的空隙变大,体积增大,密度减小
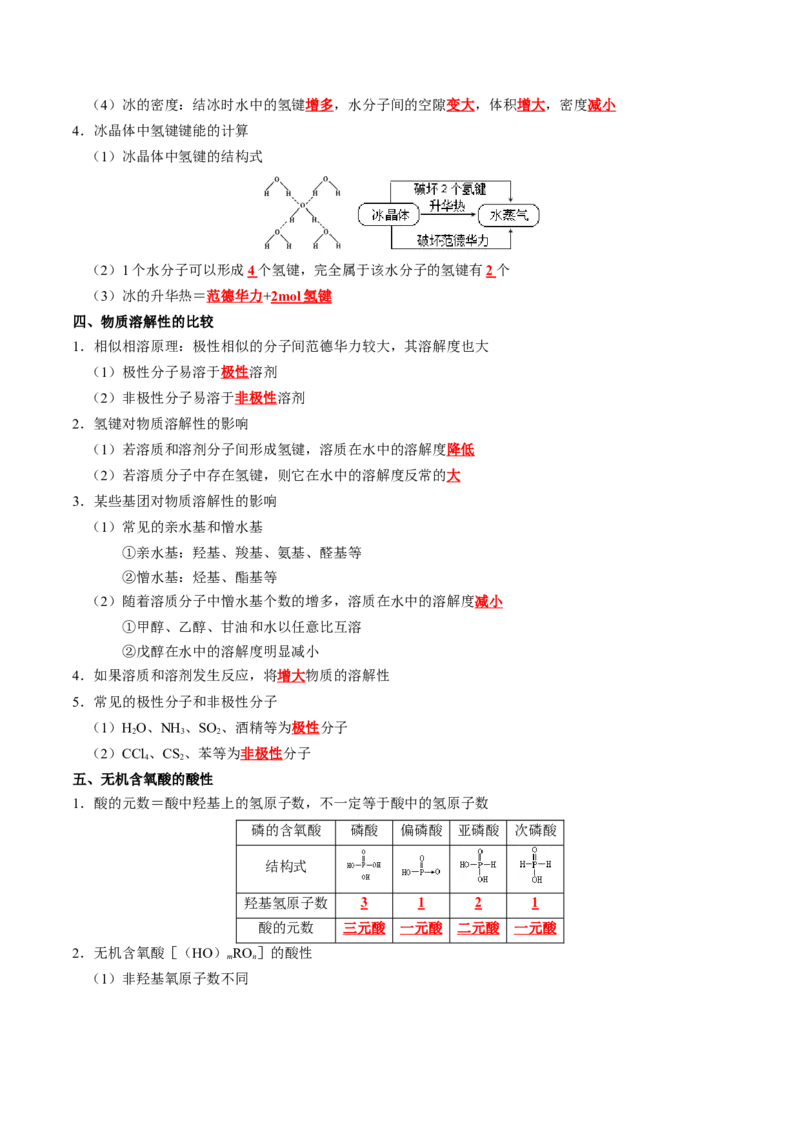
4.冰晶体中氢键键能的计算
(1)冰晶体中氢键的结构式
(2)1个水分子可以形成4 个氢键,完全属于该水分子的氢键有2 个
(3)冰的升华热=范德华力+ 2mol 氢键
四、物质溶解性的比较
1.相似相溶原理:极性相似的分子间范德华力较大,其溶解度也大
(1)极性分子易溶于极性溶剂
(2)非极性分子易溶于非极性溶剂
2.氢键对物质溶解性的影响
(1)若溶质和溶剂分子间形成氢键,溶质在水中的溶解度降低
(2)若溶质分子中存在氢键,则它在水中的溶解度反常的大
3.某些基团对物质溶解性的影响
(1)常见的亲水基和憎水基
①亲水基:羟基、羧基、氨基、醛基等
②憎水基:烃基、酯基等
(2)随着溶质分子中憎水基个数的增多,溶质在水中的溶解度减小
①甲醇、乙醇、甘油和水以任意比互溶
②戊醇在水中的溶解度明显减小
4.如果溶质和溶剂发生反应,将增大物质的溶解性
5.常见的极性分子和非极性分子
(1)HO、NH 、SO 、酒精等为极性分子
2 3 2
(2)CCl 、CS、苯等为非极性分子
4 2
五、无机含氧酸的酸性
1.酸的元数=酸中羟基上的氢原子数,不一定等于酸中的氢原子数
磷的含氧酸 磷酸 偏磷酸 亚磷酸 次磷酸
结构式
羟基氢原子数 3 1 2 1
酸的元数 三元酸 一元酸 二元酸 一元酸
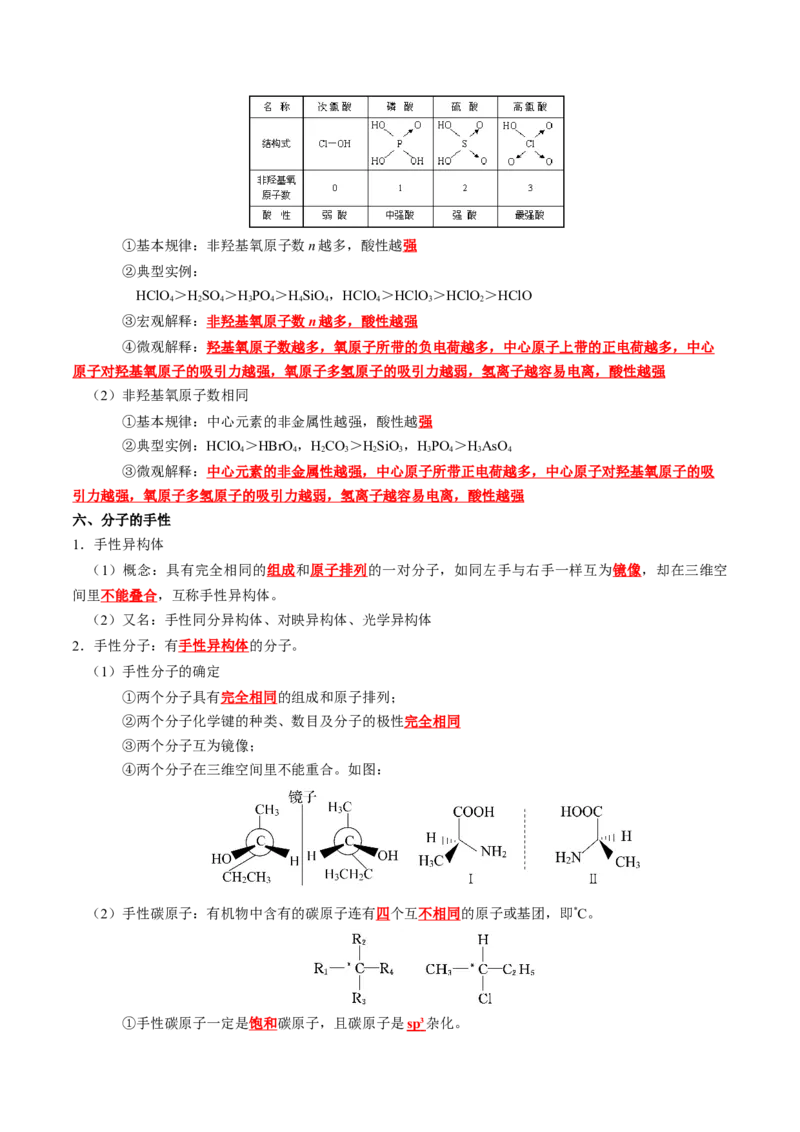
2.无机含氧酸[(HO) RO]的酸性
m n
(1)非羟基氧原子数不同①基本规律:非羟基氧原子数n越多,酸性越强
②典型实例:
HClO>HSO >HPO >HSiO,HClO>HClO>HClO>HClO
4 2 4 3 4 4 4 4 3 2
③宏观解释: 非羟基氧原子数 n 越多 , 酸性越强
④微观解释:羟基氧原子数越多,氧原子所带的负电荷越多,中心原子上带的正电荷越多,中心
原子对羟基氧原子的吸引力越强,氧原子多氢原子的吸引力越弱,氢离子越容易电离,酸性越强
(2)非羟基氧原子数相同
①基本规律:中心元素的非金属性越强,酸性越强
②典型实例:HClO>HBrO ,HCO>HSiO,HPO >HAsO
4 4 2 3 2 3 3 4 3 4
③微观解释:中心元素的非金属性越强,中心原子所带正电荷越多,中心原子对羟基氧原子的吸
引力越强,氧原子多氢原子的吸引力越弱,氢离子越容易电离,酸性越强
六、分子的手性
1.手性异构体
(1)概念:具有完全相同的组成和原子排列的一对分子,如同左手与右手一样互为镜像,却在三维空
间里不能叠合,互称手性异构体。
(2)又名:手性同分异构体、对映异构体、光学异构体
2.手性分子:有手性异构体的分子。
(1)手性分子的确定
①两个分子具有完全相同的组成和原子排列;
②两个分子化学键的种类、数目及分子的极性完全相同
③两个分子互为镜像;
④两个分子在三维空间里不能重合。如图:
(2)手性碳原子:有机物中含有的碳原子连有四个互不相同的原子或基团,即*C。
①手性碳原子一定是饱和碳原子,且碳原子是 sp 3 杂化。②不饱和碳原子(如碳碳双键、-C≡C-等中的碳原子)一定不是手性碳原子。
③有机物分子中如果有一个手性碳原子,则该有机物分子就是手性分子,具有手性异构体。
3.手性分子的应用
(1)医药领域
①现今使用的药物中手性药物超过50%
②对于手性药物,一个异构体可能有效,而另一个异构体可能是无效甚至是 有害 的
(2)合成领域
①手性催化剂:只催化或者主要催化一种手性分子的合成
②用手性催化剂生产药物,可以只得到或者主要得到一种手性分子,这种独特的合成方法称为手
性合成
七、超分子
1.概念:由两种或两种以上的分子通过分子间相互作用形成的分子聚集体。
2.应用
(1)分离C 和C
60 70
将C 和C 的混合物加入一种空腔大小适配C 的“杯酚”中,得到超分子“杯酚”C 和C ;加入
60 70 60 60 70
甲苯溶剂,甲苯将C 溶解,经过滤后分离出C ;再向不溶物中加入氯仿,氯仿溶解“杯酚”而将不溶解
70 70
的C 释放出来并沉淀。从而将C 和C 分离开来。
60 60 70
(2)冠醚识别碱金属离子
冠醚分子中有大小不同的空穴适配不同大小的碱金属离子,而形成冠醚-碱金属离子超分子。
3.重要特征:分子识别和自组装。
【典例01】 下列说法中不正确的是( )
A.所有含氢元素的化合物中都存在氢键,氢键是一种类似于共价键的化学键
B.离子键、氢键、范德华力本质上都是静电作用
C.只有电负性很强、半径很小的原子(如F、O、N)才能形成氢键
D.氢键是一种分子间作用力,氢键比范德华力强
【答案】A
【解析】氢键不是化学键,本质上还是一种分子间作用力,氢键要比化学键弱的多,一般只有电负性很强、
半径很小的原子才能形成氢键,所以A不正确。
【典例02】下列说法中正确的是( )
A.极性溶质一定易溶于极性溶剂,非极性溶质一定易溶于非极性溶剂
B.溴分子和水分子是极性分子,四氯化碳分子是非极性分子,所以溴难溶于水而易溶于四氯化碳
C.白磷分子是非极性分子,水分子是极性分子,而二硫化碳是非极性分子,所以白磷难溶于水而易
溶于二硫化碳
D.水分子是极性分子,二氧化碳可溶于水,因此二氧化碳是极性分子
【答案】A【解析】很多有机物分子都是极性分子,但因为极性很弱,所以大部分难溶于水,而有机物之间的溶解度
却很大,所以A项错误;溴分子是非极性分子,故B项错误;二氧化碳(O===C===O)是非极性分子,D项
错误。