文档内容
第02讲 物质的量浓度与溶液的配制(精练)
完卷时间:50分钟
一、选择题(每小题只有一个正确选项,共12*5分)
1.(2021·上海静安区·高三二模)将V L浓度为0.3mol/L的盐酸浓度扩大一倍,采取的措施合理的是
A.将溶液加热浓缩至原来体积的一半
B.通入标准状况下的HCl气体6.72L
C.加入3mol/L的盐酸0.2V L,再稀释至1.5V L
D.加入等体积0.9mol/L的盐酸,混合均匀
【答案】C
【解析】A.将溶液加热浓缩至原来体积的一半时,由于HCl的挥发,不能使其浓度扩大一倍,A不合理;
B.标准状况下6.72LHCl的物质的量为0.3mol,但向溶液中通入HCl气体时溶液的体积会发生变化,所以
浓度不能扩大一倍,B不合理;C.V L浓度为0.3mol/L的盐酸中有0.3VmolHCl,3mol/L的盐酸0.2V L含
HCl的物质的量为0.6Vmol,稀释至1.5V L,浓度为 =0.6mol/L,C合理;D.两种盐酸
混合后,溶液的体积不能直接加和,所以混合后溶液的物质的量浓度不是原来的2倍,D不合理;综上所
述答案为C。
2.(2020·宝鸡市渭滨中学高三月考)下列表述正确的是
A.22.4LHCl溶于水制得1L盐酸时,其浓度为1 mol•L-1
B.1L0.3mol•L-1的CuCl 溶液中含有Cu2+和Cl-的总物质的量为0.9mol
2
C.在KSO 和NaCl的中性混合水溶液中,如果c(Na+)=c(SO2-),则c(K+)=c(Cl-)
2 4 4
D.10℃时,100mLKCl饱和溶液蒸发掉5g水,冷却到10℃时,它仍为饱和溶液
【答案】D
【解析】A. 未说明温度和压强,故无法确定22.4LHCl的物质的量,无法计算浓度,A错误;B. 由于铜离
子在水溶液中会水解,故1L0.3mol•L-1的CuCl 溶液中含有Cu2+的物质的量小于0.3mol,Cu2+和Cl-的总物
2
质的量小于0.9mol,B错误;C. 根据电荷守恒,KSO 和NaCl的混合溶液中,
2 4
,由于溶液呈中性,则 ,所以
,若c(Na+)=c(SO2-),则 ,C错误;D.
4
10℃时,100mLKCl饱和溶液蒸发掉5g水,冷却到10℃时,有晶体析出,但溶液仍为饱和溶液,D正确;
故答案选D。3.已知单位体积的稀溶液中,非挥发性溶质的分子或离子数越多,该溶液的沸点就越高。则下列溶液沸点
最高的是
A.0.01mol/L的蔗糖溶液 B.0.01mol/L的MgCl 溶液
2
C.0.02mol/L的HS溶液 D.0.02mol/L的NaNO 溶液
2 3
【答案】D
【解析】1L蔗糖溶液中蔗糖分子的物质的量为1L×0.01mol/L=0.01mol,1LMgCl 溶液溶质的离子的总物质
2
的量为1L×0.01mol/L×3=0.03mol,HS是挥发性溶质,1L溶液中硫化氢分子的物质的量最多为
2
1L×0.02mol/L=0.02mol,1LNaNO 溶液中溶质的离子的总物质的量为1L×0.02mol/L×2=0.04mol,D中含
3
0.04 mol离子,离子数最多,沸点最高,故选D。
4.(2021·全国高三)36.5gHCl溶解在1L水中(水的密度近似为1 gmL-1),所得溶液的密度为ρ
gmL-1,质量分数为w,物质的量浓度为c gmL-1,N 表示阿伏加德罗常数,下列说法正确的是
A
A.所得溶液的物质的量浓度:c=1 gmL-1
B.所得溶液中含有N 个HCl分子
A
C.36.5 gHCl气体占有的体积为22.4L
D.所得溶液的质量分数: w=
【答案】D
【解析】A. 物质的量浓度单位是mol/L,不是gmL-1,故A错误;B. 氯化氢溶于水形成盐酸溶液是强电
解质,溶液中无氯化氢分子,故B错误;C. 36.5gHCl气体物质的量为1mol,标准状况下占有的体积为
22.4L,选项中温度压强不知,故C错误;D. 所得溶液的质量分数:ω= =
,故D正确;答案选D。
5.(2020·北京高三)阅读体检报告呈现的的部分内容,判断下列说法不正确的是
项目名称 检查结果 单位 参考范围
钾 4.1 mmol/L 3.5~5.5
钙 2.15 mmol/L 2.13~2.70
胱抑素C 0.78 mg/L 0.59~1.03
尿素 4.18 mmol/L 2.78~7.14甘油三酯 1.50 mmol/L 0.45~1.70
A.体检指标均以物质的量浓度表示
B.表中所示的检查项目均正常
C.尿素是蛋白质的代谢产物
D.甘油三酯的结构可表示为 (R、R、R 为烃基)
1 2 3
【答案】A
【解析】A.物质的量浓度单位为mol/L或mmol/L,胱抑素C 的单位为mg/L ,不是以物质的量浓度表示;
B.根据参考范围可知,表中所示的检查项目均在正常范围内;C.蛋白质的代谢产物为尿素等;D.甘油三酯
是羧酸与甘油形成的酯,结构可表示为 (R、R、R 为烃基);答案选A。
1 2 3
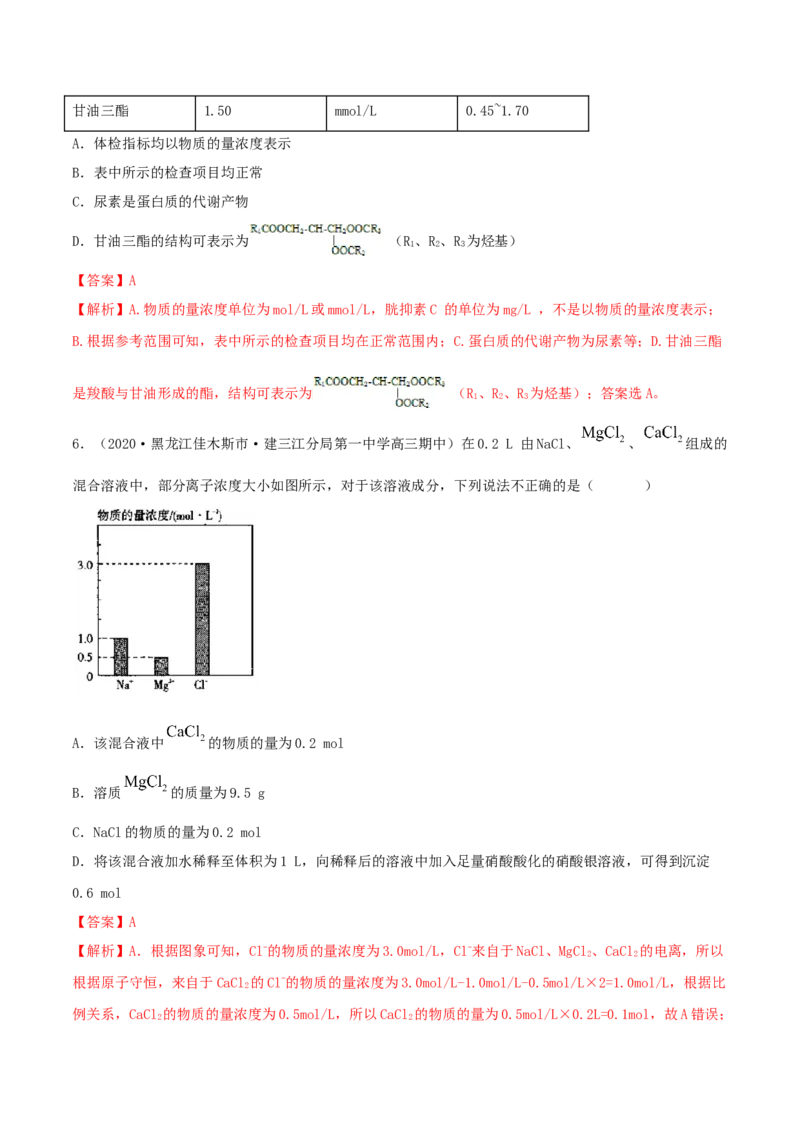
6.(2020·黑龙江佳木斯市·建三江分局第一中学高三期中)在0.2 L 由NaCl、 、 组成的
混合溶液中,部分离子浓度大小如图所示,对于该溶液成分,下列说法不正确的是( )
A.该混合液中 的物质的量为0.2 mol
B.溶质 的质量为9.5 g
C.NaCl的物质的量为0.2 mol
D.将该混合液加水稀释至体积为1 L,向稀释后的溶液中加入足量硝酸酸化的硝酸银溶液,可得到沉淀
0.6 mol
【答案】A
【解析】A.根据图象可知,Cl-的物质的量浓度为3.0mol/L,Cl-来自于NaCl、MgCl、CaCl 的电离,所以
2 2
根据原子守恒,来自于CaCl 的Cl-的物质的量浓度为3.0mol/L-1.0mol/L-0.5mol/L×2=1.0mol/L,根据比
2
例关系,CaCl 的物质的量浓度为0.5mol/L,所以CaCl 的物质的量为0.5mol/L×0.2L=0.1mol,故A错误;
2 2B.根据图象可知,Mg2+的物质的量浓度为0.5mol/L,Mg2+来自于MgCl 的电离,所以MgCl 的物质的量浓度
2 2
为0.5mol/L,所以MgCl 的物质的量为0.5mol/L×0.2L=0.1mol,MgCl 的质量为95g/mol×0.1mol=9.5g,
2 2
故B正确;C.根据图象可知,Na+的物质的量浓度为1.0mol/L,Na+来自于NaCl的电离,NaCl的物质的量
浓度为1.0mol/L,所以NaCl的物质的量为1.0mol/L×0.2L=0.2mol,故C正确;D.根据图象可知,Cl-的
物质的量浓度为3.0mol/L,Cl-的物质的量为3.0mol/L×0.2L=0.6mol,溶液稀释前后,溶质的物质的量不
变,根据Ag++Cl-=AgCl↓可知,最终得到沉淀的物质的量为0.6mol,故D正确;故选A。
7.(2020·陕西省黄陵县中学高三期中)下列溶液中溶质的物质的量浓度为1 mol·L-1的是 ( )
A.将58.5 g NaCl溶解于1 L水中配成的溶液
B.将40g NaOH溶于水并配成1 L溶液
C.将0.5 mol·L-1的NaNO 溶液100 mL加热蒸发掉50 g水的溶液
3
D.含K+为2 mol的KSO 溶液
2 4
【答案】B
【解析】A. 选项中“1L水”是指溶剂的体积,溶液体积不一定为1L,故A错误;B. 40g NaOH为1mol,
溶液体积为1L,所得溶液的物质的量浓度为1mol/L,故B正确;C. NaNO 溶液的密度不是1g/mL,蒸发掉
3
50g水所得的溶液不是50mL,故C错误;D. 含K+为2mol的KSO 溶液体积不知道,无法计算浓度,故D错
2 4
误;答案选B。
8.(2020·全国高三)下列关于物质的量浓度表述中正确的是( )
A.0.3mol·L-1NaSO 溶液中含有Na+和SO 总物质的量为0.9mol
2 4
B.当1L水吸收22.4L氨气时所得氨水的浓度不是1mol·L-1,只有当22.4L氨气溶于水制得1L氨水时,其
浓度才是1mol·L-1
C.在KSO 和NaCl的中性混合水溶液中,如果Na+和SO 的物质的量浓度相等,那么K+和Cl-的物质的量
2 4
浓度一定相同
D.10℃时0.35mol·L-1的KCl饱和溶液100mL,蒸发掉5g水,冷却到10℃时其体积小于100mL,物质的量
浓度仍为0.35mol·L-1
【答案】D
【解析】A.已知NaSO 溶液的浓度,而未知体积,则无法求出NaSO 的物质的量,也就无法求出Na+和
2 4 2 4
的总物质的量,故A不正确;B. 只告诉NH 的体积,而没有告诉该体积是否是标准状况下的体积,
3
所以无法确定22.4LNH 的物质的量,故B不正确;C. 在KSO 和NaCl的中性混合水溶液中,根据电荷守恒,
3 2 4如果Na+和SO 的物质的量相等,则K+的物质的量浓度是Cl-的物质的量浓度的2倍,故C不正确;D.
蒸发溶剂后恢复到10℃,该溶液仍为饱和溶液,同一温度下,同一种物质的饱和溶液浓度应是相同的,故
D正确。答案选D。
9.(2020·广东广州市·华南师大附中高三专题练习)与50mL0.1mol/LNaCO 溶液中Na+的物质的量浓度
2 3
相同的溶液是( )
A.25mL0.2mol/L的NaCl溶液 B.100mL0.1mol/L的NaCl溶液
C.25mL0.2mol/L的NaSO 溶液 D.10mL0.5mol/L的NaCO 溶液
2 4 2 3
【答案】A
【解析】50mL 0.1mol/L的NaCO 溶液中Na+的物质的量浓度为0.1mol/L×2=0.2mol/L;A.25mL0.2mol/L
2 3
的NaCl溶液中Na+的物质的量浓度为0.2mol/L×1=0.2mol/L,故A符合题意;B.100mL0.1mol/L的NaCl
溶液中Na+的物质的量浓度为0.1mol/L×1=0.1mol/L,故B不符合题意;C.25mL0.2mol/L的NaSO 溶液中
2 4
Na+的物质的量浓度为0.2mol/L×2=0.4mol/L,故C不符合题意;D.10mL0.5mol/L的NaCO 溶液中Na+的
2 3
物质的量浓度为0.5mol/L×2=1mol/L,故D不符合题意;答案选A。
10.(2020·全国高三1)等体积NaCl,MgCl,AlCl 三种溶液分别于等体积等物质的量浓度的AgNO 溶液
2 3 3
恰好完全反应,则NaCl,MgCl,AlCl 三种溶液的物质的量浓度之比为( )
2 3
A.1:2:3 B.3:2:1 C.6:3:2 D.1:1:1
【答案】C
【解析】设NaC1、MgCl、A1Cl 的物质的量分别为x、y、z,分别加入等量的AgNO 溶液,恰好都完全反应,
2 3 3
说明三种溶液中Cl-的物质的量相等,x=y×2=z×3,解得x:y:z=6:3:2,因溶液的体积相同,则物质
的量之比等于浓度之比,所以浓度之比为6:3:2,故答案为C。
11.(2020·黑龙江哈尔滨市·哈九中高三开学考试)下列实验操作中正确的是( )
A.配制一定物质的量浓度的 溶液时,用量筒量取一定体积的浓硫酸倒入烧杯后,再用蒸馏水洗涤
量筒2~3次,并将洗涤液一并倒入烧杯中稀释
B. 溶液的物质的量浓度为 ,用水稀释到物质的量浓度为 ,需要水
C.配制一定物质的量浓度的氯化钾溶液:准确称取一定质量的氯化钾固体,放入 的容量瓶中,加入 溶解,振荡摇匀
D.将 溶解在 水中,配制溶质质量分数为10%的 溶液
【答案】D
【解析】A. 浓硫酸稀释放热,应将浓硫酸倒入水中,而不能将水倒入浓硫酸中,故A错误;B. 稀释后溶
液体积为浓硫酸体积2倍,由于浓硫酸的密度大于稀硫酸,故稀释后溶液质量小于200g,则加入水的质量
小于100g,故B错误;C. 容量瓶为精密仪器,不能在容量瓶中进行溶解操作,故C错误;D. 所得溶液中
溶质的质量分数为 ×100%=10%,故D正确;故答案为D。
12.(2021·浙江高三)体积为V(mL)、密度为ρ (g·mL-1)的溶液中,含有摩尔质量为M(g·mol-1)的溶
质m(g),其物质的量浓度为c(mol·L-1),溶质的质量分数为a%。下列有关关系式不正确的是
A.m=V×ρ×a% B.c=1000×ρ·a×M mol·L-1
C.c= ×L-1 D.a%= ×100%
【答案】B
【解析】A.溶液的质量为ρg·mL-1×VmL=ρ×Vg,溶液中溶质的质量为m=ρ×V×a%g,故A正确;B.溶
液中溶质的物质的量为n= = mol,体积为V(mL),则其物质的量浓度为c=
= mol·L-1,故B错误;C.溶液中溶质的物质的量为n= mol,溶液的体
积为0.001VL,则该溶液的浓度为c= = = mol·L-1,故C正确;D.根据c=
可得,溶质质量分数为a%= ×100%,故D正确;答案为B。
二、主观题(共3小题,共40分)13.(10分)在花瓶中加入“鲜花保鲜剂”可延长鲜花的寿命。下表是1 L“鲜花保鲜剂”的成分,阅读后
并回答下列问题:
成分 质量/g 摩尔质量/(g·mol-1)
蔗糖 50.00 342
硫酸钾 0.50 174
阿司匹林 0.35 180
高锰酸钾 0.50 158
硝酸银 0.04 170
(1)“鲜花保鲜剂”中物质的量浓度最大的成分是__________(填写名称)。
(2)“鲜花保鲜剂”中K+的物质的量浓度为(阿司匹林中不含K+)__________________(只要求写表达式,
不需计算)mol·L-1。
(3)下图所示的仪器中,在配制“鲜花保鲜剂”溶液时肯定不需要的是________(填字母),还缺少的玻
璃仪器有__________________(填仪器名称)。
(4)配制过程中,下列操作对配制结果没有影响的是__________(填字母)。
A.容量瓶在使用前未干燥,里面有少量蒸馏水
B.定容时仰视液面
C.容量瓶在使用前刚刚配制完一定物质的量浓度的NaCl溶液而未洗净
D.定容摇匀后发现液面低于容量瓶的刻度线,但未做任何处理
(5)欲确定“鲜花保鲜剂”中硝酸银的浓度,可加入的试剂中要含有__________。(填化学符号)
【答案】(除标注外,每空2分)(1)蔗糖(1分)(2) (或 或 或 )a
(3)c玻璃棒、烧杯(4)AD(5)Cl— (或Br—)(1分)
【解析】(1)同一溶液,体积相等,则物质的量越大溶液浓度越大,蔗糖的物质的量为:=0.146mol;硫酸钾的物质的量为: =0.00287mol;阿司匹林的物质的量为: =0.00194mol;高
锰酸钾的物质的量: =0.0032mol;硝酸银的物质的量: =0.00024mol;所以蔗糖的物质的量最
大,溶液中蔗糖的物质的量浓度最多;故答案为:蔗糖;
(2)溶液中钾离子的物质的量为则依据c= ,V=1L,溶液中钾离子的物质的量浓度为= =
(2× + )mol/L;故答案为:2× + ;
(3)配制一定物质的浓度溶液一般步骤:计算、称量、溶解、移液、洗涤、定容等,用到的仪器:托盘
天平、烧杯、玻璃棒、药匙、1000 mL容量瓶、胶头滴管;用不到烧瓶和分液漏斗,还缺少的仪器:玻璃
棒、烧杯,故答案为:ac;玻璃棒、烧杯;
(4)A.容量瓶在使用前未干燥,里面有少量蒸馏水,对溶质的物质的量和溶液体积都不产生影响,溶液
浓度不变,故A选;B.定容时仰视液面,导致溶液体积偏大,溶液浓度偏小,故B不选;C.容量瓶在使
用前刚刚配制完一定物质的量浓度的NaCl溶液而未洗净,容量瓶中沾有氯化钠,氯化钠能够消耗银离子,
导致溶液中银离子浓度偏小,故C不选;D.定容摇匀后发现液面低于容量瓶的刻度线,但未做任何处理,
属于正确操作,溶液浓度准确,故D选;故选AD;
(5)银离子能够与氯离子反应生成氯化银白色沉淀,向待测液中加入少量氯化钠,若产生白色沉淀即可
证明溶液中含有银离子;故答案为:Cl-。
14.(15分)在标准状况下,将224 L HCl气体溶于635 mL水中,所得盐酸的密度为1.18 g·cm-3。试计算:
(1)所得盐酸的质量分数和物质的量浓度分别是____________________、
____________________。
(2)取这种盐酸100 mL,稀释至1.18 L,所得稀盐酸的物质的量浓度是________。
(3)在40.0 mL 0.065 mol·L-1NaCO 溶液中,逐滴加入上述稀释后的稀盐酸,边加边振荡。若使反应不产生
2 3
CO 气体,加入稀盐酸的体积的最多不超过_______mL。
2
(4)将不纯的NaOH样品1 g(样品含少量NaCO 和水),放入50 mL 2 mol·L-1的盐酸中,充分反应后,溶液
2 3
呈酸性,中和多余的酸又用去40 mL 1 mol·L-1的NaOH溶液。蒸发中和后的溶液,最终得到________g固
体。
【答案】(每空3分)(1)36.5% 11.8 mol·L-1 (2)1 mol·L-1 (3)2.6 (4)5.85
【解析】(1)n(HCl)= =10 mol,
m(HCl)=10 mol×36.5 g·mol-1=365 g,盐酸的质量分数w= ×100%=36.5%,
c(HCl)= =
=11.8 mol·L-1。
(2)由c(浓)·V(浓)=c(稀)·V(稀)可知,
c(稀)=11.8 mol·L-1× =1 mol·L-1。
(3)n(Na CO)=0.040 L×0.065 mol·L-1=0.002 6 mol,设加入稀盐酸的体积最多不超过x mL,则n(HCl)=1
2 3
mol·L-1×0.001x L=0.001x mol,根据反应NaCO+HCl==NaHCO +NaCl得0.002 6=0.001x,x=2.6。
2 3 3
(4)经过反应,蒸发中和后的溶液,最后所得固体为NaCl,根据氯原子守恒:n(NaCl)=n(HCl)=0.050 L×2
mol·L-1=0.1 mol,m(NaCl)=0.1 mol×58.5 g·mol-1=5.85 g。
15.(15分)已知某“84消毒液”瓶体部分标签如图所示,该“84消毒液”通常在稀释体积为原来的100
倍后使用。请填写下列空白。
(1)该“84消毒液”的物质的量浓度约为 mol·L-1。
84消毒液
有效成分 NaClO
规格 1 000 mL
质量分数 25%
密度 1.19 g·cm-3
(2)某同学取100 mL该“84消毒液”,稀释后用于消毒,稀释后的溶液中c(Na+)= mol·L-1。
(3)该同学参阅该“84消毒液”的配方,欲用NaClO固体配制480 mL含NaClO质量分数为25%的消毒液。
下列说法正确的是 (填字母)。
A.如图所示的仪器中,有三种是不需要的,还需要一种玻璃仪器
B.容量瓶用蒸馏水洗净后,应烘干后才能用于溶液配制C.配制过程中,未用蒸馏水洗涤烧杯和玻璃棒可能导致结果偏低
D.需要称量NaClO固体的质量为143.0 g
(4)“84消毒液”与稀硫酸混合使用可增强消毒能力,某消毒小组人员用98%(密度为1.84 g·cm-3)的浓硫酸配
制2 L 2.3 mol·L-1的稀硫酸用于增强“84消毒液”的消毒能力。
①所配制的稀硫酸中,H+的物质的量浓度为 mol·L-1。
②需用浓硫酸的体积为 mL。
【答案】(每空3分)(1)4.0 (2)0.04 (3)C (4)①4.6 ②250
【解析】(1)由关系式c= 可得,c(NaClO)= mol·L-1≈4.0 mol·L-1。
(2)稀释前后溶液中NaClO的物质的量不变,则有100 mL×10-3L·mL-1×4.0 mol·L-1=100 mL×100×10-
3L·mL-1×c(NaClO),解得稀释后c(NaClO)=0.04 mol·L-1,c(Na+)=c(NaClO)=0.04 mol·L-1。
(3)选项A,需用托盘天平称量NaClO固体,需用烧杯来溶解NaClO,需用玻璃棒进行搅拌和引流,需用容
量瓶和胶头滴管来定容,图示中的A、B不需要,但还需要玻璃棒和胶头滴管;选项B,配制过程中需要
加水,所以经洗涤干净的容量瓶不必烘干后再使用;选项C,未洗涤烧杯和玻璃棒将导致配制的溶液中溶
质的物质的量减小,结果偏低;选项D,应选取500 mL的容量瓶进行配制,然后取出480 mL即可,所以
需要NaClO的质量为0.5 L×4.0 mol·L-1×74.5 g· mol-1=149.0 g。
(4)①根据HSO 的组成可知,溶液中c(H+)=2c(H SO )=4.6 mol·L-1。②2 L 2.3 mol·L-1的稀硫酸中溶质的物
2 4 2 4
质的量为2 L×2.3 mol·L-1=4.6 mol,设需要98%(密度为1.84 g·cm-3)的浓硫酸的体积为V,则有
=4.6 mol,解得V=250 mL。