文档内容
第 02 讲 离子反应
1.下列属于弱电解质的是
A.CaCO B.SO C.NH ·H O D.Ba(OH)
3 2 3 2 2
【答案】C
【解析】CaCO 属于盐,属于强电解质,故A不符合题意;SO 是非金属性氧化物,属于非电解质,故B
3 2
不符合题意;NH ·H O属于弱碱,属于弱电解质,故C符合题意;Ba(OH) 属于强碱,属于强电解质,故
3 2 2
D不符合题意。综上所述,答案为C。
2.下列方程式不正确的是
A.用 溶液清洗银镜:
B.氢氧化亚铁露置在空气中变为红褐色:
C.向苯酚钠溶液中通入 溶液变浑浊:
D.向 溶液中滴加少量硫酸,溶液橙色加深:
【答案】C
【解析】铁离子具有氧化性,可用 溶液清洗银镜: ,A正确;氢氧化亚铁
露置在空气中被氧化为氢氧化铁而变为红褐色: ,B正确;向苯酚钠溶液
中通入 溶液变浑浊,生成的是苯酚和碳酸氢钠,得不到碳酸钠,C错误;向 溶液中滴加少量硫
酸,溶液橙色加深,说明平衡: 逆向移动,D正确;答案选C。
3.粗盐中除 外,还含有 、 、 以及泥沙等杂质。粗盐提纯的操作流程如下:下列说法正确的是
A.为确认 是否完全沉淀,可向上层清液中继续滴加 溶液
B.试剂 、 、 分别为过量的 、 和
C.滤液中含有的阴离子有两种: 、
D.过滤和调pH的顺序可以颠倒
【答案】A
【分析】粗盐中除NaCl外,还含有Mg2+、Ca2+、 以及泥沙等杂质,粗盐溶解后,分别加入NaOH、
BaCl 、NaCO,然后过滤除去沉淀,滤液中除含有NaCl外,还含有NaOH、NaCO 等,加入盐酸调节溶
2 2 3 2 3
液的pH稍小于7,然后蒸发结晶,便可获得纯净的氯化钠晶体。
【解析】A.为确认 是否完全沉淀,可向上层清液中继续滴加BaCl 溶液,若无白色沉淀生成,则表
2
明溶液中不含有 ,从而表明 完全沉淀,A正确;
B.除杂质时,不能引入新的杂质,所以试剂X应为NaOH,若使用KOH,则会引入K+,B不正确;
C.由分析可知,滤液中含有过量的NaOH、NaCO 等,则阴离子有Cl-、OH-、 ,C不正确;
2 3
D.沉淀中含有氢氧化镁、碳酸钙,加入盐酸会导致沉淀溶解,故过滤和调pH的顺序不可以颠倒,D不正
确;故选A。
4.某无色溶液含有 、 、 、 、 中的2种离子,取该溶液进行了下列实验:
(1)取少量溶液,滴加 溶液,有沉淀产生,加足量硝酸,沉淀全部溶解;
(2)取实验(1)静置后的溶液,滴加 溶液,无现象。
根据上述实验,可以确定该无色溶液中存在的离子是
A. 和 B. 和 C. 和 D. 和
【答案】D
【解析】溶液无色,说明没有 ,向溶液中滴加 溶液,有沉淀,加足量硝酸,沉淀全部溶解,说明有 ,没有 ,取(1)后的溶液,滴加 溶液,无现象,说明没有 ,根据电荷守恒可知
溶液中一定有阳离子 ,因此溶液中一定存在 和 ,故D符合题意。
综上所述,答案为D。
5.某溶液中可能含有H+、NH 、Mg2+、Fe3+、Al3+、 、 等离子。当向该溶液中加入一定物质的
量浓度的NaOH溶液时,发现生成沉淀的物质的量随加入NaOH溶液的体积变化如图所示,下列说法正确
的是
A.d点溶液中含有的溶质只有NaSO 和
2 4
B.原溶液中含有的Fe3+和Al3+的物质的量之比为1:1
C.ab段发生的离子反应为:Al3++3OH-=Al(OH) ↓,Mg2++2OH-=Mg(OH) ↓
3 2
D.原溶液中含有的阳离子必定有H+、 、Al3+,且Mg2+和Fe3+至少存在一种
【答案】D
【分析】根据图中信息得到oa是氢离子或碳酸氢根和氢氧根反应,cd段是氢氧化铝和氢氧根反应,说明
没有碳酸氢根,一定含有氢离子,再根据电荷守恒,则一定含有硫酸根,bc段是铵根和氢氧根反应,ab段
一定有铝离子和氢氧根反应,可能至少有镁离子或铁离子中一种离子与氢氧根反应。
【解析】根据前面分析溶液中硫酸和氢氧化钠反应生成硫酸根,bc段生成一水合氨,d点氢氧化铝刚好变
为偏铝酸根,因此d点溶液中含有的溶质有NaSO 、 和NH ∙H O,故A错误;原溶液中无法确定
2 4 3 2
是否含有的Fe3+,故B错误;原溶液中无法确定是否含有的Mg2+,故C错误;根据前面分析原溶液中含有
的阳离子必定有H+、 、Al3+,且Mg2+和Fe3+至少存在一种,故D正确。综上所述,答案为D。
6.现有下列实验探究摩尔盐 的化学性质。
装置 实验 试剂a 现象① 紫色石蕊溶液 溶液变红色
② 溶液 产生白色沉淀
③ 稀硝酸溶液 溶液变黄色
④ 浓 溶液 产生具有刺激性气味的气体
下列离子方程式不能准确解释相应实验现象的是
A.①中溶液变红: 、
B.②中产生白色沉淀:
C.③中溶液变黄:
D.④中产生有刺激性气体:
【答案】C
【解析】铵根离子、亚铁离子水解使得溶液显酸性,酸性溶液使紫色石蕊试液变红色,能准确解释相应实
验现象,A不符合题意;硫酸根离子和钡离子生成硫酸钡白色沉淀,能准确解释相应实验现象,B不符合
题意;亚铁离子和硝酸根离子生成铁离子和一氧化氮气体, ,不能准
确解释相应实验现象,C符合题意;铵根离子和氢氧根离子生成刺激性气体氨气,能准确解释相应实验现
象,D不符合题意;故选C。
7.某学习小组为探究氯化铜与亚硫酸钠的反应,设计了如下实验:
已知 。
下列分析中,错误的是
A.2mL0.2 溶液中含 数目小于 ( 为阿伏加德罗常数的值)
B.由实验可知,生成橙黄色沉淀的速率较快,而生成白色沉淀的反应趋势更大C.已知橙黄色沉淀中只含有 、 、 ,可利用稀硫酸检验其中的 ,若溶液变蓝,则说明含
有
D.本实验中, 溶液和 溶液的总反应离子方程式为:
【答案】C
【解析】 会发生水解,所以2mL0.2 溶液中含 数目小于 ,故A正确;先
生成橙黄色沉淀,说明生成橙黄色沉淀的速率较快,最终得到的是白色沉淀,说明白色沉淀物更稳定,而
生成白色沉淀的反应趋势更大,故B正确;由于橙黄色沉淀中还含有 ,溶于稀硫酸,溶液也会变蓝,
故不能依据溶液变蓝的现象来检验其中的 ,故C错误;根据信息可知 溶液和 溶液发生最
终得到了白色沉淀 ,可知该过程中 做氧化剂, 做还原剂被氧化,总反应离子方程式为:
,故D正确;故选C。
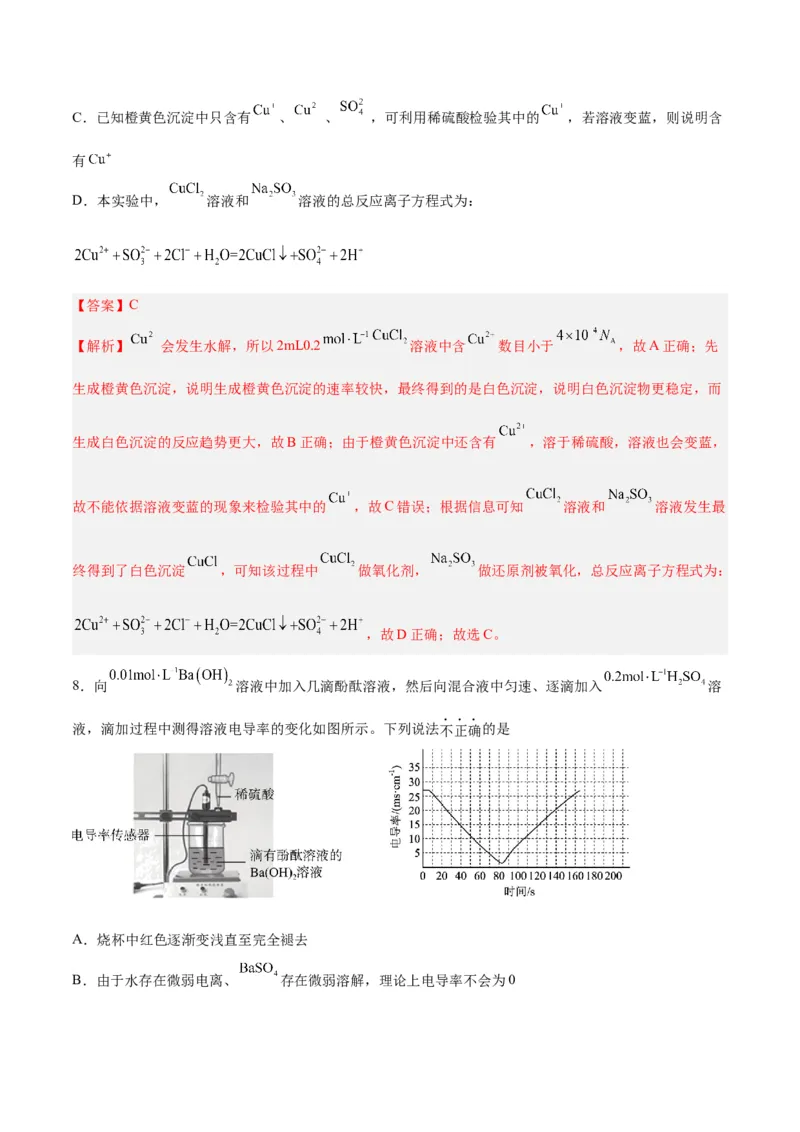
8.向 溶液中加入几滴酚酞溶液,然后向混合液中匀速、逐滴加入 溶
液,滴加过程中测得溶液电导率的变化如图所示。下列说法不正确的是
A.烧杯中红色逐渐变浅直至完全褪去
B.由于水存在微弱电离、 存在微弱溶解,理论上电导率不会为0C.电导率减小的过程中,发生反应:
D.若用同浓度的 溶液代替稀硫酸重复上述实验,电导率变化与原实验相同
【答案】D
【解析】A. 浓度减小直至反应完全,烧杯中红色逐渐变浅直至完全褪去,A正确;
B.由于水存在微弱电离、 存在微弱溶解,溶液中存在少量离子,理论上电导率不会为0,B正确;
C.电导率减小的过程中,离子浓度减小,发生反应: ,C正
确;
D.若用同浓度的 溶液代替稀硫酸重复上述实验,反应生成硫酸钡沉淀,溶液中存在钠离子和氢氧
根,电导率不会减少到几乎为0,电导率变化与原实验不相同,D错误;故选D。
9.常温下,下列各组离子在指定溶液中可能大量共存的是
A. 的 溶液中:
B.滴加几滴 溶液显红色的溶液中:
C.加入铝粉能生成 的溶液:加入
D. 的溶液中:
【答案】C
【解析】1.0mol/L的KNO 溶液中含有的 和H+、Fe2+三者之间因发生氧化还原反应而不能大量共存,A
3
不合题意; 滴加几滴 溶液显红色的溶液中含有的Fe3+和I-因发生氧化还原反应而不能大量共存,B
不合题意; 加入铝粉能生成H 的溶液可能是强酸性溶液,则 能够大量共存,也可能
2
是强碱性溶液,则不能含有大量的H+,C符合题意; 的溶液中含有大量的OH-,则OH-与Mg2+、OH-与 不能大量共存,D不合题意;故答案为C。
10.下列离子方程式正确的是
A.利用覆铜板制作电路板的原理: 2FeCl + Cu = Cu2+ + 2Fe2+ + 6Cl-
3
B.泡沫灭火器灭火原理: 2A13+ + 3 + 3H O = 2Al(OH) ↓ + 3CO ↑
2 3 2
C.向硫化钠溶液中通入过量SO : 2S2- + 5SO + 2H O=3S↓+ 4
2 2 2
D.纯碱溶液吸收Br : + Br= + Br-+ CO↑
2 2 2
【答案】C
【解析】利用覆铜板制作电路板,氯化铁和铜反应生成氯化亚铁和氯化铜,反应的离子方程式是2Fe3++ Cu
= Cu2+ + 2Fe2+,A错误;泡沫灭火器灭火原理是硫酸铝和碳酸氢钠溶液混合发生双水解反应生成氢氧化铝
沉淀、氯酸钠、二氧化碳,反应的离子方程式为 A13+ + 3 = Al(OH) ↓ + 3CO ↑,故B错误;向硫化
3 2
钠溶液中通入过量SO 生成亚硫酸氢钠、S沉淀,反应的离子方程式是2S2- + 5SO + 2H O=3S↓+ 4 ,
2 2 2
故C正确;纯碱溶液吸收Br 生成溴酸钠、溴化钠、二氧化碳,反应的离子方程式为3 +3Br =
2 2
+ 5Br-+ 3CO↑,故D错误;选C。
2
11.下列反应的离子方程式正确的是
A.向NaSO 溶液中滴加稀HNO 溶液: +2H+=SO↑+ H O
2 3 3 2 2
B.用过量氨水吸收废气中的SO :NH ·H O+SO = +
2 3 2 2
C.电解MgCl 水溶液的离子方程式:2Cl- +2H O H↑+Cl↑+ 2OH-
2 2 2 2
D.酸性KCr O 溶液遇NaNO 变成绿色: + 3 + 8H+= 3 + 2Cr3+ +4H O
2 2 7 2 2
【答案】D
【解析】向稀HNO 中滴加NaSO 溶液的离子反应为3 +2NO +2H+=3SO +2NO↑+HO,故A错误;
3 2 3 2用过量氨水吸收工业尾气中的SO ,离子方程式:2NH •H O+SO ═2NH + +H O,故B错误;电解
2 3 2 2 2
MgCl 水溶液生成氯气和氢氧化镁沉淀,离子方程式为:2Cl- +Mg2++2H O H↑+Cl↑+ Mg(OH) ,故
2 2 2 2 2
C错误;
酸性KCr O 溶液遇NaNO 变成绿色,说明 被 还原为Cr3+,离子方程式为: + 3 +
2 2 7 2
8H+= 3 + 2Cr3+ +4H O,故D正确;故选D。
2
12.通过实验、观察、类比、推理等方法得出正确结论是化学学习的方法之一,下列实验操作、现象和推
理或结论正确的是
选
实验操作及现象 推理或结论
项
NaO 与水反应生成氢氧
A 向装NaO 固体的试管中加水并滴加酚酞,只变红 2 2
2 2 化钠
向某溶液中加入足量盐酸酸化的BaCl 溶液,振荡,观察溶液中有白色
B 2 该溶液中一定含有SO
沉淀生成
C 将潮湿的氯气通过盛有干燥红纸条的集气瓶,褪色 氯气具有漂白性
D 向某溶液中滴加新制的氯水,再滴加KSCN溶液,溶液变红 原溶液中不一定有Fe2+
【答案】D
【解析】A.向装NaO 固体的试管中加水并滴加酚酞,先变红后褪色,NaO 与水反应生成氢氧化钠,还
2 2 2 2
有强氧化性,故A错误;
B.向某溶液中加入足量盐酸酸化的BaCl 溶液,振荡,观察溶液中有白色沉淀生成,溶液中存在硫酸根或
2
者银离子,故B错误;
C.将潮湿的氯气通过盛有干燥红纸条的集气瓶,褪色,是氯气和水反应生成的次氯酸有漂白性,故C错
误;
D.向某溶液中滴加新制的氯水,再滴加KSCN溶液,溶液变红,原溶液中不一定有Fe2+也可能含有铁离
子,故D正确;故选D。
13.下列是对某气体或溶液中离子进行检测的方法和结论,其中正确的是
A.将某气体通入品红溶液,若品红溶液褪色,则气体中一定含有SO
2B.取样,先加入盐酸酸化,无现象,再加入 BaCl 溶液,若产生白色沉淀,则溶液中含
2
C.取样,加入氯水,再加入KSCN溶液,若出现红色,则溶液中含有Fe2+
D.取样,加入适量盐酸酸化,再加入 AgNO 溶液,若产生白色沉淀,则含 Cl-
3
【答案】B
【解析】A.能使品红溶液褪色的气体有氯气、SO 等,选项A错误;
2
B.该选项考察硫酸根的检验方法,操作正确,选项B正确;
C.检验Fe2+,应先加KSCN溶液,无明显现象,再加入氯水,若溶液变红,则含Fe2+,选项C错误;
D.检验Cl-,不能引入Cl-,故不能用稀盐酸酸化,选项D错误;答案选B。
14.根据下列实验操作和现象能得到相应结论的是
选项 实验操作和现象 相应结论
A 用洁净铂丝蘸取少量溶液在酒精灯火焰上灼烧,火焰呈黄色 该溶液含 ,不含
B 向某溶液中加入盐酸酸化的硝酸银溶液产生白色沉淀 该溶液中一定含有
向某溶液中加入稀盐酸,产生能使澄清石灰水变浑浊的无色气
C 该溶液中不一定含有
体
D 将绿豆大小的钠块投入水中,钠熔为小球,浮于水面 钠的密度为
【答案】C
【解析】A.焰色反应为黄色,则溶液中一定含Na+,因为黄光会遮盖紫光,透过蓝色钴玻璃,滤去黄光,
看是否能观察到紫色,才能判断是否含K+,A错误;
B.向某无色溶液中,先加入适量稀硝酸酸化,无沉淀生成,再加入硝酸银溶液,产生白色沉淀,该溶液
中一定含有 ,B错误;
C.溶液中含有碳酸氢根离子,也会产生相似的现象,C正确;
D.将绿豆大小的钠块投入水中,钠熔为小球,浮于水面,能说明钠的密度小于水的,但不能说明为
0.97g/cm3,D错误;故选C。
15.下列除杂试剂选用不合理的是
选项 物质 杂质 除杂试剂
A Cl HCl 饱和NaCl溶液
2
B FeSO 溶液 Fe (SO ) 足量铁粉
4 2 4 3C Mg(OH) Al(OH) 足量NaOH溶液
2 3
D CO SO 饱和NaCO 溶液
2 2 2 3
【答案】D
【解析】Cl 在饱和食盐水中的溶解度小,用饱和NaCl溶液除氯气中的氯化氢,故A正确;Fe (SO ) 和铁
2 2 4 3
反应生成FeSO ,用铁粉除溶Fe (SO ) 液中的FeSO ,故B正确;Al(OH) 和足量NaOH溶液反应生成偏铝
4 2 4 3 4 3
酸钠溶液,用氢氧化钠溶液除Mg(OH) 中的Al(OH) ,故C正确;SO 、CO 都能与NaCO 溶液反应,不
2 3 2 2 2 3
能用饱和NaCO 溶液除CO 中的SO ,用饱和NaHCO 溶液除CO 中的SO ,故D错误;选D。
2 3 2 2 3 2 2
16.某同学向一份溶液样品(可能含有: 、 、 、 、 、 中的一种或几种)中加入一定
量的 溶液,产生白色沉淀,继续滴加稀盐酸,发现沉淀部分溶解,并产生能使澄清石灰水变浑浊的
气体,则此溶液样品中一定含有
A. B. C. D. 和
【答案】A
【解析】原溶液中加入一定量的 溶液,产生白色沉淀,继续滴加稀盐酸,发现沉淀部分溶解,并产
生能使澄清石灰水变浑浊的气体,说明沉淀中一定含硫酸钡,还形成一种可溶于盐酸的沉淀,可能为亚硫
酸钡或碳酸钡,故不能确定含亚硫酸根或碳酸根,氯离子和钠离子无法确定,故选A。
17.某溶液由Na+、Al3+、Fe3+、NH 、Cl-、NO 、CO 、SO 中的若干种离子所组成,且各离子的物质
的量浓度相同。为确定其组成,现取适量溶液进行如下实验。
步骤一 加入过量NaOH溶液,加热,出现气泡和沉淀;
步骤二 过滤,得滤液、滤渣;
步骤三 取滤渣,洗涤、灼烧,得固体a;
步骤四 取少量滤液,加入足量BaCl 溶液,出现白色沉淀;
2
根据实验,下列推断错误的是
A.根据步骤一,肯定存在NH 、Fe3+
B.步骤三所得固体a为氧化铁
C.原溶液一定不存在Al3+、COD.原溶液可能存在Na+
【答案】D
【分析】取该溶液加入过量NaOH溶液,加热,出现气泡和沉淀,说明含有NH 、Fe3+,Fe3+与CO 会发
生完全双水解而不能共存,则一定不含CO ,步骤四中取少量滤液,加入足量BaCl 溶液,出现白色沉淀,
2
说明含有SO ,根据以上分析可知,原溶液中含有NH 、Fe3+、SO ,由于各离子的物质的量浓度相同,
根据溶液呈电中性规则可知,原溶液中一定含有Cl-、NO ,一定不含Na+、Al3+;
【解析】A.据分析可知,根据步骤一,肯定存在NH 、Fe3+,A正确;
B.Fe3+与NaOH反应生成Fe(OH) 沉淀,Fe(OH) 沉淀灼烧得到Fe O,则步骤三所得固体a为氧化铁,B
3 3 2 3
正确;
C.据分析可知,原溶液一定不存在Al3+、CO ,C正确;
D.据分析可知,原溶液一定不存在Na+,D错误;
故选D。
18.有一澄清透明的溶液,可能含有大量的 、 、 、 、 、 、 中的几种,向该
溶液中滴入 溶液一定体积后才产生沉淀。下列判断正确的是
A.溶液中可能含有 B.溶液中一定不含
C.溶液中可能含有 D.溶液中一定不含
【答案】D
【分析】向该溶液中滴入 溶液一定体积后才产生沉淀,溶液中一定含有 ,因为 与
反应, ,所以溶液中一定不含 , 与 反应生成 , 一定不
存在,溶液中一定含有阴离子为 , 在酸性条件下有强氧化性, 一定不存在,加入 产生沉淀, 和 可能都存在,或者存在其中之一。
【解析】A.根据以上分析,该溶液中 一定不存在,A错误;
B.加入 产生沉淀, 和 可能都存在,或者存在其中之一,B错误;
C.根据以上分析,溶液中一定含有 ,C错误;
D.溶液中含有 ,一定不含 ,D正确; 故选D。
19.某溶液仅由 、Cl-、 、 、 、Fe3+、Al3+和K+中的若干种离子组成,且各离子浓度相
等,取适量溶液进行如下实验:
①取该溶液加入过量NaOH溶液,加热,产生无色气体;
②将①过滤、洗涤、灼烧,得到固体a;
③向上述滤液中加足量BaCl 溶液,产生白色沉淀:
2
根据以上实验,下列推断错误的是
A.根据操作①,推断一定存在
B.②中固体a为氧化铁
C.原溶液中一定不存在 、Al3+,可能含有K+
D.说明原溶液中一定存在 、Cl-、 、 、Fe3+、
【答案】C
【分析】加入过量的碱产生气体为NH ,溶液有 。信息②知加入过量的碱产生了沉淀Fe(OH) ,溶液
3 3
中有Fe3+, 与Fe3+会发生双水解不能共存,则溶液中不存在 。信息③知加溶液中有 。
【解析】A.由上分析溶液中一定有 ,A项正确;
B.Fe(OH) 受热分解为氧化铁Fe O,B项正确;
3 2 3
C.由上分析溶液中一定有 和Fe3+而阴离子有 ,又溶液中各离子浓度相同,溶液中电荷不守恒,所以一定还有Cl-和 。溶液中这五种离子刚好电荷守恒,所以一定不存在 和Al3+、K+,C项错误;
D.由C项分析溶液中一定存在 、Fe3+、 、Cl-和 ,D项正确;
故选C。
20.某酸性溶液中可能含有Cl-、 、 、 、 、Fe3+、Fe2+、Al3+和Na+。某同学为了确认其
成分,设计并完成了如图实验。下列叙述正确的是
A.反应①发生反应的离子方程式3 Fe2++2 +4H+=3 Fe3++NO↑+2HO
2
B. 、 、Na+一定存在, 、Al3+一定不存在
C.溶液中可能含有Fe3+,一定含有Fe2+,可取少量原溶液加入KSCN溶液检验
D.溶液中至少有6种离子大量存在,其中Cl-一定存在,且c(Cl-)>0.6mol•L-1
【答案】D
【分析】酸性溶液中一定不存在 、 ,加入硝酸钾反应生成气体,遇空气变为红棕色即NO ,该气
2
体为NO,为Fe2+、 、H+反应生成,反应的离子方程式为3Fe2++ +4H+=3Fe3++NO↑+2HO,
2
生成0.01molNO可知n(Fe3+)=0.03mol;加入过量NaOH溶液并加热反应生成气体即氨气,则含有0.01mol
,产生红褐色沉淀即Fe(OH) ,灼烧得到3.2g固体是Fe O,物质的量为0.02mol,n(Fe3+)=0.04mol,
3 2 3
原溶液一定含有0.01molFe3+;滤液通过焰色反应观察有黄色火焰说明含Na+,由于加入NaOH也含有钠离
子,因此不确定原溶液是否含Na+,通入足量二氧化碳无现象说明不含有Al3+,否则过量NaOH与Al3+反应生成 ,加入二氧化碳会生成Al(OH) 沉淀;加入足量氯化钡溶液生成难溶于盐酸的固体即BaSO,
3 4
4.66g BaSO 固体的物质的量为0.02mol,说明含有0.02mol ,即原溶液一定不含有: 、 、Al3
4
+,一定含有:0.02mol 、0.01mol 、0.01molFe3+、0.03molFe2+、H+,根据电荷守恒一定含有
Cl−,且n(Cl−)>2×0.03mol+3×0.01mol+1×0.01mol−2×0.02mol=0.06mol,可能存在Na+。据此分析解
题。
【解析】A.反应①中Fe2+、 、H+反应生成Fe3+和NO,发生反应的离子方程式为3Fe2++ +4H+
=3Fe3++NO↑+2HO,故A错误;
2
B.据分析可知,可能存在Na+,故B错误;
C.由 可知,生成0.01molNO同时生成0.03molFe3+,由分析知灼烧
得到3.2g固体是Fe O,物质的量为0.02mol,则n(Fe3+)=0.04mol,则原溶液含0.01molFe3+,证明原溶液
2 3
一定含Fe3+、Fe2+,故C错误;
D.根据分析,溶液中一定不含有: 、 、Al3+,一定含有:0.02mol 、0.01
mol 、0.01molFe3+、0.03molFe2+、H+,根据电荷守恒一定含有Cl−,且n(Cl−)>2×0.03mol+
3×0.01mol+1×0.01mol−2×0.02mol=0.06mol,浓度是0.6mol/L,故D正确;;
故答案选D。