文档内容
第 02 讲 离子反应
1.下列属于弱电解质的是
A.CaCO B.SO C.NH ·H O D.Ba(OH)
3 2 3 2 2
2.下列方程式不正确的是
A.用 溶液清洗银镜:
B.氢氧化亚铁露置在空气中变为红褐色:
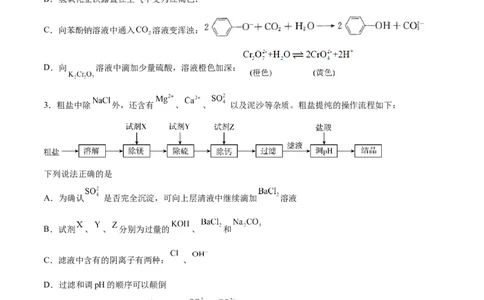
C.向苯酚钠溶液中通入 溶液变浑浊:
D.向 溶液中滴加少量硫酸,溶液橙色加深:
3.粗盐中除 外,还含有 、 、 以及泥沙等杂质。粗盐提纯的操作流程如下:
下列说法正确的是
A.为确认 是否完全沉淀,可向上层清液中继续滴加 溶液
B.试剂 、 、 分别为过量的 、 和
C.滤液中含有的阴离子有两种: 、
D.过滤和调pH的顺序可以颠倒
4.某无色溶液含有 、 、 、 、 中的2种离子,取该溶液进行了下列实验:
(1)取少量溶液,滴加 溶液,有沉淀产生,加足量硝酸,沉淀全部溶解;
(2)取实验(1)静置后的溶液,滴加 溶液,无现象。
根据上述实验,可以确定该无色溶液中存在的离子是
A. 和 B. 和 C. 和 D. 和5.某溶液中可能含有H+、NH 、Mg2+、Fe3+、Al3+、 、 等离子。当向该溶液中加入一定物质的
量浓度的NaOH溶液时,发现生成沉淀的物质的量随加入NaOH溶液的体积变化如图所示,下列说法正确
的是
A.d点溶液中含有的溶质只有NaSO 和
2 4
B.原溶液中含有的Fe3+和Al3+的物质的量之比为1:1
C.ab段发生的离子反应为:Al3++3OH-=Al(OH) ↓,Mg2++2OH-=Mg(OH) ↓
3 2
D.原溶液中含有的阳离子必定有H+、 、Al3+,且Mg2+和Fe3+至少存在一种
6.现有下列实验探究摩尔盐 的化学性质。
装置 实验 试剂a 现象
① 紫色石蕊溶液 溶液变红色
② 溶液 产生白色沉淀
③ 稀硝酸溶液 溶液变黄色
④ 浓 溶液 产生具有刺激性气味的气体
下列离子方程式不能准确解释相应实验现象的是
A.①中溶液变红: 、
B.②中产生白色沉淀:
C.③中溶液变黄:
D.④中产生有刺激性气体:
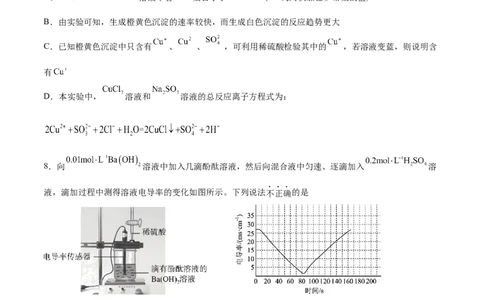
7.某学习小组为探究氯化铜与亚硫酸钠的反应,设计了如下实验:已知 。
下列分析中,错误的是
A.2mL0.2 溶液中含 数目小于 ( 为阿伏加德罗常数的值)
B.由实验可知,生成橙黄色沉淀的速率较快,而生成白色沉淀的反应趋势更大
C.已知橙黄色沉淀中只含有 、 、 ,可利用稀硫酸检验其中的 ,若溶液变蓝,则说明含
有
D.本实验中, 溶液和 溶液的总反应离子方程式为:
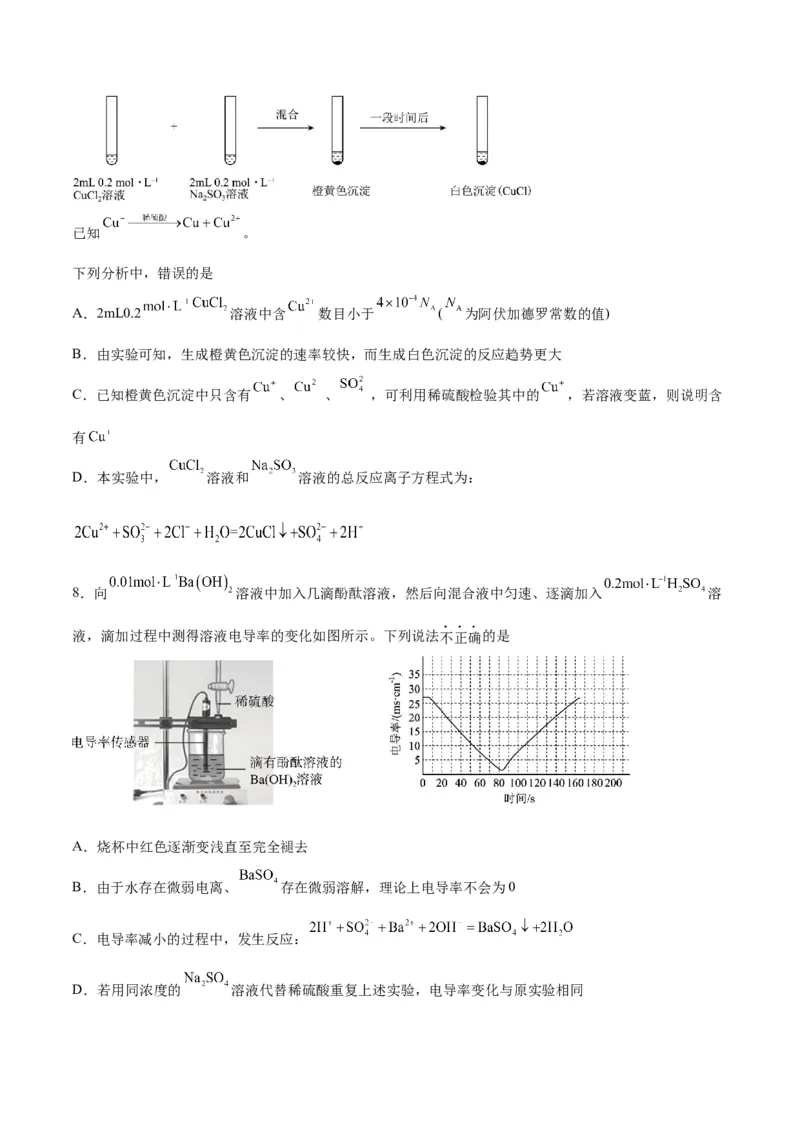
8.向 溶液中加入几滴酚酞溶液,然后向混合液中匀速、逐滴加入 溶
液,滴加过程中测得溶液电导率的变化如图所示。下列说法不正确的是
A.烧杯中红色逐渐变浅直至完全褪去
B.由于水存在微弱电离、 存在微弱溶解,理论上电导率不会为0
C.电导率减小的过程中,发生反应:
D.若用同浓度的 溶液代替稀硫酸重复上述实验,电导率变化与原实验相同9.常温下,下列各组离子在指定溶液中可能大量共存的是
A. 的 溶液中:
B.滴加几滴 溶液显红色的溶液中:
C.加入铝粉能生成 的溶液:加入
D. 的溶液中:
10.下列离子方程式正确的是
A.利用覆铜板制作电路板的原理: 2FeCl + Cu = Cu2+ + 2Fe2+ + 6Cl-
3
B.泡沫灭火器灭火原理: 2A13+ + 3 + 3H O = 2Al(OH) ↓ + 3CO ↑
2 3 2
C.向硫化钠溶液中通入过量SO : 2S2- + 5SO + 2H O=3S↓+ 4
2 2 2
D.纯碱溶液吸收Br : + Br= + Br-+ CO↑
2 2 2
11.下列反应的离子方程式正确的是
A.向NaSO 溶液中滴加稀HNO 溶液: +2H+=SO↑+ H O
2 3 3 2 2
B.用过量氨水吸收废气中的SO :NH ·H O+SO = +
2 3 2 2
C.电解MgCl 水溶液的离子方程式:2Cl- +2H O H↑+Cl↑+ 2OH-
2 2 2 2
D.酸性KCr O 溶液遇NaNO 变成绿色: + 3 + 8H+= 3 + 2Cr3+ +4H O
2 2 7 2 2
12.通过实验、观察、类比、推理等方法得出正确结论是化学学习的方法之一,下列实验操作、现象和推
理或结论正确的是
选
实验操作及现象 推理或结论
项
NaO 与水反应生成氢氧
A 向装NaO 固体的试管中加水并滴加酚酞,只变红 2 2
2 2 化钠
B 向某溶液中加入足量盐酸酸化的BaCl 溶液,振荡,观察溶液中有白色 该溶液中一定含有SO
2沉淀生成
C 将潮湿的氯气通过盛有干燥红纸条的集气瓶,褪色 氯气具有漂白性
D 向某溶液中滴加新制的氯水,再滴加KSCN溶液,溶液变红 原溶液中不一定有Fe2+
13.下列是对某气体或溶液中离子进行检测的方法和结论,其中正确的是
A.将某气体通入品红溶液,若品红溶液褪色,则气体中一定含有SO
2
B.取样,先加入盐酸酸化,无现象,再加入 BaCl 溶液,若产生白色沉淀,则溶液中含
2
C.取样,加入氯水,再加入KSCN溶液,若出现红色,则溶液中含有Fe2+
D.取样,加入适量盐酸酸化,再加入 AgNO 溶液,若产生白色沉淀,则含 Cl-
3
14.根据下列实验操作和现象能得到相应结论的是
选项 实验操作和现象 相应结论
A 用洁净铂丝蘸取少量溶液在酒精灯火焰上灼烧,火焰呈黄色 该溶液含 ,不含
B 向某溶液中加入盐酸酸化的硝酸银溶液产生白色沉淀 该溶液中一定含有
向某溶液中加入稀盐酸,产生能使澄清石灰水变浑浊的无色气
C 该溶液中不一定含有
体
D 将绿豆大小的钠块投入水中,钠熔为小球,浮于水面 钠的密度为
15.下列除杂试剂选用不合理的是
选项 物质 杂质 除杂试剂
A Cl HCl 饱和NaCl溶液
2
B FeSO 溶液 Fe (SO ) 足量铁粉
4 2 4 3
C Mg(OH) Al(OH) 足量NaOH溶液
2 3
D CO SO 饱和NaCO 溶液
2 2 2 3
16.某同学向一份溶液样品(可能含有: 、 、 、 、 、 中的一种或几种)中加入一定
量的 溶液,产生白色沉淀,继续滴加稀盐酸,发现沉淀部分溶解,并产生能使澄清石灰水变浑浊的
气体,则此溶液样品中一定含有
A. B. C. D. 和17.某溶液由Na+、Al3+、Fe3+、NH 、Cl-、NO 、CO 、SO 中的若干种离子所组成,且各离子的物质
的量浓度相同。为确定其组成,现取适量溶液进行如下实验。
步骤一 加入过量NaOH溶液,加热,出现气泡和沉淀;
步骤二 过滤,得滤液、滤渣;
步骤三 取滤渣,洗涤、灼烧,得固体a;
步骤四 取少量滤液,加入足量BaCl 溶液,出现白色沉淀;
2
根据实验,下列推断错误的是
A.根据步骤一,肯定存在NH 、Fe3+
B.步骤三所得固体a为氧化铁
C.原溶液一定不存在Al3+、CO
D.原溶液可能存在Na+
18.有一澄清透明的溶液,可能含有大量的 、 、 、 、 、 、 中的几种,向该
溶液中滴入 溶液一定体积后才产生沉淀。下列判断正确的是
A.溶液中可能含有 B.溶液中一定不含
C.溶液中可能含有 D.溶液中一定不含
19.某溶液仅由 、Cl-、 、 、 、Fe3+、Al3+和K+中的若干种离子组成,且各离子浓度相
等,取适量溶液进行如下实验:
①取该溶液加入过量NaOH溶液,加热,产生无色气体;
②将①过滤、洗涤、灼烧,得到固体a;
③向上述滤液中加足量BaCl 溶液,产生白色沉淀:
2
根据以上实验,下列推断错误的是
A.根据操作①,推断一定存在
B.②中固体a为氧化铁
C.原溶液中一定不存在 、Al3+,可能含有K+D.说明原溶液中一定存在 、Cl-、 、 、Fe3+、
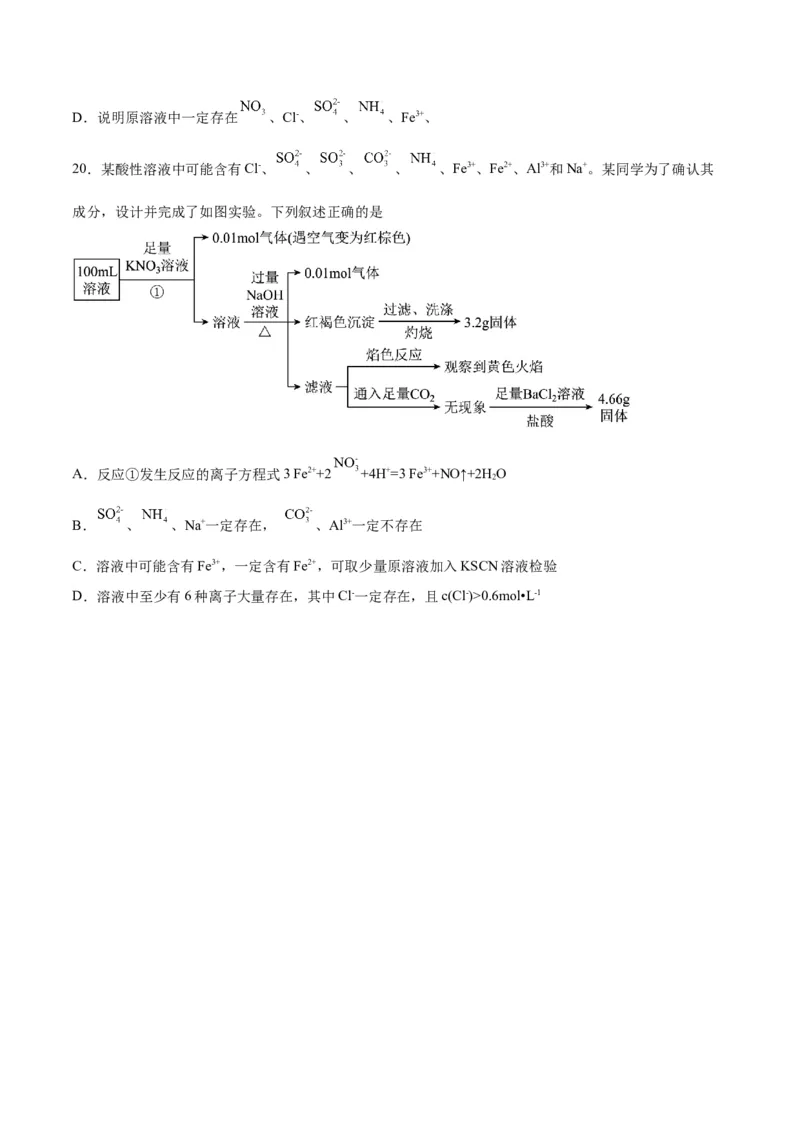
20.某酸性溶液中可能含有Cl-、 、 、 、 、Fe3+、Fe2+、Al3+和Na+。某同学为了确认其
成分,设计并完成了如图实验。下列叙述正确的是
A.反应①发生反应的离子方程式3 Fe2++2 +4H+=3 Fe3++NO↑+2HO
2
B. 、 、Na+一定存在, 、Al3+一定不存在
C.溶液中可能含有Fe3+,一定含有Fe2+,可取少量原溶液加入KSCN溶液检验
D.溶液中至少有6种离子大量存在,其中Cl-一定存在,且c(Cl-)>0.6mol•L-1