文档内容
专题 02 海水中的重要元素——钠和氯
第 06 练 物质的量
1.“物质的量”是国际单位制中的一个基本物理量,下列有关说法正确的是( )
A.2gH 含有1mol氢分子 B.2mol氧气的摩尔质量为64g·mol-1
2
C.1mol任何物质都含有6.02×1023个分子 D.质量相等的CO和CO,物质的量之比为2∶3
2
【答案】A
【解析】A项,2gH 的物质的量为 =1mol,即含有1mol氢分子,故A正确;B项,氧气的摩
2
尔质量为32g/mol,与氧气的物质的量无关,故B错误;C项,并不是所有物质都是由分子构成,如NaCl
由离子构成,所以并不是1mol任何物质都含有6.02×1023个分子,故C错误;D项,1gCO的物质的量为
mol,1gCO 的物质的量为 mol,二者物质的量之比为 : =11:7,故D错误;故选A。
2
2.下列物质所含分子数最少的是( )
A.0.8 mol HO B.1.7 g NH (NH 的摩尔质量是17g/mol)
2 3 3
C.标准状况下22.4 L O D.0.5N 个H (N 为阿伏加德罗常数的值)
2 A 2 A
【答案】B
【解析】0.8 mol HO中分子个数为0.8N ;1.7 g NH 的物质的量= =0.1mol,则分子个数为
2 A 3
0.1N ;标准状况下22.4 L O 的物质的量= =1mol,则分子个数为1N ;0.5N 个H,则所含分子
A 2 A A 2
数最小的是B,故选B。
3.下列对摩尔(mol)的有关说法中不正确的是( )
A.摩尔是一个单位而非物理量
B.氧气的摩尔质量就是其相对分子质量
C.1mol任何气体所含气体的分子数目都相等
D.0.5mol氦气约含有3.01×1023个原子【答案】B
【解析】A项,物质的量是国际单位制中七个基本物理量之一,摩尔是物质的量的单位,不是物理量,
故A正确;B项,摩尔质量的单位为g/mol,相对分子质量无单位,所以氧气的摩尔质量在数值上等于其
相对分子质量,故B错误;C项,1mol任何气体都含有阿伏伽德罗常数个气体分子,所以1mol任何气体
所含气体的分子数目都相等,故C正确;D项,氦气是单原子分子,0.5mol氦气约含有原子的数目为
0.5mol×6.02×1023=3.01×1023个,故D正确;故选B。
4.相同条件下,下列各组中分子数相同的是( )
A.14gN 与32gNO B.34gNH 与4gH
2 2 3 2
C.2LCO 与2LHO D.11.2LCO与0.5molO
2 2 2
【答案】B
【解析】A项,14gN 的物质的量为 ,32gNO 的物质的量为 ,二
2 2
者物质的量不同,分子数一定不同,故A不符合题意;B项,34gNH 的物质的量为 ,4gH
3 2
的物质的量为 ,二者物质的量相同,分子数一定相同,故B符合题意;C项,未指明二氧化
碳和水所处的状态,不能计算两者物质的量,不能确定两者分子数是否相等,故C不符合题意;D项,未
说明CO处于标准状况,11.2LCO的物质的量不一定为0.5mol,11.2LCO与0.5molO 分子数不一定相同,
2
故D不符合题意;故选B。
5.下列关于物质的量的叙述,错误的是( )
A.1molNe中含有10×6.02×1023个电子
B.0.012 kg 12C含有约6.02×1023个C
C.1molH O中含有2mol氢原子和1mol氧原子
2
D.1mol任何物质都含有 个分子
【答案】D
【解析】A项,1个氖原子核外有10个电子,则1 mol Ne中含有10×6.02×1023个电子, A正确;B项,
0.012 kg 12C的物质的量为1mol,则含有约6.02×1023个C原子,B正确;C项,一个水分子中含两个氢原
子和一个氧原子,因此1molH O中含有2molH和1molO,C正确;D项,因为有些物质是由分子构成的
2
(例如水、硫酸等),有些物质是由离子构成的[例如NaCl、Ca(OH) 等],还有些物质是由原子直接构成的
2
(例如金刚石等),所以不是1mol 任何物质都含有6.02×1023个分子,D错误;故选D。6.下列溶液中氯离子浓度最大的是( )
A.15 mL 1 mol•L﹣1的AlCl B.10 mL 2 mol•L﹣1的CaCl
3 2
C.20 mL 2 mol•L﹣1的NH Cl D.50 mL 1 mol•L﹣1的KCl
4
【答案】B
【解析】A项,15 mL 1 mol•L-1的AlCl ,氯离子的浓度为:1mol/L×3=3mol/L;B项,10 mL 2 mol•L-1
3
的CaCl 中氯离子浓度为:2mol/L×2=4mol/L;C项,20 mL 2 mol•L-1的NH Cl溶液中,氯离子浓度为
2 4
2mol/L×1=2mol/L;D项,50 mL 1 mol•L-1的KCl溶液中,氯离子浓度为1mol/L×1=1mol/L;综上分析,10
mL 2 mol•L-1的CaCl 中氯离子浓度最大,故选B。
2
7.下列关于物质的量浓度说法中正确的是( )
A.在1mol/L硫酸钠溶液中含2mol钠离子
B.将标准状况下44.8LHCl通入1L水中,则此溶液的物质的量浓度为2mol·L-1
C.相同体积和相同物质的量浓度的强酸和强碱相混合,所得溶液一定是中性的
D.500mL0.2mol/L的氯化钠溶液中含钠离子0.1mol
【答案】D
【解析】A项,没有明确溶液体积,不能计算1mol/L硫酸钠溶液中钠离子的物质的量,故A错误;B
项,将标准状况下44.8LHCl通入1L水中,所得溶液的体积不是1L,则此溶液的物质的量浓度不是
2mol·L-1,故B错误;C项,相同体积和相同物质的量浓度的硫酸和氢氧化钠溶液混合,所得溶液呈酸性,
故C错误;D项,500mL0.2mol/L的氯化钠溶液中含钠离子的物质的量为0.5L×0.2mol/L= 0.1mol,故D正
确;故选D。
8.用N 表示阿伏加德罗常数的值。下列说法正确的是( )
A
A.CO 的摩尔质量是44g
2
B.1L0.5mol/LKSO 溶液中含有K+的质量是78g
2 4
C.常温常压下,22.4LO 含分子数为N
2 A
D.l6gCH 中含有氢原子的总数为4N
4 A
【答案】D
【解析】A项,二氧化碳的摩尔质量为44g/mol,故A错误;B项,1L0.5mol/L硫酸钾溶液中钾离子
的质量为0.5mol/L×1L×2×39g/mol=39g,故B错误;C项,常温常压下,气体摩尔体积大于22.4L/mol,则
22.4L含有的分子数小于 ×N mol—1=N ,故C错误;D项,16g甲烷中含有氢原子的总数为
A A×4×N mol—1=4N ,故D正确;故选D。
A A
9.CH 与Cl 光照条件下充分反应生成一系列卤代烃,设N 为阿伏加德罗常数的值。下列说法正确
4 2 A
的是( )
A.标准状况下,22.4LCHCl 含有的氯原子数为3N
3 A
B.标准状况下,22.4L Cl 完全反应后得到的HCl分子数为2N
2 A
C.16 g CH 与足量Cl 充分反应后得到的卤代烃分子总数为N
4 2 A
D.1molCH 和1mol Cl 充分反应可以得到CHCl的分子数为N
4 2 3 A
【答案】C
【解析】A项,标准状况下,三氯甲烷不是气态,无法使用22.4L/mol计算物质的量,选项A错误;B
项,标准状况下,22.4L Cl 与CH 完全反应,无论生成哪种卤代烃,每消耗1molCl 生成1molHCl,所以得
2 4 2
到HCl分子数为N ,选项B错误;C项,根据碳原子守恒,16 g CH 为即1mol,与足量Cl 充分反应后得
A 4 2
到的卤代烃分子总数为N ,选项C正确;D项,甲烷和氯气发生多步反应,生成一氯甲烷、二氯甲烷、三
A
氯甲烷、四氯化碳和HCl,无法计算得到的CHCl的分子数,选项D错误;故选C。
3
10.N 表示阿伏加德罗常数的值,下列说法正确的是( )
A
A.常温常压下,1molNO的体积为22.4L
B.5.6g铁与硝酸反应,转移电子数一定为0.3N
A
C.SO 与SO 含氧原子数相同,则其物质的量之比为3∶2
2 3
D.1mol/L的稀硫酸中SO 2-数目为N
4 A
【答案】C
【解析】A项,常温常压下,气体摩尔体积不是22.4L/mol,1molNO的体积不是22.4L,故A错误;B
项,Fe和足量硝酸反应生成Fe 3+,和少量硝酸反应生成Fe2+,且铁和浓硝酸发生钝化现象,硝酸的浓度及
硝酸的量未知,无法判断Fe失电子数,故B错误;C项,SO 与SO 含氧原子数相同,
2 3
N(O)=n(SO)×2=n(SO )×3,则物质的量之比为3∶2,故C正确;D项,未知溶液体积,无法计算物质的量,
2 3
SO 2-数目不确定,故D错误;故选C。
4
11.N 为阿伏伽德罗常数的值。下列叙述正确的是( )
A
A.1molOH-中含有9N 个电子
A
B.1molCl 与NaOH完全反应,转移2N 个电子
2 A
C.14gC H 与C H 混合物中含有2N 个氢原子
2 4 3 6 A
D.10mL0.1mol·L-1NaAlO 溶液中含有2×10-3N 个氧原子
2 A
【答案】C【解析】A项,已知1个OH-含有10个电子,则1molOH-中含有1mol ×10×N mol-1=10N 个电子,A
A A
错误; B项,已知Cl+2NaOH=NaCl+NaClO+H O,故1molCl 与NaOH完全反应,转移N 个电子,B错
2 2 2 A
误;C项,已知C H 和C H 的最简式均为CH,则14gC H 与C H 混合物中含有
2 4 3 6 2 2 4 3 6
=2N 个氢原子,C正确;D项,由于水分子中也含有O原子,故无法计算10mL0.1mol·L-1NaAlO 溶液中含
A 2
有氧原子的数目,D错误;故选C。
12.阿伏加德罗常数为N 。下列说法正确的是( )
A
A.lmolCl 和足量Fe充分反应,转移电子数为3N
2 A
B.1mol乙醇中含有C—H共价键数为5N
A
C.标准状况下,2.24LH O含有H—O键的数为0.2N
2 A
D.0.5mol乙酸乙酯在酸性条件下水解,生成乙醇的分子数为0.5N
A
【答案】B
【解析】A项,lmolCl 和足量Fe充分反应生成氯化铁,氯元素由0价变为-1价, Cl 有两个氯原子,
2 2
所以lmolCl 反应转移电子数为2N ,故A错误;B项,乙醇分子式为CHCHOH,所以1mol乙醇中含有
2 A 3 2
C—H共价键数为5N ,故B正确;C项,标准状况下水为液体,所以不能根据气体摩尔体积来计算其物质
A
的量,故C错误;D项,乙酸乙酯在酸性条件下水解是一个可逆反应,所以0.5mol乙酸乙酯在酸性条件下
水解,生成乙醇的分子数小于0.5N ,故D错误;故选B。
A
13.配制一定物质的量浓度的NaCO 溶液时,下列操作对实验结果没有影响的是( )
2 3
A.容量瓶中原有少量蒸馏水
B.洗涤烧杯和玻璃棒的溶液未转入容量瓶中
C.定容时观察液面俯视
D.容量瓶中原有少量NaCO 溶液
2 3
【答案】A
【解析】A项,若容量瓶中原有少量蒸馏水,不影响溶质的物质的量及溶液的体积,因此对配制溶液
的浓度无影响,A符合题意;B项,洗涤烧杯和玻璃棒的溶液未转入容量瓶中,导致溶质的物质的量减少,
由于溶液的体积不变,最终导致配制的溶液浓度偏低,B不符合题意;C项,定容时观察液面俯视,溶液
的体积偏少,由于溶质的物质的量不变,则最终导致配制的溶液浓度偏高,C不符合题意;D项,容量瓶
中原有少量NaCO 溶液,使溶液中溶质的物质的量偏多,由于溶液的体积不变,最终导致配制的溶液浓度
2 3
偏高,D不符合题意;故选A。
14.实验室用氢氧化钠固体配制1.00mo/L的NaOH溶液480mL,以下配制步骤及分析正确的是( )A.用烧杯在托盘天平上称取19.2g NaOH固体,加蒸馏水溶解
B.待溶液冷却后,将烧杯中的溶液沿玻璃棒转移到容量瓶中,并洗涤烧杯和玻璃棒2-3次,将洗涤液
移至容量瓶中
C.定容时仰视刻度线
D.定容后塞上瓶塞、振荡、摇匀、静置后,液面低于刻度线,再加水至刻度线
【答案】B
【解析】A项,验室无480mL容量瓶,应选择500mL容量瓶,配制500mL溶液,所需的氢氧化钠的
质量m=cVM=1mol/L×0.5L×40g/mol=20.0g, 故A错误;B项,氢氧化钠固体溶于水放热,因此应冷却至
室温,移液时应用玻璃棒引流,否则溶液溅出会导致浓度偏低,并洗涤烧杯 2~3 次,将洗涤液全部转移
至容量瓶中,避免溶质损失,故B正确;C项,定容时,应平视刻度线,故C错误;D项,定容后塞上瓶
塞反复摇匀,静置后,液面低于刻度线是正常的,再加水至刻度线,会导致溶液浓度偏低,故D错误;故
选B。
15.配制100mL NaOH溶液的操作如下所示。下列说法不正确的是( )
A.操作1前称取NaOH的质量为4.00g B.操作2前NaOH溶液需恢复至室温
C.操作4若俯视刻度线定容,结果偏大D.操作5后液面下降,需补充少量水至刻度线
【答案】D
【解析】A项,操作1前称取NaOH的质量m(NaOH)=0.1L×1.00mol∙L−1×40g∙mol−1=4.00g,故A正确;
B项,转移溶液之前应将溶液冷却至室温即操作2前NaOH溶液需恢复至室温,故B正确;C项,操作4
若俯视刻度线定容,溶液体积减小,物质的量浓度偏大,故C正确;D项,操作5后液面下降,液体可能
在容量瓶和瓶塞之间,不能补充水,故D错误。故选D。
16.下列有关溶液配制说法不正确的是( )
A.在溶液配制过程中,定容时俯视会导致所配溶液浓度偏高
B.取58.5gNaCl固体溶于1L水中,所得溶液物质的量浓度为1mol·L-1
C.取16.0gCuSO 固体溶于水并加水稀释至500mL,所得溶液物质的量浓度为0.2mol·L-1
4
D.10mL5mol·L-1NaSO 溶液加水稀释至100mL,所得溶液浓度为0.5mol·L-1
2 4【答案】B
【解析】A项,在溶液配制过程中,定容时俯视会导致所配溶液的体积偏小,则所配溶液的浓度偏高,
A项正确;B项,58.5gNaCl物质的量为 =1mol,水的体积为1L,所配溶液的体积不等于1L,所
配溶液物质的量浓度不为1mol/L,B项错误;C项,16.0gCuSO 物质的量为 =0.1mol,所配溶液
4
的体积为500mL,则所配CuSO 溶液的物质的量浓度为 =0.2mol/L,C项正确;D项,根据稀释前
4
后NaSO 物质的量不变,0.01L×5mol/L=0.1L×c(Na SO ) ,解得c(Na SO ) =0.5mol/L,D项正确;故选
2 4 2 4 后 2 4 后
B。
1.下列说法正确的是( )
A.把100 mL 3 mol·L-1的HSO 跟100 mL H O混合,硫酸的物质的量浓度为1.5 mol·L-1
2 4 2
B.把100 g 20%的NaCl溶液跟100 g HO混合后,NaCl溶液的质量分数是10%
2
C.把200 mL 3 mol·L-1的BaCl 溶液跟100 mL 3 mol·L-1的KCl溶液混合后,溶液中的c(Cl-)仍然是
2
3 mol·L-1
D.把100 mL 20%的NaOH溶液跟100 mL H O混合后,NaOH溶液的质量分数是10%
2
【答案】B
【解析】A项错误,因为100 mL 3 mol·L-1的HSO 跟100 mL H O混合后的体积不等于200 mL;B项
2 4 2
正确,w=100 g×20%÷(100 g+100 g)=10%;C项错误,因为3 mol·L-1的BaCl 溶液中的氯离子浓度为6
2
mol·L-1,混合后溶液中氯离子浓度大于3 mol·L-1;D项错误,因为NaOH溶液的密度大于1 g·mL-1,加
入水的质量等于100 g,所以混合后溶液中溶质的质量分数大于10%。
2.NH N (叠氮化铵)易发生分解反应生成N 和H,且两种气体的物质的量相等。若得到NH N 的分
4 3 2 2 4 3
解产物(简称a) 28g,则下列说法错误的是( )
A.叠氮化铵中N元素不止一种价态 B.a中两种气体的质量比为14:1
C.a的平均摩尔质量为14.5g ·mol-1 D.同温同压下,a中两种气体的体积比为1:1
【答案】C
【解析】A项,NH N 中NH + 的N元素的化合价为-3价,N-的N元素的化合价为 ,故A正确;B
4 3 4 3
项,两种气体的物质的量相等,则其质量比为等于摩尔质量之比,即为28g/mol:2g/mol=14:1,故B正确;C项,分解产物质量为28g,两种气体的物质的量相等,则 ,
,故C错误;D项,同温同压下,气体体积与物质的量成正比,则两种气体的体积此为
1:1,故D正确;故选C。
3.在甲、乙两个体积不同的密闭容器中,分别充入质量相等的CO、CO 气体时,两容器的温度和压
2
强均相同,则下列说法正确的是( )
A.充入的CO分子数比CO 分子数少
2
B.甲容器的体积比乙容器的体积小
C.CO的摩尔体积比CO 的摩尔体积小
2
D.若将压强相同改为体积相同,则甲容器中的压强比乙容器的压强大
【答案】D
【解析】由于M(CO)<M(CO),所以m相同时,n(CO)>n(CO)。A项,由分析知,n(CO)>n(CO),
2 2 2
则充入的CO分子数比CO 分子数多,A不正确;B项,两容器的温度和压强相同,则两容器内气体的体
2
积与气体的总物质的量成正比,由于n(CO)>n(CO),所以甲容器的体积比乙容器的体积大,B不正确;C
2
项,温度、压强相同时,气体的摩尔体积相同,所以CO的摩尔体积与CO 的摩尔体积相同,C不正确;D
2
项,根据阿伏伽德罗定律及推论可知,同温同体积的气体下,压强与气体的总物质的量成正比,由于
n(CO)>n(CO),所以甲容器中的压强比乙容器的压强大,D正确;故选D。
2
4.如图所示,抽去装置中的玻璃片,使两种气体充分反应(整个过程中认为装置气密性良好),等恢复
到原来温度。下列说法正确的是( )
A.反应后瓶内压强是反应前的
B.装置中氢元素的总质量为0.42 gC.生成物的分子数目为0.01N
A
D.反应结束后,两个集气瓶很容易分开
【答案】B
【解析】A项,反应后剩余HCl气体为0.02 mol,总体积为2.2VL,混合前两容器内压强相等,由阿
伏加德罗定律推论知混合后压强是混合前的 ,A错误;B项,由氢原子守恒知装置中氢元素的总质量为
0.42mol×1g/mol=0.42 g,B正确;C项,NH 与HCl反应生成了离子化合物NH Cl,组成中不存在分子这
3 4
种微粒,C错误;D项,反应后容器内气压比大气压小许多,故两个集气瓶不易分开,D错误。故选B。
5.化学计量在人类生产生活中起着至关重要的作用,下表是生活中一些常见行业的数据,以下数据
描述的物理量为c(物质的量浓度)的是( )
选项 行业 数据来源 数据描述
A 建筑业 废水综合排放标准 六价铬的最高允许排放浓度为0.5mg/L
B 医疗行业 体检报告 直接胆红素(DBIL)的正常参考值为1.70~6.80μmol/L
某品牌面包营养成分
C 食品制造业 6.6g蛋白质/100g食品
表
D 服装制造业 某品牌羽绒服标签 含绒量为90%
【答案】B
【解析】A项,排放标准是单位体积溶液内的溶质质量,不属于物质的量浓度,故A错误;B项,胆
红素的正常参考值描述的是物质的量浓度,故B正确;C项,面包营养成分表描述的是蛋白质的质量含量,
不属于物质的量浓度,故C错误;D项,羽绒服含绒量描述的是质量分数,不属于物质的量浓度,故D错
误;故选B。
6.假定把 的相对原子质量改为 ,那么下列叙述错误的是( )
A.此时16O的相对原子质量为 B.N 个O 与N 个H 的质量比为16:1
A 2 A 2
C.N 的摩尔质量为56g/mol D.标准状况下,16g O 的体积约为11.2L
2 2
【答案】D
【解析】A项,氧原子的实际质量没变,但标准却由12C质量的 变为 ,所以氧原子的相对原子
质量由16变为32,A正确;B项,N 个氧分子的质量为64g,N 个氢分子的质量为4g,二者质量比为
A A16:1,B正确;A项,氮原子的实际质量没变,但标准却由12C质量的 变为 ,所以氮原子的相对原
子质量由14变为28,N 的摩尔质量为56g/mol,C正确;D项,此时氧气的相对分子质量为32×2=64,因
2
此氧气的摩尔质量为64 g/mol,16g O 的物质的量为16g÷64g/mol=0.25mol。故在标准状况下的体积V=
2
0.25mol×22.4L/mol=5.6L,D错误;故选D。
7.体检时的一些指标常用物质的量浓度表示(可将元素近似折算成相应离子)。根据如图相关数据,
项目名称 结果 状态单位 参考值范围
总钙TCa 2.57 2.1-2.7
磷P 0.8-1.5
镁Mg 0.95 0.75-1.25
铁Fe 7.52-11.82
钾K 仪器故障报修 3.5-5.5
钠Na 135-160
下列分析不正确的是( )
A.在某些酱油中加入铁强化剂,可减少缺铁性贫血问题的发生
B.可用焰色反应测定钾离子的含量
C.该报告中Mg2+指标正常
D.若某人10mL血清样本中含钙离子1.2毫克,侧其钙含量略偏高
【答案】B
【解析】A项,血红蛋白中含亚铁,缺少亚铁会引起缺铁性贫血,则在某些酱油中加入铁强化剂,可
减少缺铁性贫血问题的发生,A正确;B项,焰色反应只能定性测定含钾元素,不能测定钾离子的含量,
B错误;C项,由报告单可知,Mg含量在参考范围值之内,该报告中Mg2+指标正常,C正确;D项,总钙
浓度为2.1~2.7 ,则10mL血清样本中含钙离子正常范围为2.1 ×0.010L×40g/mol~2.7
×0.010L×40g/mol( 0.84~1.08mg),若某人10mL血清样本中含钙离子1.2毫克,侧其钙含量略偏高,
D正确;故选B。
8.设N 代表阿伏加德罗常数的数值,下列说法正确的是( )
A
A.标准状况下11.2L的O、CO 混合气体含有的氧原子数为N
2 2 A
B.1mol·L-1NaNO 溶液中含有的Na+的数目为2N
2 4 A
C.将7.1g Cl 通入足量氢氧化钠溶液中,转移电子数0.2N
2 AD.18gNH +所含的电子数目为11N
4 A
【答案】A
【解析】A项,O、CO 中均含有2个氧原子,标准状况下11.2L的O、CO 混合气体的物质的量为
2 2 2 2
0.5mol,含有的氧原子数为N ,故A正确;B项,溶液体积未知,不能计算Na +数目,故B错误;C项,
A
7.1g Cl 的物质的量为0.1mol,通入足量氢氧化钠溶液中反应,Cl 转化为ClO-、Cl-,转移电子数0.1N ,
2 2 A
故C错误;D项,1个NH +含有10个电子,18gNH +的物质的量为1mol,所含的电子数目为10N ,故D
4 4 A
错误;故选A。
9.设N 为阿伏伽德罗常数的值,下列说法正确的是( )
A
A.过量Fe与1 mol稀HNO 反应,转移2N 个电子
3 A
B.16g甲烷中含有非极性共价键的数目为4N
A
C.28g乙烯和丙烯的混合气体含有原子的数目为6N
A
D.标准状况下2.24L氯仿(CHCl )含有分子的数目为0.1N
3 A
【答案】C
【解析】A项,根据过量的铁与稀硝酸反应的关系式8HNO~2NO~6e-,当1mol稀硝酸发生反应时
3
转移的电子数为0.75N ,故A不正确;B项,甲烷分子中只存在碳氢键属于极性共价键,不存在非极性共
A
价键,故B不正确;C项,乙烯和丙烯最简式都为CH,故28g混合物含有CH 的物质的量为2mol,则原
2 2
子数为6N ,故C正确;D项,标准状况下,氯仿是液体,不是气体,不能用气体摩尔体积计算,故D不
A
正确;故选C。
10.溶液浓度是常用的物理量,下列说法中正确的是( )
A.质量分数为98%的浓硫酸和等质量的水混合后,硫酸溶液的质量分数大于49%
B.配制250mL1.0mo/LHSO 溶液,需要量取18mol/LHSO 溶液的体积为13.9mL
2 4 2 4
C.从1L0.15mol/LNa SO 溶液中取出100mL,取出溶液中NaSO 的物质的量浓度为0.015mol/L
2 4 2 4
D.50mL0.1mol/LNaCl溶液和25mL0.1molLMgCl 溶液中的Cl—浓度相同
2
【答案】B
【解析】A项,质量分数为98%的浓硫酸和等质量的水混合后,硫酸溶液的质量分数为
=49%,故A错误;B项,由稀释定律可知,18mol/L硫酸溶液的体积为 ×103mL/
L=13.9mL,故B正确;C项,从1L0.15mol/L硫酸钠溶液中取出100mL,取出溶液中硫酸钠的物质的量浓
度还是0.15mol/L,故C错误;D项,50mL0.1mol/L氯化钠溶液中氯离子浓度为0.1mol/L,25mL0.1molL
氯化镁溶液中氯离子浓度为0.1mol/L×2=0.2mol/L,两溶液中氯离子浓度不相等,故D错误;故选B。11.Al遇到极稀的硝酸发生反应:8Al+30HNO =3NHNO +8Al(NO)+9H O。设N 为阿伏加德罗常数
3 4 3 3 3 2 A
的值。下列说法正确的是( )
A.反应中每消耗2.7g金属Al,转移的电子数为3N
A
B.1molNH +含有的质子数为10N
4 A
C.1.0g由H18O与DO组成的混合物中所含有的中子总数为0.5N
2 2 A
D.0.1mol·L-1Al(NO ) 溶液中,所含阳离子数目为0.1N
3 3 A
【答案】C
【解析】A项,该反应转移电子情况:8Al+30HNO =3NHNO +8Al(NO)+9H O ~24e-。反应中每消耗
3 4 3 3 3 2
2.7g金属Al,物质的量为0.1mol,则转移的电子数为0.3 N ,A错误;B项,一个NH +含有质子数
A 4
7+4=11,1molNH +含有的质子数为11N ,B错误;C项,H18O分子含有中子数10,DO分子含有中子数
4 A 2 2
10,H18O摩尔质量为20g/mol,与摩尔质量同为20g/mol的DO组成的混合物,平均摩尔质量是20g/mol,
2 2
1.0g该混合物物质的量为0.05mol,所含有的中子总数为0.5N ,C正确;D项,未给出该溶液的体积,无
A
法计算阳离子数目,D错误;故选C。
12.过氧化钠(Na O,其中氧元素显—1价)和水的反应2NaO+2H O=4NaOH+O ↑是潜艇中氧气来源
2 2 2 2 2 2
之一。用N 表示阿伏加德罗常数,下列说法正确的是( )
A
A.每转移2N 个电子生成还原产物2mol
A
B.22.4LO 含2N 个氧原子
2 A
C.O 既是氧化产物又是还原产物
2
D.4gNaOH溶于100mL水中,所得溶液的物质的量浓度为1mol·L-1
【答案】A
【解析】A项,由方程式可知,反应中过氧化钠即是氧化剂又是还原剂,氢氧化钠是还原产物、氧气
是氧化产物,反应转移2N 个电子生成2mol氢氧化钠,故A正确;B项,缺标准状况,无法计算22.4L氧
A
气的物质的量和含有的氧原子个数,故B错误;C项,由方程式可知,反应中过氧化钠即是氧化剂又是还
原剂,氢氧化钠是还原产物、氧气是氧化产物,故C错误;D项,4g氢氧化钠溶于水配成100mL溶液,
所得溶液的物质的量浓度为1mol·L-1,故D错误;故选A。
13.下列各组数据中,前者刚好是后者两倍的是( )
A.2molH O的摩尔质量和1molH O的摩尔质量
2 2
B.200mL1mol·L-1的氯化钙溶液中c(Cl-)和100mL2mol·L-1的氯化钾溶液中c(Cl-)
C.250mL1mol·L-1的碳酸钠溶液中Na+数和20gNaOH中Na+数
D.常温下8g氧气与钠反应转移电子数和标准状况下5.6L二氧化碳中氧原子数【答案】D
【解析】A项,2mol水的质量是1mol水的质量的2倍,但水的摩尔质量为定值是18g/mol,故A选项
错误;B项,1mol/L氯化钙溶液中,c(Cl-)=2mol/L,2mol/L氯化钾溶液中c(Cl-)=2mol/L,氯离子浓度后
者等于前者,故B选项错误;C项,250mL1mol·L-1的碳酸钠溶液中Na+数为:0.25L×1mol·L-1×2×N =0.5
A
N ,20gNaOH中Na+数为: ,Na+数相等,故C选项错误;D项,常温下8g氧气为
A
0.25mol,与钠反应生成NaO,转移电子数为:0.25×N ×4=N ;标准状况下5.6L二氧化碳物质的量为
2 A A
5.6L÷22.4L/mol=0.25mol,一个CO 中有2个氧原子,则5.6L二氧化碳中氧原子数为
2
0.25mol×N ×2=0.5N ,前者刚好是后者两倍,故D选项正确。故选D选项。
A A
1.(2022•全国甲卷)N 为阿伏加德罗常数的值,下列说法正确的是( )
A
A.25℃,101kPa下, 氢气中质子的数目为2.5N
A
B.2.0L 1.0 mol/L溶液中, 的数目为2.0N
A
C.0.2mol苯甲酸完全燃烧,生成CO 的数目为1.4N
2 A
D.电解熔融CuCl ,阴极增重6.4g,外电路中通过电子的数目为0.10N
2 A
【答案】C
【解析】A项,25℃、101kPa不是标准状况,不能用标况下的气体摩尔体积计算氢气的物质的量,故
A错误;B项,Al3+在溶液中会发生水解生成Al(OH) ,因此2.0L 1.0 mol/L的AlCl 溶液中Al3+数目小于
3 3
2.0N ,故B错误;C项,苯甲酸燃烧的化学方程式为 ,1mol苯甲酸燃
A
烧生成7molCO ,则0.2mol苯甲酸完全燃烧生成1.4molCO,数目为1.4N ,故C正确;D项,电解熔融
2 2 A
CuCl 时,阳极反应为2Cl--2e- =Cl↑,阴极反应为Cu2++2e- =Cu,阴极增加的重量为Cu的质量,6.4gCu的
2 2
物质的量为0.1mol,根据阴极反应可知,外电路中通过电子的物质的量为0.2mol,数目为0.2N ,故D错
A
误;故选C。
2.(2022·浙江省1月选考)设N 为阿伏加德罗常数的值,下列说法正确的是( )
A
A.在25℃时,1LpH为12的Ba(OH) 溶液中含有OH-数目为0.01N
2 A
B.1.8g重水(D O)中所含质子数为N
2 A
C.足量的浓盐酸与8.7gMnO 反应,转移电子的数目为0.4N
2 AD.32g甲醇的分子中含有C—H键的数目为4N
A
【答案】A
【解析】A项,1LpH为12的Ba(OH) 溶液中含有OH-的浓度为0.01mol/L,物质的量0.01mol/L
2
×1L=0.01mol,OH-的数目为0.01N ,A正确;B项,1.8g重水(D O)的物质的量为:0.09mol,所含质子数
A 2
为0.9N ,B错误;C项,足量的浓盐酸与8.7gMnO(0.1mol)反应,+4价Mn转化生成Mn2+,转移电子的数
A 2
目为0.2N ,C错误;D项,甲醇的结构简式为:CHOH,32g (1mol)的分子中含有C—H键的数目为
A 3
3N ,D错误;故选A。
A
3.(2022·浙江省6月选考)N 为阿伏加德罗常数的值,下列说法正确的是( )
A
A.12 g NaHSO 中含有0.2N 个阳离子
4 A
B. 乙烷和丙烯的混合气体中所含碳氢键数为3N
A
C.8 gCH 含有中子数为3N
4 A
D.0.1mol H 和0.1mol I 于密闭容器中充分反应后, 分子总数为0.2N
2 2 A
【答案】C
【解析】A项,NaHSO 由钠离子和硫酸氢根离子构成,其中的阳离子只有钠离子,8 gCH 的物质的
4 4
量为0.1mol,因此,其中只含有0.1N 个阳离子,A不正确;B项,没有指明气体的温度和压强,无法确
A
定11.2L乙烷和丙烯的混合气体的物质的量是多少,因此,无法确定其中所含碳氢键的数目,B不正确;
C项,CH 分子中有6个中子,8 gCH 的物质的量为0.5mol,因此,8 gCH 含有的中子数为3N ,C正确;
4 4 4 A
D项,H 和I 发生反应生成HI,该反应是可逆反应,反应物不能完全转化为生成物,因此,0.1mol H 和
2 2 2
0.1mol I 于密闭容器中充分反应后,HI分子总数小于0.2N ,D不正确。故选C。
2 A
4(2021•全国甲卷)N 为阿伏加德罗常数的值。下列叙述正确的是( )
A
A. 重水(D O)中含有的质子数为10 N
2 A
B.3mol的NO 与HO完全反应时转移的电子数为4N
2 2 A
C.32g环状 ( )分子中含有的S-S键数为1N
A
D.1L pH=4的0.1mol·L-1 KCr O 溶液中Cr O2-离子数为0.1 N
2 2 7 2 7 A
【答案】C
【解析】A项,DO的质子数为10,18g D O的物质的量为 0.9mol, 则18g重水(D O)中
2 2 2
所含质子数为9 N ,A错误;B项,NO 与HO反应的化学方程式为:3NO +H O=2HNO +NO,该反应消
A 2 2 2 2 3耗3个NO 分子转移的电子数为2个,则有3mol的NO 参与反应时,转移的电子数为2 N ,B错误;C项,
2 2 A
一个 ( )分子中含有的S-S键数为8个,32gS 的物质的量为 mol,则含有的
8
S-S键数为 ,C正确;D项,酸性KCr O 溶液中存在:Cr O2-+H O 2CrO2-+2H+,含
2 2 7 2 7 2 4
Cr元素微粒有Cr O2-和CrO2-,则1L pH=4的0.1mol·L-1 KCr O 溶液中Cr O2-离子数应小于0.1 N ,D错
2 7 4 2 2 7 2 7 A
误;故选C。
5.(2021•浙江6月选考)设N 为阿伏加德罗常数的值,下列说法不正确的是( )
A
A.标准状况下,1.12L18O 中含有中子数为N
2 A
B.31gP (分子结构: )中的共价键数目为1.5N
4 A
C.100mL 0.1mol·Lˉ1的NaOH水溶液中含有氧原子数为0.01N
A
D.18.9g三肽C H NO (相对分子质量:189)中的肽键数目为0.2N
6 33 3 4 A
【答案】C
【解析】A项,标准状况下,1.12L18O 的物质的量为:0.05mol,一个18O中含有中子数为:18-8=10
2
个,所以1.12L18O 中含有中子数为N ,A正确;B项,31gP 的物质的量为:0.25mol,根据白磷的分子结
2 A 4
构可知一个白磷分子里含有六条共价键,所以共价键数目为1.5N ,B正确;C项,100mL 0.1mol·Lˉ1的
A
NaOH水溶液中含有溶质氢氧化钠和溶剂水,氧原子数目为二者氧原子数目的加和,C错误;D项,18.9g
三肽C H NO 的物质的量为:0.1mol,三分子氨基酸脱水缩合形成三肽,三肽中含有两个肽键,所以
6 33 3 4
18.9g三肽C H NO 中的肽键数目为0.2N ,D正确;故选C。
6 33 3 4 A
6.(2021•湖南选择性考试)N 为阿伏加德罗常数的值。下列说法正确的是( )
A
A.18g H 18O含有的中子数为10N
2 A
B.0.1mol•L﹣1HClO 溶液中含有的H+数为0.1N
4 A
C.2mol NO与1mol O 在密闭容器中充分反应后的分子数为2N
2 A
D.11.2L CH 和22.4L Cl (均为标准状况)在光照下充分反应后的分子数为1.5N
4 2 A
【答案】D
18g
【解析】A项,18g H 18O的物质的量为: =0.9mol,含有中子的物质的量为:0.9mol×10=
2 20g/mol9mol,含有的中子数为9N ,故A错误;B项,缺少0.1mol•L﹣1HClO 溶液的体积,无法计算溶液中含有
A 4
的H+数,故B错误;C项,2molNO与1molO 反应生成2molNO ,由于存在平衡:2NO NO ,导
2 2 2 2 4
致分子数减少,容器中含有的分子数小于 2N ,故 C 错误;D 项,标况下 11.2L CH 的物质的量为
A 4
11.2L 22.4L
=0.5mol,22.4L Cl 的物质的量为 =1mol,由于甲烷与氯气的反应前后气体分子
22.4L/mol 2 22.4L/mol
数始终不变,则反应后气体总物质的量仍然为0.5mol+1mol=1.5mol,反应后的分子数为1.5N ,故D正确;
A
故选D。
7.(2021•河北选择性考试)N 是阿伏加德罗常数的值,下列说法错误的是( )
A
A.22.4L(标准状况)氟气所含的质子数为18N
A
B.1mol碘蒸气和1mol氢气在密闭容器中充分反应,生成的碘化氢分子数小于2N
A
C.电解饱和食盐水时,若阴阳两极产生气体的总质量为73g,则转移电子数为N
A
D.1L1mol•L-1溴化铵水溶液中NH +与H+离子数之和大于N
4 A
【答案】C
【解析】A项,在标准状况下22.4L氟气的物质的量为1mol,其质子数为1mol×9×2×N =18N ,A正
A A
确;B项,碘蒸气与氢气发生的反应为:H(g)+I (g) 2HI(g),反应为可逆反应,有一定的限度,所以
2 2
充分反应,生成的碘化氢分子数小于2N ,B正确;C项,电解饱和食盐水时电极总反应为:2NaCl+2H O
A 2
2NaOH+H ↑+Cl↑,若阴阳两极产生气体分别是氢气与氯气,且物质的量之比为1:1,若气体的总质
2 2
量为73g,则说明反应生成的氢气与氯气的物质的量各自为1mol,根据关系式H 2e-可知,转移的电子数
2
为2N ,C错误;D项,1L1 mol·L-1溴化铵水溶液存在电荷守恒,即c(NH +)+c(H+)=c(Br-)+c(OH-),则物质
A 4
的量也满足n(NH +)+n(H+)=n(Br-)+n(OH-),因为n(Br-)=1L×1 mol·L-1=1 mol,所以该溶液中NH +与H+离子
4 4
数之和大于N ,D正确;故选C。
A
8.(2021•广东选择性考试)设N 为阿伏加德罗常数的值。下列说法正确的是
A
A.1molCHCl 含有C-Cl键的数目为3N
3 A
B.1L1.0mol·L-1的盐酸含有阴离子总数为2N
A
C.11.2LNO与11.2LO 混合后的分子数目为N
2 A
D.23g Na与足量HO反应生成的H 分子数目为N
2 2 A
【答案】A
【解析】A项,1个CHCl 分子中含有3个C-Cl键,微粒个数与物质的量成正比,故1molCHCl 含有
3 3
3molC-Cl键,C-Cl键的数目为3N ,A正确;B项,盐酸为氯化氢的水溶液,氯化氢会全部电离出阴离子
ACl-,水会部分电离出阴离子OH-,水的质量及电离程度未知,故无法计算1L1.0mol·L-1的盐酸含有阴离子
总数,B错误;C项,未提到具体的温度、压强(如标况下),故无法计算1.2LNO与1.2LO 混合后的分子数
2
目,C错误;D项,23g Na为1mol,钠与足量的水反应生成氢气的关系式为: 2 Na~H ,故1mol Na应对
2
应生成0.5mol H ,H 分子数目应为0.5N ,D错误;故选A。
2 2 A
9.(2021•天津卷)设N 为阿伏加德罗常数的值,下列叙述正确的是( )
A
A.1mol/LHCl溶液中,HCl分子的数目为N
A
B.22.4L氢气中,H 分子的数目为N
2 A
C.180g葡萄糖中,C原子的数目为6N
A
D.1molN 中,σ键的数目为3N
2 A
【答案】C
【解析】A项,体积未知,HCl分子的数目不能计算,故A错误;B项,没有标准状态,不能计算H
2
分子的数目,故B错误;C项,葡萄糖的分子式为C H O,故180g葡萄糖的分子的物质的量为1mol,C
6 12 6
原子的数目为6N ,故C正确;D项,1molN 中有2molσ键,故σ键的数目为2N ,故D错误;故选C。
A 2 A
10.(2021•湖北选择性考试) N 为阿伏加德罗常数的值。下列说法错误的是( )
A
A.23 g C HOH中sp3杂化的原子数为N
2 5 A
B.0.5 mol XeF 中氙的价层电子对数为3N
4 A
C.1 mol [Cu(H O) ]2+中配位键的个数为4N
2 4 A
D.标准状况下,11.2 L CO和H 的混合气体中分子数为0.5N
2 A
【答案】A
【解析】n(CHCHOH)=0.5 mol,乙醇分子中C、O原子都是采取sp3杂化,0.5 mol 乙醇含1 mol碳
3 2
原子、0.5 mol氧原子,故0.5 mol CH CHOH共含sp3杂化的原子为1.5 mol,A项错误;Xe原子价层有8
3 2
个电子,XeF 中Xe原子价层电子对数为=6,故0.5 mol XeF 中Xe的价层电子对为3 mol,B项正确;
4 4
HO中O原子是配位原子,1个氧原子只提供1个孤电子对形成配位键,故1mol [Cu(H O) ]2+含4 mol配位
2 2 4
键。标准状况下,11.2 L气体相当于0.5 mol,D项正确。
11.现有两种金属单质X和Y,取等物质的量的X、Y分别与足量稀硫酸完全反应,同温同压下产生
气体的体积分别为VmL、VmL。下列推断正确的是( )
1 2
A.参与反应的X、Y的质量之比为V:V
2 1
B.X、Y的摩尔质量之比为V:V
1 2
C.反应产物中X、Y对应元素的化合价之比为V:V
1 2
D.X、Y消耗稀硫酸的体积之比为2V:V
1 2【答案】C
【解析】设金属为M、化合价为n,金属与酸反应的离子方程式为2M+nH+=Mn++nH ↑。A项,设X和
2
Y的摩尔质量分别为M和N。化合价分别为a、b,由等物质的量的X、Y分别与足量稀硫酸完全反应,同
温同压下产生气体的体积分别为VmL、VmL可得参与反应的X、Y的质量之比为: ×M:
1 2
×N= : ,故A错误;B项,设等物质的量的X和Y的质量分别为m 和m,化合价分别为a、
1 2
b,由等物质的量的X、Y分别与足量稀硫酸完全反应,同温同压下产生气体的体积分别为VmL、VmL
1 2
可得X、Y的摩尔质量之比为: : ×N= : ,故B错误;C项,设化合价分别为a、
b,由等物质的量的X、Y分别与足量稀硫酸完全反应,同温同压下产生气体的体积分别为VmL、VmL
1 2
可得: = ,则a:b= V:V,故C正确;D项,硫酸的浓度未知,无法计算X、Y消耗稀硫
1 2
酸的体积之比,故D错误;故选C。
12.铁和铝都是用途广泛的金属,同温、同压下,将 铁与足量稀硫酸反应,生成 体积为 ;
将 铝与足量浓氢氧化钠溶液反应,生成 体积为 。下列说法正确的是( )
A.两反应生成 的物质的量之比为
B. 铁与足量稀硫酸反应,生成 的物质的量一定为
C.保持温度压强不变,将 铝与足量稀硫酸反应,生成 体积大于
D.参加反应的铁与铝的质量比【答案】A
【解析】A项,同温、同压下,气体的物质的量之比等于体积之比,故两反应生成H 的物质的量之比
2
为 ,故A正确;B项,不知道温度和压强的具体值,也就不知道气体摩尔体积,故无法计算H 的物质
2
的量,故B错误;C项,Al都被反应完,Al的质量不变,产生H 的量也不变,故C错误;D项,根据关
2
系式:Fe~H ,Fe的物质的量=氢气的物质的量= ;根据关系式:2Al~3H ,Al的物质的量= 氢气的物
2 2
质的量= ;有 , ,故D错误。故选A。
13.某混合物X由Al O、Fe O、Cu、SiO 中的一种或几种物质组成,某校课外兴趣小组设计如图实
2 3 2 3 2
验方案进行探究:
途径a:
途径b:
下列对混合物X成分的分析正确的是( )
A.Cu的质量为1.92g B.Fe O 的质量为3.2g
2 3
C.Al O 的质量为3g D.SiO 的质量为4.92g
2 3 2
【答案】B
【解析】途径a得到的4.92 g固体部分溶于NaOH溶液,说明X中含有二氧化硅,且m(SiO )=4.92
2
g-1.92 g=3 g,剩余的1.92 g固体为单质铜,又途径a加入过量盐酸时得到蓝色溶液,则发生反应
Fe O+6H+ =2Fe3+ +3H O、Cu十2Fe3+=2Fe2+ +Cu2+,铜有剩余,说明Fe3+全部转化为Fe2+,则加入过量盐
2 3 2
酸时发生的反应可写成Fe O+6H+ +Cu=2Fe2++Cu2++3H O。途径b溶于NaOH溶液的固体质量为9.4 g-6.4
2 3 2
g=3 g,说明X中不含Al O;6.4 g固体为Fe O、Cu 的混合物,加入过量盐酸发生反应Fe O+6H+
2 3 2 3 2 3+Cu=2Fe2++Cu2++3H O,剩余1.92 g Cu,故Fe O 的质量为 ,Cu的质量为6.4
2 2 3
g-3.2 g=3.2 g。A项,由分析可知Cu的质量为3.2g,A错误;B项,由分析可知Fe O 的质量为3.2g,B正
2 3
确;C项,由分析可知X中不含Al O,C错误;D项,由分析可知SiO 的质量为3g,D错误;故选B。
2 3 2
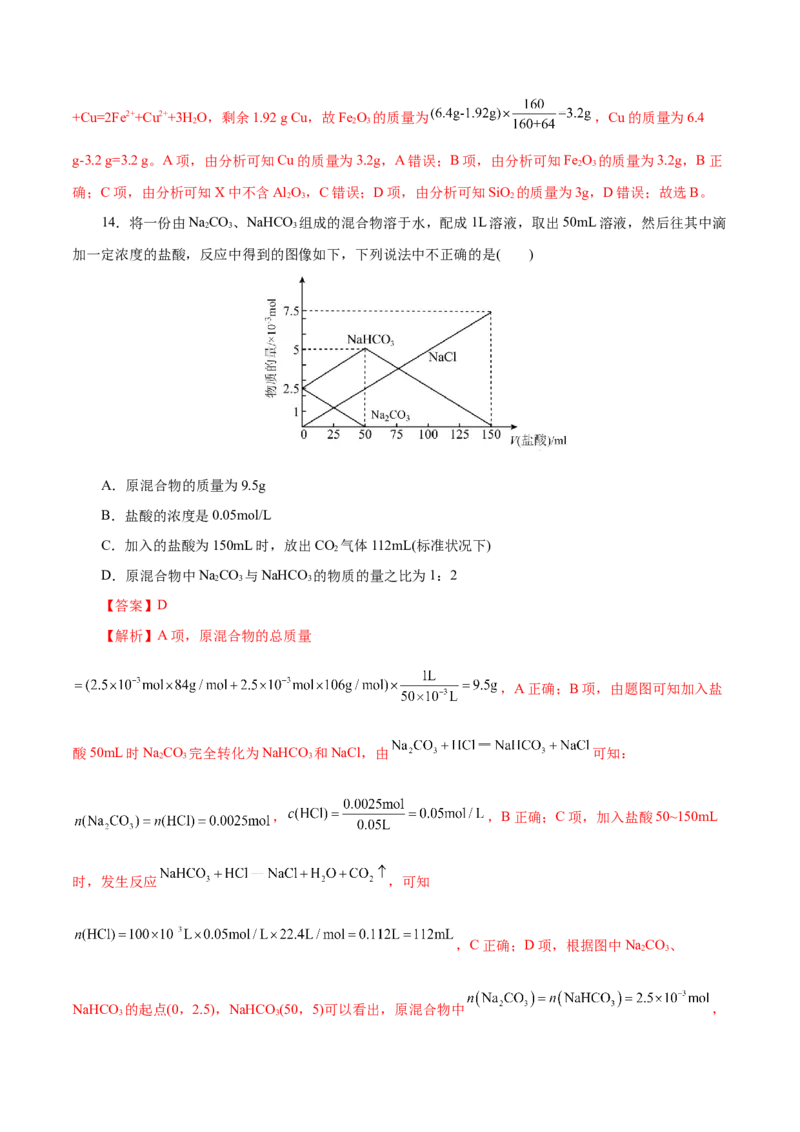
14.将一份由NaCO、NaHCO 组成的混合物溶于水,配成1L溶液,取出50mL溶液,然后往其中滴
2 3 3
加一定浓度的盐酸,反应中得到的图像如下,下列说法中不正确的是( )
A.原混合物的质量为9.5g
B.盐酸的浓度是0.05mol/L
C.加入的盐酸为150mL时,放出CO 气体112mL(标准状况下)
2
D.原混合物中NaCO 与NaHCO 的物质的量之比为1:2
2 3 3
【答案】D
【解析】A项,原混合物的总质量
,A正确;B项,由题图可知加入盐
酸50mL时NaCO 完全转化为NaHCO 和NaCl,由 可知:
2 3 3
, ,B正确;C项,加入盐酸50~150mL
时,发生反应 ,可知
,C正确;D项,根据图中NaCO、
2 3
NaHCO 的起点(0,2.5),NaHCO (50,5)可以看出,原混合物中 ,
3 3故NaCO 与NaHCO 的物质的量之比为1:1,D错误;故选D。
2 3 3