文档内容
第二章 化学物质及其变化
第06讲 氧化还原反应(精练)
完卷时间:50分钟
可能用到的相对原子质量:N 14 O 16 Mg 24 Mn 55 Cu 64 Zn 65
一、选择题(每小题只有一个正确选项,共12*5分)
1.(2021·浙江高考真题)关于反应8NH+6NO=7N+12HO,下列说法正确的是
3 2 2 2
A.NH 中H元素被氧化
3
B.NO 在反应过程中失去电子
2
C.还原剂与氧化剂的物质的量之比为3:4
D.氧化产物与还原产物的质量之比为4:3
【答案】D
【解析】由反应8NH+6NO==7N+12HO可知,其中NH 的N元素的化合价由-3升高到0、NO 中的N元素的化
3 2 2 2 3 2
合价由-+4降低到0,因此,NH 是还原剂, NO 是氧化剂。
3 2
A.NH 中H元素的化合价没有发生变化,故其未被氧化,被氧化的是N元素,A不正确;B.NO 在反应过程
3 2
中得到电子,B不正确;C.该反应中,NH 是还原剂,NO 是氧化剂。由化学方程式可知,还原剂与氧化剂
3 2
的物质的量之比为4:3,C说法不正确;D.该反应中氧化产物和还原产物均为N。还原剂被氧化后得到氧
2
化产物,氧化剂被还原后得到还原产物,还原剂与氧化剂的物质的量之比为4:3,因此,氧化产物与还原
产物的质量之比为4:3 ,D说法正确。
综上所述,本题选D。
2.(2021·江苏常州市·高三二模)燃煤和工业生产中产生的 过量排放会形成酸雨。 是重要的
化工原料,可作漂白剂。在接触法制硫酸的工业中, 发生的反应为:
。下列关于 的说法正确的是
A. 分子呈直线形,是非极性分子
B. 的水溶液能导电, 是电解质
C. 和 反应,每生成1mol S,转移的电子数为2mol
D.用石灰石浆液吸收烟气中的 ,可减少酸雨的形成,最终转化为石膏【答案】D
【解析】A. 的价层电子对数为2+ (6-2 2)=3,且有一对孤对电子,构型为V形,是极性分子,故
A错误;B. 的水溶液能导电是因为和水反应生成了亚硫酸, 是非电解质,故B错误;C. 和
反应生成S单质,S元素由+4价下降到0价,又由-2价上升到0价,方程式为:2HS +
2
SO=3S↓+2HO,每生成1mol S,转移的电子数为 mol,故C错误;D.石灰石浆吸收废气中的二氧化硫的
2 2
化学方程式为:2CaCO+2SO+O═2CaSO+2CO,可减少酸雨的形成,最终转化为石膏,故D正确;故选D。
3 2 2 4 2
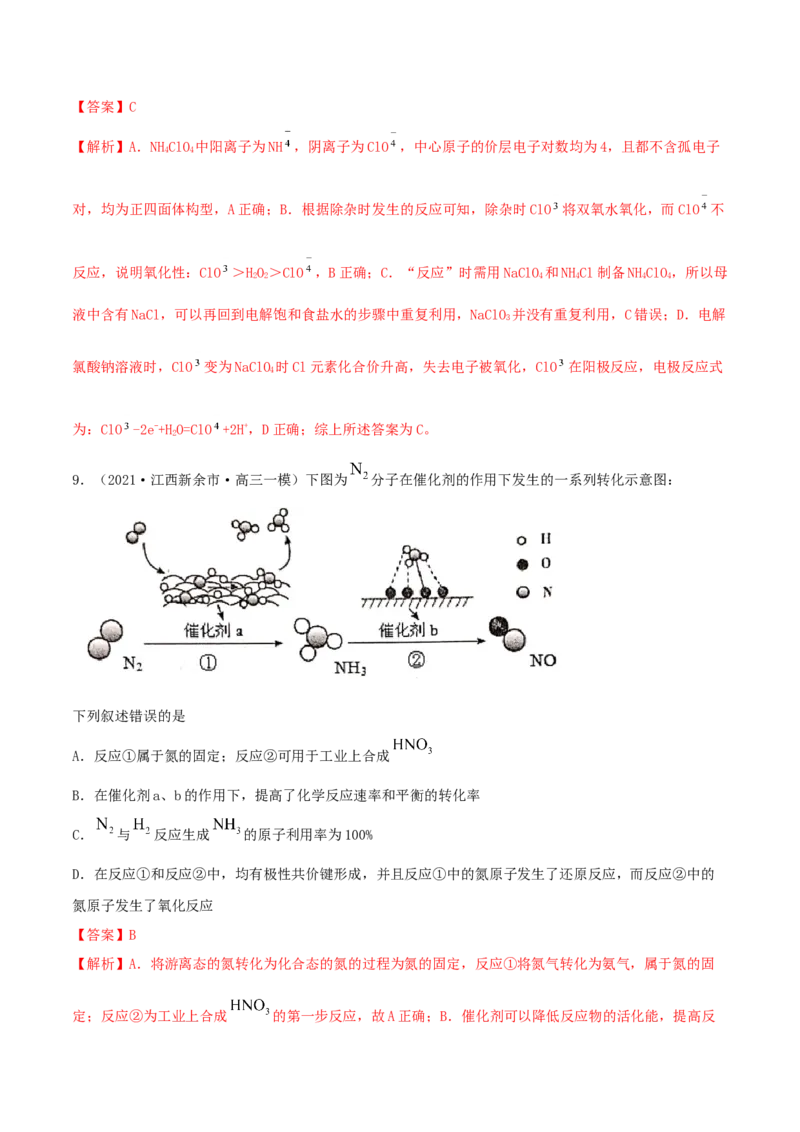
3.(2021·山东潍坊市·高三二模)光催化甲烷重整技术利用太阳光作为反应动力。以 为载
体,激发产生电子(e-)—空穴(h+),反应机理如图所示。下列说法错误的是
A.该催化重整过程中,C原子的成键数目不变
B. 在 上发生还原反应
C.在 表面,每生成 ,向空穴转移电子数为
D.该反应可表示为
【答案】A
【解析】A. 的结构式为O=C=O,甲烷与 中C原子成键数均为4,CO的结构式为C O,C原子成键数位3,C原子的成键数目改变,故A错误;B.在Rh上 →CO,C元素的化合价降低,发生还原反应,
故B正确;C.在 表面, ,每生成 ,向空穴转移电子数为 ,
故C正确;D.在 上 + ,结合C选项解析得该反应可表示为
,故D正确;故选A。
4.(2021·天津河西区·高三二模)工业上将NH 和NO在催化剂表面转化为N 和HO的反应进程中相对能
3 2 2
量变化如下图所示。下列说法正确的是
A.NHNO是该反应的催化剂
2
B.总反应中n(氧化剂)∶n(还原剂)=2∶3
C.平衡后当升高温度时,总反应v <v
(正) (逆)
D.H的移除过程因相对能量较低,故此步反应速率很快
【答案】C
【解析】A.观察相对能量-反应进程曲线可知,NH 吸附在催化剂表面后,经过一定的反应形成NHNO,
3 2
NHNO又经过反应得到N 和HO,所以NHNO是该反应过程的活性中间体,而不是催化剂。A项错误;B.由
2 2 2 2
题中:NH 和NO在催化剂表面转化为N 和HO,可知总反应方程式为6NO+4NH 5N+6HO。其中,
3 2 2 3 2 2
NO中N元素的化合价由+2价变为0价,化合价降低,NO作氧化剂。NH 中N元素的化合价由-3价变为0价,
3
化合价升高,NH 作还原剂,由总反应可知,n(氧化剂)∶n(还原剂)=3∶2,B项错误;C.由曲线图可
3
知,起始相对能量高于终态,说明这是一个放热反应,升高温度平衡向逆反应反向移动。所以平衡后,升
高温度,正反应速率的增大程度小于逆反应速率的增大程度,总反应v <v ,C项正确;D.相对能
(正) (逆)量-反应进程曲线表明,全过程只有H的移除过程相对能量逐渐升高,这是一个需要吸收能量越过能垒的反
应,其速率是全过程中几个反应中最慢的,D项错误;答案选C。
5.(2021·山东德州市·高三二模)为探究某些硫的含氧酸盐的部分性质,进行如下实验,并记录实验
现象:
①测得0.01mol·L-1NaHSO 溶液的pH约为5。
3
②向0.01mol·L-1NaHSO 溶液中滴加少量酸性KMnO 溶液,溶液的紫红色褪去。
3 4
③向0.1mol·L-1NaSO 溶液中滴加稀盐酸,产生无色刺激性气味的气体,且出现淡黄色沉淀。
2 2 3
④在Ag+催化条件下,向0.1mol·L-1KSO 无色溶液中滴加MnSO 溶液,溶液变为紫红色。
2 2 8 4
由上述实验现象得出的结论不合理是
A.实验①说明:K(HSO)·K(HSO)HIO
3 3
d.氯化钠、碘化钠与浓硫酸共热,分别生成氯化氢、单质碘
(5)检验亚硫酸钠固体是否氧化变质的方法是___________。【答案】(每空2分)(1)2,5,3,2,1,1
(2)IO +5I-+6H+→3I+3HO 5:1 (3)分子间作用力(范德华力) (4) bd (5)取样溶于水,加入
2 2
过量盐酸后,再加氯化钡,产生白色沉淀则已变质,若无白色沉淀生成,则未变质
【解析】(1)根据氧化还原反应的配平原则,先分析各物质化合价的升降变化,I从+5价降低到0价,至少
转移10个电子,S元素从+4升高到+6至少转移2个电子,则NaIO 与NaHSO 的化学计量数之比为2:5,再
3 3
结合原子守恒规律配平该化学方程式为:2NaIO+5NaHSO=3NaHSO+2NaSO+I+HO,用单线桥可表示出电子
3 3 4 2 4 2 2
转移的方向和数目如下: ,故答案为:2,5,3,2,1,1; ;
(2)第二步反应有碘单质生成,第(1)问总反应的离子方程式为:②2IO +5HSO →3H++5SO +I+HO,则根
2 2
据第一步反应①IO +3HSO →3SO +I-+3H+可看出HSO 已经被氧化为SO ,第二步不需要HSO ,则② 3-
① 5消去HSO 得到第二步离子方程式为:IO +5I-+6H+→3I+3HO;从第二步可看出,最终要得到3mol
2 2
I,其中第一步提供5mol IO 转化为第二步所需的I-,因此若要使碘酸钠的利用率最高,IO 完全反应完,
2
即碘酸钠在第一步和第二步反应中的用量之比是5:1,故答案为:IO +5I-+6H+→3I+3HO;5:1;
2 2
(3)碘升华为物理变化,没有化学键的断裂,因此克服的微粒间作用力为分子间作用力,故答案为:分子
间作用力(范德华力);
(4) a.原子的最外层电子数目不能决定元素的非金属性强弱,故a错误;b.ICl中碘元素为+1价,说明
Cl更易容易得到电子,非金属性更强,故b正确;c.酸性:HClO>HIO,不是最高价氧化物对应水化物的
3 3
酸性,所以无法判断非金属性,故c错误;d.氯化钠与浓硫酸共热制备氯化氢,利用的是高沸点酸制备低
沸点酸的原理,氯化碘与浓硫酸共热可制备碘单质,这说明碘离子更易被氧化,其还原性比氯离子的更强,
所以氯气的氧化性强于碘单质的氧化性,即可说明氯、碘两种元素非金属性得相对强弱,故d正确;
故答案为:bd;
(5)亚硫酸钠固体容易被空气氧化为硫酸钠,若检验是否变质,主要检验溶于水后是否存在硫酸根离子,
其方法如下:取样溶于水,加入过量盐酸后,再加氯化钡,产生白色沉淀则已变质,若无白色沉淀生成,
则未变质。14.(2021·陕西安康市·高三一模)(14分)SO 在生产、生活中具有重要的作用,据所学知识回答相
2
关问题。
(1) SO 通入NaCO 溶液中有CO 生成,说明HSO 具有___________(填“酸性”、“氧化性”、“还原性”
2 2 3 2 2 3
或“漂白性”,下同),SO 通入品红溶液中,品红溶液褪色,说明SO 具有___________。
2 2
(2)已知SO 通入FeCl 溶液会发生反应,还原产物为___________(填化学式,下同),氧化产物为
2 3
___________。
(3)向含锌粉的悬浊液中通入SO 可制备ZnSO
2 2 4。
①该反应的化学方程式为___________,若反应中有0.1mol电子转移,则生成ZnSO___________g。
2 4
②向反应后的溶液中加入过量盐酸,溶液出现黄色浑浊,且有刺激性气体产生,反应的化学方程式为
___________。
(4)已知室温下,ZnSO 微溶于水,Zn(HSO) 易溶于水。ZnO水悬浊液常用于吸收烟气中的SO。向ZnO水悬
3 3 2 2
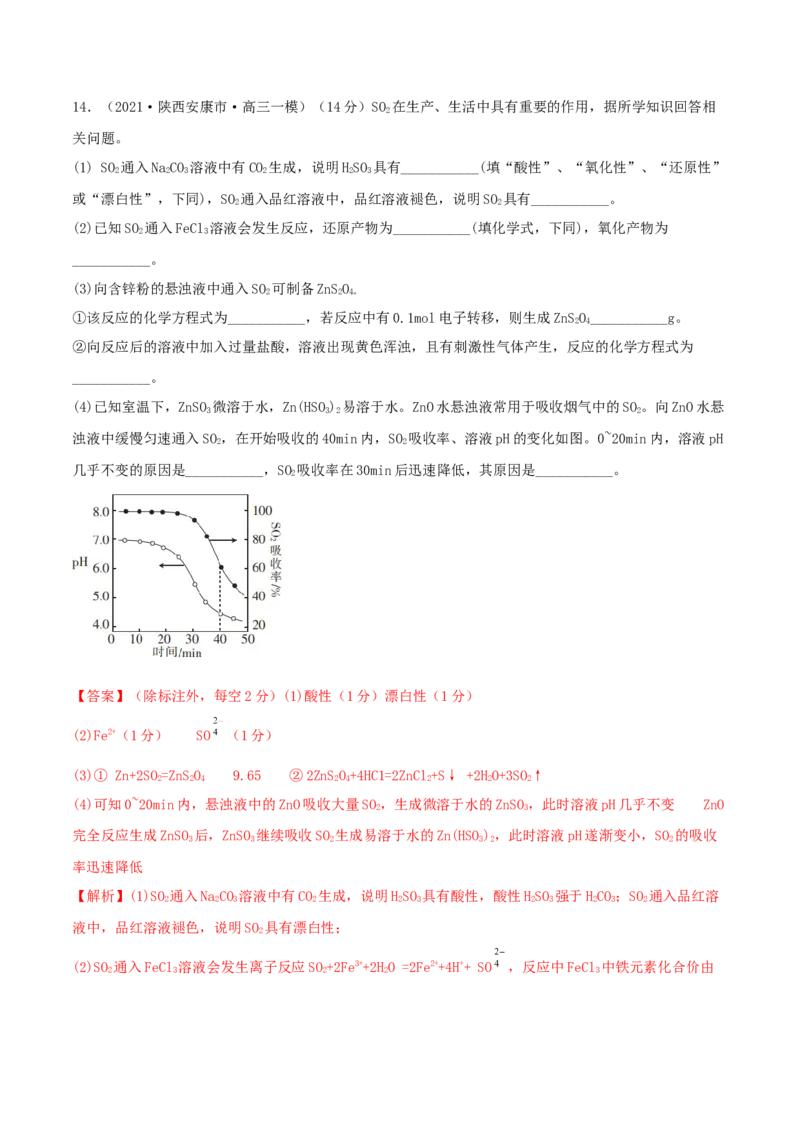
浊液中缓慢匀速通入SO,在开始吸收的40min内,SO 吸收率、溶液pH的变化如图。0~20min内,溶液pH
2 2
几乎不变的原因是___________,SO 吸收率在30min后迅速降低,其原因是___________。
2
【答案】(除标注外,每空2分)(1)酸性(1分)漂白性(1分)
(2)Fe2+(1分) SO (1分)
(3)① Zn+2SO=ZnSO 9.65 ②2ZnSO+4HC1=2ZnCl+S↓ +2HO+3SO↑
2 2 4 2 4 2 2 2
(4)可知0~20min内,悬浊液中的ZnO吸收大量SO,生成微溶于水的ZnSO,此时溶液pH几乎不变 ZnO
2 3
完全反应生成ZnSO 后,ZnSO 继续吸收SO 生成易溶于水的Zn(HSO),此时溶液pH遂渐变小,SO 的吸收
3 3 2 3 2 2
率迅速降低
【解析】(1)SO 通入NaCO 溶液中有CO 生成,说明HSO 具有酸性,酸性HSO 强于HCO;SO 通入品红溶
2 2 3 2 2 3 2 3 2 3 2
液中,品红溶液褪色,说明SO 具有漂白性;
2
(2)SO 通入FeCl 溶液会发生离子反应SO+2Fe3++2HO =2Fe2++4H++ SO ,反应中FeCl 中铁元素化合价由
2 3 2 2 3+3价降为+2价被还原,生成Fe2+,则还原产物为Fe2+;SO 中硫元素化合价由+4价升为+6价,生成SO ,
2
则氧化产物为SO ;
(3)①向含锌粉的悬浊液中通入SO 可制备ZnSO,根据元素守恒可知发生反应的化学方程式为
2 2 4
Zn+2SO=ZnSO;当该反应中有0.1mol电子转移时,则生成0.05molZnSO,质量为0.05mol ×193g/
2 2 4 2 4
mol=9.65g;
②向反应后的溶液中加入过量盐酸,溶液出现黄色浑浊,且有刺激性气体产生,则生成硫单质和二氧化硫,
根据氧化还原反应配平可得反应的化学方程式为2ZnSO+4HCl=2ZnCl+S↓ +2HO+3SO↑;
2 4 2 2 2
(4)根据图中信息可知0~20min内,悬浊液中的ZnO吸收大量SO,生成微溶于水的ZnSO,此时溶液pH几
2 3
乎不变;一旦ZnO完全反应生成ZnSO 后,ZnSO 继续吸收SO 生成易溶于水的Zn(HSO),此时溶液pH遂渐
3 3 2 3 2
变小,SO 的吸收率迅速降低。
2
15.(2021·北京丰台区·高三一模)(12分)锰广泛存在于自然界中,工业可用软锰矿(主要成分是
MnO)制备锰。
2
资料:①MnCO 难溶于水,可溶于稀酸。
3
②在Mn2+催化下,SO 在水溶液中被氧化成HSO。
2 2 4
I.制备
(1)写出铝热法还原MnO 制备锰的化学方程式_______。
2
(2)工业上制备锰时,会产生大量废水和锰渣。锰渣煅烧会产生含高浓度SO 的烟气,可用以下方法处理。
2
处理方法一:
①用软锰矿进行脱硫可生成硫酸锰,从而达到资源的循环使用。写出一定条件下利用MnO 进行脱硫的化学
2
方程式_______。
②研究表明,用Fe2+/Fe3+可强化脱硫效果,其过程如下所示:
过程I:……
过程II :2Fe3++SO+2HO=2Fe2++ +4H+
2 2
过程I的离子方程式是_______。
处理方法二:③用MnCO 进行脱硫,可提高脱硫率。结合化学用语解释原因:_______。
3
II.废水中锰含量的测定
(3)取1 mL废水置于20 mL磷酸介质中,加入HClO ,将溶液中的Mn2+氧化为Mn3+,用c mol/L (NH)
4 4 2
Fe(SO) 溶液进行滴定,达到滴定终点时,滴定管刻度由VmL变为V mL,废水中锰的含量为____ g/mL。
4 2 0 1
【答案】(除标注外,每空2分)(1)4Al+3MnO 3Mn+2AlO
2 2 3
(2)① MnO+SO MnSO ②2Fe2++MnO+4H+=Mn2++2Fe3++2HO
2 2 4 2 2
③溶液中存在平衡:MnCO(s)=Mn2+(aq)+ (aq), 消耗溶液中的H+,促进SO 溶解:
3 2
SO+HO HSO,HSO H++ 生成Mn2+有催化作用,可促进反应2SO+O+2HO 2HSO 发生(3分)
2 2 ⇌ 2 3 2 3⇌ 2 2 2 2 4
(3)55 c(V-V)×10-3 (3分)
1 0
【解析】(1)铝热法还原MnO 制备锰即高温条件下铝单质和MnO 反应得到氧化铝和Mn单质,化学方程式为
2 2
4Al+3MnO 3Mn+2AlO;
2 2 3
(2)①根据题意可知MnO 会将SO 氧化得到MnSO,化学方程式应为MnO+SO MnSO;
2 2 4 2 2 4
②据图可知过程I中MnO 被Fe2+还原生成Mn2+,Fe2+被氧化为Fe3+,根据电子守恒和元素守恒可得离子方程
2
式为2Fe2++MnO+4H+=Mn2++2Fe3++2HO;
2 2
③溶液中存在平衡:MnCO(s)=Mn2+(aq)+ (aq), 消耗溶液中的H+,促进SO 溶解:
3 2
SO+HO HSO,HSO H++ ,同时生成的Mn2+有催化作用,可促进反应2SO+O+2HO 2HSO 发生;
2 2 ⇌ 2 3 2 3⇌ 2 2 2 2 4
(3)滴定时发生反应Fe2++Mn3+=Fe3++Mn2+,所以n(Mn)=c(V-V)×10-3mol,所取废水为1mL,所以废水中锰的
1 0
含量为55 c(V-V)×10-3g/mL。
1 0