文档内容
第 07 讲 钠及其重要化合物
第一部分:高考真题感悟
1.(2022·山东·高考真题)实验室用基准 配制标准溶液并标定盐酸浓度,应选甲基橙为指示剂,
并以盐酸滴定 标准溶液。下列说法错误的是
A.可用量筒量取 标准溶液置于锥形瓶中
B.应选用配带塑料塞的容量瓶配制 标准溶液
C.应选用烧杯而非称量纸称量 固体
D.达到滴定终点时溶液显橙色
2.(2009·全国·高考真题)为了检验某含有NaHCO 杂质的NaCO 样品的纯度,现将w g 样品加热,其
3 2 3 1
质量变为w g ,则该样品的纯度(质量分数)是
2
A. B. C. D.
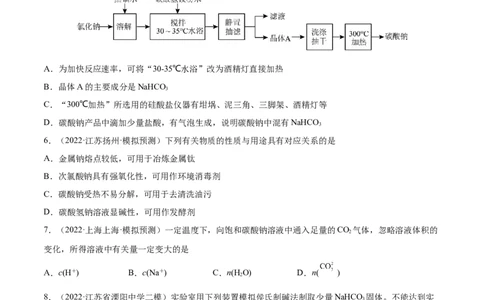
3.(2016·江苏·高考真题)根据侯氏制碱原理制备少量NaHCO 的实验,经过制取氨气、制取NaHCO 、
3 3
分离NaHCO 、干燥NaHCO 四个步骤,下列图示装置和原理能达到实验目的的是
3 3
A. 制取氨气 B. 制取碳酸氢钠
C. 分离碳酸氢钠 D. 干燥碳酸氢钠
4.(2011·北京·高考真题)下列实验方案中,不能测定NaCO 和NaHCO 混合物中NaCO 质量分数的是
2 3 3 2 3A.取a克混合物与足量稀硫酸充分反应,逸出气体用碱石灰吸收,增重b克
B.取a克混合物与足量稀盐酸充分反应,加热、蒸干、灼烧,得b克固体
C.取a克混合物充分加热,减重b克
D.取a克混合物与足量Ba(OH) 溶液充分反应,过滤、洗涤、烘干,得b克固体
2
5.(2007·全国·高考真题)在一定条件下,将钠与氧气反应的生成物1.5g溶于水,所得溶液恰好能被
80mL浓度为0.50mol/L的HCl溶液中和,则该生成物的成分是
A.NaO B.NaO C.NaO和NaO D.NaO 和NaO
2 2 2 2 2 2 2 2 2
第二部分:最新模拟精练
完卷时间:50分钟
一、选择题(每小题只有一个正确选项,共12*5分)
1.(2022·上海·模拟预测)16.8g由NaCO 和NaOH组成的混合物与200g质量分数为7.3%的盐酸恰好反
2 3
应,蒸干反应后的溶液,最终得到的固体质量为
A.8g B.15.5g C.11.7g D.23.4g
2.(2022·北京·模拟预测)下列过程不涉及氧化还原反应的是
A.电解熔融氯化钠制备金属钠 B.用氯气制消毒液
C.过氧化钠做供氧剂 D.用NaHCO 治疗胃酸过多
3
3.(2022·辽宁·抚顺市第二中学模拟预测)以NaCl为原料,可制取Na、NaO、NaOH和NaCO 等。
2 2 2 3
NaCO,可用侯氏制碱法制取,主要涉及如下反应:
2 3
N(g)+3H(g) 2NH (g) ΔH=-92.4kJ·mol-1
2 2 3
NaCl+NH +CO +H O=NaHCO ↓+NHCl
3 2 2 3 4
2NaHCO NaCO+CO ↑+H O
3 2 3 2 2
在指定条件下,下列选项所示的物质间转化不能实现的是
A.Na(s) NaO(s) B.NaO(s) NaCO(s)
2 2 2 2 2 3
C.NaCl(aq) Cl(g) D.NaOH(aq) Al(OH) (s)
2 3
4.(2022·重庆·三模)下列关于钠及其化合物的说法正确的是
A. 与 都具有强还原性B. 和 长期露置于空气中最终产物不相同
C.将足量的 、 和 分别加入含有酚酞的水中,最终溶液均变为红色
D.将少量 和 分别投入 溶液中,均既有沉淀生成又有气体放出
5.(2022·湖北黄冈·模拟预测)碳酸钠俗称纯碱,是一种重要的化工原料。以碳酸氢铵和氯化钠为原料制
备碳酸钠的流程如图所示。下列说法正确的是
A.为加快反应速率,可将“30-35℃水浴”改为酒精灯直接加热
B.晶体A的主要成分是NaHCO
3
C.“300℃加热”所选用的硅酸盐仪器有坩埚、泥三角、三脚架、酒精灯等
D.碳酸钠产品中滴加少量盐酸,有气泡生成,说明碳酸钠中混有NaHCO
3
6.(2022·江苏扬州·模拟预测)下列有关物质的性质与用途具有对应关系的是
A.金属钠熔点较低,可用于冶炼金属钛
B.次氯酸钠具有强氧化性,可用作环境消毒剂
C.碳酸钠受热不易分解,可用于去清洗油污
D.碳酸氢钠溶液显碱性,可用作发酵剂
7.(2022·上海上海·模拟预测)一定温度下,向饱和碳酸钠溶液中通入足量的CO 气体,忽略溶液体积的
2
变化,所得溶液中有关量一定变大的是
A.c(H+) B.c(Na+) C.n(H O) D.n( )
2
8.(2022·江苏省溧阳中学二模)实验室用下列装置模拟侯氏制碱法制取少量NaHCO 固体。不能达到实
3
验目的的是
A.装置Ⅰ制取CO
2B.装置Ⅱ中NaCO 溶液可除去CO 中的少量HCl
2 3 2
C.装置Ⅲ中冰水浴有利于析出NaHCO 固体
3
D.装置Ⅳ可获得少量NaHCO 固体
3
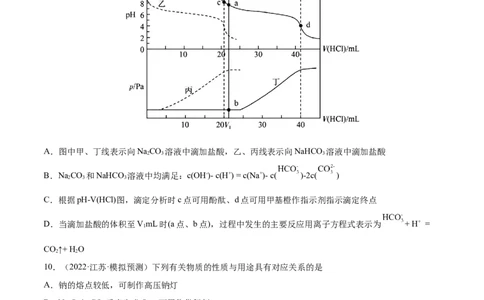
9.(2022·四川·树德中学模拟预测)某同学在两个相同的特制容器中分别加入20 mL 0.4 mol·L-1NaCO 溶
2 3
液和40 mL 0.2 mol·L-1NaHCO 溶液,再分别用0.4 mol·L-1盐酸滴定,用pH计和压力传感器检测,得到如
3
下曲线,下列说法不正确的是
A.图中甲、丁线表示向NaCO 溶液中滴加盐酸,乙、丙线表示向NaHCO 溶液中滴加盐酸
2 3 3
B.NaCO 和NaHCO 溶液中均满足:c(OH-)- c(H+) = c(Na+)- c( )-2c( )
2 3 3
C.根据pH-V(HCl)图,滴定分析时c点可用酚酞、d点可用甲基橙作指示剂指示滴定终点
D.当滴加盐酸的体积至VmL时(a点、b点),过程中发生的主要反应用离子方程式表示为 + H+ =
1
CO↑+ H O
2 2
10.(2022·江苏·模拟预测)下列有关物质的性质与用途具有对应关系的是
A.钠的熔点较低,可制作高压钠灯
B.NaO 与CO 反应生成O,可用作供氧剂
2 2 2 2
C.NaOH固体易潮解,可用于吸收SO
2
D.NaHCO 能溶于水,可用于治疗胃酸过多
3
11.(2022·江苏泰州·一模)下列有关钠及其化合物的性质与用途具有对应关系的是
A.Na具有强还原性,可用于冶炼金属钛
B.NaOH具有强碱性,可用作干燥剂
C.NaO 具有强氧化性,可用作呼吸面具供氧剂
2 2
D.NaS具有还原性,可用于除去工业废水中的Hg2+
212.(2022·陕西·长安一中模拟预测)向100mLNaOH溶液中通入一定量的CO 气体,充分反应后,再向
2
所得溶液中逐滴加入0.2mol/L的盐酸,产生CO 的体积与所加盐酸体积之间关系如图所示。下列判断正确
2
的是
A.原NaOH溶液的浓度为0.2mol/L
B.通入CO 的体积为448mL
2
C.所得溶液的溶质成分的物质的量之比为n(NaOH):n(Na CO)=1:3
2 3
D.所得溶液溶质成分的物质的量之比为n(NaHCO ):n(Na CO)=1:1
3 2 3
13.(2022·江苏·模拟预测)下列选项所示的物质间转化均能实现的是
A.
B.
C.
D.
14.(2022·江苏江苏·三模)下列有关物质的性质与用途具有对应关系的是
A.NaHCO 受热易分解,可用于治疗胃酸过多
3
B.NaOH具有吸湿性,可用于干燥NH
3
C.NaSO 具有还原性,可用于吸收含SO 的尾气
2 3 2
D.NaCO 能与酸反应,可用于去除油脂
2 3
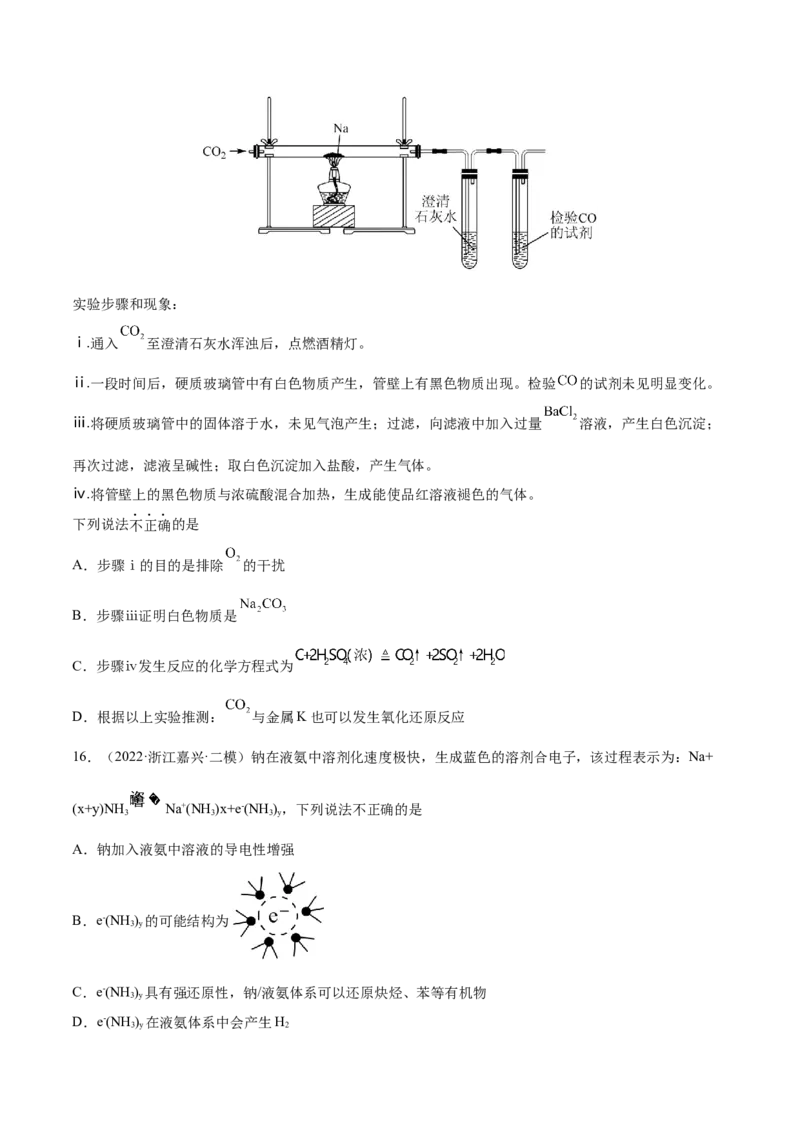
15.(2022·北京·101中学三模)实验小组研究 与 的反应,装置、步骤和现象如下:实验步骤和现象:
ⅰ.通入 至澄清石灰水浑浊后,点燃酒精灯。
ⅱ.一段时间后,硬质玻璃管中有白色物质产生,管壁上有黑色物质出现。检验 的试剂未见明显变化。
ⅲ.将硬质玻璃管中的固体溶于水,未见气泡产生;过滤,向滤液中加入过量 溶液,产生白色沉淀;
再次过滤,滤液呈碱性;取白色沉淀加入盐酸,产生气体。
ⅳ.将管壁上的黑色物质与浓硫酸混合加热,生成能使品红溶液褪色的气体。
下列说法不正确的是
A.步骤ⅰ的目的是排除 的干扰
B.步骤ⅲ证明白色物质是
C.步骤ⅳ发生反应的化学方程式为
D.根据以上实验推测: 与金属K也可以发生氧化还原反应
16.(2022·浙江嘉兴·二模)钠在液氨中溶剂化速度极快,生成蓝色的溶剂合电子,该过程表示为:Na+
(x+y)NH Na+(NH )x+e-(NH ),下列说法不正确的是
3 3 3 y
A.钠加入液氨中溶液的导电性增强
B.e-(NH ) 的可能结构为
3 y
C.e-(NH ) 具有强还原性,钠/液氨体系可以还原炔烃、苯等有机物
3 y
D.e-(NH ) 在液氨体系中会产生H
3 y 2二、主观题(共3小题,共40分)
13.(2021·河南信阳市·高三零模)(16分)大苏打 、苏打、小苏打被称为“苏氏三兄
弟”。它们在生活、生产中有广泛应用。
(1)工业上,将 和 以 的物质的量之比配成溶液。再通入 可制取 ,同时放出
,写出该反应的化学方程___________。 溶液在空气中久置,会生成浅黄色物质,经测定该物
质具有与过氧化钠相似的结构,该物质的电子式为___________。
(2) 标准溶液常用于滴定碘的含量,若滴定的溶液呈酸性,测定结果会偏高。用离子方程式表示
其原因___________。
(3)下列关于苏打和小苏打的说法正确的是___________(选填字母序号)。
A.纯碱是一种重要的化工原料,在玻璃、肥皂、造纸等工业中都有重要的应用
B.苏打和小苏打的相互转化属于可逆反应
C.苏打(含氯化钠杂质)可用滴定法测苏打的质量分数,使用石蕊溶液做指示剂更准确
D.牙膏中加入小苏打可以让小苏打颗粒直接摩擦牙齿,帮助清洁牙垢
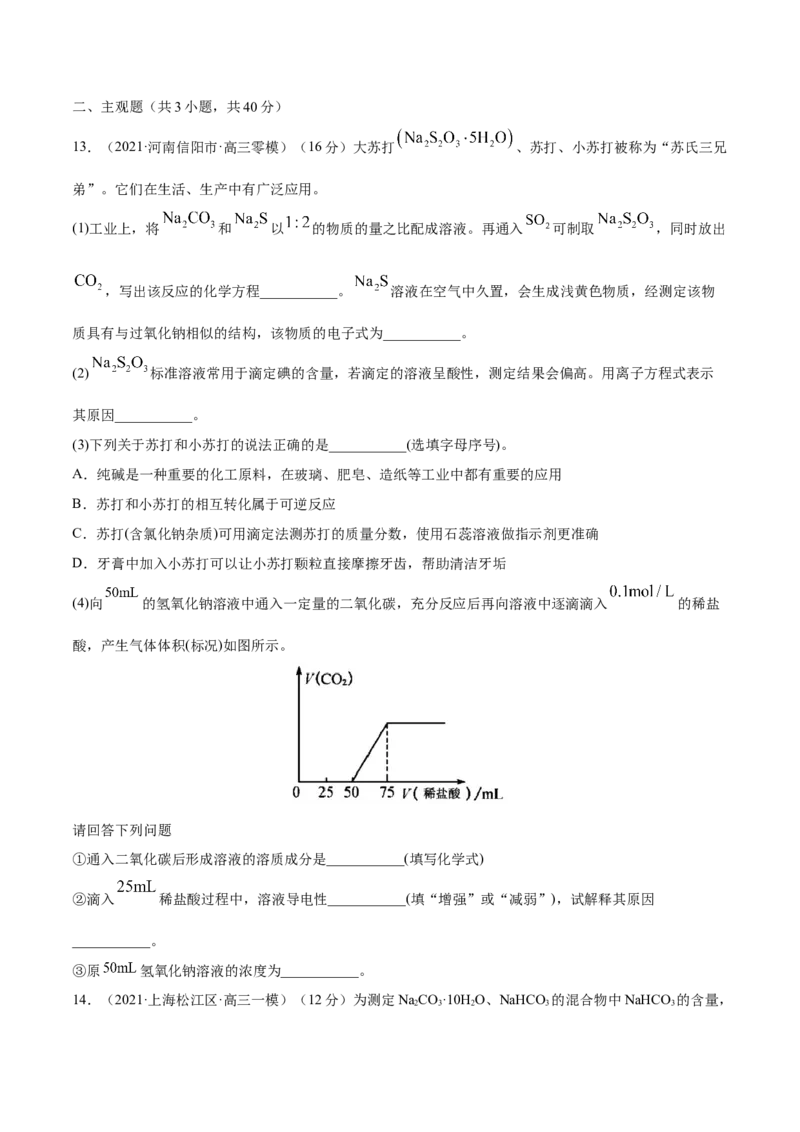
(4)向 的氢氧化钠溶液中通入一定量的二氧化碳,充分反应后再向溶液中逐滴滴入 的稀盐
酸,产生气体体积(标况)如图所示。
请回答下列问题
①通入二氧化碳后形成溶液的溶质成分是___________(填写化学式)
②滴入 稀盐酸过程中,溶液导电性___________(填“增强”或“减弱”),试解释其原因
___________。
③原 氢氧化钠溶液的浓度为___________。
14.(2021·上海松江区·高三一模)(12分)为测定NaCO·10H O、NaHCO 的混合物中NaHCO 的含量,
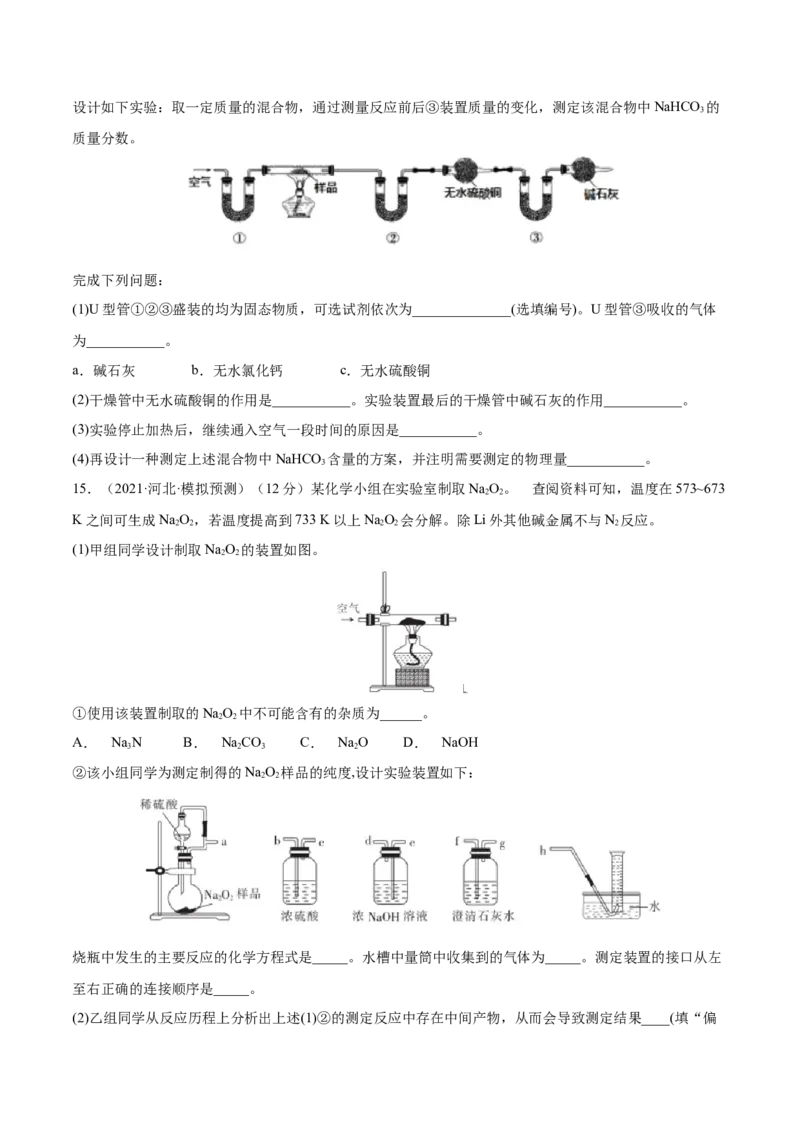
2 3 2 3 3设计如下实验:取一定质量的混合物,通过测量反应前后③装置质量的变化,测定该混合物中NaHCO 的
3
质量分数。
完成下列问题:
(1)U型管①②③盛装的均为固态物质,可选试剂依次为______________(选填编号)。U型管③吸收的气体
为___________。
a.碱石灰 b.无水氯化钙 c.无水硫酸铜
(2)干燥管中无水硫酸铜的作用是___________。实验装置最后的干燥管中碱石灰的作用___________。
(3)实验停止加热后,继续通入空气一段时间的原因是___________。
(4)再设计一种测定上述混合物中NaHCO 含量的方案,并注明需要测定的物理量___________。
3
15.(2021·河北·模拟预测)(12分)某化学小组在实验室制取NaO。 查阅资料可知,温度在573~673
2 2
K之间可生成NaO,若温度提高到733 K以上NaO 会分解。除Li外其他碱金属不与N 反应。
2 2 2 2 2
(1)甲组同学设计制取NaO 的装置如图。
2 2
①使用该装置制取的NaO 中不可能含有的杂质为______。
2 2
A. NaN B. NaCO C. NaO D. NaOH
3 2 3 2
②该小组同学为测定制得的NaO 样品的纯度,设计实验装置如下:
2 2
烧瓶中发生的主要反应的化学方程式是_____。水槽中量筒中收集到的气体为_____。测定装置的接口从左
至右正确的连接顺序是_____。
(2)乙组同学从反应历程上分析出上述(1)②的测定反应中存在中间产物,从而会导致测定结果____(填“偏大”或“偏小”)。为证明其分析的正确性,设计实验方案如下:
实验方案 产生的现象
Ⅰ.取烧瓶中的反应液,加入少量MnO 粉末 有大量气泡逸出
2
Ⅱ.向NaOH稀溶液中加入2~3滴酚酞溶液,然后加入少量的反应
溶液先变红后褪色
液
Ⅲ.向反应液中加入2~3滴酚酞溶液,充分振荡,然后逐滴加入过 开始无明显现象,加NaOH溶液后先
量的NaOH稀溶液 变红后褪色
实验方案I中发生反应的化学方程式为_______。 根据上述实验可知,反应溶液中存在的中间产物与酚酞
作用的条件是______。