文档内容
第 07 讲 铁及其化合物
【化学学科素养】
1.宏观辨识与微观探析:认识铁及其化合物的性质及应用,能以“铁三角”转化关系理解变价元素的
转化条件。
2.科学态度与社会责任:利用铁及其化合物的性质,科学认识铁及其化合物的提纯和制备工艺流程,
形成严谨求实的科学态度和崇尚真理的意识。
3.科学探究与创新意识:能提出有价值的氢氧化亚铁及其他铁的化合物的制备方案,并进行实验探
究。
【必备知识解读】
一、铁
1.自然界中铁的存在
铁元素在地壳中的含量仅次于氧、硅、铝元素,居第四位。
铁元素在自然界中主要以+2价和+3价化合物的形式存在于铁矿石。
2.铁的冶炼(高炉炼铁)
(1)原料:铁矿石、焦炭、石灰石、空气
(2)工业炼铁得到的铁是:生铁(混合物)
(3)高炉(炼铁炉):从下到上化学方程式为:
C+O =====CO C+CO =====2CO(吸收热量) 3CO + Fe O=====2Fe + 3CO
2 2 2 2 3 2
(4)焦炭的作用:
①提供热量C+O ===== CO(放热反应) ②提供还原剂:C+CO =====2CO
2 2 2
(5)炼铁过程中石灰石的主要作用是:将矿石中的二氧化硅转变为炉渣。
3.铁的物理性质和应用
(1)物理性质
纯铁具有银白色金属光泽,质软,有良好的延展性,密度是7.86g.cm-3,熔点为1535℃,沸点为
2750℃,铁是电和热的良导体,铁可以被磁铁吸引。
(2)应用
钢铁是人类生活和生产中非常重要的材料,广泛应用用于生活用具、生产工具、建筑、机械、电力、
桥梁、国防等领域。
二、铁的化学性质
1.铁与非金属单质反应(1)铁与氧气反应:3Fe+2O (纯) =====Fe O
2 3 4
现象:剧烈燃烧,放出大量热,火星四射,产生黑色固体。
(2)铁与氯气反应: 2Fe+3Cl ======2FeCl S的氧化性较强,生成三价铁
2 3
现象:剧烈燃烧,放出大量热,产生棕黄色烟。
(3)铁与硫反应:Fe+S=====FeS S的氧化性较弱,生成二价铁
2.铁与酸反应
(1)铁与非氧化性酸反应
Fe+2H+===Fe2++H↑
2
(2)铁与稀硝酸反应情况:
①铁少量:Fe+4HNO(稀)=Fe(NO )+NO↑+2HO
3 3 3 2
②铁过量:3Fe+8HNO(稀)=3Fe(NO )+2NO↑+4HO
3 3 2 2
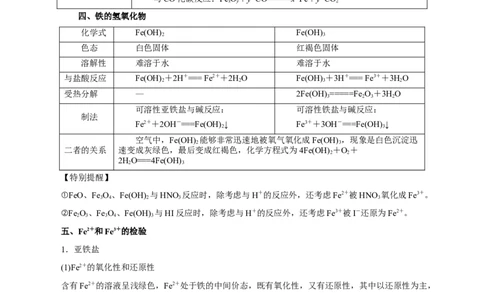
可用数轴表示如下:
3.铁与盐(溶液)反应
(1)与铜盐:Fe+Cu2+= Fe2++Cu
(2)与铁盐:Fe+ 2Fe3+=3Fe2+
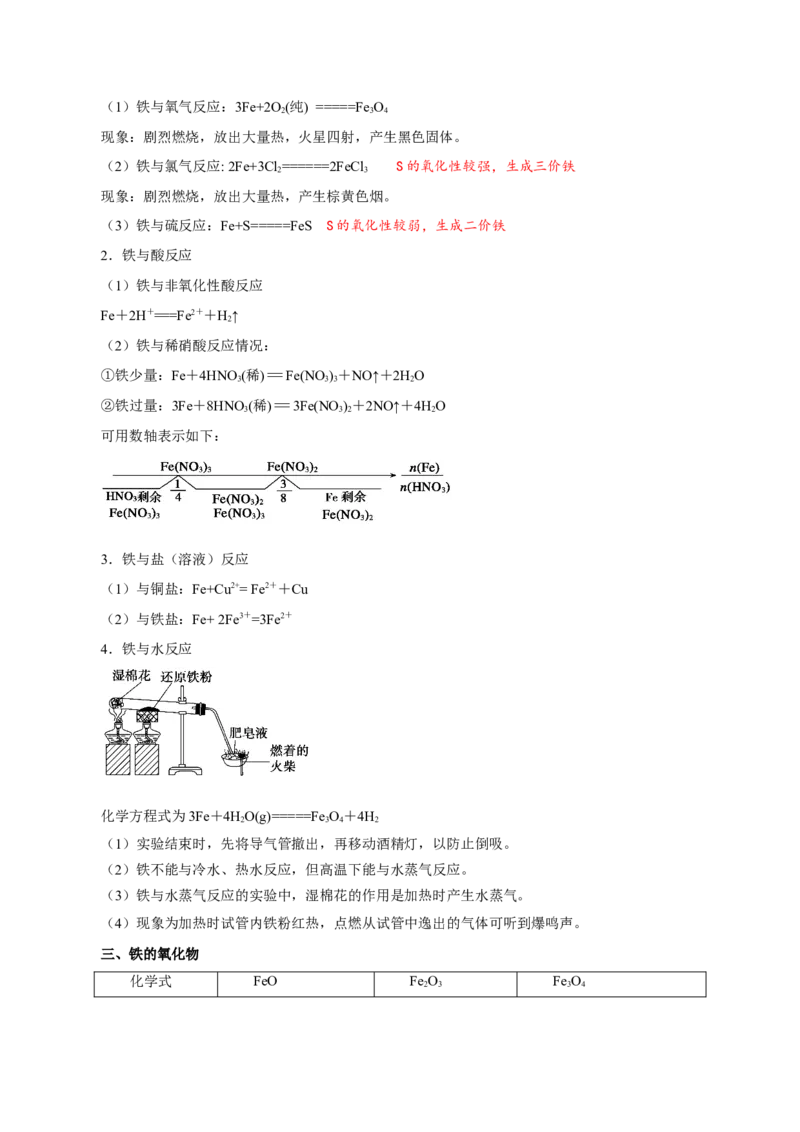
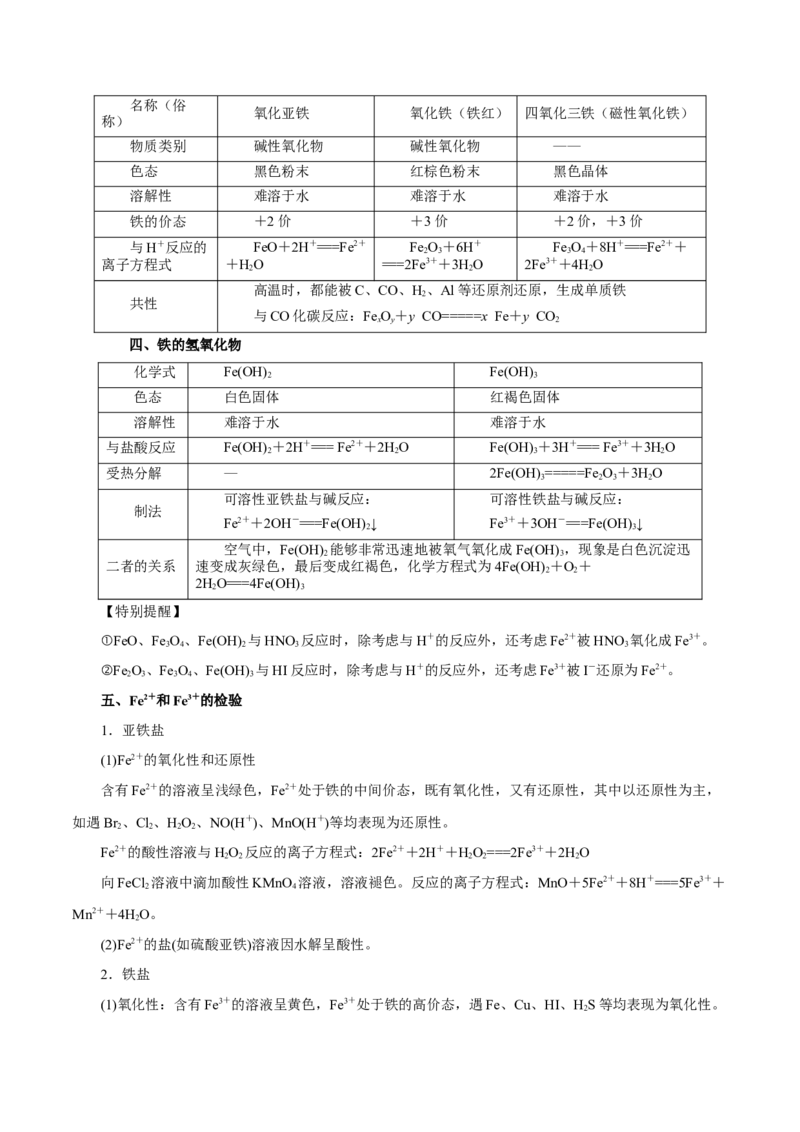
4.铁与水反应
化学方程式为3Fe+4HO(g)=====Fe O+4H
2 3 4 2
(1)实验结束时,先将导气管撤出,再移动酒精灯,以防止倒吸。
(2)铁不能与冷水、热水反应,但高温下能与水蒸气反应。
(3)铁与水蒸气反应的实验中,湿棉花的作用是加热时产生水蒸气。
(4)现象为加热时试管内铁粉红热,点燃从试管中逸出的气体可听到爆鸣声。
三、铁的氧化物
化学式 FeO Fe O Fe O
2 3 3 4名称(俗
氧化亚铁 氧化铁(铁红) 四氧化三铁(磁性氧化铁)
称)
物质类别 碱性氧化物 碱性氧化物 ——
色态 黑色粉末 红棕色粉末 黑色晶体
溶解性 难溶于水 难溶于水 难溶于水
铁的价态 +2价 +3价 +2价,+3价
与H+反应的 FeO+2H+===Fe2+ Fe O+6H+ Fe O+8H+===Fe2++
2 3 3 4
离子方程式 +HO ===2Fe3++3HO 2Fe3++4HO
2 2 2
高温时,都能被C、CO、H、Al等还原剂还原,生成单质铁
2
共性
与CO化碳反应:FeO+y CO=====x Fe+y CO
x y 2
四、铁的氢氧化物
化学式 Fe(OH) Fe(OH)
2 3
色态 白色固体 红褐色固体
溶解性 难溶于水 难溶于水
与盐酸反应 Fe(OH) +2H+=== Fe2++2HO Fe(OH) +3H+=== Fe3++3HO
2 2 3 2
受热分解 — 2Fe(OH) =====Fe O+3HO
3 2 3 2
可溶性亚铁盐与碱反应: 可溶性铁盐与碱反应:
制法
Fe2++2OH-===Fe(OH) ↓ Fe3++3OH-===Fe(OH) ↓
2 3
空气中,Fe(OH) 能够非常迅速地被氧气氧化成Fe(OH) ,现象是白色沉淀迅
2 3
二者的关系 速变成灰绿色,最后变成红褐色,化学方程式为4Fe(OH) +O+
2 2
2HO===4Fe(OH)
2 3
【特别提醒】
①FeO、Fe O、Fe(OH) 与HNO 反应时,除考虑与H+的反应外,还考虑Fe2+被HNO 氧化成Fe3+。
3 4 2 3 3
②Fe O、Fe O、Fe(OH) 与HI反应时,除考虑与H+的反应外,还考虑Fe3+被I-还原为Fe2+。
2 3 3 4 3
五、Fe2+和Fe3+的检验
1.亚铁盐
(1)Fe2+的氧化性和还原性
含有Fe2+的溶液呈浅绿色,Fe2+处于铁的中间价态,既有氧化性,又有还原性,其中以还原性为主,
如遇Br 、Cl、HO、NO(H+)、MnO(H+)等均表现为还原性。
2 2 2 2
Fe2+的酸性溶液与HO 反应的离子方程式:2Fe2++2H++HO===2Fe3++2HO
2 2 2 2 2
向FeCl 溶液中滴加酸性KMnO 溶液,溶液褪色。反应的离子方程式:MnO+5Fe2++8H+===5Fe3++
2 4
Mn2++4HO。
2
(2)Fe2+的盐(如硫酸亚铁)溶液因水解呈酸性。
2.铁盐
(1)氧化性:含有Fe3+的溶液呈黄色,Fe3+处于铁的高价态,遇Fe、Cu、HI、HS等均表现为氧化性。
2如用FeCl 溶液腐蚀印刷电路板上的铜箔,反应的离子方程式2Fe3++Cu===2Fe3++Cu2+。
3
(2)易水解:Fe3+极易水解,只能存在于酸性较强的溶液中。
3.亚铁盐、铁盐性质应用
(1)盐溶液的配制与保存
(2)物质的制备
(3)判断离子能否共存
Fe2+NO(H+)、ClO-、MnO(H+)
Fe3+S2-、I-、SO
Fe3+HCO、CO等水解相互促进的离子
【关键能力拓展】
一、防止Fe(OH) 被氧化的方法
2
(1)将配制溶液的蒸馏水煮沸,驱除溶液中的氧气。
(2)将盛有NaOH溶液的胶头滴管尖端插入试管的亚铁盐溶液底部,并慢慢挤出NaOH溶液。
(3)在亚铁盐溶液上面充入保护气,如H、N、稀有气体等。
2 2
(4)在亚铁盐溶液上面加保护层,如苯、植物油等。
(5)用Fe作阳极,石墨作阴极,电解NaOH溶液,在溶液上面加苯、汽油等保护层,利用新产生的Fe2
+与OH-反应制取Fe(OH) 。
2
二、Fe2+、Fe3+的检验方法
(1)Fe2+的检验
方法1 ―――――――→无现象―――――――→溶液变红色,证明含有Fe2+
――――――――→产生白色絮状沉淀,迅速变成灰绿色,最终变为红褐色,证
方法2
明含有Fe2+
方法3 ―――――――――→生成蓝色沉淀,证明含有Fe2+
(2)Fe3+的检验
方法1 ――――――――→溶液变红色,证明含有Fe3+方法2 ―――――――→产生红褐色沉淀,证明含有Fe3+
(3)混合溶液中Fe3+、Fe2+的检验
①Fe3+的检验
a.――→溶液变血红色,说明含有Fe3+
b.――→试纸变蓝色,说明含有Fe3+
②Fe2+的检验
a.――→KMnO 溶液褪色,说明含有Fe2+
4
b.――→溴水褪色,说明含有Fe2+
c.――→生成蓝色沉淀,说明含有Fe2+
三、铁及其化合物的相互转化
1. Fe、Fe2+ 、Fe3+的相互转化-----铁三角
(1)Fe只具有还原性,可以被氧化剂氧化为Fe2+、Fe3+
①Fe→Fe2+(与较弱氧化剂反应:如I、S、Fe3+、H+、Cu2+、Ag+)
2
Fe+S=====FeS
Fe+2Fe3+===3Fe2+
Fe+Cu2+===Cu+Fe2+
②Fe→Fe3+(与较强氧化剂反应:如Cl、Br 、浓HSO 、稀硝酸(足量)等)
2 2 2 4
2Fe+3Cl=====2FeCl
2 3
③Fe→Fe O(与氧化剂反应:如O、HO(g))
3 4 2 2
3Fe+4HO(g)=====Fe O+4H。
2 3 4 2
(2)Fe2+既具有氧化性又具有还原性
①Fe2+→Fe3+(与强氧化剂反应:如O、Cl、Br 、HO、HNO、KMnO (H+)、浓HSO 、等)
2 2 2 2 2 3 4 2 4
2Fe2++Cl===2Fe3++2Cl-,
2
2Fe2++HO+2H+===2Fe3++2HO,
2 2 2
5Fe2++MnO+8H+===5Fe3++Mn2++4HO
2
3Fe2++4H++NO===3Fe3++NO↑+2HO
2
②Fe2+→Fe(与还原剂反应:如C、CO、Al、Zn等)Zn+Fe2+===Zn2++Fe FeO+CO=====Fe+CO。
2
(3)Fe3+具有较强氧化性,可被还原为Fe2+或Fe
①Fe3+→Fe2+(与还原剂反应:如Fe、Cu、I-、S2-等)
2Fe3++Cu===2Fe2++Cu2+,
2Fe3++HS===2Fe2++S↓+2H+。
2
2Fe3++2I-===I +2Fe2+
2
②Fe3+→Fe(与还原剂反应:如C、CO、Al等)
Fe O+3CO=====2Fe+3CO Fe O+2Al=====2Fe+Al O。
2 3 2 2 3 2 3
四、铁和铁的氧化物的混合物与酸(H+)反应的计算
用终态法、关系式法、守恒法等方法巧解这类计算问题
1.终态法:固体和盐酸(硫酸)恰好完全反应,溶液中没有Fe3+,即多个反应后的“终态”是溶质只
有FeCl (FeSO )的溶液,因此有n(Fe2+):n(Cl-)=1:2[n(Fe2+):n(SO)=1:1],混合物中n(Fe)与盐酸(硫酸)中
2 4
n(H+)之比为1:2等结论。
2.关系式法:由 Fe+2H+===Fe2++H↑,Fe+Fe O+6H+===3Fe2++3HO可知,若没有Fe3+生成,
2 2 3 2
则反应的Fe(不产生H)与Fe O 的关系是Fe------ Fe O,则有n(Fe)=n(Fe O)+n(H)等关系。
2 2 3 2 3 2 3 2
3.守恒法:主要有Fe原子守恒、Cl-(SO)守恒、溶液中电荷守恒、Fe失去的电子与H+和Fe3+得到的
电子守恒。
【核心题型例解】
高频考点一 铁及其氧化物的性质
例1.人体血液中如果缺乏亚铁离子,就会造成缺铁性贫血。市场出售的某种麦片中含有微量、颗粒
细小的铁粉,这些铁粉在人体胃酸(胃酸的主要成分是HCl)作用下转化成亚铁盐。下列叙述错误的是
A.铁粉具有还原性 B.铁是人体必需的微量元素
C.常温下,铁能与水发生置换反应 D.Fe2+用K[Fe(CN) ]溶液检验生成蓝色沉淀
3 6
【答案】C
【解析】Fe粉可以失电子,具有还原性,故A正确;铁是合成血红蛋白的,所以铁是人体必需的微量
元素,故B正确;高温条件下,铁和水蒸气发生置换反应,故C错误; 可用 溶液有蓝色
沉淀,故D正确;故选C。
【变式探究】关于铁的三种氧化物(FeO、Fe O、Fe O)的下列叙述正确的是
2 3 3 4
A.铁的三种氧化物中铁元素的化合价完全相同
B.都是碱性氧化物,都能与盐酸反应生成氯化铁和水C.氧化亚铁可应用于瓷器制作中使釉呈绿色
D.四氧化三铁中铁元素有+2价和+3价,它是一种混合物
【答案】C
【解析】FeO中铁元素的化合价为+2价,Fe O 中铁元素的化合价为+3价,Fe O 为复杂的氧化物,
2 3 3 4
其中铁元素的化合价可以看作是由+2、+3价组成的,A错误;FeO、Fe O 为碱性氧化物,FeO与盐酸反
2 3
应:FeO+2HCl=FeCl +HO,Fe O 与盐酸反应:Fe O+6HCl=2FeCl +3HO,Fe O 不属于碱性氧化物,
2 2 2 3 2 3 3 2 3 4
与盐酸反应:Fe O+8HCl=FeCl +2FeCl +4HO,B错误;氧化亚铁是一种黑色粉末,可用作色素,应用
3 4 2 3 2
于瓷器制作中使釉呈绿色,C正确;四氧化三铁是复杂的氧化物,属于纯净物,D错误;故选C。
高频考点二 铁及其化合物的转化
例2.铁元素的价类二维图如图所示。下列说法错误的是
A.④可用作红色涂料
B.⑦的溶液可用于清洗青铜文物表面的锈迹
C.⑤被溶液中的氧气氧化为⑥的化学方程式为
D.③溶于过量稀硝酸的离子方程式为
【答案】B
【分析】铁元素的价类二维图分析可知,①为Fe,②为FeO,③为Fe O,④为Fe O,⑤为
3 4 2 3
Fe(OH) ,⑥为Fe(OH) ,⑦为Fe3+的盐,⑧为Fe2+的盐。
2 3
【解析】氧化铁为红色固体,可用作红色涂料,故A正确;Fe3+的溶液和铜反应,2Fe3++Cu=2Fe2+
+Cu2+,不可用于清洗青铜文物表面的锈迹,故B错误;氢氧化亚铁被溶液中的氧气氧化,白色沉淀迅速转
化为灰绿色,最后变为红褐色,生成氢氧化铁,反应的化学方程式为:4Fe(OH) +O +2H O═4Fe(OH) ,故
2 2 2 3
C正确;Fe O 溶于过量稀硝酸反应生成硝酸铁、一氧化氮和水,电子守恒、电荷守恒和原子守恒配平写
3 4
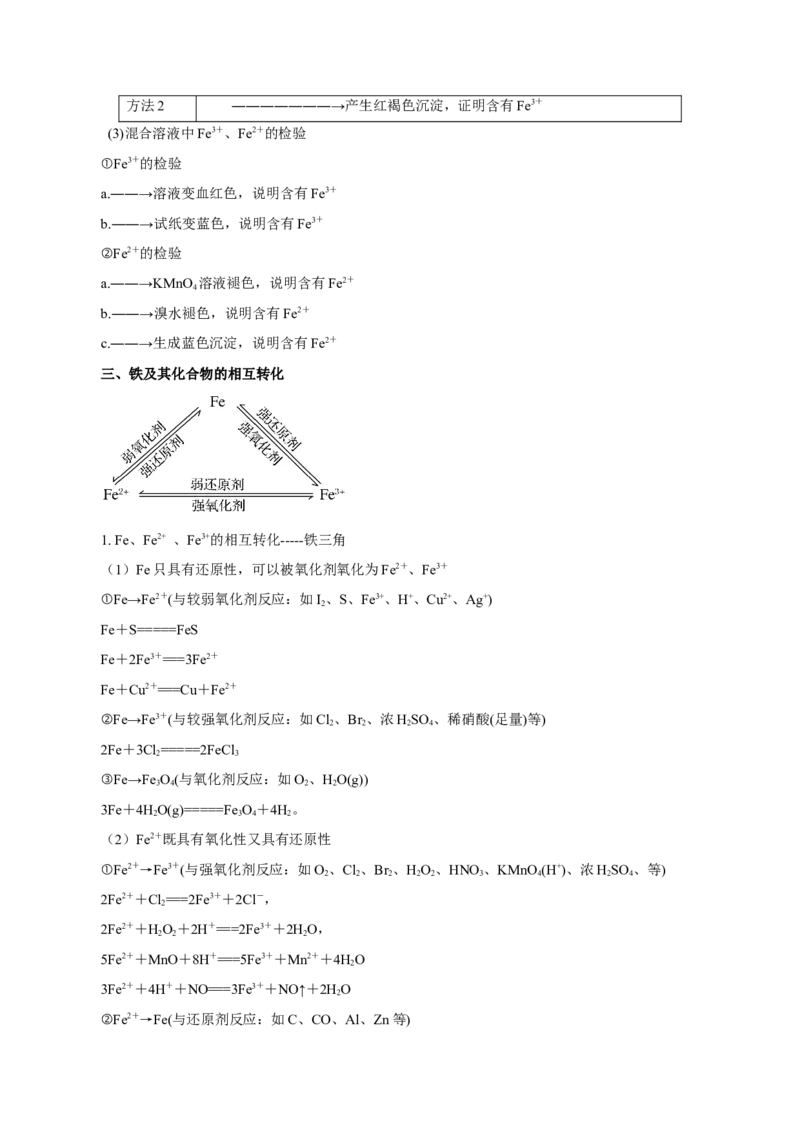
出,反应的离子方程式为: ,故D正确;故选B。【变式探究】部分含铁物质的分类与相应化合价关系如图所示。下列推断不合理的是( )
A.a可与e反应生成b
B.b既可被氧化,也可被还原
C.可将e加入浓碱液中制得d的胶体
D.可存在b→c→d→e→b的循环转化关系
【答案】C
【解析】由题图可知,a为Fe,b中含有Fe2+,c为Fe(OH) ,d为Fe(OH) ,e中含有Fe3+。Fe+2Fe3+
2 3
===3Fe2+,a可与e反应生成b,A推断合理;Fe2+既可以被氧化为Fe3+,也可以被还原为Fe,B推断合
理;可将饱和的Fe3+溶液加入沸水中制得Fe(OH) 胶体,而不是浓碱液中,C推断不合理;可存在Fe2+
3
――→Fe(OH) ――→Fe(OH) ――→Fe3+――→Fe2+的循环转化关系,D推断合理。
2 3
高频考点三、铁及其化合物的实验探究
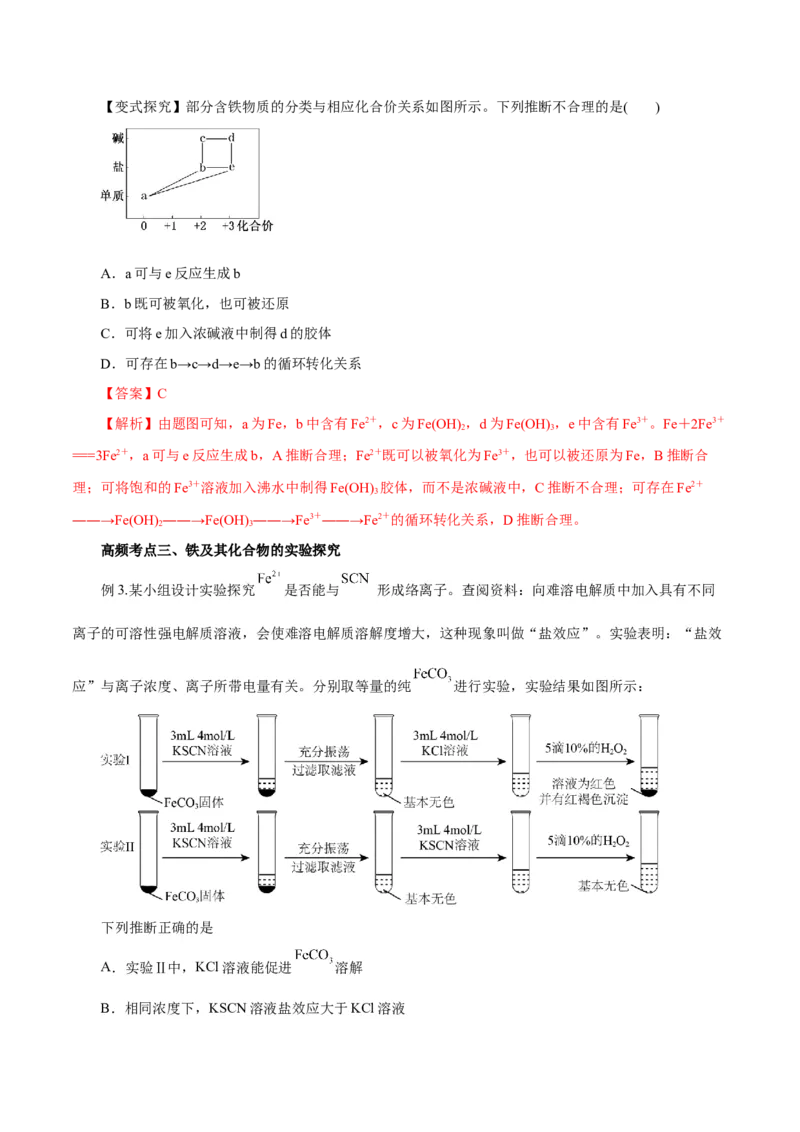
例3.某小组设计实验探究 是否能与 形成络离子。查阅资料:向难溶电解质中加入具有不同
离子的可溶性强电解质溶液,会使难溶电解质溶解度增大,这种现象叫做“盐效应”。实验表明:“盐效
应”与离子浓度、离子所带电量有关。分别取等量的纯 进行实验,实验结果如图所示:
下列推断正确的是
A.实验Ⅱ中,KCl溶液能促进 溶解
B.相同浓度下,KSCN溶液盐效应大于KCl溶液C.滤液中+2价铁离子总浓度:实验Ⅰ=实验Ⅱ
D.实验表明, 和 不能形成络离子
【答案】A
【分析】两个为对比实验,通过实验现象的不同可知,实验Ⅰ中 浓度较大, 和 能形成无
色络离子,会促进 溶解的溶解,使 在KSCN溶液中溶解度大于 在KCl溶液中的溶解
度,据此分析。
【解析】盐效应实质是阴、阳离子之间静电吸引力,促进平衡向溶解方向移动,A正确;根据盐效应
的影响因素可知,KSCN和KCl的阳离子相同、阴离子所带电荷数相等,在浓度相同条件下它们的盐效应
相近,B错误;实验Ⅰ最终产生红褐色沉淀,说明对应的滤液中含有 总浓度较大,实验Ⅱ中 总浓
度较小,C错误;通过实验说明, 和 能形成无色络离子,D错误;故选A。
【变式探究】为探究铁及其化合物的性质,某化学兴趣小组利用铁与水蒸气反应所得的固体进行了实
验,先用过量盐酸溶解,并分成4份,继续如下实验:
实
操作与现象
验
① 加入高锰酸钾溶液,紫色褪去
② 加入 溶液,生成蓝色沉淀
③ 加入KSCN溶液,无明显现象
④ 加入NaOH溶液,生成的白色沉淀逐渐变为灰绿色,最后变为红褐色
依据上述实验现象,下列结论合理的是
A.实验①说明溶液中一定含有
B.实验③说明该固体中不含三价铁
C.实验②③说明反应后的固体中有铁粉剩余
D.实验④中灰绿色的沉淀是
【答案】C【解析】高锰酸钾溶液会与盐酸发生氧化还原反应而褪色,A错误;实验③说明溶液中不含 ,但
不能说明固体中没有三价铁,也可能溶于盐酸时,过量的铁单质把三价铁还原了,B错误;实验②说明溶
液中含有 ,实验③说明溶液中不含 ,而铁与水蒸气能生成三价铁,所以可以推知反应后的固体中
有铁粉剩余,C正确;灰绿色的沉淀是 转化为 的中间过程,D错误; 故选C。
高频考点四 氢氧化亚铁制备
例4.下列各图示中不能较长时间看到Fe(OH) 白色沉淀的是
2
A. B. C. D.
【答案】C
【分析】Fe(OH) 在空气中很容易被氧化为红褐色的Fe(OH) ,即发生反应:4Fe(OH) +O+
2 3 2 2
2HO===4Fe(OH) ,因此要较长时间看到Fe(OH) 白色沉淀,就要排除装置中的空气或氧气。
2 3 2
【解析】A中先用铁与稀硫酸反应产生的氢气将装置中的空气排尽,并使生成的Fe(OH) 处在氢气的
2
保护中,因此可以长时间看到白色沉淀,故A不符合题意;B中的原理为铁作为阳极产生Fe2+,与阴极产
生的OH-结合生成 Fe(OH) ,且液面用汽油保护,能防止空气进入,因此可以长时间看到白色沉淀,故B
2
不符合题意; C中由于空气中的氧气能迅速将Fe(OH) 氧化,因而不能较长时间看到白色沉淀,故C符合
2
题意;D中液面加苯阻止了空气进入,故D不符合题意;故选C。
【方法技巧】制备Fe(OH) 常用的三种方法
2
(1)有机层覆盖法
将吸有NaOH溶液的胶头滴管插到液面以下,并在液面上覆盖一层苯或煤油(不能用CCl ),以防止
4
空气与Fe(OH) 接触发生反应,如图1所示。
2
(2)还原性气体保护法
用H 将装置内的空气排尽后,再将亚铁盐与NaOH溶液混合,这样可较长时间观察到白色沉淀,如图
2
2所示。(3)电解法
用铁做阳极,电解NaCl(或NaOH)溶液,并在液面上覆盖苯(或煤油),如图3所示。
另外,反应液要现用现配,且配制亚铁盐溶液和碱溶液所用的蒸馏水都需要加热煮沸除氧。
【变式探究】如图所示,此装置可用来制取和观察Fe(OH) 在空气中被氧化的颜色变化。实验时必
2
须使用铁屑和6mol·L-1的硫酸,其他试剂任选。填写下列空白:
(1)B中盛有一定量的NaOH溶液,A中烧瓶内应预先加入的药品是 。A中反应的离子方程
式是_________________________________________________________________________________。
(2)实验开始时先将止水夹a (填“打开”或“关闭”)。
(3)简述生成Fe(OH) 的操作过程:___________________________________________________。
2
(4)实验完毕,打开b处止水夹,放入一部分空气,此时B中发生反应的化学方程式为
________________________________________________________________________。
【解析】Fe+2H+===Fe2++H↑,产生的H 将Fe2+压入B中,发生反应:Fe2++2OH-==Fe(OH) ↓;
2 2 2
Fe(OH) 在空气中很容易被氧化为红褐色的Fe(OH) ,即发生反应:4Fe(OH) +O+2HO=4Fe(OH) 。
2 3 2 2 2 3
【答案】(1)铁屑 Fe+2H+===Fe2++H↑
2
(2)打开
(3)待A装置反应一段时间后关闭止水夹a,产生的H 将FeSO 溶液压入B中进行反应
2 4
(4)4Fe(OH)+O+2HO===4Fe(OH)
2 2 2 3
高频考点五 考查与铁有关的离子方程式
例5.下列反应的离子方程式书写正确的是
A.向氯化亚铁溶液中滴入 溶液:B.向次氯酸钠溶液中通入足量二氧化硫:
C.将氯气通入冷的石灰乳中制漂白粉:
D.向磁性氧化铁粉末中加入稀盐酸:
【答案】A
【解析】Fe2+遇 溶液:生成蓝色沉淀, ,A
正确;次氯酸钠具有强氧化性,二氧化硫具有还原性,两者会发生氧化还原反应:
,B错误;石灰乳应写成化学式,将氯气通入冷的中制漂白粉:
,C错误;磁性氧化铁为四氧化三铁,和稀盐酸反应生成盐和水,
题中所给离子方程式电荷不守恒,应为 ,D错误;故选A。
【变式探究】下列有关离子方程式的书写正确的是
A.明矾溶液与过量氨水混合:Al3++4NH•H O=AlO +2H O+4NH
3 2 2
B.FeCl 溶液刻蚀电路铜板:2Fe3++3Cu=2Fe+3Cu2+
3
C.向水垢中滴加足量醋酸:CaCO +2H+=Ca2++CO ↑+H O
3 2 2
D.稀硫酸滴入NaSO 溶液中:2H++S O =SO↑+S↓+H O
2 2 3 2 2 2
【答案】D
【解析】Al(OH) 只溶于强碱不溶于氨水,所以离子方程式为Al3++3NH•H O=Al(OH) ↓+3NH ,A项
3 3 2 3
错误;FeCl 将Cu氧化为CuCl 而自身被还原为FeCl ,离子方程式为2Fe3++Cu=2Fe+Cu2+,B项错误;醋酸
3 2 2
为弱电解质,离子方程式中不能拆写为离子,离子方程为CaCO +2CH COOH=Ca2+
3 3
+CO ↑+H O+2CHCOO-,C项错误;NaSO 在酸性条件下发生气化反应产生SO 和S,离子方程式为2H+
2 2 3 2 2 3 2
+S O =SO↑+S↓+H O,D项正确;故选D。
2 2 2
【举一反三】下列反应对应的离子方程式书写正确的是A.将等物质的量浓度的 和 溶液以体积比1:2混合:
B.向 溶液中通入少量的 :
C. 溶于过量氢碘酸溶液中:
D.明矾溶液与过量氨水混合:
【答案】A
【解析】1mol 中含有1mol Ba2+、2mol OH-,2mol 中含有2mol 、2mol H+、2mol
,二者混合过程中Ba2+完全反应,复分解反应中酸碱中和优先,因此OH-完全与H+反应, 不反
应,因此反应离子方程式为 ,故A项正确;向 溶液中通
入少量的 ,SO 发生氧化还原反应 , 与Ca2+反应生成微溶物
2
CaSO,由于 过量,H+与ClO-再反应生成HClO,因此总反应离子方程式为
4
,故B项错误; 溶于过量氢碘酸溶液中, 与
H+反应生成Fe3+,Fe3+与I-能发生氧化还原反应,反应离子方程式为 ,
故C项错误;Al(OH) 不溶于弱碱,因此明矾溶液与过量氨水混合反应离子方程式为
3
,故D项错误;综上所述,正确的是A项。