文档内容
第 64 讲 醛、酮、羧酸、酯、酰胺
[复习目标] 1.掌握醛、酮、羧酸、酯、酰胺典型代表物的结构与性质。2.掌握醛、酮、羧
酸、酯之间的转化以及合成方法。
考点一 醛、酮
1.醛、酮的概述
(1)醛、酮的概念
物质 概念 表示方法
醛 由____________与______相连而构成的化合物
酮 ________与两个________相连的化合物
(2)醛的分类
醛
(3)饱和一元醛的通式:________________,饱和一元酮的通式:____________________。
2.几种重要的醛、酮物质 主要物理性质 用途
无色、有强烈刺激性气味的
气体,易溶于水,其水溶液
甲醛(蚁醛) (HCHO) 称____________,具有 化工原料,制作生物标本
______、______性能
_____________等互溶
无色、具有刺激性气味的液
乙醛(CHCHO) 化工原料
3
体,易______,能与
有苦杏仁气味的无色液体, 制造染料、香料及药物的重
苯甲醛( ) 俗称苦杏仁油 要原料
无色透明液体,易挥发,能
有机溶剂和化工原料
与________等互溶
丙酮( )
思考 小分子的醛、酮均易溶于水,原因是什么?
________________________________________________________________________
3.醛类的化学性质
醛类物质既有氧化性又有还原性,其氧化、还原关系为
醇醛――→羧酸
以乙醛为例写出醛类主要反应的化学方程式:
(1)氧化反应
①银镜反应
________________________________________________________________________。
②与新制的Cu(OH) 的反应
2
________________________________________________________________________。
(2)还原反应(催化加氢)
________________________________________________________________________。
4.酮类的化学性质(以丙酮为例)
丙酮不能被____________、____________等弱氧化剂氧化,在催化剂存在的条件下,可与
H 发生________反应,生成2-丙醇。
2
5.醛基的检验
与新制的银氨溶液反应 与新制的氢氧化铜反应
在洁净的试管中加入1 mL 2% AgNO 溶
3
在试管中加入2 mL
液,然后
10%____________,加入5
实验操作 ____________________________________
滴5%__________,得到新制
______________,制得银氨溶液;再滴入
的Cu(OH) ,振荡后加入0.5
2
3滴乙醛,振荡后将试管放在______________ mL乙醛溶液,________
产生____________(1 mol
实验现象 产生__________(1 mol RCHO~2 mol Ag)
RCHO~1 mol Cu O)
2
①配制Cu(OH) 悬浊液时,
2
①试管内部必须洁净; 所用的NaOH溶液必须过
②银氨溶液要随用随配,不可久置; 量;
注意事项
③水浴加热,不可用酒精灯直接加热; ②Cu(OH) 悬浊液要随用随
2
④乙醛用量不宜太多,一般3~5滴 配,不可久置;
③反应液直接加热煮沸
思考 1 mol HCHO与足量的银氨溶液反应,最多产生______mol Ag。
醛、酮在有机合成中常用到的化学反应
(1)醛、酮与具有极性键共价分子的羰基的加成反应
(2)羟醛缩合
1.凡是能发生银镜反应的有机物都是醛( )
2.甲醛是常温下唯一呈气态的烃的含氧衍生物( )
3.丙醛和丙酮互为同分异构体,不能用核磁共振氢谱鉴别( )
4.醛类物质发生银镜反应或与新制的Cu(OH) 的反应均需在碱性条件下( )
2
5.醛类化合物既能发生氧化反应又能发生还原反应( )
一、醛、酮的性质及应用
1.下列有关利用乙醛制备银镜过程的说法不正确的是( )A.试管先用热烧碱溶液洗涤,然后用蒸馏水洗涤
B.边振荡盛有2%的氨水的试管,边滴入2%的AgNO 溶液至最初的沉淀恰好溶解为止
3
C.将盛有乙醛与银氨溶液混合液的试管置于热水浴中加热
D.在银氨溶液的配制过程中,溶液pH增大
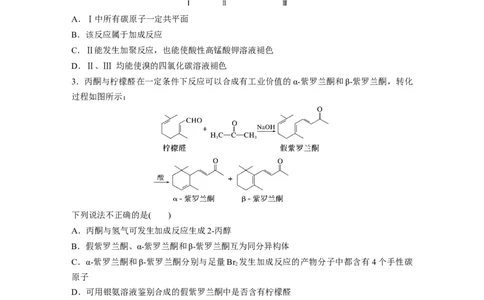
2.(2022·成都石室中学模拟)贝里斯—希尔曼反应条件温和,其过程具有原子经济性,示例
如图。下列说法错误的是( )
A.Ⅰ中所有碳原子一定共平面
B.该反应属于加成反应
C.Ⅱ能发生加聚反应,也能使酸性高锰酸钾溶液褪色
D.Ⅱ、Ⅲ 均能使溴的四氯化碳溶液褪色
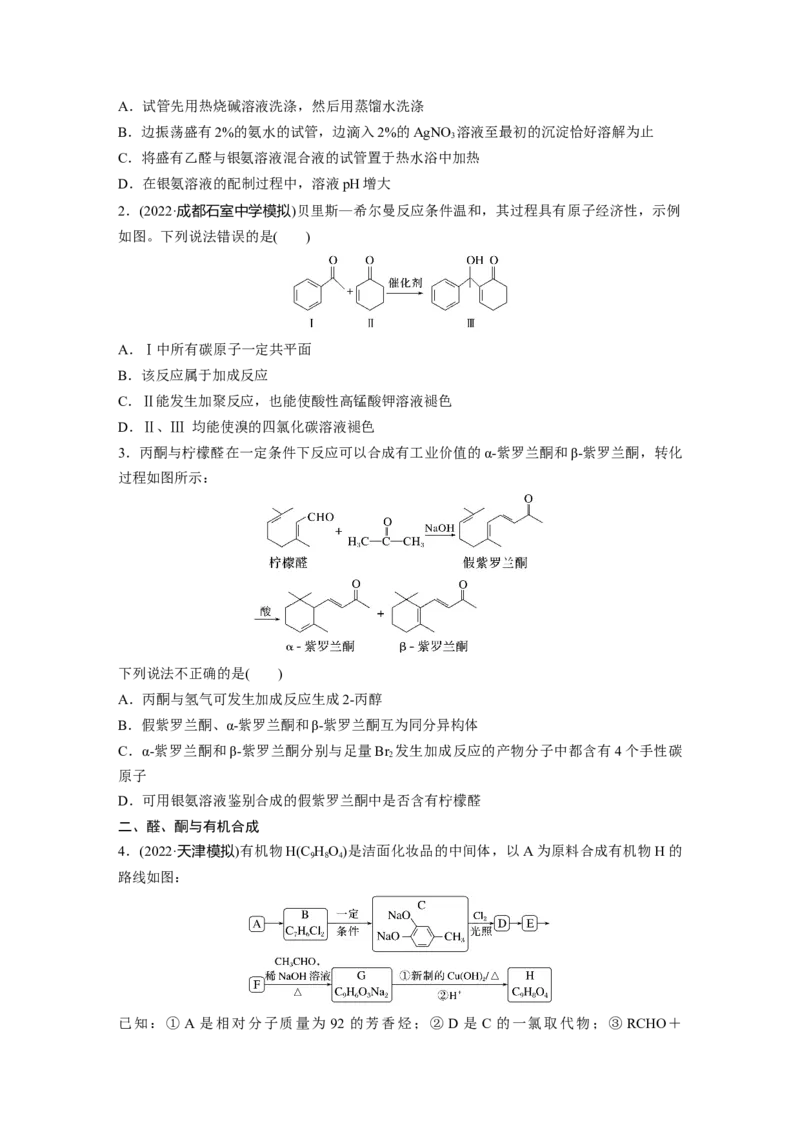
3.丙酮与柠檬醛在一定条件下反应可以合成有工业价值的α-紫罗兰酮和β-紫罗兰酮,转化
过程如图所示:
下列说法不正确的是( )
A.丙酮与氢气可发生加成反应生成2-丙醇
B.假紫罗兰酮、α-紫罗兰酮和β-紫罗兰酮互为同分异构体
C.α-紫罗兰酮和β-紫罗兰酮分别与足量Br 发生加成反应的产物分子中都含有4个手性碳
2
原子
D.可用银氨溶液鉴别合成的假紫罗兰酮中是否含有柠檬醛
二、醛、酮与有机合成
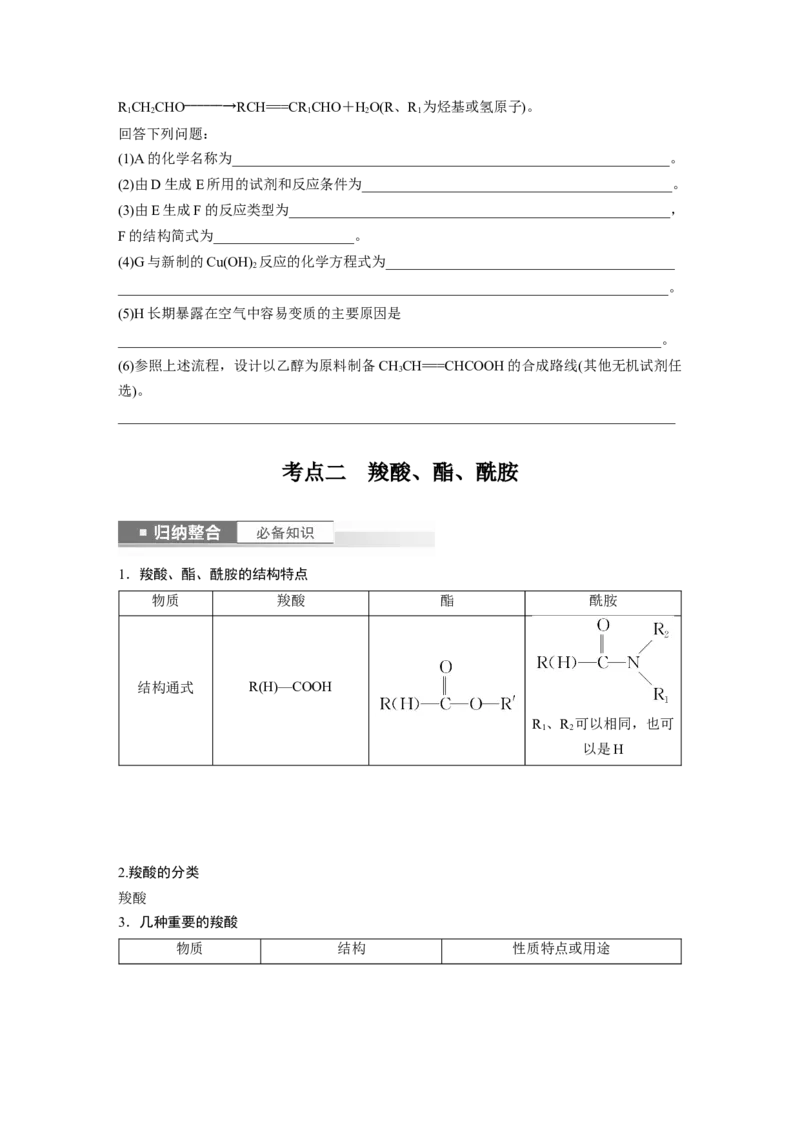
4.(2022·天津模拟)有机物H(C HO)是洁面化妆品的中间体,以A为原料合成有机物H的
9 8 4
路线如图:
已知:① A 是相对分子质量为 92 的芳香烃;② D 是 C 的一氯取代物;③ RCHO+R CHCHO――――――→RCH===CR CHO+HO(R、R 为烃基或氢原子)。
1 2 1 2 1
回答下列问题:
(1)A的化学名称为______________________________________________________________。
(2)由D生成E所用的试剂和反应条件为____________________________________________。
(3)由E生成F的反应类型为______________________________________________________,
F的结构简式为____________________。
(4)G与新制的Cu(OH) 反应的化学方程式为_________________________________________
2
______________________________________________________________________________。
(5)H长期暴露在空气中容易变质的主要原因是
_____________________________________________________________________________。
(6)参照上述流程,设计以乙醇为原料制备CHCH===CHCOOH的合成路线(其他无机试剂任
3
选)。
_______________________________________________________________________________
考点二 羧酸、酯、酰胺
1.羧酸、酯、酰胺的结构特点
物质 羧酸 酯 酰胺
结构通式 R(H)—COOH
R 、R 可以相同,也可
1 2
以是H
2.羧酸的分类
羧酸
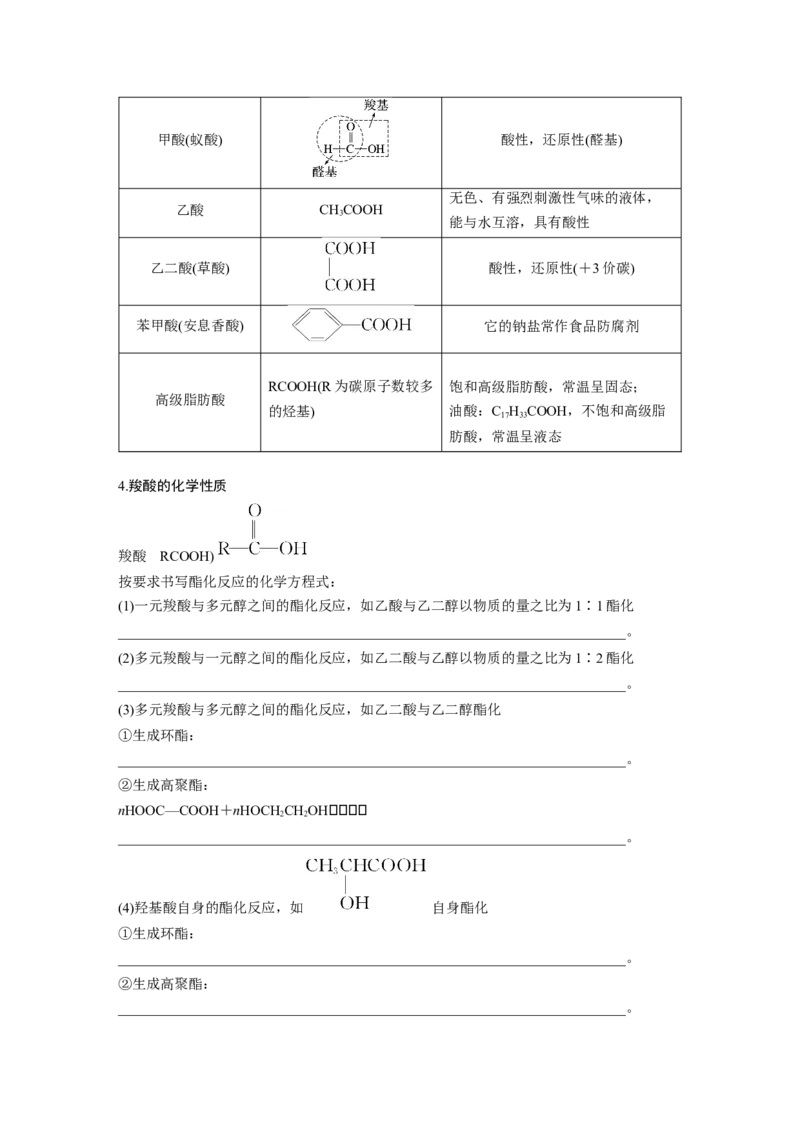
3.几种重要的羧酸
物质 结构 性质特点或用途甲酸(蚁酸) 酸性,还原性(醛基)
无色、有强烈刺激性气味的液体,
乙酸 CHCOOH
3
能与水互溶,具有酸性
乙二酸(草酸) 酸性,还原性(+3价碳)
苯甲酸(安息香酸) 它的钠盐常作食品防腐剂
RCOOH(R为碳原子数较多 饱和高级脂肪酸,常温呈固态;
高级脂肪酸
的烃基) 油酸:C H COOH,不饱和高级脂
17 33
肪酸,常温呈液态
4.羧酸的化学性质
羧酸RCOOH
按要求书写酯化反应的化学方程式:
(1)一元羧酸与多元醇之间的酯化反应,如乙酸与乙二醇以物质的量之比为1∶1酯化
________________________________________________________________________。
(2)多元羧酸与一元醇之间的酯化反应,如乙二酸与乙醇以物质的量之比为1∶2酯化
________________________________________________________________________。
(3)多元羧酸与多元醇之间的酯化反应,如乙二酸与乙二醇酯化
①生成环酯:
________________________________________________________________________。
②生成高聚酯:
nHOOC—COOH+nHOCH CHOH
2 2
________________________________________________________________________。
(4)羟基酸自身的酯化反应,如 自身酯化
①生成环酯:
________________________________________________________________________。
②生成高聚酯:
________________________________________________________________________。5.酯的通性
(1)物理性质
酯的密度一般______水,易溶于有机溶剂;酯可用作溶剂,也可用作制备饮料和糖果的香料;
低级酯通常有芳香气味。
(2)化学性质——水解反应(取代反应)
酯在酸性或碱性环境下,均可以与水发生水解反应。如乙酸乙酯的水解:
①酸性条件下水解:______________________________________(可逆)。
②碱性条件下水解:________________________________________(进行彻底)。
特 别 提 醒 酚 酯 在 碱 性 条 件 下 水 解 , 消 耗 NaOH 的 定 量 关 系 , 如 1 mol
消耗2 mol NaOH。
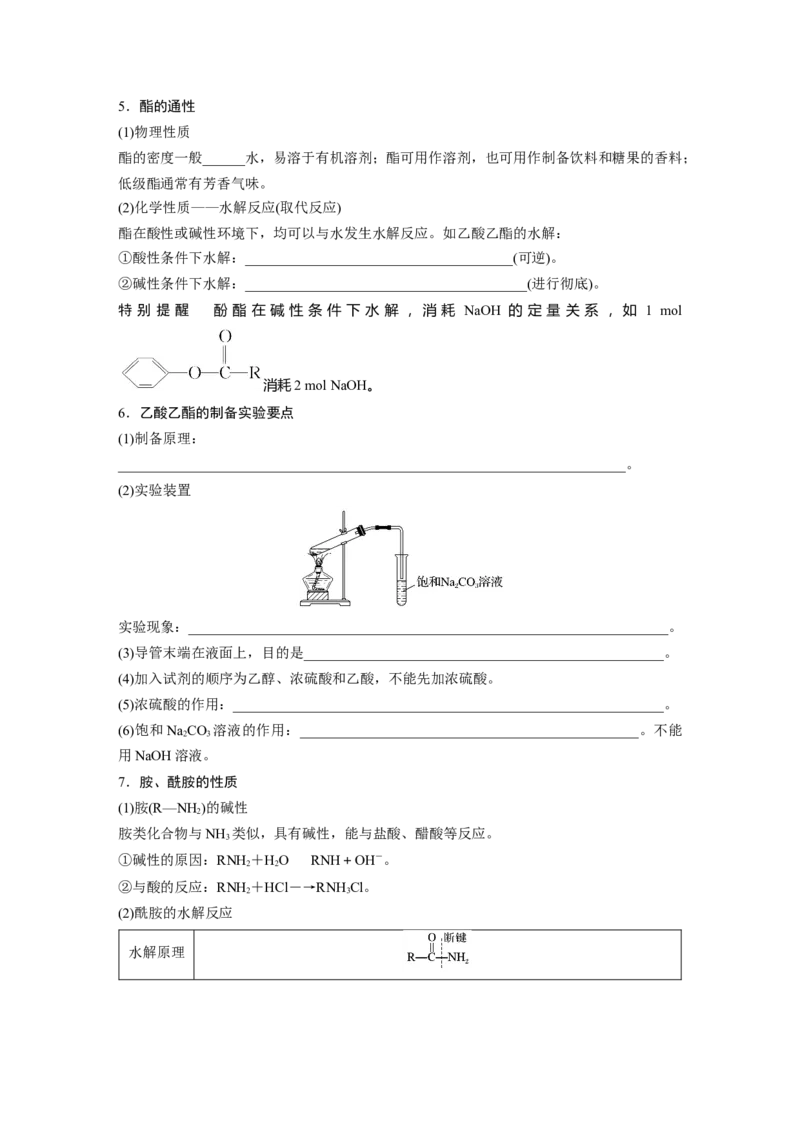
6.乙酸乙酯的制备实验要点
(1)制备原理:
________________________________________________________________________。
(2)实验装置
实验现象:____________________________________________________________________。
(3)导管末端在液面上,目的是___________________________________________________。
(4)加入试剂的顺序为乙醇、浓硫酸和乙酸,不能先加浓硫酸。
(5)浓硫酸的作用:_____________________________________________________________。
(6)饱和NaCO 溶液的作用:________________________________________________。不能
2 3
用NaOH溶液。
7.胺、酰胺的性质
(1)胺(R—NH )的碱性
2
胺类化合物与NH 类似,具有碱性,能与盐酸、醋酸等反应。
3
①碱性的原因:RNH +HORNH+OH-。
2 2
②与酸的反应:RNH +HCl―→RNH Cl。
2 3
(2)酰胺的水解反应
水解原理酸性条件
+HO+H+――→RCOOH+NH
2
碱性条件
+OH-――→RCOO-+NH ↑
3
1.分子式相同的羧酸和酯互为同分异构体( )
2.甲酸能发生银镜反应,能与新制的氢氧化铜反应生成砖红色沉淀( )
3.酯化反应和酯的水解反应都属于取代反应( )
4.可以用NaOH溶液来除去乙酸乙酯中的乙酸( )
5.1 mol酚酯基水解时,最多可消耗2 mol NaOH( )
6.C HO 的同分异构体的类型有羧酸、酯、羟基醛等( )
4 8 2
7.制备乙酸乙酯时,向浓HSO 中缓慢加入乙醇和冰醋酸( )
2 4
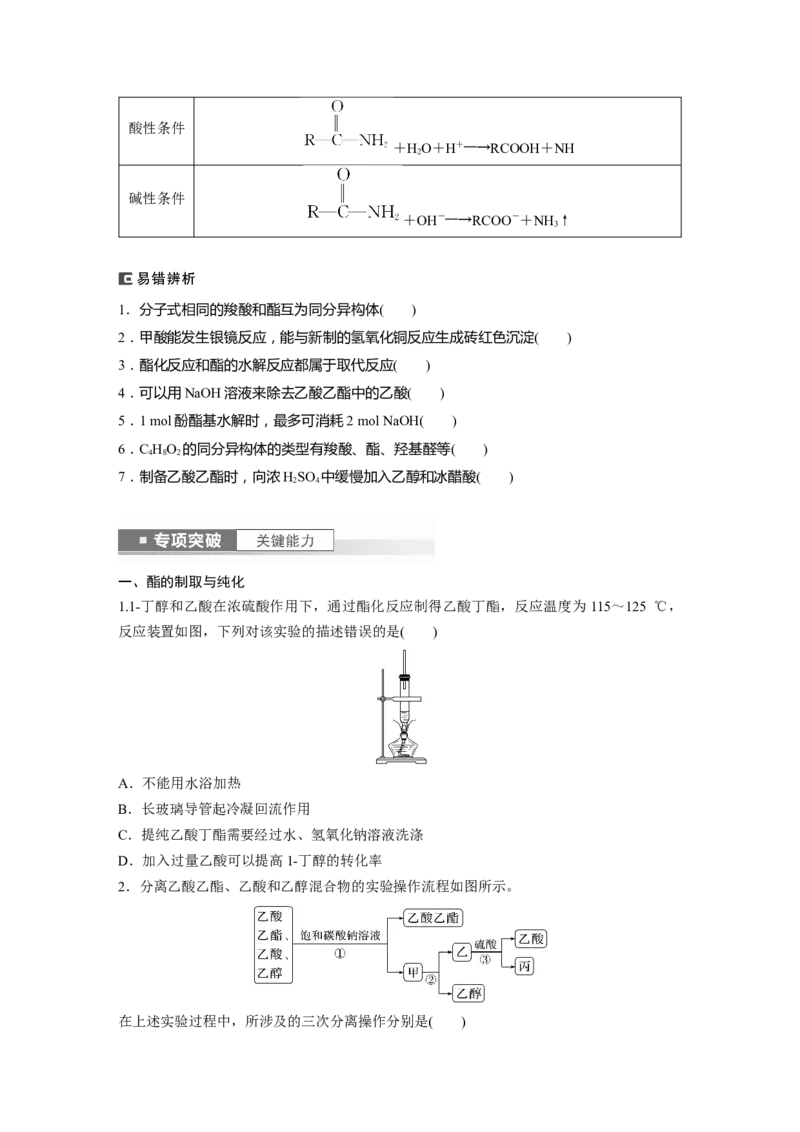
一、酯的制取与纯化
1.1-丁醇和乙酸在浓硫酸作用下,通过酯化反应制得乙酸丁酯,反应温度为115~125 ℃,
反应装置如图,下列对该实验的描述错误的是( )
A.不能用水浴加热
B.长玻璃导管起冷凝回流作用
C.提纯乙酸丁酯需要经过水、氢氧化钠溶液洗涤
D.加入过量乙酸可以提高1-丁醇的转化率
2.分离乙酸乙酯、乙酸和乙醇混合物的实验操作流程如图所示。
在上述实验过程中,所涉及的三次分离操作分别是( )A.①蒸馏 ②过滤 ③分液
B.①分液 ②蒸馏 ③结晶、过滤
C.①蒸馏 ②分液 ③分液
D.①分液 ②蒸馏 ③蒸馏
二、羧酸及其衍生物的性质
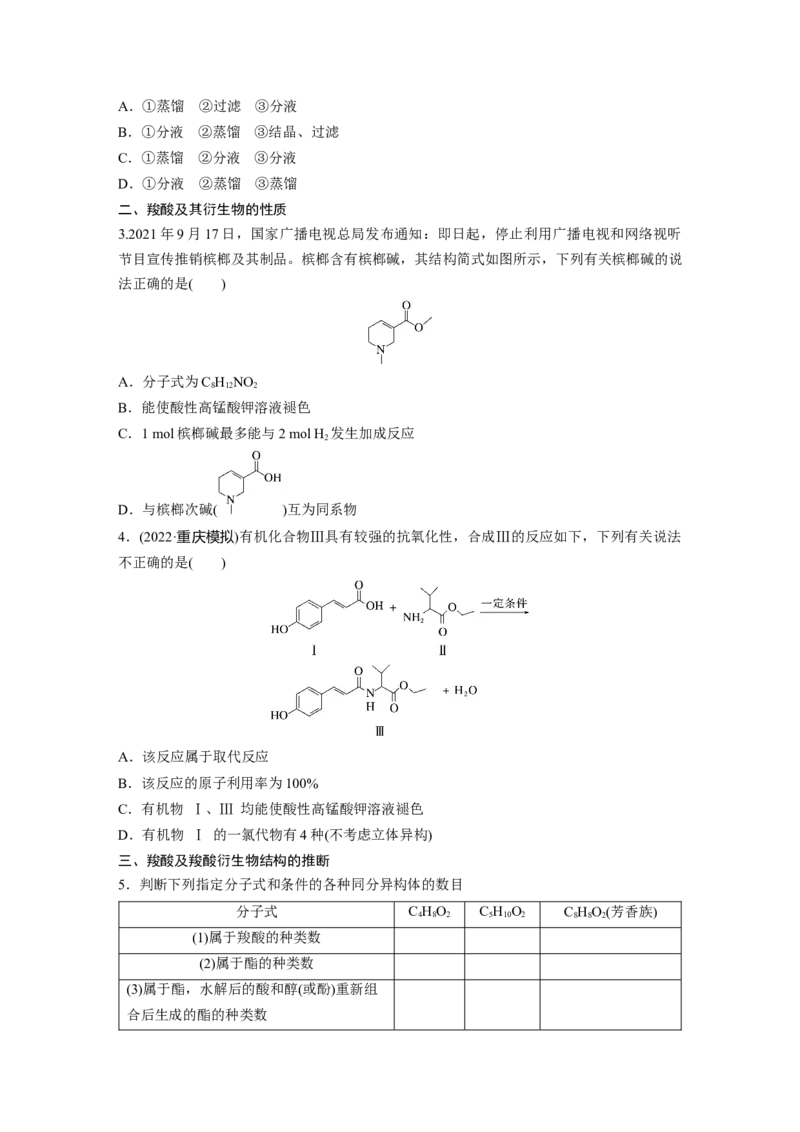
3.2021年9月17日,国家广播电视总局发布通知:即日起,停止利用广播电视和网络视听
节目宣传推销槟榔及其制品。槟榔含有槟榔碱,其结构简式如图所示,下列有关槟榔碱的说
法正确的是( )
A.分子式为C H NO
8 12 2
B.能使酸性高锰酸钾溶液褪色
C.1 mol槟榔碱最多能与2 mol H 发生加成反应
2
D.与槟榔次碱( )互为同系物
4.(2022·重庆模拟)有机化合物Ⅲ具有较强的抗氧化性,合成Ⅲ的反应如下,下列有关说法
不正确的是( )
A.该反应属于取代反应
B.该反应的原子利用率为100%
C.有机物 Ⅰ、Ⅲ 均能使酸性高锰酸钾溶液褪色
D.有机物 Ⅰ 的一氯代物有4种(不考虑立体异构)
三、羧酸及羧酸衍生物结构的推断
5.判断下列指定分子式和条件的各种同分异构体的数目
分子式 C HO C H O C HO(芳香族)
4 8 2 5 10 2 8 8 2
(1)属于羧酸的种类数
(2)属于酯的种类数
(3)属于酯,水解后的酸和醇(或酚)重新组
合后生成的酯的种类数(4)属于醛,同时能与钠反应放出氢气
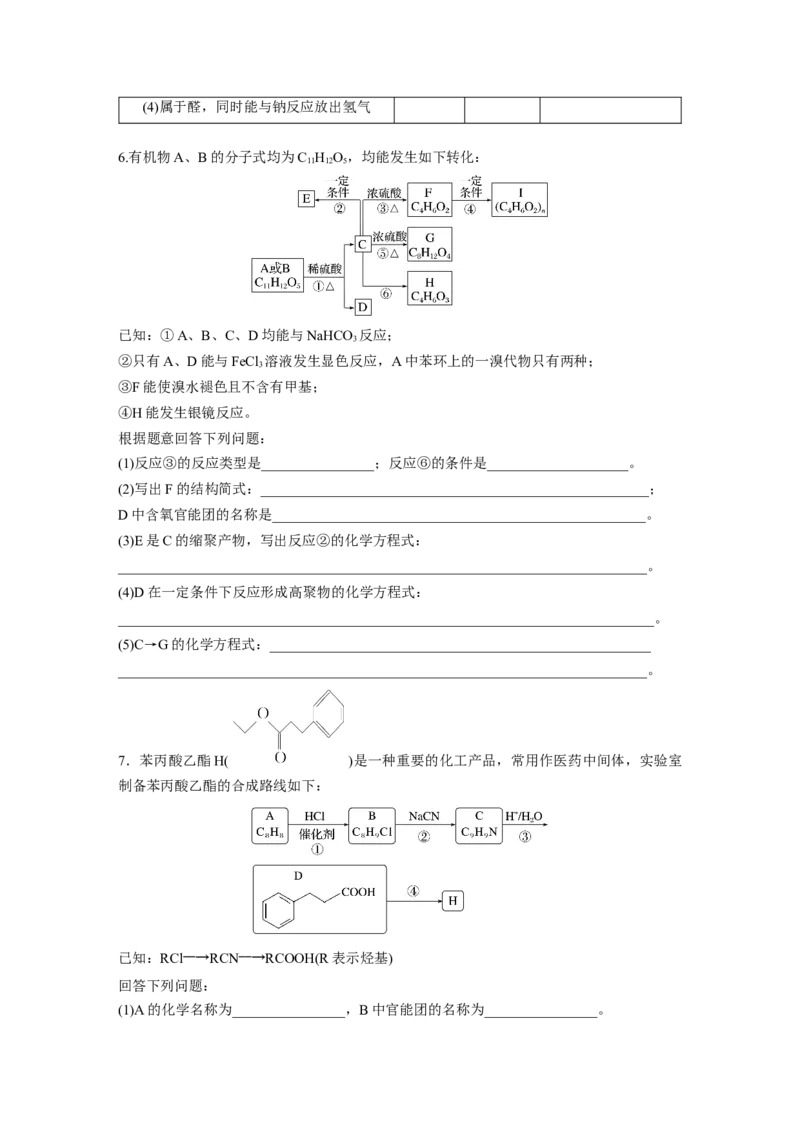
6.有机物A、B的分子式均为C H O,均能发生如下转化:
11 12 5
已知:①A、B、C、D均能与NaHCO 反应;
3
②只有A、D能与FeCl 溶液发生显色反应,A中苯环上的一溴代物只有两种;
3
③F能使溴水褪色且不含有甲基;
④H能发生银镜反应。
根据题意回答下列问题:
(1)反应③的反应类型是________________;反应⑥的条件是____________________。
(2)写出F的结构简式:_______________________________________________________;
D中含氧官能团的名称是_____________________________________________________。
(3)E是C的缩聚产物,写出反应②的化学方程式:
___________________________________________________________________________。
(4)D在一定条件下反应形成高聚物的化学方程式:
____________________________________________________________________________。
(5)C→G的化学方程式:______________________________________________________
___________________________________________________________________________。
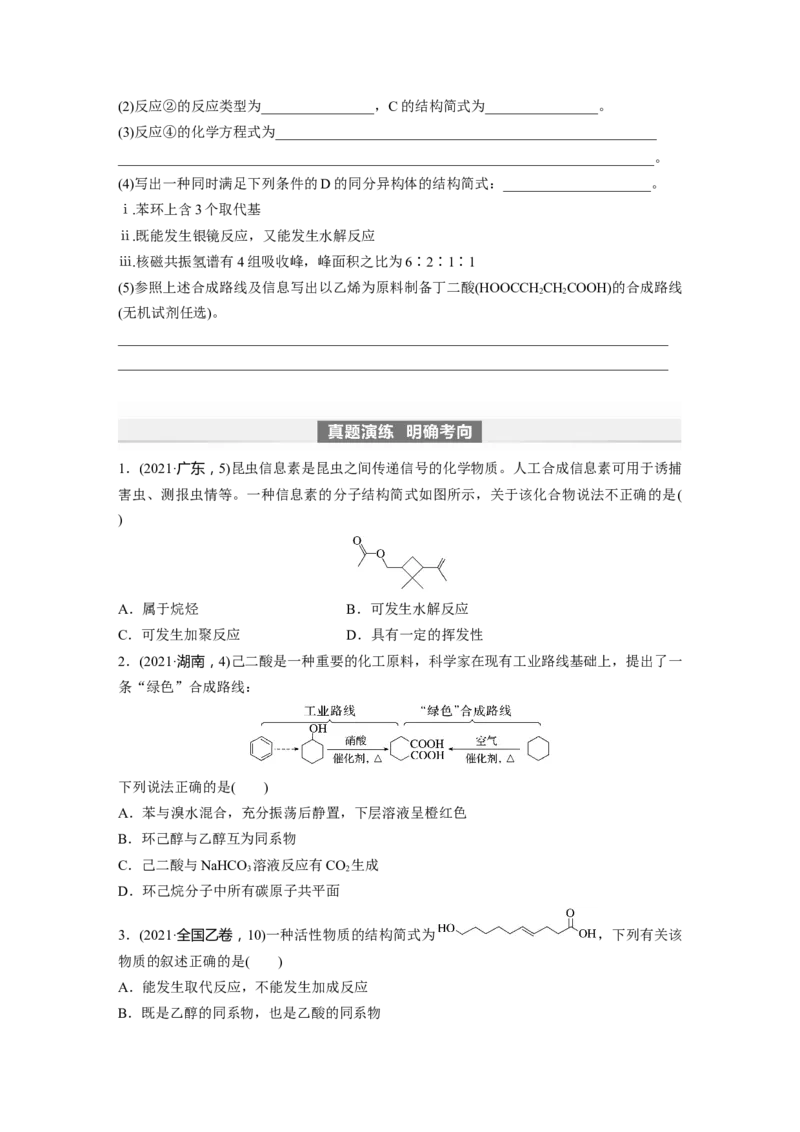
7.苯丙酸乙酯H( )是一种重要的化工产品,常用作医药中间体,实验室
制备苯丙酸乙酯的合成路线如下:
已知:RCl――→RCN――→RCOOH(R表示烃基)
回答下列问题:
(1)A的化学名称为________________,B中官能团的名称为________________。(2)反应②的反应类型为________________,C的结构简式为________________。
(3)反应④的化学方程式为______________________________________________________
____________________________________________________________________________。
(4)写出一种同时满足下列条件的D的同分异构体的结构简式:_____________________。
ⅰ.苯环上含3个取代基
ⅱ.既能发生银镜反应,又能发生水解反应
ⅲ.核磁共振氢谱有4组吸收峰,峰面积之比为6∶2∶1∶1
(5)参照上述合成路线及信息写出以乙烯为原料制备丁二酸(HOOCCH CHCOOH)的合成路线
2 2
(无机试剂任选)。
______________________________________________________________________________
______________________________________________________________________________
1.(2021·广东,5)昆虫信息素是昆虫之间传递信号的化学物质。人工合成信息素可用于诱捕
害虫、测报虫情等。一种信息素的分子结构简式如图所示,关于该化合物说法不正确的是(
)
A.属于烷烃 B.可发生水解反应
C.可发生加聚反应 D.具有一定的挥发性
2.(2021·湖南,4)己二酸是一种重要的化工原料,科学家在现有工业路线基础上,提出了一
条“绿色”合成路线:
下列说法正确的是( )
A.苯与溴水混合,充分振荡后静置,下层溶液呈橙红色
B.环己醇与乙醇互为同系物
C.己二酸与NaHCO 溶液反应有CO 生成
3 2
D.环己烷分子中所有碳原子共平面
3.(2021·全国乙卷,10)一种活性物质的结构简式为 ,下列有关该
物质的叙述正确的是( )
A.能发生取代反应,不能发生加成反应
B.既是乙醇的同系物,也是乙酸的同系物C.与 互为同分异构体
D.1 mol该物质与碳酸钠反应得44 g CO
2
4.(2022·海南,12改编)化合物“E7974”具有抗肿瘤活性,结构简式如下,下列有关该化
合物说法正确的是( )
A.能使Br 的CCl 溶液褪色
2 4
B.分子中含有3种官能团
C.分子中含有4个手性碳原子
D.1 mol该化合物最多与2 mol NaOH反应