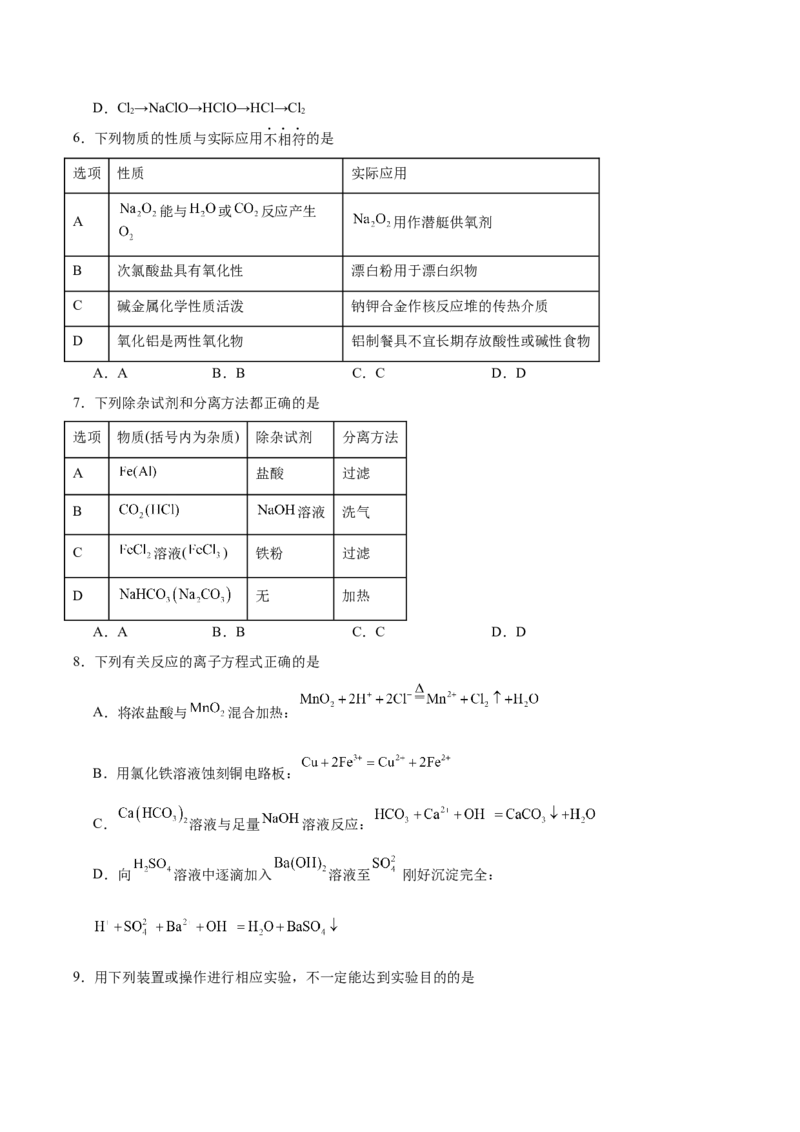文档内容
吉林省友好学校第80届期末联考2025-2026学年高一上学期1月期末化学
试题
一、单选题
1.化学与生活紧密相关,下列有关说法不正确的是
A.重庆素有雾都之称,雾是一种气溶胶,光束透过大雾可观察到丁达尔效应
B.FeSO 作补血剂时可与维生素C同时服用
4
C.生铁的含碳量比钢的含碳量高,合金的熔点一般比其成分金属的熔点高
D.漂白粉可用于漂白棉、麻、纸张等,其长期露置在空气中会失效
2.下列表示反应中相关微粒的化学用语正确的是
A.中子数为18的氯原子: B. 的结构式:
C. 的结构示意图: D.水的电子式:
3.在酸性溶液中能大量共存而且为无色透明的溶液是
A.NH +,Al3+,SO 2-,NO -
4 4 3
B.K+,Na+,NO -,CO2-,
3 3
C.K+,MnO -,NH +,NO -
4 4 3
D.Na+,K+,HCO -,NO -
3 3
4.用 表示阿伏加德罗常数的值。下列说法正确的是
A.含 个 的 溶解于 水中, 的物质的量浓度为
B.足量的 与 完全反应时,转移的电子数为
C. 中含有的离子数为
D. 金属镁变成镁离子时失去的电子数为
5.物质间存在着转化关系。下列选项中的各步转化无法通过一步反应实现的是
A.Na→Na O→NaCO→NaCl→Na
2 2 2 3
B.Fe→FeCl →Fe(OH) →Fe O→Fe
3 3 2 3
C.Al→Al O→Al(OH) →AlCl →Al
2 3 3 3D.Cl→NaClO→HClO→HCl→Cl
2 2
6.下列物质的性质与实际应用不相符的是
选项 性质 实际应用
能与 或 反应产生
A 用作潜艇供氧剂
B 次氯酸盐具有氧化性 漂白粉用于漂白织物
C 碱金属化学性质活泼 钠钾合金作核反应堆的传热介质
D 氧化铝是两性氧化物 铝制餐具不宜长期存放酸性或碱性食物
A.A B.B C.C D.D
7.下列除杂试剂和分离方法都正确的是
选项 物质(括号内为杂质) 除杂试剂 分离方法
A 盐酸 过滤
B 溶液 洗气
C 溶液( ) 铁粉 过滤
D 无 加热
A.A B.B C.C D.D
8.下列有关反应的离子方程式正确的是
A.将浓盐酸与 混合加热:
B.用氯化铁溶液蚀刻铜电路板:
C. 溶液与足量 溶液反应:
D.向 溶液中逐滴加入 溶液至 刚好沉淀完全:
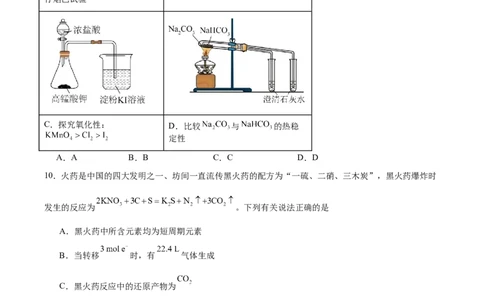
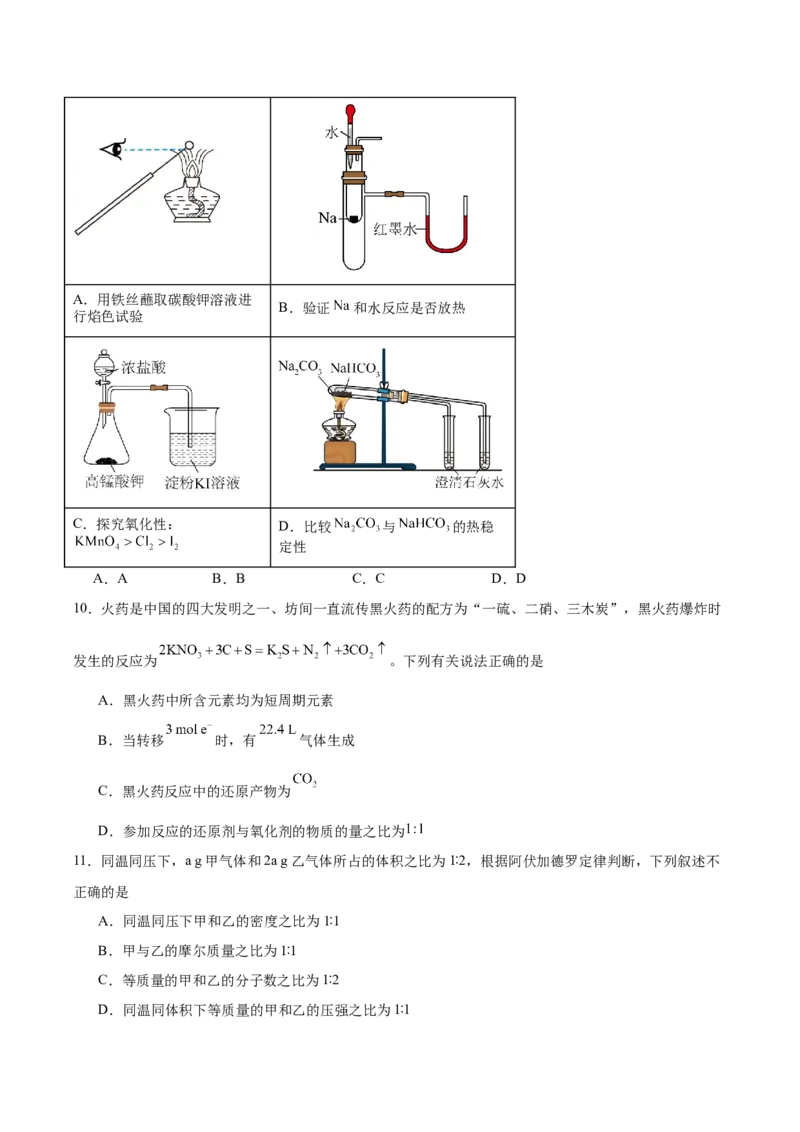
9.用下列装置或操作进行相应实验,不一定能达到实验目的的是A.用铁丝蘸取碳酸钾溶液进
B.验证 和水反应是否放热
行焰色试验
C.探究氧化性: D.比较 与 的热稳
定性
A.A B.B C.C D.D
10.火药是中国的四大发明之一、坊间一直流传黑火药的配方为“一硫、二硝、三木炭”,黑火药爆炸时
发生的反应为 。下列有关说法正确的是
A.黑火药中所含元素均为短周期元素
B.当转移 时,有 气体生成
C.黑火药反应中的还原产物为
D.参加反应的还原剂与氧化剂的物质的量之比为
11.同温同压下,a g甲气体和2a g乙气体所占的体积之比为1∶2,根据阿伏加德罗定律判断,下列叙述不
正确的是
A.同温同压下甲和乙的密度之比为1∶1
B.甲与乙的摩尔质量之比为1∶1
C.等质量的甲和乙的分子数之比为1∶2
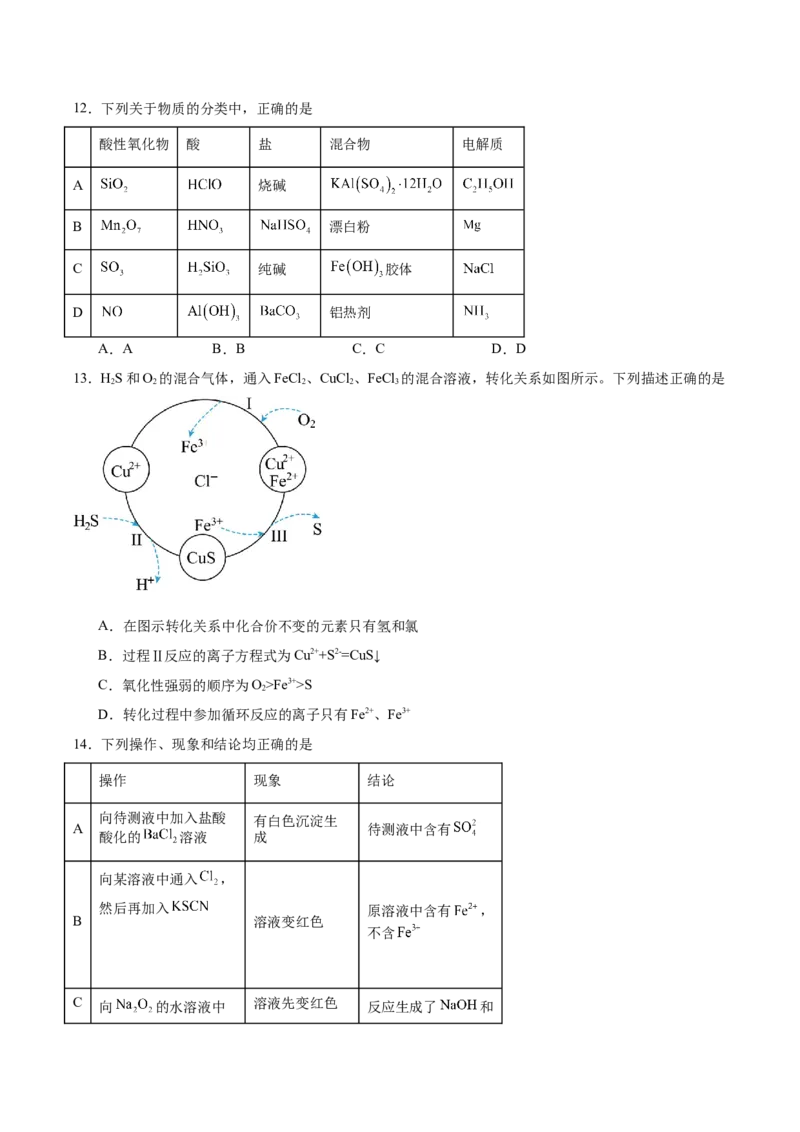
D.同温同体积下等质量的甲和乙的压强之比为1∶112.下列关于物质的分类中,正确的是
酸性氧化物 酸 盐 混合物 电解质
A 烧碱
B 漂白粉
C 纯碱 胶体
D 铝热剂
A.A B.B C.C D.D
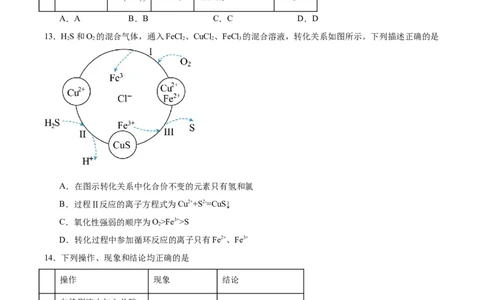
13.HS和O 的混合气体,通入FeCl 、CuCl 、FeCl 的混合溶液,转化关系如图所示。下列描述正确的是
2 2 2 2 3
A.在图示转化关系中化合价不变的元素只有氢和氯
B.过程Ⅱ反应的离子方程式为Cu2++S2-=CuS↓
C.氧化性强弱的顺序为O>Fe3+>S
2
D.转化过程中参加循环反应的离子只有Fe2+、Fe3+
14.下列操作、现象和结论均正确的是
操作 现象 结论
向待测液中加入盐酸 有白色沉淀生
A 待测液中含有
酸化的 溶液 成
向某溶液中通入 ,
然后再加入 原溶液中含有 ,
B 溶液变红色
不含
C 向 的水溶液中 溶液先变红色 反应生成了 和滴入酚酞 后褪色 漂白性的物质
向盛满氯气的集气瓶
D 花瓣褪色 氯气具有漂白性
中放入新鲜的花瓣
A.A B.B C.C D.D
15.下列叙述正确的是
①胶体、溶液、浊液的本质区别是是否具有丁达尔效应
②氢气在氯气中安静燃烧,发出苍白色火焰
③钠的金属性比镁强,故可用钠置换氯化镁溶液中的镁
④碳酸钠和碳酸氢钠均可用作食用碱或工业用碱
⑤金刚石、石墨、 和都是碳的同位素,氕、氘、氚互称为同素异形体
⑥碱金属单质的密度和熔沸点随原子序数的增大而增大
⑦漂白液、漂白粉和漂粉精既可作漂白剂,又可用作游泳池等场所的消毒剂
⑧卤素单质的氧化性随原子序数的逐渐增大而减弱
A.②④⑦⑧ B.①③④⑦ C.②④⑤⑥ D.④⑤⑦⑧
二、解答题
16.现用质量分数为 、密度为 的浓硫酸来配制 的稀硫酸。
可供选择的仪器:①玻璃棒 ②烧瓶 ③烧杯 ④量筒 ⑤托盘天平 ⑥药匙 请回答下列问题:
(1)上述仪器中,在配制稀硫酸时用不到的仪器有 (填代号)。缺少的仪器是 。
(2)经计算,需浓硫酸的体积为 。现有① ② ③ 三种规格的量筒,应选用的
量筒是 (填代号)。
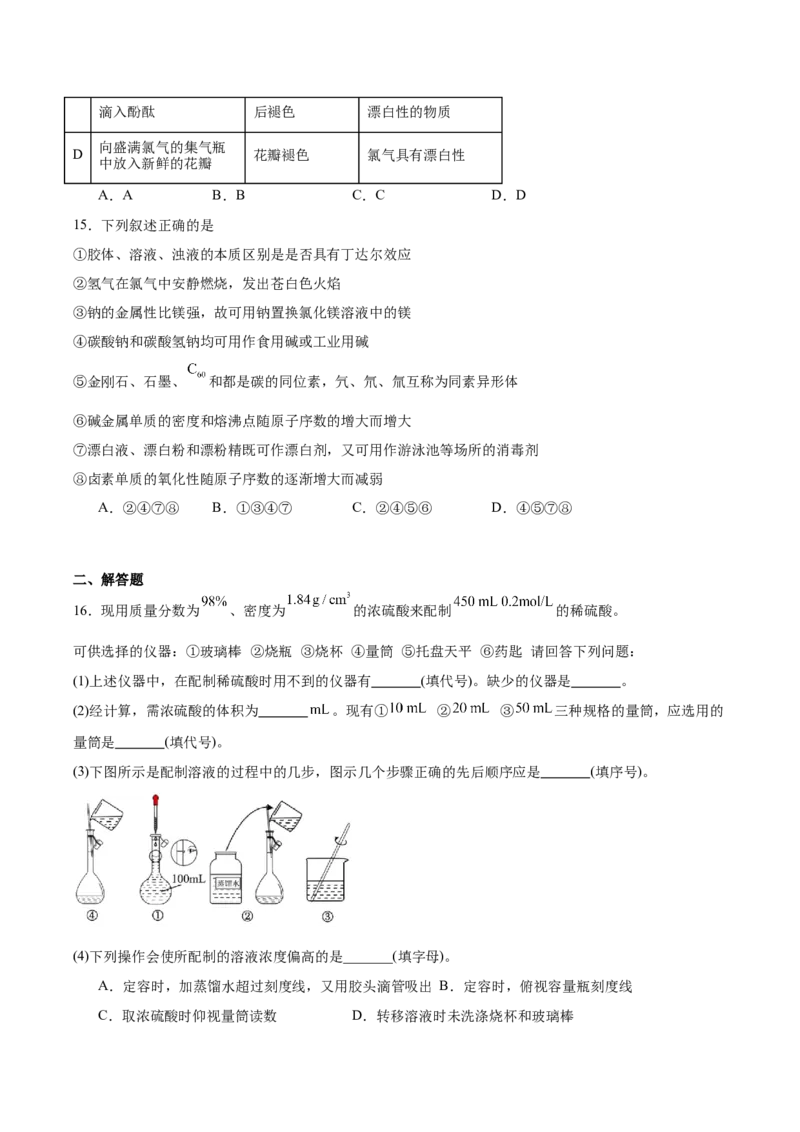
(3)下图所示是配制溶液的过程中的几步,图示几个步骤正确的先后顺序应是 (填序号)。
(4)下列操作会使所配制的溶液浓度偏高的是_______(填字母)。
A.定容时,加蒸馏水超过刻度线,又用胶头滴管吸出 B.定容时,俯视容量瓶刻度线
C.取浓硫酸时仰视量筒读数 D.转移溶液时未洗涤烧杯和玻璃棒17.现有金属单质A、B、C和气体甲、乙、丙及物质D、E、F、G,它们之间能发生如下反应(图中有些
反应的产物和反应的条件没有全部标出)。
请根据以上信息回答下列问题:
(1)写出下列物质的化学式
A、 B、 C、 乙
(2)写出下列反应化学方程式:
反应①
反应③
(3)写出下列反应离子方程式:
反应④
反应⑥
三、填空题
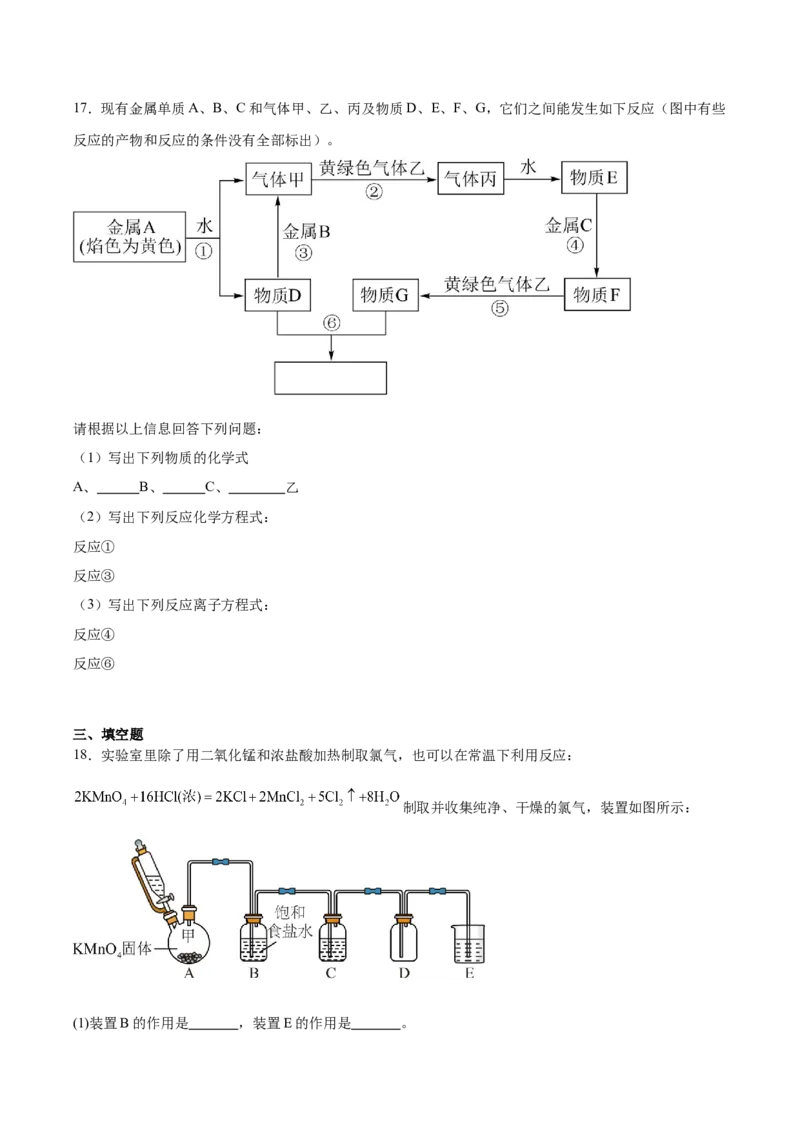
18.实验室里除了用二氧化锰和浓盐酸加热制取氯气,也可以在常温下利用反应:
制取并收集纯净、干燥的氯气,装置如图所示:
(1)装置B的作用是 ,装置E的作用是 。(2)装置C中盛放的药品是 ,装置E中发生反应的化学方程式是 。
(3)用单线桥标明该化学方程式电子转移方向和数目 。
若产生 ,则转移的电子数目为 ,浓盐酸体现了 性质(选填字母编号)。
A.酸性 B.碱性 C.氧化性 D.还原性
四、解答题
19.下表为元素周期表的一部分,请参照元素①~⑨在表中的位置,用相应化学用语回答下列问题:
(1)画出表中形成化合物种类最多元素的原子与原子半径最小的原子形成10电子化合物的结构式 。
(2)写出含有④、⑤元素且既具有离子键又具有非极性共价键化合物的电子式 。
(3)用电子式表示⑤和⑧形成化合物的过程 。
(4)这些元素最高价氧化物对应的水化物中,既能与强酸又能与强碱反应的是 (填化学式),④⑤⑧形
成的简单离子半径由大到小的顺序为 (填离子符号);写出由①②④⑤形成的化合物的化学键类型
。
(5)下列事实能用元素周期律解释并正确的是 (填字母序号)。
a.对应阴离子还原性由强到弱的顺序为⑧>⑨
b.⑧的气态氢化物的稳定性大于④的氢化物
c.原子序数为35的元素最高价氧化物的水化的酸性比⑨最高价氧化物的水化的酸性强
d.④的简单氢化物的沸点高于⑧的氢化物
e.原子半径由小到大的顺序为④<⑧<⑥<⑤参考答案
1.C
2.A
3.A
4.B
5.C
6.C
7.C
8.B
9.A
10.D
11.C
12.C
13.C
14.C
15.A
16.(1) ②⑤⑥ 500mL容量瓶、胶头滴管
(2) 5.4 ①
(3)③④②①
(4)BC
17. Na Al Fe C1 2Na+2H O=2NaOH+H ↑ 2
2 2 2
Al+2NaOH+2H O=2NaAlO +3H ↑ Fe+2H+= Fe2++H↑ Fe3++3OH-=Fe(OH) ↓
2 2 2 2 3
18.(1) 除去氯气中的氯化氢 除去多余的氯气,防止污染空气
(2) 浓硫酸
(3) 0.2N AD
A
19.(1)
(2)(3)
(4) Al(OH) 离子键、共价键(极性键)
3
(5)ae