文档内容
第 71 讲 以性质为主的探究类综合实验
[复习目标] 1.能根据不同情景、不同类型实验特点评价或设计解决问题的简单方案。2.建
立解答探究类综合实验的思维模型。
类型一 物质性质的探究
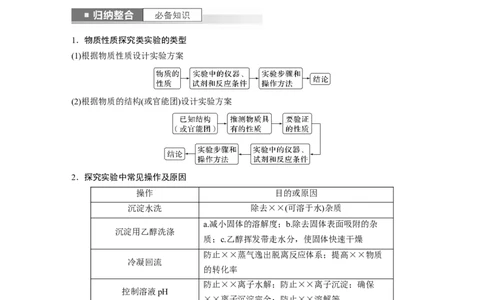
1.物质性质探究类实验的类型
(1)根据物质性质设计实验方案
(2)根据物质的结构(或官能团)设计实验方案
2.探究实验中常见操作及原因
操作 目的或原因
沉淀水洗 除去××(可溶于水)杂质
a.减小固体的溶解度;b.除去固体表面吸附的杂
沉淀用乙醇洗涤
质;c.乙醇挥发带走水分,使固体快速干燥
防止××蒸气逸出脱离反应体系;提高××物质
冷凝回流
的转化率
防止××离子水解;防止××离子沉淀;确保
控制溶液pH
××离子沉淀完全;防止××溶解等
“趁热过滤”后,有时先
向滤液中加入少量水,加 稀释溶液,防止降温过程中杂质析出,提高产品
热至沸腾,然后再“冷却 的纯度
结晶”
加过量A试剂 使B物质反应完全(或提高B物质的转化率等)
温度过高××物质分解(如HO、浓硝酸、
2 2
温度不高于××℃ NH HCO 等)或××物质挥发(如浓硝酸、浓盐酸)
4 3
或××物质氧化(如NaSO 等)或促进××物质水
2 3解(如AlCl 等)
3
减小压强,使液体沸点降低,防止××物质受热
减压蒸馏(减压蒸发)
分解(如HO、浓硝酸、NH HCO 等)
2 2 4 3
抑制××离子的水解(如加热蒸发AlCl 溶液时需
3
蒸发、反应时的气体氛围 在HCl气流中进行,加热MgCl ·6H O制MgCl 时
2 2 2
需在HCl气流中进行等)
配制某溶液前先煮沸水 除去溶解在水中的氧气,防止××物质被氧化
反应容器中用玻璃管和大
指示容器中压强大小,避免反应容器中压强过大
气相通
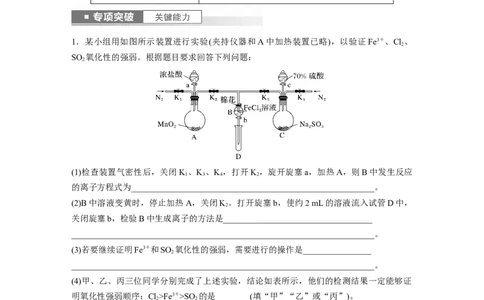
1.某小组用如图所示装置进行实验(夹持仪器和A中加热装置已略),以验证Fe3+、Cl 、
2
SO 氧化性的强弱。根据题目要求回答下列问题:
2
(1)检查装置气密性后,关闭K 、K 、K ,打开K ,旋开旋塞a,加热A,则B中发生反应
1 3 4 2
的离子方程式为_________________________________________________________。
(2)B中溶液变黄时,停止加热A,关闭K 。打开旋塞b,使约2 mL的溶液流入试管D中,
2
关闭旋塞b,检验B中生成离子的方法是___________________________________
_______________________________________________________________________。
(3)若要继续证明Fe3+和SO 氧化性的强弱,需要进行的操作是________________
2
_______________________________________________________________________。
(4)甲、乙、丙三位同学分别完成了上述实验,结论如表所示,他们的检测结果一定能够证
明氧化性强弱顺序:Cl>Fe3+>SO 的是________(填“甲”“乙”或“丙”)。
2 2
过程(2)B中溶液含有的离子 过程(3)B中溶液含有的离子
甲 既有Fe3+又有Fe2+ 有SO
乙 有Fe3+无Fe2+ 有SO
丙 有Fe3+无Fe2+ 有Fe2+
(5)验证结束后,将D换成盛有NaOH溶液的烧杯,打开K、K、K 和K,关闭旋塞a、c,
1 2 3 4
打开旋塞b,从两端鼓入N,这样做的目的是________________________________
2
________________________________________________________________________。2.某研究性学习小组通过下列实验验证AgI沉淀的生成会使I 的氧化能力增强,可将Fe2+
2
氧化。
回答下列问题:
(1)由 AgNO 固体配制 0.1 mol·L-1的 AgNO 溶液 50 mL,下列仪器中不需要使用的有
3 3
______________________(填名称),配制好的溶液应转移到______________(填试剂瓶的名
称)中保存。
(2)步骤1的实验现象是________________;步骤2无明显现象;步骤3最终的实验现象是溶
液中生成黄色沉淀,___________。由此可知,步骤3反应的离子方程式为____________。
(3)为了确证AgI的生成使I 的氧化能力增强而将Fe2+氧化,学习小组在上述实验基础上进
2
行补充实验:分别取少量的______________和步骤3试管中的上层清液于试管a和试管b中,
向两支试管中加入过量的____________,观察到的现象为______________________
________________________________________________________________________。
类型二 反应产物、反应机理的探究
1.解答产物确定题的思路分析
由性质确定反应产物是解此类题目的根本思路,而题目中所涉及的物质,一般分为两类。
要注意物质的特殊性质,比如颜色、状态、气味、溶
第一类 常见的熟悉物质 解性等物理性质,或能与哪些物质反应生成特殊的沉
淀、气体等化学性质
虽然平时接触不多,但其某种组成成分、结构成分
能类比迁移的陌生
第二类 (如离子、原子团、官能团等)必然学过,则可以考虑
物质
与其结构相似的物质的性质,进而推断其具体组成
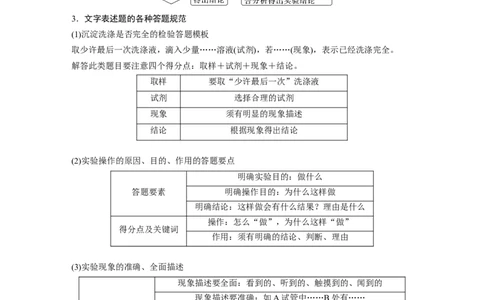
2.寻求反应机理类探究性实验解题流程3.文字表述题的各种答题规范
(1)沉淀洗涤是否完全的检验答题模板
取少许最后一次洗涤液,滴入少量……溶液(试剂),若……(现象),表示已经洗涤完全。
解答此类题目要注意四个得分点:取样+试剂+现象+结论。
取样 要取“少许最后一次”洗涤液
试剂 选择合理的试剂
现象 须有明显的现象描述
结论 根据现象得出结论
(2)实验操作的原因、目的、作用的答题要点
明确实验目的:做什么
答题要素 明确操作目的:为什么这样做
明确结论:这样做会有什么结果?理由是什么
操作:怎么“做”,为什么这样“做”
得分点及关键词
作用:须有明确的结论、判断、理由
(3)实验现象的准确、全面描述
现象描述要全面:看到的、听到的、触摸到的、闻到的
现象描述要准确:如A试管中……B处有……
答题要素
按“现象+结论”格式描述,忌现象结论不分、由理论推现象、
指出具体生成物的名称
溶液中:颜色由……变成……,液面上升或下降(形成液面差),
溶液变浑浊,生成(产生)……沉淀,溶液发生倒吸,产生大量气
泡(或有气体从溶液中逸出),有液体溢出等
得分点及关键词
固体:表面产生大量气泡,逐渐溶解,体积逐渐变小,颜色
由……变成……等
气体:生成……色(味)气体,气体由……色变成……色,先变……后……(加深、变浅、褪色)等
(4)试剂的作用的答题模板
答题要素 试剂的作用是什么?要达到的目的是什么
作用类:“除去”“防止”“抑制”“使……”等,回答要准确
得分点及关键词 作用—目的类:“作用”是“……”,“目的”是“……”,回
答要准确全面
1.某实验小组利用如图装置(部分固定装置略)进行氮气与钙的反应,并探究其产物的性质
及化学式。请回答下列问题。
(1)仪器B的名称是______________,B中固体物质为________。
(2)反应过程中导管末端必须插入试管C的水中,目的是________(填字母)。
A.吸收反应剩余的氮气
B.控制通入气体的流速
C.防止空气中的氧气倒流进入反应装置,干扰反应
(3)将下列操作步骤补充完整:
①打开活塞K并通入N;
2
②点燃酒精灯,进行反应;
③反应结束后,________________________________________________________。
(4)该小组同学认为根据相应的质量关系可以求出生成物的化学式,数据记录如下:
A的质量m/g A与钙的质量m/g A与产物的质量m/g
0 1 2
14.80 15.08 15.15
①通过计算得到化学式CaN,其中x=________。
x 2
②小组同学查阅资料得知产物为Ca N ,能与水强烈反应,请写出Ca N 与水反应的化学方
3 2 3 2
程式:__________________________________________________________________,
设计实验检验Ca N 与水反应的产物(写出必要的操作及现象):_________________
3 2
________________________________________________________________________
________________________________________________________________________
________________________________________________________________________。
2.(2022·海口高三模拟)实验室以浓硫酸、铜与NaOH溶液为原料制取少量NaHSO 并探究
3
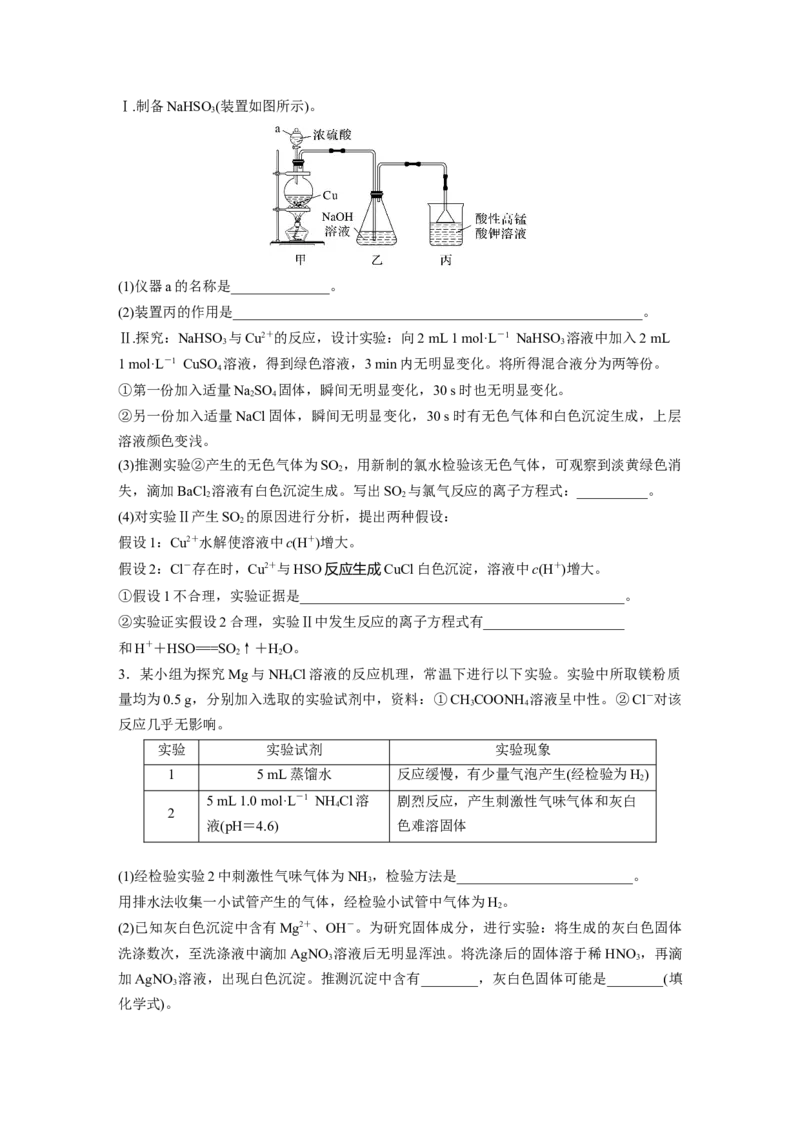
其性质,已知CuCl为白色难溶于水的化合物。Ⅰ.制备NaHSO(装置如图所示)。
3
(1)仪器a的名称是______________。
(2)装置丙的作用是__________________________________________________________。
Ⅱ.探究:NaHSO 与Cu2+的反应,设计实验:向2 mL 1 mol·L-1 NaHSO 溶液中加入2 mL
3 3
1 mol·L-1 CuSO 溶液,得到绿色溶液,3 min内无明显变化。将所得混合液分为两等份。
4
①第一份加入适量NaSO 固体,瞬间无明显变化,30 s时也无明显变化。
2 4
②另一份加入适量NaCl固体,瞬间无明显变化,30 s时有无色气体和白色沉淀生成,上层
溶液颜色变浅。
(3)推测实验②产生的无色气体为SO ,用新制的氯水检验该无色气体,可观察到淡黄绿色消
2
失,滴加BaCl 溶液有白色沉淀生成。写出SO 与氯气反应的离子方程式:__________。
2 2
(4)对实验Ⅱ产生SO 的原因进行分析,提出两种假设:
2
假设1:Cu2+水解使溶液中c(H+)增大。
假设2:Cl-存在时,Cu2+与HSO反应生成CuCl白色沉淀,溶液中c(H+)增大。
①假设1不合理,实验证据是______________________________________________。
②实验证实假设2合理,实验Ⅱ中发生反应的离子方程式有____________________
和H++HSO===SO ↑+HO。
2 2
3.某小组为探究Mg与NH Cl溶液的反应机理,常温下进行以下实验。实验中所取镁粉质
4
量均为0.5 g,分别加入选取的实验试剂中,资料:①CHCOONH 溶液呈中性。②Cl-对该
3 4
反应几乎无影响。
实验 实验试剂 实验现象
1 5 mL蒸馏水 反应缓慢,有少量气泡产生(经检验为H)
2
5 mL 1.0 mol·L-1 NH Cl溶 剧烈反应,产生刺激性气味气体和灰白
4
2
液(pH=4.6) 色难溶固体
(1)经检验实验2中刺激性气味气体为NH ,检验方法是_________________________。
3
用排水法收集一小试管产生的气体,经检验小试管中气体为H。
2
(2)已知灰白色沉淀中含有Mg2+、OH-。为研究固体成分,进行实验:将生成的灰白色固体
洗涤数次,至洗涤液中滴加AgNO 溶液后无明显浑浊。将洗涤后的固体溶于稀HNO,再滴
3 3
加AgNO 溶液,出现白色沉淀。推测沉淀中含有________,灰白色固体可能是________(填
3
化学式)。(3)甲同学认为实验2比实验1反应剧烈的原因是NH Cl溶液中c(H+)大,与Mg反应快。用
4
化学用语解释NH Cl溶液显酸性的原因是____________________________________
4
________________________________________________________________________。
(4)乙同学通过实验3证明甲同学的说法不合理。
实验 实验装置
3
①X是__________________________________________________________________。
②由实验3获取的证据为__________________________________________________。
(5)为进一步探究实验2反应剧烈的原因,进行实验4。
实验 实验试剂 实验现象
4 5 mL NH Cl乙醇溶液 有无色无味气体产生(经检验为H)
4 2
依据上述实验,可以得出Mg能与NH反应生成H。乙同学认为该方案不严谨,需要补充的
2
实验方案是______________________________________________________________。
(6)由以上实验可以得出的结论是____________________________________________
________________________________________________________________________。
1.(2020·全国卷Ⅰ,27)为验证不同化合价铁的氧化还原能力,利用下列电池装置进行实验。
回答下列问题:
(1)由 FeSO ·7H O 固体配制 0.10 mol·L-1 FeSO 溶液,需要的仪器有药匙、玻璃棒、
4 2 4
____________________________________________________(从下列图中选择,写出名称)。
(2)电池装置中,盐桥连接两电极电解质溶液。盐桥中阴、阳离子不与溶液中的物质发生化
学反应,并且电迁移率(u∞)应尽可能地相近。根据下表数据,盐桥中应选择________作为电
解质。
阳离子 u∞×108/(m2·s-1·V-1) 阴离子 u∞×108/(m2·s-1·V-1)
Li+ 4.07 HCO 4.61
Na+ 5.19 NO 7.40Ca2+ 6.59 Cl- 7.91
K+ 7.62 SO 8.27
(3)电流表显示电子由铁电极流向石墨电极。可知,盐桥中的阳离子进入________电极溶液
中。
(4)电池反应一段时间后,测得铁电极溶液中c(Fe2+)增加了0.02 mol·L-1。石墨电极上未见
Fe析出。可知,石墨电极溶液中c(Fe2+)=______________。
(5)根据(3)、(4)实验结果,可知石墨电极的电极反应式为________________________,铁电
极的电极反应式为_________________。因此,验证了Fe2+氧化性小于________,还原性小
于________。
(6)实验前需要对铁电极表面活化。在FeSO 溶液中加入几滴Fe (SO ) 溶液,将铁电极浸泡
4 2 4 3
一段时间,铁电极表面被刻蚀活化。检验活化反应完成的方法是________________
________________________________________________________________________。
2.(2022·广东,17)食醋是烹饪美食的调味品,有效成分主要为醋酸(用HAc表示)。HAc的
应用与其电离平衡密切相关。25 ℃时,HAc的K=1.75×10-5≈10-4.76。
a
(1)配制250 mL 0.1 mol·L-1的HAc溶液,需5 mol·L-1 HAc溶液的体积为__________ mL。
(2)下列关于250 mL容量瓶的操作,正确的是_________________________________。
(3)某小组研究25 ℃下HAc电离平衡的影响因素。
提出假设 稀释HAc溶液或改变Ac-浓度,HAc电离平衡会发生移动。
设计方案并完成实验 用浓度均为0.1 mol·L-1的HAc和NaAc溶液,按下表配制总体积相
同的系列溶液,测定pH,记录数据。
序号 V(HAc) /mL V(NaAc) /mL V(H O) /mL n(NaAc)∶n(HAc) pH
2
Ⅰ 40.00 / / 0 2.86
Ⅱ 4.00 / 36.00 0 3.36
… … … … … …
Ⅶ 4.00 a b 3∶4 4.53
Ⅷ 4.00 4.00 32.00 1∶1 4.65
①根据表中信息,补充数据:a=____________________________________________,
b=____________。
②由实验Ⅰ和Ⅱ可知,稀释HAc溶液,电离平衡______(填“正”或“逆”)向移动;结合表中数据,给出判断理由:__________________________________________________
________________________________________________________________________。
③由实验Ⅱ~Ⅷ可知,增大Ac-浓度,HAc电离平衡逆向移动。
实验结论 假设成立。
(4)小组分析上表数据发现:随着的增加,c(H+)的值逐渐接近HAc的K。
a
查阅资料获悉:一定条件下,按=1配制的溶液中,c(H+)的值等于HAc的K。
a
对比数据发现,实验Ⅷ中pH=4.65与资料数据K=10-4.76存在一定差异;推测可能由物质
a
浓度准确程度不够引起,故先准确测定HAc溶液的浓度再验证。
①移取20.00 mL HAc溶液,加入2滴酚酞溶液,用0.100 0 mol·L-1NaOH溶液滴定至终点,
消耗体积为22.08 mL,则该HAc溶液的浓度为________ mol·L-1。画出上述过程的滴定曲线
示意图并标注滴定终点。
________________________________________________________________________
________________________________________________________________________
②用上述HAc溶液和0.100 0 mol·L-1NaOH溶液,配制等物质的量的HAc与NaAc混合溶液,
测定pH,结果与资料数据相符。
(5)小组进一步提出:如果只有浓度均约为0.1 mol·L-1的HAc和NaOH溶液,如何准确测定
HAc的K?小组同学设计方案并进行实验。请完成下表中Ⅱ的内容。
a
Ⅰ 移取20.00 mL HAc溶液,用NaOH溶液滴定至终点,消耗NaOH溶液V mL
1
Ⅱ ____________________________________________,测得溶液的pH为4.76
实验总结 得到的结果与资料数据相符,方案可行。
(6)根据K 可以判断弱酸的酸性强弱。写出一种无机弱酸及其用途:________________。
a
3.(2021·北京,16)某小组实验验证“Ag++Fe2+Fe3++Ag↓”为可逆反应并测定其平
衡常数。
(1)实验验证
实验Ⅰ.将0.010 0 mol·L-1 Ag SO 溶液与0.040 0 mol·L-1 FeSO 溶液(pH=1)等体积混合,
2 4 4
产生灰黑色沉淀,溶液呈黄色。
实验Ⅱ.向少量Ag粉中加入0.010 0 mol·L-1Fe (SO ) 溶液(pH=1),固体完全溶解。
2 4 3
①取Ⅰ中沉淀,加入浓硝酸,证实沉淀为Ag。现象是________________________。
②Ⅱ中溶液选用Fe (SO ),不选用Fe(NO ) 的原因是________________________。
2 4 3 3 3
综合上述实验,证实“Ag++Fe2+Fe3++Ag↓”为可逆反应。
③小组同学采用电化学装置从平衡移动角度进行验证。补全电化学装置示意图,写出操作及
现象:__________________________________________________________________
________________________________________________________________________。(2)测定平衡常数
实验Ⅲ.一定温度下,待实验Ⅰ中反应达到平衡状态时,取V mL上层清液,用c mol·L-1
1
KSCN标准溶液滴定Ag+,至出现稳定的浅红色时消耗KSCN标准溶液V mL。
1
资料:Ag++SCN-AgSCN↓(白色) K=1012
Fe3++SCN-FeSCN2+(红色) K=102.3
①滴定过程中Fe3+的作用是_________________________________________________。
②测得平衡常数K=______________________。
(3)思考问题
①取实验Ⅰ的浊液测定c(Ag+),会使所测K值_____________________(填“偏高”“偏低”
或“不受影响”)。
②不用实验Ⅱ中清液测定K的原因是________________________________________
________________________________________________________________________。