文档内容
第 11 讲 碳、硅及无机非金属材料
第一部分:高考真题感悟
1.正误判断,正确的打“√”,错误的打“×”
(1)河姆渡出土陶灶,属于陶器,兽首玛瑙杯主要成分为二氧化硅(2021·广东,1BC)( √ )
(2)利用氢氟酸刻蚀石英制作艺术品,是利用了氢氟酸可与SiO 反应(2021·广东,4C)( √ )
2
(3)硅酸钠是一种难溶于水的硅酸盐(2021·浙江6月选考,9A)( × )
(4)SiO 可用来制造光导纤维(2020·浙江7月选考,9B)( √ )
2
(5)向NaSiO 溶液中滴加稀盐酸:NaSiO+2H+===H SiO↓+2Na+(2019·江苏,7D)( × )
2 3 2 3 2 3
(6)高纯硅可用于制作光感电池(2019·全国卷Ⅲ,7A)( √ )
2.(2020·浙江7月选考,24)Ca SiO 是硅酸盐水泥的重要成分之一,其相关性质的说法不正确的是( )
3 5
A.可发生反应:Ca SiO+4NH Cl=====CaSiO +2CaCl +4NH ↑+2HO
3 5 4 3 2 3 2
B.具有吸水性,需要密封保存
C.能与SO 反应生成新盐
2
D.与足量盐酸作用,所得固体产物主要为SiO
2
【答案】D
【解析】Ca SiO 可看作 CaSiO ·2CaO,它与 NH Cl 固体混合加热,反应生成 CaSiO 、CaCl 、NH 和
3 5 3 4 3 2 3
HO,A正确;Ca SiO 能够吸水,故需要密封保存,B正确;由于HSO 的酸性强于HSiO ,Ca SiO 与
2 3 5 2 3 2 3 3 5
SO 反应可生成CaSO ,C正确;Ca SiO 与足量盐酸作用,析出 HSiO 沉淀,故所得固体产物主要是
2 3 3 5 2 3
HSiO,D错误。
2 3
3.(2019·全国卷Ⅰ,7)陶瓷是火与土的结晶,是中华文明的象征之一,其形成、性质与化学有着密切的关
系。下列说法错误的是( )
A.“雨过天晴云破处”所描述的瓷器青色,来自氧化铁
B.闻名世界的秦兵马俑是陶制品,由黏土经高温烧结而成
C.陶瓷是应用较早的人造材料,主要化学成分是硅酸盐
D.陶瓷化学性质稳定,具有耐酸碱侵蚀、抗氧化等优点
【答案】A
【解析】“雨过天晴云破处”所描述的瓷器青色与氧化亚铁有关,而氧化铁显红棕色,A项错误;秦兵马
俑是陶制品,由黏土经高温烧结而成,B项正确;陶瓷以黏土为原料,经高温烧制而成,属于人造材料,
主要成分是硅酸盐,C项正确;陶瓷主要成分是硅酸盐,硅酸盐中硅元素化合价处于最高价,化学性质稳
定,具有耐酸碱侵蚀、抗氧化等优点,D项正确。
4.(2017·全国卷Ⅱ,26)水泥是重要的建筑材料。水泥熟料的主要成分为CaO、SiO,并含有一定量的铁、
2
铝和镁等金属的氧化物。实验室测定水泥样品中钙含量的过程如图所示:回答下列问题:
(1)在分解水泥样品过程中,以盐酸为溶剂,氯化铵为助溶剂,还需加入几滴硝酸。加入硝酸的目的是
__________________,还可以使用____________代替硝酸。
(2)沉淀 A 的主要成分是__________,其不溶于强酸但可与一种弱酸反应,该反应的化学方程式为
___________________________________________________________________________。
(3)加氨水过程中加热的目的是___________________________________________。
沉淀B的主要成分为____________、____________(填化学式)。
(4)草酸钙沉淀经稀HSO 处理后,用KMnO 标准溶液滴定,通过测定草酸的量可间接获知钙的含量,滴
2 4 4
定反应为:MnO+H++HC O―→Mn2++CO +HO。实验中称取0.400 g水泥样品,滴定时消耗了0.050
2 2 4 2 2
0 mol·L-1的KMnO 溶液36.00 mL,则该水泥样品中钙的质量分数为_____________________。
4
【答案】(1)将样品中可能存在的 Fe2+氧化为 Fe3+ HO (2)SiO(或 HSiO) SiO +4HF===SiF ↑+
2 2 2 2 3 2 4
2HO(或HSiO+4HF===SiF ↑+3HO) (3)防止胶体生成,易于沉淀分离 Al(OH) Fe(OH) (4)45.0%
2 2 3 4 2 3 3
【解析】(1)水泥样品中含有铁的氧化物。加入盐酸后的溶液中可能含有Fe3+、Fe2+,Fe2+在pH为4~5时
不能形成沉淀除去,所以需要先加入氧化剂将Fe2+氧化为Fe3+,故加入硝酸的目的是将样品中可能存在的
Fe2+氧化为Fe3+;双氧水是一种强氧化剂,可将Fe2+氧化为Fe3+,本身被还原为水,不会引入新的杂质离
子,故可用双氧水代替硝酸。
(2)钙、铁、铝和镁等金属的氧化物都能溶于盐酸和硝酸的混合液,而二氧化硅不与盐酸、硝酸反应,故沉
淀A的主要成分为SiO ;二氧化硅可与氢氟酸反应,生成四氟化硅和水,该反应的化学方程式为SiO +
2 2
4HF===SiF ↑+2HO。
4 2
(3)Fe3+和Al3+在pH为4~5时可水解生成氢氧化铁、氢氧化铝,水解过程中会生成氢氧化铁胶体和氢氧化
铝胶体,不利于分离出沉淀,加热可使胶体聚沉,有利于分离出沉淀,所以加热可防止胶体的生成,易于
沉淀分离,故沉淀B的主要成分为Al(OH) 、Fe(OH) 。
3 3
(4)根据化合价升降法、电荷守恒和质量守恒配平可得:2MnO+6H++5HC O===2Mn2++10CO↑+
2 2 4 2
8HO,设含钙的物质的量为x mol,由反应方程式和钙元素守恒可得关系式:
2
5Ca2+ ~ 5HC O ~ 2MnO
2 2 4
5 mol 2 mol
x mol 0.050 0 mol·L-1×36.00×10-3L
解得x=4.5×10-3,则0.400 g水泥样品中钙元素的质量为4.5×10-3 mol×40 g·mol-1=0.180 g,故该水泥样
品中钙的质量分数为×100%=45.0%。
第二部分:最新模拟精练
完卷时间:50分钟
一、选择题(每小题只有一个正确选项,共12*5分)1.(2022·江苏苏州·模拟预测)工业可通过Al O+N +3C 2AlN+3CO制得高温陶瓷材料AlN。下列说
2 3 2
法正确的是
A.传统陶瓷主要成分是硅酸盐 B.AlN是分子晶体
C.N 发生氧化反应 D.反应为复分解反应
2
【答案】A
【解析】A.玻璃、水泥和陶瓷均属于无机硅酸盐产品,则传统陶瓷主要成分是硅酸盐,A正确;B.AlN
具有很高的熔点,故不是分子晶体,而是共价晶体(或者称为原子晶体),B错误;C.Al O+N +3C
2 3 2
2AlN+3CO反应中N的化合价由0价降低到-3价,故N 发生还原反应,C错误;D.复分解反应是指两种
2
化合物互相交换成分生成两种新的化合物的反应,故该反应不属于复分解反应,属于氧化还原反应,D错
误;故答案为:A。
2.(2022·江苏·模拟预测)我国拟定于2022年底发射“爱因斯坦”探针卫星,首次填补时域天文观测和
高能天体物理研究的国际空白。X射线主探器单体结构如图,下列有关物质的性质与用途不具有对应关系
的是
A.金属铍有延展性,可作主探器的射线窗
B.石英对光线全反射,可作光导材料
C.SiO 属于原子晶体,可作耐高温材料
2
D.NaI、CsI遇光易分解,作为闪烁体
【答案】D
【解析】A.铍窗利用了铍的延展性,将铍做成铍片,A不选;B.石英对光线全反射,传导光的能力非常
强,可作光导材料,B不选;C.SiO 属于原子晶体,熔点很高,可作耐高温材料,C不选;D.NaI、CsI
2能作为闪烁体的原因是:吸收高能粒子,闪烁体中的电子被激发跃迁后又回到基态,释放光能而发光,不
涉及化学变化,即不涉及NaI、CsI的分解,D选;答案选D。
3.(2022·上海虹口·模拟预测)天然 晶体称为水晶,是古代重要宝石品种。有关 的说法错误的
是
A.属于原子晶体 B.属于非电解质 C.属于酸性氧化物 D.含有 键
【答案】D
【解析】A.SiO 属于原子晶体,A正确;B.SiO 难溶于水,在熔融状态下也不能导电,属于非电解质,
2 2
B正确;C.SiO 属于酸性氧化物,能和强碱反应生成硅酸盐和水,C正确;D.SiO 晶体中只含有Si-O键,
2 2
不含Si=O键,D错误;故选D。
4.(2022·江苏·模拟预测)“十四五”工作报告强调,中国将加速建设新能源供给消纳体系。硅基能源逐
步取代碳基能源的革命,必须举全国之力破解芯片技术受制于人的困局。以下说法不正确的是
A.碳基能源主要指煤、石油、天然气,我国的煤炭资源禀赋优于石油
B.硅在地壳中的含量仅次于氧,从沙滩到用户,硅发生了还原反应
C.半导体工艺中一般需要在晶硅中掺杂第IIIA族与第VA族元素
D.半导体工艺中用刻蚀剂-电子级氟化氢可加压保存在玻璃罐体中
【答案】D
【解析】A.碳基能源主要指煤、石油、天然气,我国的煤炭储量及开发技术均优于石油,A说法正确;
B.硅在地壳中的含量仅次于氧,从沙滩到用户,硅由SiO 转化为硅单质,化合价下降,发生了还原反应,
2
B说法正确;C.晶硅中掺杂第IIIA族与第VA族元素,形成PN结,在接通电源或受光的激发,自由电子
可向空穴方向移动(单向移动) (见图), C说法正确;D.氟化氢可
与玻璃容器中二氧化硅发生反应,故D说法错误。故选D。
5.(2022·北京·模拟预测)近年来我国取得让世界瞩目的科技成果,化学功不可没。下列说法不正确的是
A.“天和核心舱”电推进系统中的腔体采用氮化硼陶瓷属于有机物
B.“北斗系统”组网成功,北斗芯片中的半导体材料为硅C.“嫦娥五号”运载火箭用液氧液氢推进剂,产物对环境无污染
D.“奋斗者”号潜水器外壳材料为钛合金,22号钛元素属于过渡元素
【答案】A
【解析】A.氮化硼陶瓷属于无机物,A说法错误;B.硅单质是常用的半导体材料,可用于制作芯片,B
说法正确;C.液氧液氢作推进剂,产物是水,对环境没有污染,C说法正确;D.钛位于元素周期表第四
周期第ⅡB族,属于过渡金属元素,D说法正确;答案选A。
6.(2022·河北沧州·二模)作为我国将“碳达峰、碳中和”纳入生态文明建设整体布局后的首个世界级体
育盛会,北京2022年冬奥会向世界展现了我国的科技实力。下列说法错误的是
A.速滑运动员佩戴的头盔使用的碳纤维属于无机材料
B.可穿戴式智能测温设备“测温创可贴”的测温芯片主要成分是二氧化硅
C.二氧化碳取代氟利昂作为制冷剂,对保护臭氧层作出重要贡献
D.可降解餐具的原料玉米淀粉、甘蔗渣的主要成分都属于糖类
【答案】B
【解析】A.碳纤维是由碳单质形成的,属于无机材料,A正确;B.硅是良好的半导体材料,可用于制作
芯片,则测温芯片主要成分是硅,B错误;C.释放氟利昂对臭氧层有损害,用二氧化碳取代氟利昂作为
制冷剂,可保护臭氧层,C正确;D.淀粉属于多糖、甘蔗中蔗糖属于二糖,它们都属于糖类,D正确;
故选:B。
7.(2022·上海·三模)由于石墨烯独特的结构,在石墨烯薄膜上施加较低的电压(1-10V)即可产生较高的热
量,平昌冬奥会“北京8分钟”主创团队用石墨烯制作了20℃能发热4h的智能服饰,向世界展现了新时
代的中国形象,下列说法中错误的是
A.石墨烯是能导热的金属材料
B.石墨烯属于单质
C.石墨烯能导电
D.在石墨烯薄膜上施加电压,使电能转化为热能
【答案】A
【解析】A.石墨烯属于碳单质,是能够导热的非金属材料,A错误;B.石墨烯是碳的单质,B正确;C.石墨烯属于碳单质,碳单质具有良好的导电性,可以导电,C正确;D.根据题干信息可知,在石墨烯
薄膜上施加较低的电压(1-10V)即可产生较高的热量,使电能转化为热能,D正确;答案选A。
8.(2022·山东师范大学附中模拟预测)部分含碳物质的分类与相应碳元素的化合价关系如图所示。下列
说法错误的是
A.固态p可做制冷剂用于人工降雨
B.p转化为r可通过化合反应来实现
C.m转化为n或o的反应均释放能量
D.n的一种同素异形体中既存在共价键也存在范德华力
【答案】C
【解析】依据价类二维图可知:m为甲烷、n为碳单质、o为CO、p为CO、r为碳酸盐。A.p为二氧化
2
碳,可做制冷剂用于人工降雨,A项正确;B.二氧化碳与氧化钙反应生成盐碳酸钙,是化合反应实现,B
项正确;C.甲烷转化为二氧化碳是放热反应,C项错误;D.碳有多种同素异形体,如金刚石、石墨等,
石墨既存在共价键也存在范德华力,D项正确;答案选C。
9.(2022·全国·模拟预测)“千淘万漉虽辛苦,吹尽狂沙始到金。”诗句中的“沙”的主要成分是 ,
下列说法错误的是
A. 属于酸性氧化物,不与任何酸反应
B.“水玻璃”可以由 与NaOH溶液反应制得
C. 是制取传统硅酸盐产品玻璃的原料之一
D.通常所说的“从沙滩到用户”,这句话涉及工业上制备粗硅的工艺
【答案】A
【解析】A. 属于酸性氧化物,但其能与氢氟酸反应,A项错误;B.“水玻璃”是硅酸钠溶液,可由 与NaOH溶液反应制得,B项正确;C.普通玻璃的成分是硅酸钠、硅酸钙和二氧化硅, 与碳
酸钠在高温条件下反应生成硅酸钠和二氧化碳,C项正确;D.“从沙滩到用户”的实质为工业上制粗硅
的反应原理,即 ,D项正确;故选A。
10.(2022·广东茂名·一模)硅及其化合物在人类进步中发挥了重要作用。 和 用于制造芯片,
用于制造光纤, 用作木材防火剂。下列说法正确的是
A. 在自然界以游离态存在 B. 和 具有优良的导电性
C. 不与酸反应 D. 溶液可与 反应
【答案】D
【解析】A.硅在自然界中以化合态存在,而不是游离态形式存,故A错误;B. 和 属于半导体,导
电能力弱,故B错误;C.SiO 能与氢氟酸发生反应,而不是不与任何酸反应,故C错误;D.碳酸的酸
2
性比硅酸强,则NaSiO 溶液可与 反应生成HSiO,故D正确;故选:D。
2 3 2 3
11.(2022·广东·模拟预测)寿山石是中国传统四大印章石之一,含叶蜡石、高岭石等黏土矿物。下列说
法错误的是
A.寿山石的硬度与金刚石相当 B.叶蜡石、高岭石的主要成分属于硅酸盐
C.寿山石的红色条纹与Fe O 含量有关 D.寿山石印章要避免与强酸、强碱接触
2 3
【答案】A
【解析】A.已知寿山石是中国传统四大印章石之一,雕刻印章时通常用钢刀或金刚石进行,故寿山石的
硬度比金刚石小,A错误;
B.黏土属于硅酸盐,故叶蜡石、高岭石的主要成分属于硅酸盐,B正确;C.Fe O 是一种红棕色粉末,
2 3
故寿山石的红色条纹与Fe O 含量有关,C正确;D.寿山石中含有铝硅酸盐,既能与强酸又能与强碱反应,
2 3
故寿山石印章要避免与强酸、强碱接触,D正确;故答案为:A。
12.(2022·天津市咸水沽第一中学模拟预测)第24届冬奥会于2022年2月4日在北京开幕,“科技冬
奥”理念,体现在方方面面。下列说法不正确的是
A.滑雪板板心木质材料的主要成分为纤维素,属于天然有机高分子
B.开幕式专用演出服为石墨烯智能发热材料,属于新型有机非金属材料C.首钢滑雪大跳台的钢结构赛道为铁合金,属于金属材料
D.“天机芯”是全球首款异构融合类脑计算芯片,其主要成分是高纯硅
【答案】B
【解析】A.木质材料的主要成分为纤维素,纤维素属于天然有机高分子化合物,A正确;B.石墨烯是碳
单质的一种形式,属于无机非金属材料,B错误;C.钢是铁碳合金,属于金属材料,C正确;D.计算机
芯片的主要成分是硅,D正确;故答案选B。
二、主观题(共3小题,共40分)
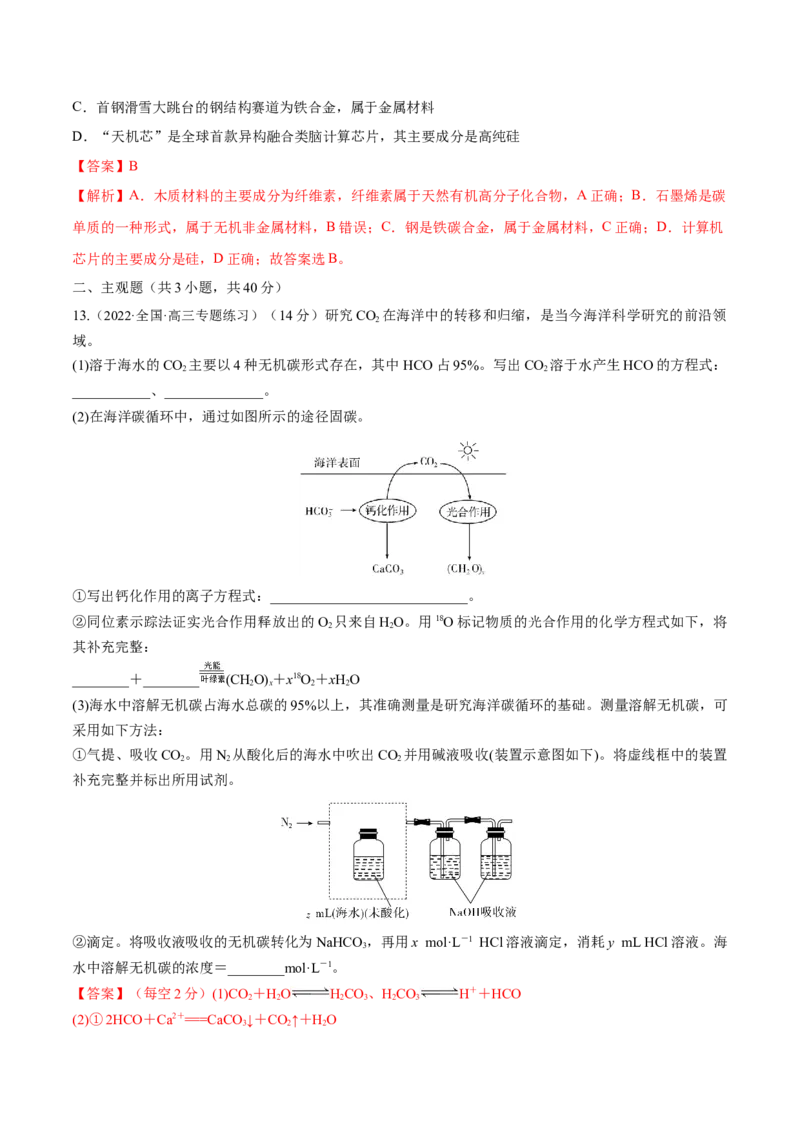
13.(2022·全国·高三专题练习)(14分)研究CO 在海洋中的转移和归缩,是当今海洋科学研究的前沿领
2
域。
(1)溶于海水的CO 主要以4种无机碳形式存在,其中HCO占95%。写出CO 溶于水产生HCO的方程式:
2 2
___________、______________。
(2)在海洋碳循环中,通过如图所示的途径固碳。
①写出钙化作用的离子方程式:____________________________。
②同位素示踪法证实光合作用释放出的O 只来自HO。用18O标记物质的光合作用的化学方程式如下,将
2 2
其补充完整:
________+________ (CHO)+x18O+xHO
2 x 2 2
(3)海水中溶解无机碳占海水总碳的95%以上,其准确测量是研究海洋碳循环的基础。测量溶解无机碳,可
采用如下方法:
①气提、吸收CO 。用N 从酸化后的海水中吹出CO 并用碱液吸收(装置示意图如下)。将虚线框中的装置
2 2 2
补充完整并标出所用试剂。
②滴定。将吸收液吸收的无机碳转化为NaHCO ,再用x mol·L-1 HCl溶液滴定,消耗y mL HCl溶液。海
3
水中溶解无机碳的浓度=________mol·L-1。
【答案】(每空2分)(1)CO +HO HCO、HCO H++HCO
2 2 2 3 2 3
(2)①2HCO+Ca2+===CaCO ↓+CO↑+HO
3 2 2②xCO 2xHO
2
(3)① ②
【解析】(1)CO 溶于水产生HCO的方程式为CO+HO HCO、HCO H++HCO。
2 2 2 2 3 2 3
(2)①根据题图找出钙化作用的反应物和生成物,可知发生反应的离子方程式为Ca2++2HCO===CaCO ↓+
3
CO↑+HO。②根据题图中光合作用及元素守恒可配平,注意18O的标记。
2 2
(3)①酸化海水不能用挥发性的酸,因为要用NaOH溶液吸收CO ,故选用HSO 溶液酸化。②NaHCO ~
2 2 4 3
HCl,海水中溶解无机碳的浓度为=mol·L-1。
14.(12分)(2022·全国·高三专题练习)硅是带来人类文明的重要元素之一,从传统材料到信息材料的发
展过程中创造了一个又一个奇迹。
(1)新型陶瓷Si N 的熔点高、硬度大、化学性质稳定。工业上可以采用化学气相沉积法,在 H 的保护下,
3 4 2
使SiCl 与N 反应生成Si N 沉积在石墨表面,写出该反应的化学方程式:________________________。
4 2 3 4
(2)一种工业用硅(含少量钾、钠、铁、铜的氧化物),已知硅的熔点是1 420 ℃,高温下氧气及水蒸气能明
显腐蚀氮化硅。一种合成氮化硅的主要工艺流程如下:
①净化N 和H 时,铜屑的作用是___________________________,
2 2
硅胶的作用是_________________________________________________。
②在氮化炉中发生反应3SiO(s)+2N(g)===Si N(s)+3O(g) ΔH=-727.5 kJ·mol-1,开始时,严格控制氮
2 2 3 4 2
气的流速以控制温度的原因是___________________________;
体系中要通入适量的氢气是为了____________________________________________________________。
③X可能是________(填“盐酸”“硝酸”“硫酸”或“氢氟酸”)。
【答案】(每空2分)(1)3SiCl +2N+6H===Si N+12HCl
4 2 2 3 4
(2)①除去原料气中的氧气 除去生成的水蒸气
②该反应是放热反应,防止局部过热,导致硅熔化成团,阻碍与N 的接触 将体系中的氧气转化为水蒸气,
2
而易被除去(或将整个体系中空气排尽)
③硝酸【解析】(1)根据原子个数守恒可写出化学方程式3SiCl +2N +6H===Si N +12HCl。(2)①由于氧气和水
4 2 2 3 4
蒸气都能腐蚀氮化硅,而氮气和氢气中含有水蒸气和氧气,所以铜屑的作用是除去氧气,硅胶的作用是除
去水蒸气。②因为该反应是放热反应,如果温度过高,局部过热,会导致硅熔化成团,阻碍与 N 的接触;
2
通入氢气能将体系中的氧气转化为水蒸气,而易被除去。③由于工业用硅中含有铜的氧化物,在反应中氧
化铜能被还原生成铜,因此要除去铜应该选择硝酸,盐酸和硫酸不能溶解铜,氢氟酸能腐蚀氮化硅。
15.(2021·全国·高三开学考试)(14分)化合物 A 由三种短周期元素组成,某兴趣小组进行了如下实
验:
已知:气体甲为纯净物且只含两种元素,在标况下体积为 672 mL;固体甲为常用的耐火材料,溶液乙为
建筑行业中常用的粘合剂。请回答下列问题:
(1)A 的组成元素为_____(用元素符号表示),A 的化学式为_____;
(2)写出A溶于盐酸的化学方程式______________________________。
(3)写出气体甲与 NaOH(aq)反应的离子方程式___________________。
(4)往溶液乙中通入少量 CO 气体发生的化学方程式___________________。
2
(5)高温下A 与足量氯气能发生剧烈爆炸,生成三种常见化合物,试写出相应的化学方程式_____。
【答案】(除标注外,每空2分)(1)Mg、Si、H(3分) MgSi H (3分)
2 4
(2)MgSi H+2HCl=Si H↑+MgCl
2 4 2 6 2
(3)Si H+4OH-+2H O=2 +7H ↑
2 6 2 2
(4)NaSiO + CO + H O=Na CO + H SiO↓
2 3 2 2 2 3 2 3
(5)MgSi H+7Cl MgCl +2SiCl +4HCl
2 4 2 2 4
【解析】2.52 gA中加入20 mL3 mol/L的盐酸发生反应生成气体甲为纯净物且只含两种元素,在标况下体
积为672 mL,物质的量 ,气体甲和120 mL1 mol/L的氢氧化钠溶液恰好完全反应
生成气体单质乙和溶液乙,溶液乙为建筑行业中常用的粘合剂,溶液乙为硅酸钠溶液,说明A中含硅元素、
氢元素,溶液甲只含一种溶质,加入过量氢氧化钠溶液生成氢氧化物白色沉淀,加热得到白色固体甲为常用的耐火材料,固体甲应为氧化镁,白色沉淀为Mg(OH) ,则判断甲溶液中含Mg元素,为MgCl 溶液,
2 2
计算得到镁的物质的量 ,则A含有的元素为Mg、Si、H元素,气体甲为纯
净物且只含两种元素为Si、H组成,气体物质的量0.03 mol,和120 mL1 mol/L的氢氧化钠溶液恰好完全反
应生成气体单质乙和溶液乙,消耗NaOH物质的量=0.12 L×1 mol/L=0.12 mol,则气体甲和氢氧化钠反应的
物质的量之比为1:4,生成 和氢气,根据原子守恒得到甲为Si H,甲和氢氧化钠溶液反应的离子方
2 6
程式:Si H+4OH-+2H O=2 -+7H ↑,n(Si)=0.06 mol,所含氢元素物质的量
2 6 2 2
,n(Mg):n(Si):n(H)=0.03mol:
0.06mol:0.12mol=1:2:4,A为MgSi H。
2 4
(1) 根据上述分析, A含有的元素为Mg、Si、H元素;A为MgSi H;故答案为:Mg、Si、H;
2 4
MgSi H;
2 4
(2) 根据上述分析,A为MgSi H,气体甲为Si H,溶液甲为MgCl ,故A溶于盐酸的化学方程式为
2 4 2 6 2
MgSi H+2HCl=Si H↑+MgCl 。
2 4 2 6 2
(3)气体甲为Si H,气体甲和氢氧化钠溶液反应生成硅酸钠和氢气,离子方程式为:Si H+4OH-+2H O=2
2 6 2 6 2
+7H ↑,故答案为:Si H+4OH-+2H O=2 +7H ↑;
2 2 6 2 2
(4) 溶液乙为硅酸钠溶液,通入少量二氧化碳反应生成硅酸沉淀和碳酸钠,化学方程式为:NaSiO + CO
2 3 2
+ H O=Na CO + H SiO↓,故答案为:NaSiO + CO + H O=Na CO + H SiO↓;
2 2 3 2 3 2 3 2 2 2 3 2 3
(5) 高温下,A与足量氯气能发生剧烈爆炸,生成三种常见化合物为氯化镁、四氯化硅和氯化氢,反应的
化学方程式:MgSi H+7Cl MgCl +2SiCl +4HCl,故答案为:MgSi H+7Cl MgCl +2SiCl +4HCl。
2 4 2 2 4 2 4 2 2 4