文档内容
第 12 练 有关
反应热的综合考查
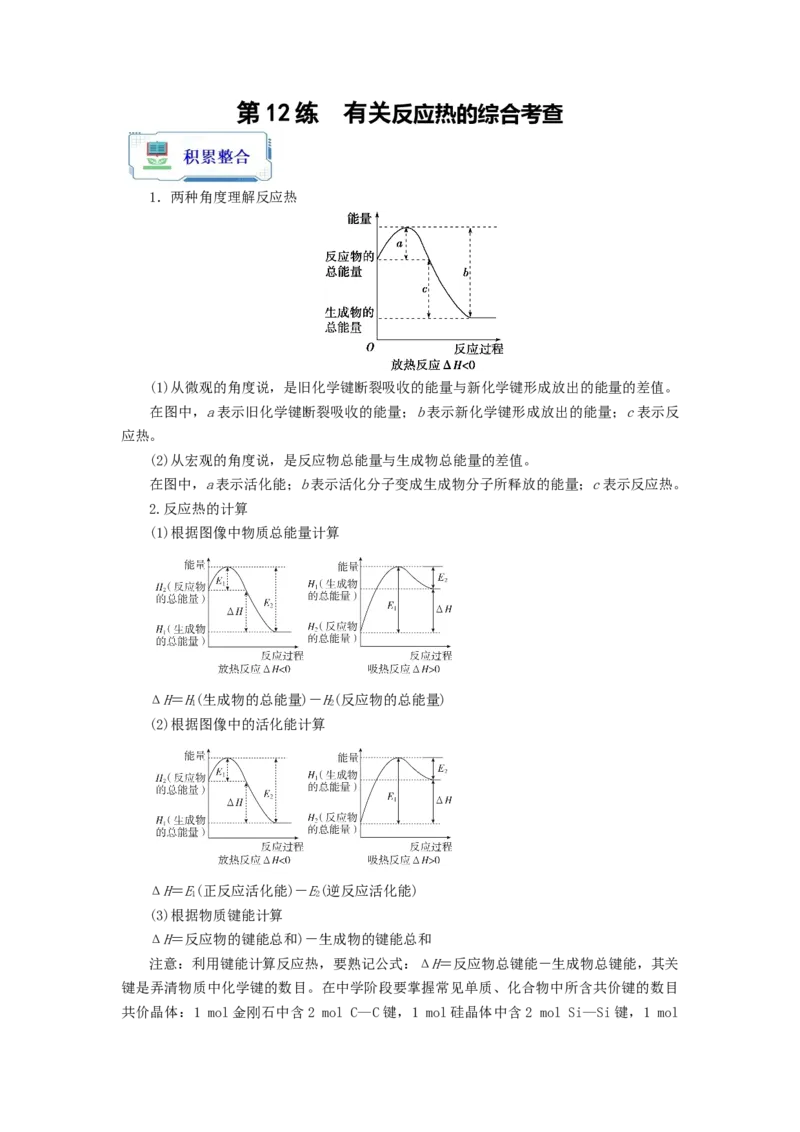
1.两种角度理解反应热
(1)从微观的角度说,是旧化学键断裂吸收的能量与新化学键形成放出的能量的差值。
在图中,a表示旧化学键断裂吸收的能量;b表示新化学键形成放出的能量;c表示反
应热。
(2)从宏观的角度说,是反应物总能量与生成物总能量的差值。
在图中,a表示活化能;b表示活化分子变成生成物分子所释放的能量;c表示反应热。
2.反应热的计算
(1)根据图像中物质总能量计算
ΔH=H(生成物的总能量)-H(反应物的总能量)
1 2
(2)根据图像中的活化能计算
ΔH=E(正反应活化能)-E(逆反应活化能)
1 2
(3)根据物质键能计算
ΔH=反应物的键能总和)-生成物的键能总和
注意:利用键能计算反应热,要熟记公式:ΔH=反应物总键能-生成物总键能,其关
键是弄清物质中化学键的数目。在中学阶段要掌握常见单质、化合物中所含共价键的数目
共价晶体:1 mol金刚石中含2 mol C—C键,1 mol硅晶体中含2 mol Si—Si键,1 molSiO 晶体中含4 mol Si—O键;分子晶体:1 mol P 中含有6 mol P—P键,1 mol CH 中
2 4 2 6
含有6 mol C—H键和1 mol C—C键。
(4)利用盖斯定律进行计算
①
ΔH=ΔH+ΔH
1 2
②根据热化学方程式中物质与反应热之间的比例关系利用加和法计算反应热。
1.(2023·福建莆田·统考模拟预测)工业上在 催化作用下生产 的反应为
,该反应可看作两步:①
(快);② (慢)。下列说法正确的是
A.该反应活化能为
B.减小 的浓度能降低 的生成速率
C. 的存在使有效碰撞次数增加,降低了该反应的焓变
D.①的活化能一定大于②的活化能
2.(2023·重庆·重庆南开中学校考三模)将2 mol 和3 mol 置于密闭容器中,在
250℃下只发生如下两个反应:
kJ/mol
kJ/mol
一段时间后, 和 恰好全部消耗,共放出303 kJ热量。
已知:部分化学键的键能如下表所示
化学键 (ClF中) ( 中)
键能/(kJ/mol) 157 243 248 X
则X的值为
A.172 B.202 C.238 D.258
3.(2023·浙江·统考模拟预测)叔丁基溴在乙醇中反应的能量变化如图所示:
反应1:(CH)CBr→(CH)C=CH +HBr
3 3 3 2 2
反应2:C HOH+(CH )CBr→(CH)COC H+HBr
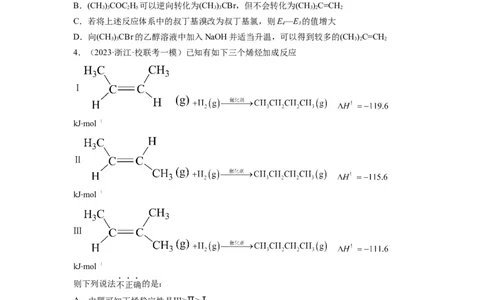
2 5 3 3 3 3 2 5下列说法不正确的是
A.过渡态能量:①>②>③
B.(CH)COC H 可以逆向转化为(CH)CBr,但不会转化为(CH)C=CH
3 3 2 5 3 3 3 2 2
C.若将上述反应体系中的叔丁基溴改为叔丁基氯,则E—E 的值增大
4 3
D.向(CH)CBr的乙醇溶液中加入NaOH并适当升温,可以得到较多的(CH)C=CH
3 3 3 2 2
4.(2023·浙江·校联考一模)已知有如下三个烯烃加成反应
Ⅰ
kJmol
⋅
Ⅱ
kJmol
⋅
Ⅲ
kJmol
则⋅下列说法不正确的是:
A.由题可知丁烯稳定性是Ⅲ>Ⅱ>Ⅰ
B.由题可知断裂碳碳π键和氢氢σ键所消耗的能量总是小于形成两个碳氢σ键所放出的能
量
C.由题可知烯烃的稳定性与双键碳上的取代基和构型有关
D.由题可知,由于Ⅰ、Ⅱ、Ⅲ断键和成键都一样,因此反应的 不能由键能计算得到
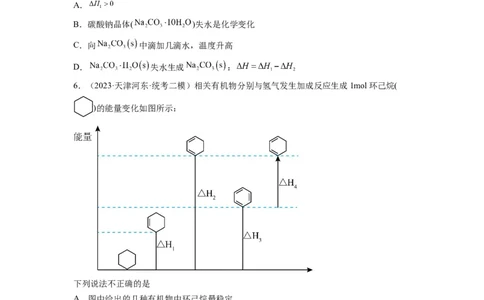
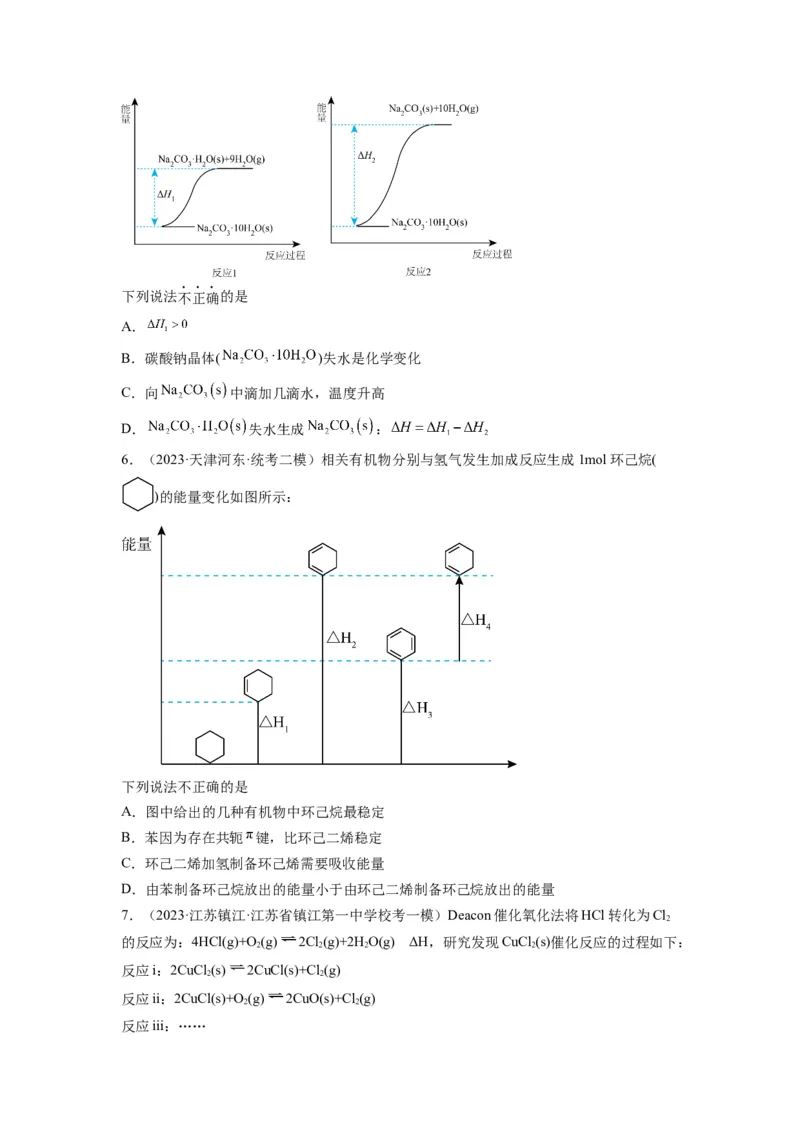
5.(2023·北京房山·统考二模)碳酸钠晶体( )失水可得到
或 ,两个化学反应的能量变化示意图如下:下列说法不正确的是
A.
B.碳酸钠晶体( )失水是化学变化
C.向 中滴加几滴水,温度升高
D. 失水生成 :
6.(2023·天津河东·统考二模)相关有机物分别与氢气发生加成反应生成1mol环己烷(
)的能量变化如图所示:
下列说法不正确的是
A.图中给出的几种有机物中环己烷最稳定
B.苯因为存在共轭 键,比环己二烯稳定
C.环己二烯加氢制备环己烯需要吸收能量
D.由苯制备环己烷放出的能量小于由环己二烯制备环己烷放出的能量
7.(2023·江苏镇江·江苏省镇江第一中学校考一模)Deacon催化氧化法将HCl转化为Cl
2
的反应为:4HCl(g)+O (g) 2Cl(g)+2HO(g) ΔH,研究发现CuCl (s)催化反应的过程如下:
2 2 2 2
反应i:2CuCl (s) 2CuCl(s)+Cl (g)
2 2
反应ii:2CuCl(s)+O (g) 2CuO(s)+Cl (g)
2 2
反应iii:……下列关于Deacon催化氧化法制Cl 的说法正确的是
2
A.反应i增大压强,达新平衡后Cl 浓度减小
2
B.反应4HCl(g)+O (g) 2Cl(g)+2HO(g)的ΔH>0
2 2 2
C.由反应过程可知催化剂参与反应,通过改变反应路径提高平衡转化率
D.推断反应iii应为CuO(s)+2HCl(g) CuCl (s)+HO(g)
2 2
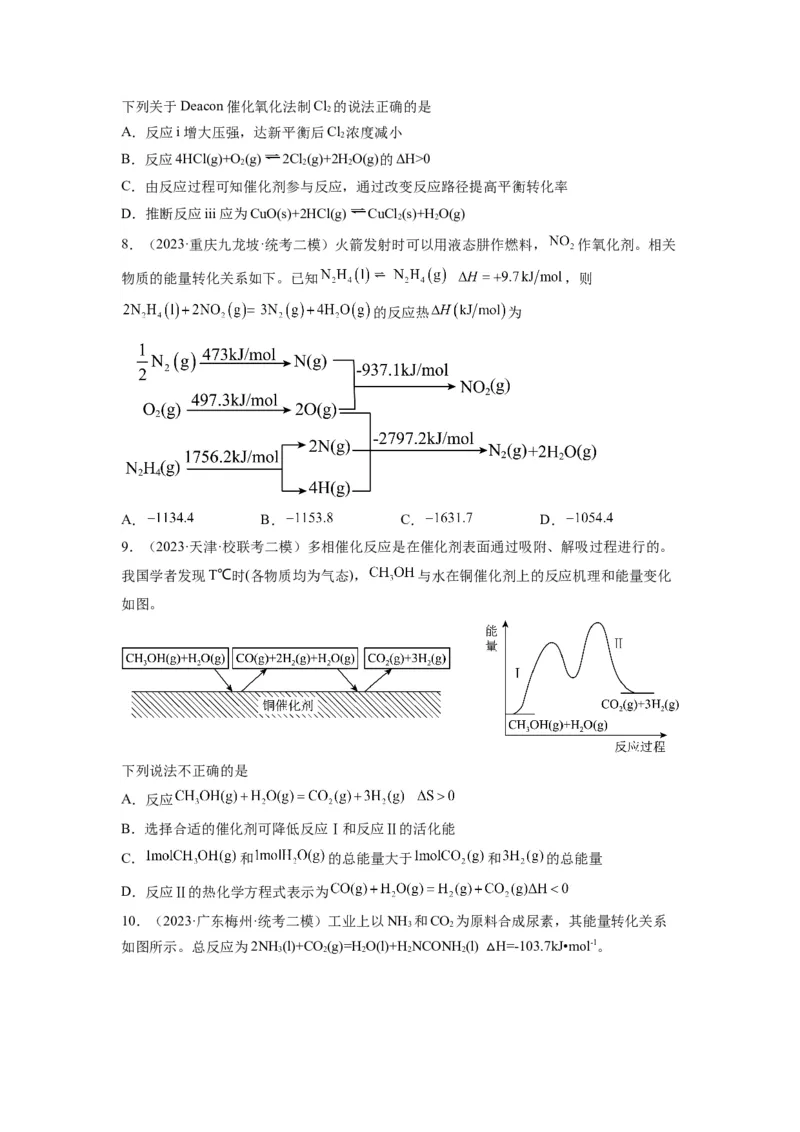
8.(2023·重庆九龙坡·统考二模)火箭发射时可以用液态肼作燃料, 作氧化剂。相关
物质的能量转化关系如下。已知 ,则
的反应热 为
A. B. C. D.
9.(2023·天津·校联考二模)多相催化反应是在催化剂表面通过吸附、解吸过程进行的。
我国学者发现T℃时(各物质均为气态), 与水在铜催化剂上的反应机理和能量变化
如图。
下列说法不正确的是
A.反应
B.选择合适的催化剂可降低反应Ⅰ和反应Ⅱ的活化能
C. 和 的总能量大于 和 的总能量
D.反应Ⅱ的热化学方程式表示为
10.(2023·广东梅州·统考二模)工业上以NH 和CO 为原料合成尿素,其能量转化关系
3 2
如图所示。总反应为2NH (l)+CO (g)=HO(l)+HNCONH(l) H=-103.7kJ•mol-1。
3 2 2 2 2
△下列有关说法正确的是
A. S>0, H>0
1 4
B.HNCOONH (l)的能量比HNCONH(l)的低,HNCOONH (l)更稳定
△2 △ 4 2 2 2 4
C.其他条件不变,增大压强,总反应速率和平衡转化率均增大
D.过程③的反应速率慢,使用合适的催化剂可减小 H 从而加快反应速率
3
△
11.(2023·浙江绍兴·统考模拟预测)甲醇与水蒸气在催化剂作用下发生如下反应:
反应Ⅰ: ,
反应Ⅱ:
根据能量变化示意图,下列说法正确的是
A.
B.反应Ⅱ决定整个反应的速率
C.催化剂可以降低总反应的焓变
D.
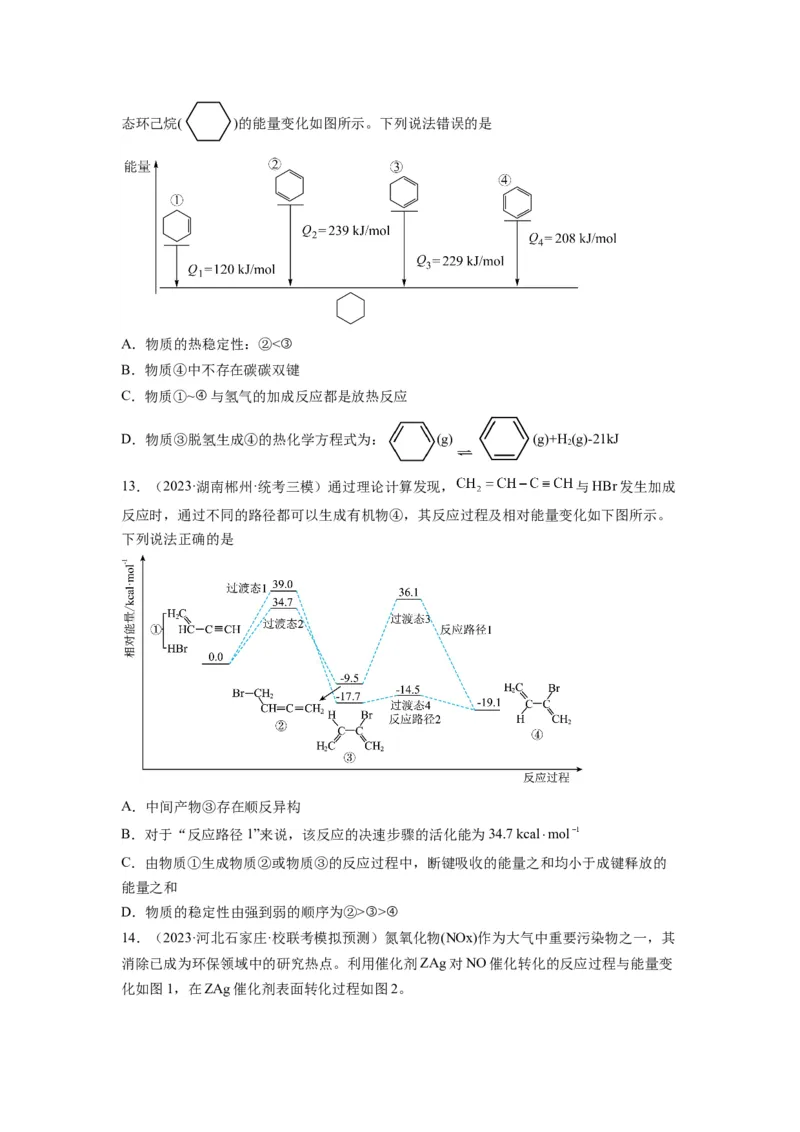
12.(2023·上海虹口·统考二模)气态有机物①~④分别与氢气发生加成反应生成1mol气态环己烷( )的能量变化如图所示。下列说法错误的是
A.物质的热稳定性:②<③
B.物质④中不存在碳碳双键
C.物质①~④与氢气的加成反应都是放热反应
D.物质③脱氢生成④的热化学方程式为: (g) (g)+H(g)-21kJ
2
13.(2023·湖南郴州·统考三模)通过理论计算发现, 与HBr发生加成
反应时,通过不同的路径都可以生成有机物④,其反应过程及相对能量变化如下图所示。
下列说法正确的是
A.中间产物③存在顺反异构
B.对于“反应路径1”来说,该反应的决速步骤的活化能为34.7 kcal⋅mol
C.由物质①生成物质②或物质③的反应过程中,断键吸收的能量之和均小于成键释放的
能量之和
D.物质的稳定性由强到弱的顺序为②>③>④
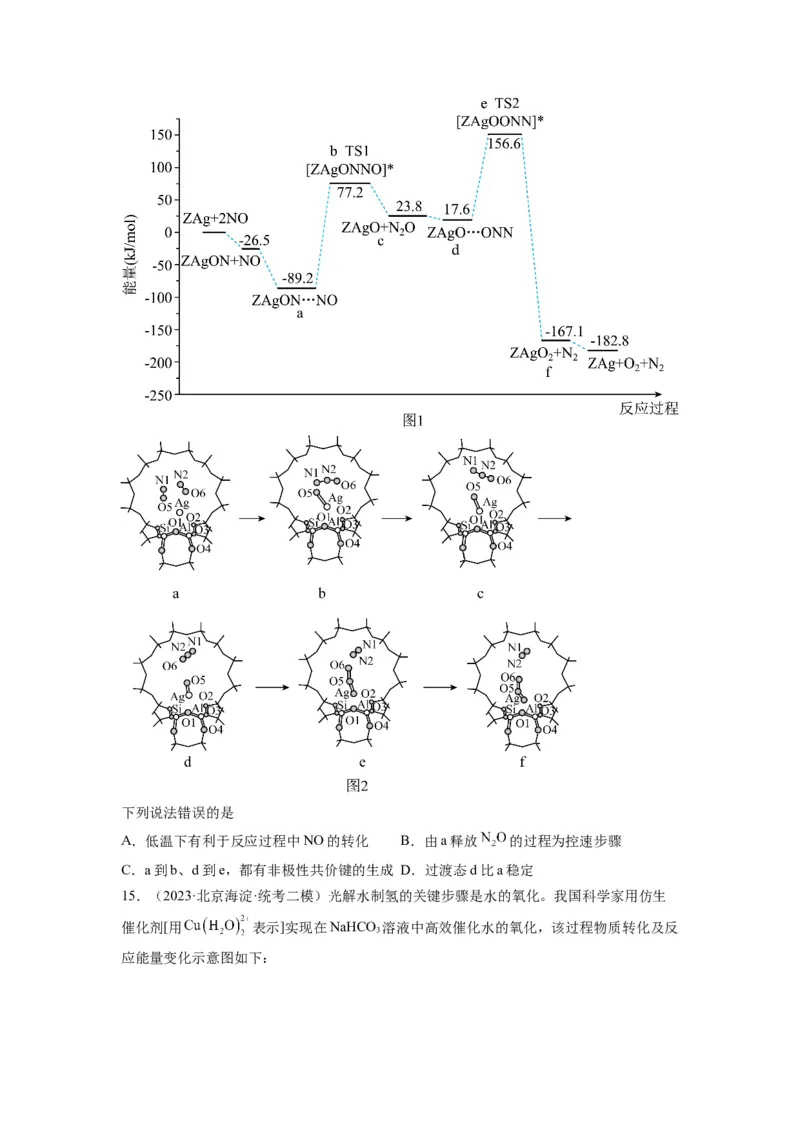
14.(2023·河北石家庄·校联考模拟预测)氮氧化物(NOx)作为大气中重要污染物之一,其
消除已成为环保领域中的研究热点。利用催化剂ZAg对NO催化转化的反应过程与能量变
化如图1,在ZAg催化剂表面转化过程如图2。下列说法错误的是
A.低温下有利于反应过程中NO的转化 B.由a释放 的过程为控速步骤
C.a到b、d到e,都有非极性共价键的生成 D.过渡态d比a稳定
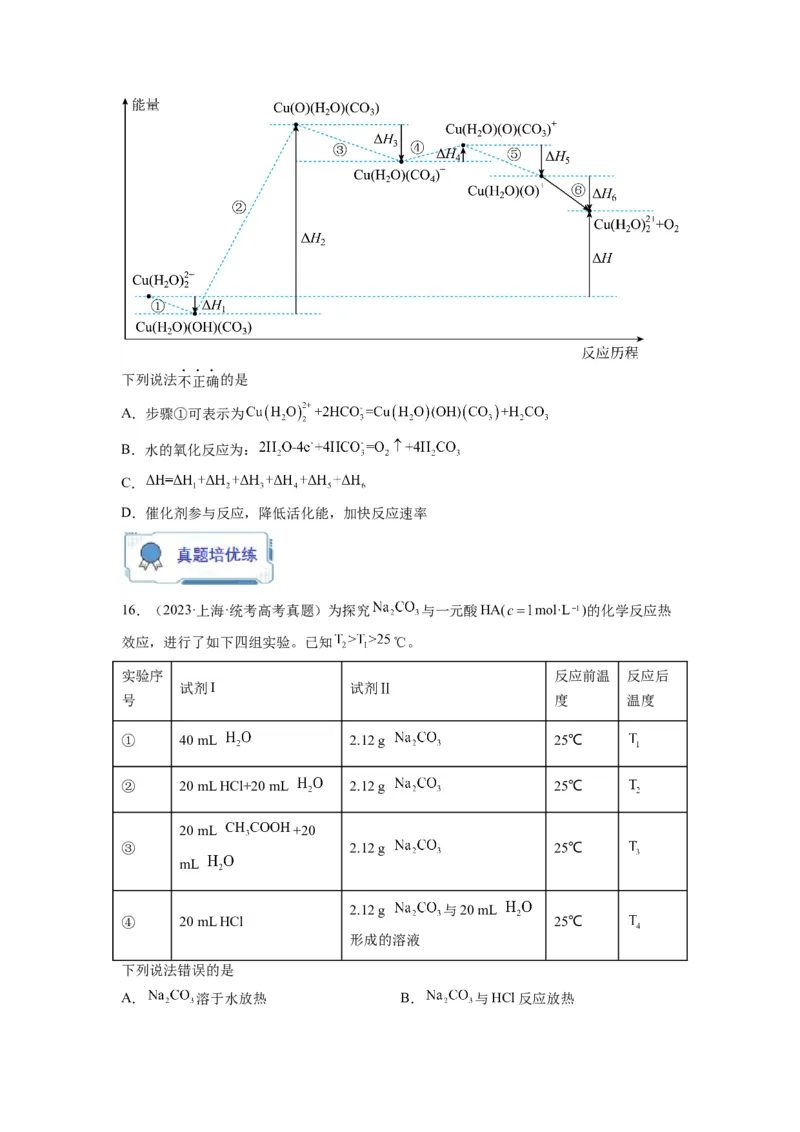
15.(2023·北京海淀·统考二模)光解水制氢的关键步骤是水的氧化。我国科学家用仿生
催化剂[用 表示]实现在NaHCO 溶液中高效催化水的氧化,该过程物质转化及反
3
应能量变化示意图如下:下列说法不正确的是
A.步骤①可表示为
B.水的氧化反应为:
C.
D.催化剂参与反应,降低活化能,加快反应速率
16.(2023·上海·统考高考真题)为探究 与一元酸HA( mol·L )的化学反应热
效应,进行了如下四组实验。已知 ℃。
实验序 反应前温 反应后
试剂I 试剂Ⅱ
号 度 温度
① 40 mL 2.12 g 25℃
② 20 mL HCl+20 mL 2.12 g 25℃
20 mL +20
③ 2.12 g 25℃
mL
2.12 g 与20 mL
④ 20 mL HCl 25℃
形成的溶液
下列说法错误的是
A. 溶于水放热 B. 与HCl反应放热C. D.
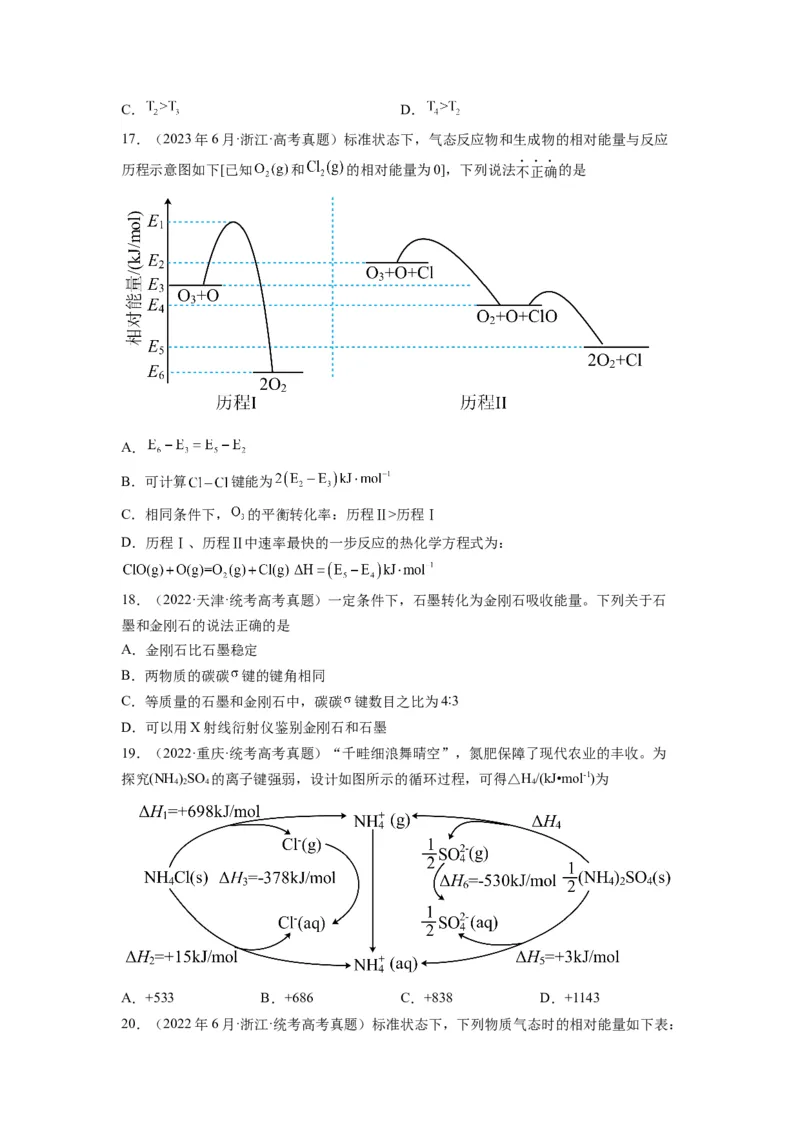
17.(2023年6月·浙江·高考真题)标准状态下,气态反应物和生成物的相对能量与反应
历程示意图如下[已知 和 的相对能量为0],下列说法不正确的是
A.
B.可计算 键能为
C.相同条件下, 的平衡转化率:历程Ⅱ>历程Ⅰ
D.历程Ⅰ、历程Ⅱ中速率最快的一步反应的热化学方程式为:
18.(2022·天津·统考高考真题)一定条件下,石墨转化为金刚石吸收能量。下列关于石
墨和金刚石的说法正确的是
A.金刚石比石墨稳定
B.两物质的碳碳 键的键角相同
C.等质量的石墨和金刚石中,碳碳 键数目之比为4∶3
D.可以用X射线衍射仪鉴别金刚石和石墨
19.(2022·重庆·统考高考真题)“千畦细浪舞晴空”,氮肥保障了现代农业的丰收。为
探究(NH )SO 的离子键强弱,设计如图所示的循环过程,可得△H/(kJ•mol-1)为
4 2 4 4
A.+533 B.+686 C.+838 D.+1143
20.(2022年6月·浙江·统考高考真题)标准状态下,下列物质气态时的相对能量如下表:物质(g) O H HO HOO
能量/ 249 218 39 10 0 0
可根据 计算出 中氧氧单键的键能为 。下列说法不
正确的是
A. 的键能为
B. 的键能大于 中氧氧单键的键能的两倍
C.解离氧氧单键所需能量:
D.
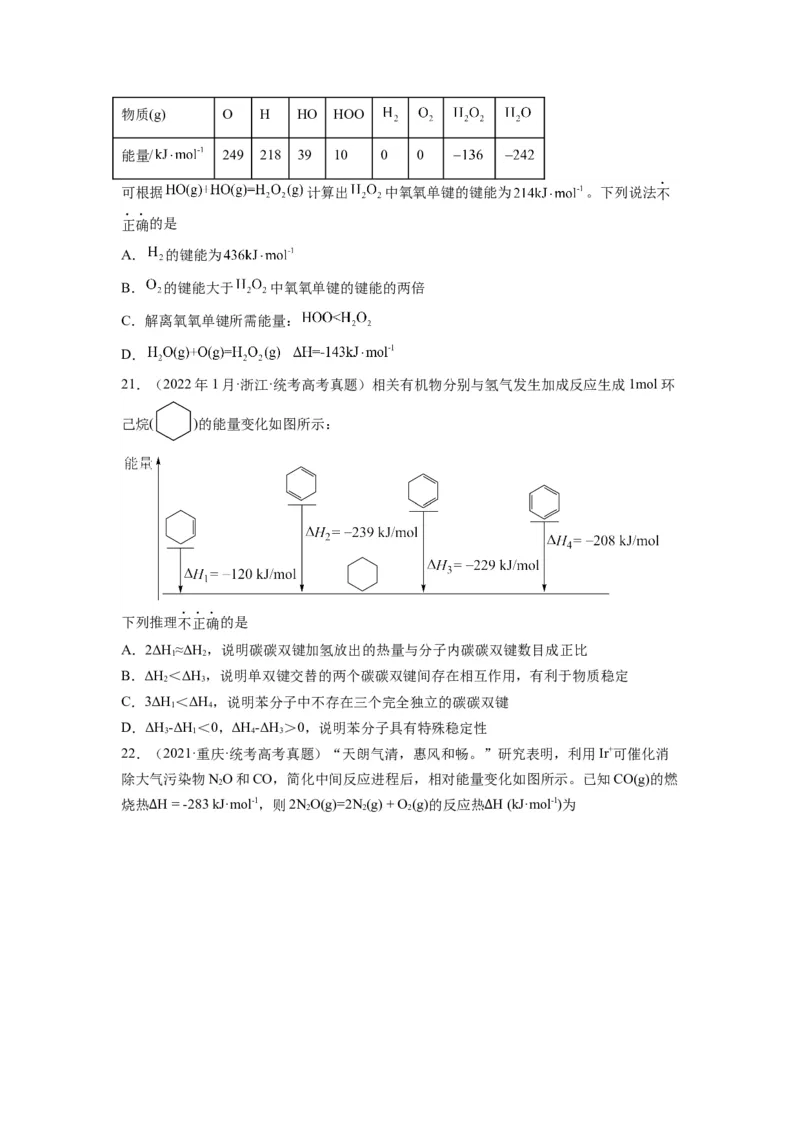
21.(2022年1月·浙江·统考高考真题)相关有机物分别与氢气发生加成反应生成1mol环
己烷( )的能量变化如图所示:
下列推理不正确的是
A.2ΔH≈ΔH,说明碳碳双键加氢放出的热量与分子内碳碳双键数目成正比
1 2
B.ΔH<ΔH,说明单双键交替的两个碳碳双键间存在相互作用,有利于物质稳定
2 3
C.3ΔH<ΔH,说明苯分子中不存在三个完全独立的碳碳双键
1 4
D.ΔH-ΔH <0,ΔH-ΔH >0,说明苯分子具有特殊稳定性
3 1 4 3
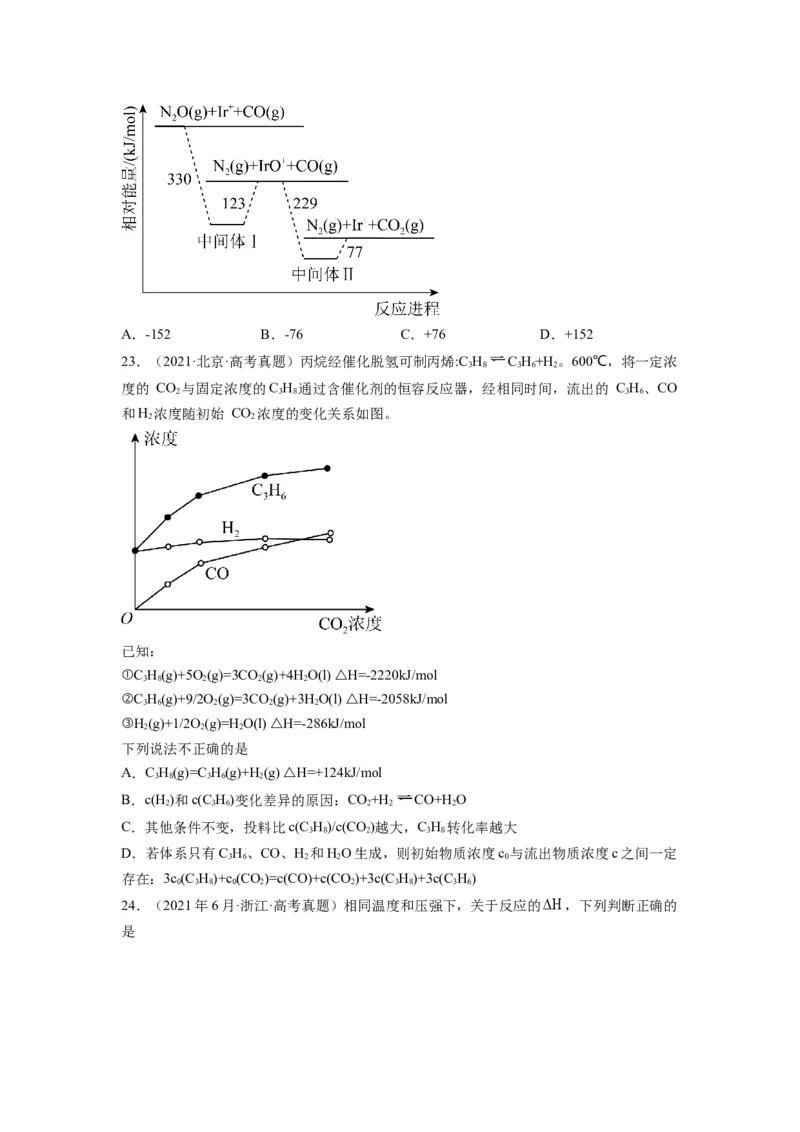
22.(2021·重庆·统考高考真题)“天朗气清,惠风和畅。”研究表明,利用Ir+可催化消
除大气污染物NO和CO,简化中间反应进程后,相对能量变化如图所示。已知CO(g)的燃
2
烧热 H = -283 kJ·mol-1,则2NO(g)=2N (g) + O(g)的反应热 H (kJ·mol-1)为
2 2 2
∆ ∆A.-152 B.-76 C.+76 D.+152
23.(2021·北京·高考真题)丙烷经催化脱氢可制丙烯:C H C H+H 。600℃,将一定浓
3 8 3 6 2
度的 CO 与固定浓度的C H 通过含催化剂的恒容反应器,经相同时间,流出的 C H、CO
2 3 8 3 6
和H 浓度随初始 CO 浓度的变化关系如图。
2 2
已知:
①C H(g)+5O(g)=3CO (g)+4HO(l) △H=-2220kJ/mol
3 8 2 2 2
②C H(g)+9/2O (g)=3CO (g)+3HO(l) △H=-2058kJ/mol
3 6 2 2 2
③H(g)+1/2O (g)=HO(l) △H=-286kJ/mol
2 2 2
下列说法不正确的是
A.C H(g)=C H(g)+H(g) △H=+124kJ/mol
3 8 3 6 2
B.c(H)和c(C H)变化差异的原因:CO+H CO+HO
2 3 6 2 2 2
C.其他条件不变,投料比c(C H)/c(CO )越大,C H 转化率越大
3 8 2 3 8
D.若体系只有C H、CO、H 和HO生成,则初始物质浓度c 与流出物质浓度c之间一定
3 6 2 2 0
存在:3c(C H)+c (CO)=c(CO)+c(CO )+3c(C H)+3c(C H)
0 3 8 0 2 2 3 8 3 6
24.(2021年6月·浙江·高考真题)相同温度和压强下,关于反应的 ,下列判断正确的
是A. B.
C. D.
25.(2021年1月·浙江·统考高考真题)已知共价键的键能与热化学方程式信息如下表:
共价键 H- H H-O
键能/(kJ·mol-1) 436 463
2H(g) + O (g)=2HO(g) ΔH=
2 2 2
热化学方程式
-482kJ·mol-1
则2O(g)=O (g)的ΔH为
2
A.428 kJ·mol-1 B.-428 kJ·mol-1 C.498 kJ·mol-1 D.-498 kJ·mol-1