文档内容
第四章 非金属及其化合物
第12讲 富集在海水中的元素——卤素(精练)
完卷时间:50分钟
可能用到的相对原子质量:O16 Cl35.5
一、选择题(每小题只有一个正确选项,共12*5分)
1.(2021·江苏无锡市·高三一模)氯气是常用的化工原料,可用作消毒剂和漂白剂;实验室用MnO 和
2
盐酸反应可制取氯气。氯气有毒,泄漏时需要妥善处理。下列有关氯气的说法不正确的是
A.Cl 是由共价键构成的非极性分子
2
B.制备漂白粉的方法是用石灰水吸收Cl
2
C.利用湿润的淀粉—KI试纸可检验Cl
2
D.工业上可用电解饱和食盐水制得Cl
2
2.(2021·上海高三二模)氯气性质非常活泼,能和很多物质反应。下列关于其相关反应的实验现象的
“解释或结论”正确的是
选项 实验现象 解释或结论
氯气能使湿润的淀粉KI试纸变蓝;氯气能使
A 氧化性:Cl>Br>I
NaBr溶液变橙色 2 2 2
B 氯气能使湿润的蓝色石蕊试纸先变红,后褪色 氯气与水生成了酸性物质
C 氯气通入HS的水溶液中,溶液的导电性增强 氯气是强电解质
2
D 氯气通入FeCl 和KSCN混合液,溶液变红色 氧化性:Cl>Fe3+
2 2
A.A B.B C.C D.D
3.(2021·全国高三三模)2020年11月10日,第三届中国国际进口博览会闭幕,该届“进博会”新设
公共卫生防疫专区、智慧出行专区、节能环保专区和体育用品及赛事专区。下列有关卫生防疫知识的描述
错误的是
A.家庭餐具可采取开水蒸煮的方式进行热力消毒
B.“84”消毒液的成分为NaClO、表面活性剂和水等,使用“84”消毒液的浓度越高越好
C.医用酒精应密封保存并远离明火
D.HO 消毒液和ClO 泡腾片的消毒原理相同
2 2 2
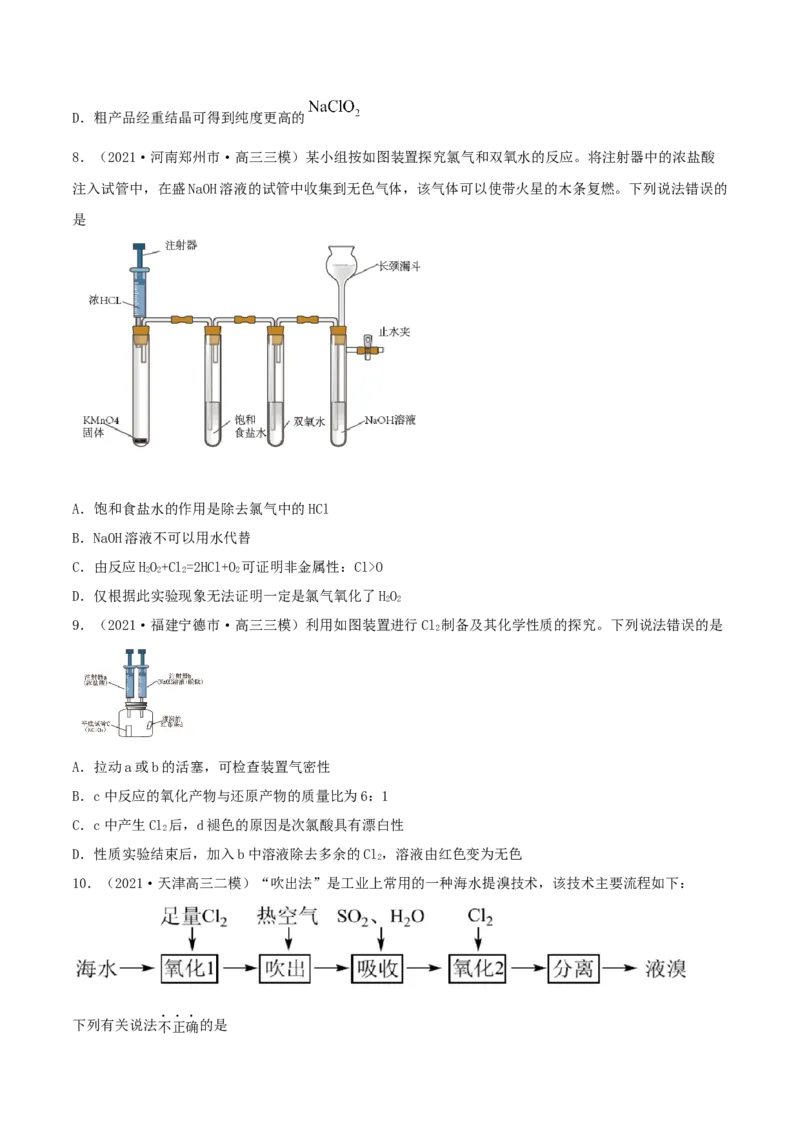
4.(2021·辽宁丹东市·高三一模)利用下列装置(夹持装置略)进行实验,能达到实验目的的是① ② ③ ④
A.图①装置可制备无水 MgCl
2
B.图②装置可证明氧化性:Cl>Br>I
2 2 2
C.图③装置可制乙烯并验证其还原性
D.图④装置可观察铁的析氢腐蚀
5.(2021·江苏南京市·高三二模)氯及其化合物在生产、生活中有广泛应用。下列物质的性质与用途
具有对应关系的是
A.Cl 能溶于水,可用于工业制盐酸
2
B.ClO 有强氧化性,可用于自来水消毒
2
C.HClO不稳定,可用作棉、麻的漂白剂
D.FeCl 溶液呈酸性,可用于蚀刻印刷电路板
3
6.(2021·上海高三一模)BrCl是一种卤素互化物,与Cl 性质相似,也能与水或碱溶液反应。下列说法
2
正确的是
A.BrCl与水反应生成HBrO和HCl,该反应属于氧化还原反应
B.1molBrCl与KBr溶液完全反应时转移的电子为1mol
C.BrCl可与Cl 反应得到Br
2 2
D.BrCl与稀氢氧化钠溶液反应可生成NaBr和NaClO
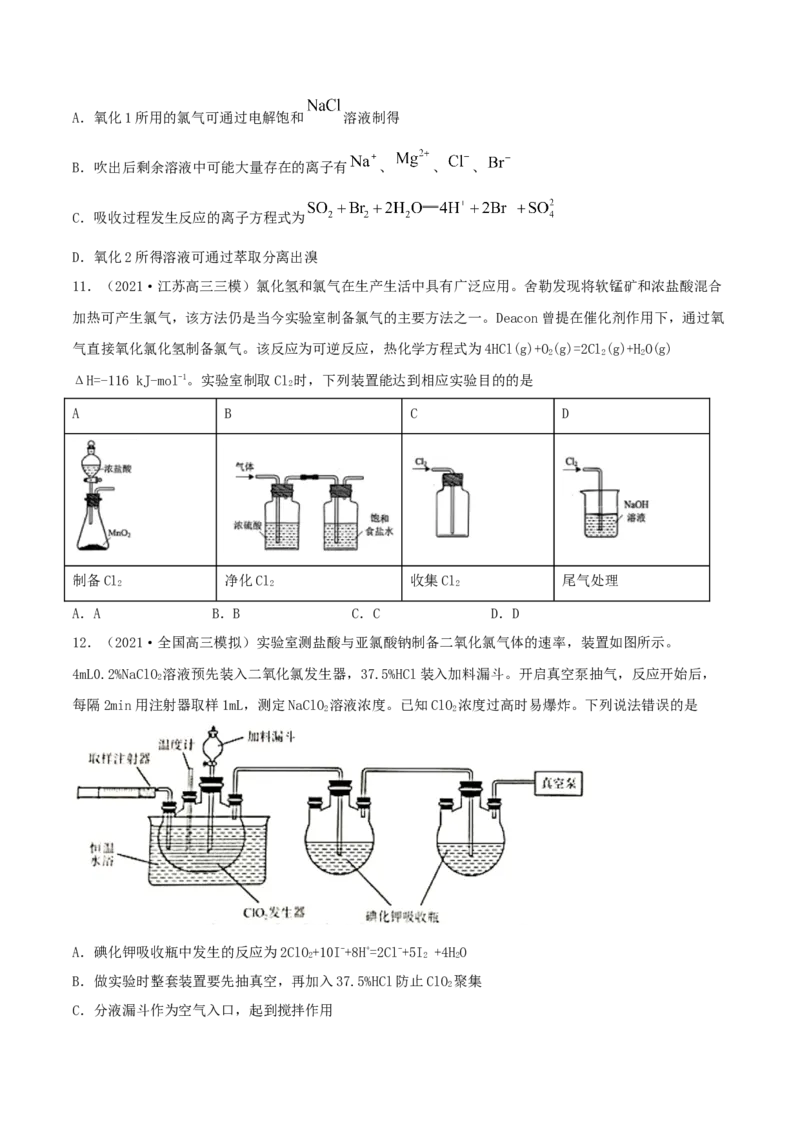
7.(2021·河北高三三模) 是一种高效的漂白剂,实验室中一种制备 的过程如图所示,
下列说法错误的是
A. 的漂白原理与 不同
B.每生成1 mol 有0.5 mol 被氧化
C.反应2过程中, 作氧化剂D.粗产品经重结晶可得到纯度更高的
8.(2021·河南郑州市·高三三模)某小组按如图装置探究氯气和双氧水的反应。将注射器中的浓盐酸
注入试管中,在盛NaOH溶液的试管中收集到无色气体,该气体可以使带火星的木条复燃。下列说法错误的
是
A.饱和食盐水的作用是除去氯气中的HCl
B.NaOH溶液不可以用水代替
C.由反应HO+Cl=2HCl+O 可证明非金属性:Cl>O
2 2 2 2
D.仅根据此实验现象无法证明一定是氯气氧化了HO
2 2
9.(2021·福建宁德市·高三三模)利用如图装置进行Cl 制备及其化学性质的探究。下列说法错误的是
2
A.拉动a或b的活塞,可检查装置气密性
B.c中反应的氧化产物与还原产物的质量比为6:1
C.c中产生Cl 后,d褪色的原因是次氯酸具有漂白性
2
D.性质实验结束后,加入b中溶液除去多余的Cl,溶液由红色变为无色
2
10.(2021·天津高三二模)“吹出法”是工业上常用的一种海水提溴技术,该技术主要流程如下:
下列有关说法不正确的是A.氧化1所用的氯气可通过电解饱和 溶液制得
B.吹出后剩余溶液中可能大量存在的离子有 、 、 、
C.吸收过程发生反应的离子方程式为
D.氧化2所得溶液可通过萃取分离出溴
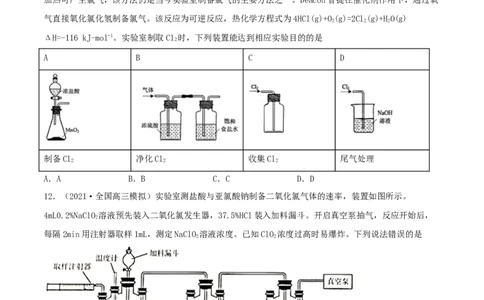
11.(2021·江苏高三三模)氯化氢和氯气在生产生活中具有广泛应用。舍勒发现将软锰矿和浓盐酸混合
加热可产生氯气,该方法仍是当今实验室制备氯气的主要方法之一。Deacon曾提在催化剂作用下,通过氧
气直接氧化氯化氢制备氯气。该反应为可逆反应,热化学方程式为4HCl(g)+O(g)=2Cl(g)+HO(g)
2 2 2
ΔH=-116 kJ-mol-1。实验室制取Cl 时,下列装置能达到相应实验目的的是
2
A B C D
制备Cl 净化Cl 收集Cl 尾气处理
2 2 2
A.A B.B C.C D.D
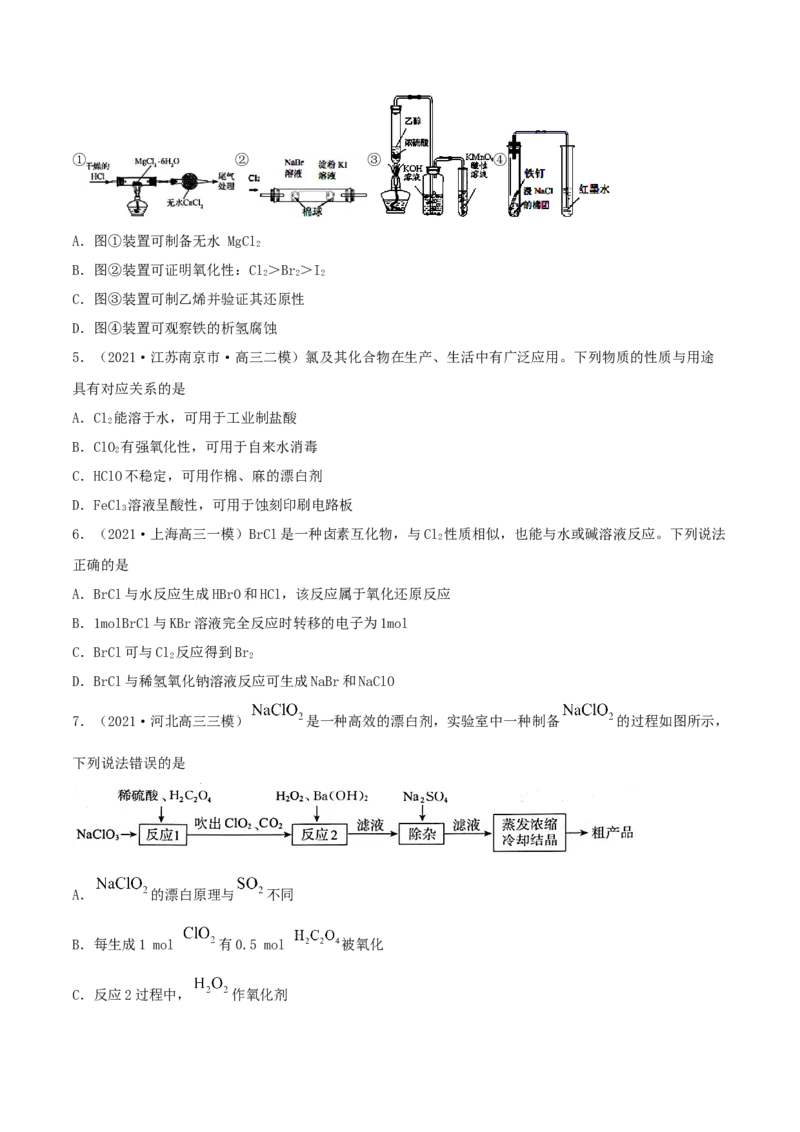
12.(2021·全国高三模拟)实验室测盐酸与亚氯酸钠制备二氧化氯气体的速率,装置如图所示。
4mL0.2%NaClO 溶液预先装入二氧化氯发生器,37.5%HCl装入加料漏斗。开启真空泵抽气,反应开始后,
2
每隔2min用注射器取样1mL,测定NaClO 溶液浓度。已知ClO 浓度过高时易爆炸。下列说法错误的是
2 2
A.碘化钾吸收瓶中发生的反应为2ClO+10I-+8H+=2Cl-+5I +4HO
2 2 2
B.做实验时整套装置要先抽真空,再加入37.5%HCl防止ClO 聚集
2
C.分液漏斗作为空气入口,起到搅拌作用D.实验过程中分液漏斗活塞保持关闭,防止ClO 逸出
2
二、主观题(共3小题,共40分)
13.(2021·全国高三)(12分) 与 的氧化性相近,在自来水消毒和果蔬保鲜等方面应用广泛。
回答下列问题:
(1)氯气的电子式为_______。
(2)氯气和氢氧化钠溶液制备漂白液的离子方程式为_______。
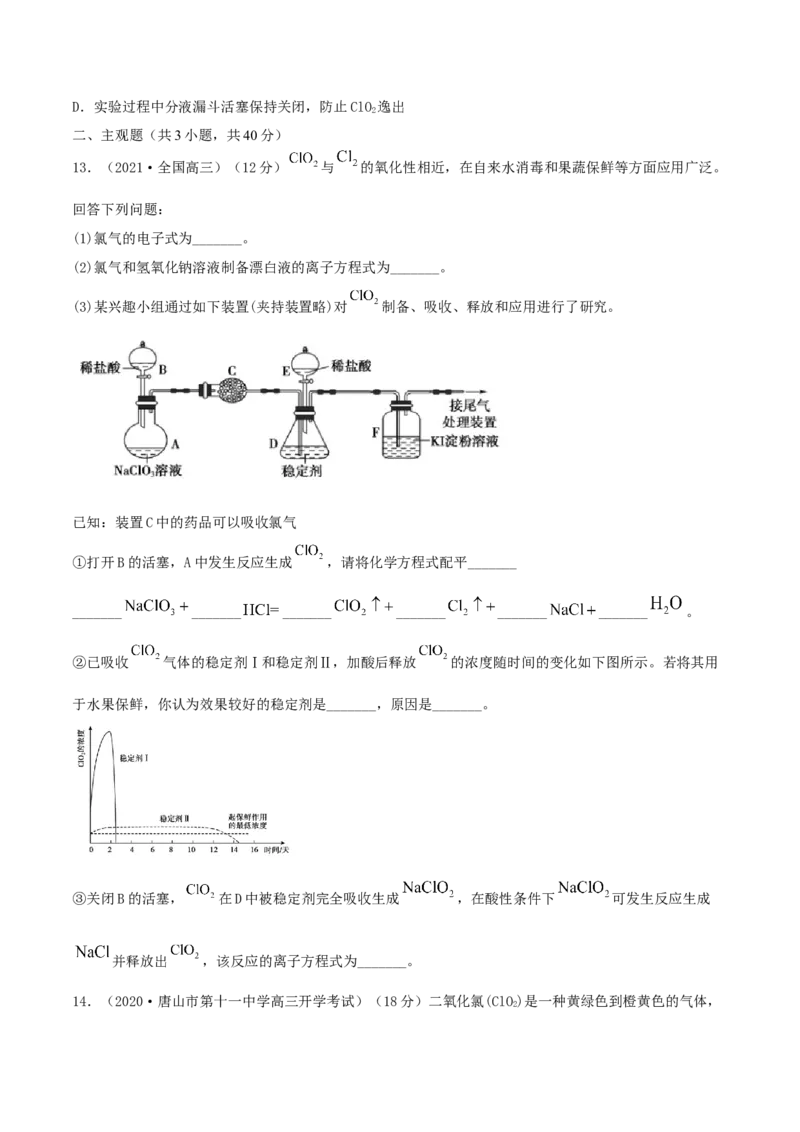
(3)某兴趣小组通过如下装置(夹持装置略)对 制备、吸收、释放和应用进行了研究。
已知:装置C中的药品可以吸收氯气
①打开B的活塞,A中发生反应生成 ,请将化学方程式配平_______
_______ _______ _______ _______ _______ _______ 。
②已吸收 气体的稳定剂Ⅰ和稳定剂Ⅱ,加酸后释放 的浓度随时间的变化如下图所示。若将其用
于水果保鲜,你认为效果较好的稳定剂是_______,原因是_______。
③关闭B的活塞, 在D中被稳定剂完全吸收生成 ,在酸性条件下 可发生反应生成
并释放出 ,该反应的离子方程式为_______。
14.(2020·唐山市第十一中学高三开学考试)(18分)二氧化氯(ClO)是一种黄绿色到橙黄色的气体,
2是国际上公认的安全、无毒的绿色消毒剂。已知:工业上制备二氧化氯的方法之一是用甲醇在酸性介质中
与氯酸钠反应。二氧化氯能与许多化学物质发生爆炸性反应,遇水则生成次氯酸、氯气和氧气。
完成下列填空:
(1)将二氧化氯通入品红试液中,看到的现象是__;理由是__。
(2)请配平下列反应的化学方程式(CHOH中H为+1价,O为-2价):
3
___CHOH+__NaClO+__→__CO↑+__C1O↑+__NaSO+__□__
3 3 2 2 2 4
(3)该反应中,被氧化的元素是__。还原产物与氧化产物的物质的量之比是__。
(4)根据上述反应可推知__。
a.氧化性:C1O>NaClO b.氧化性:NaClO>CHOH
2 3 3 3
c.还原性:CHOH>ClO d.还原性:CHOH>NaSO
3 2 3 2 4
(5)若转移的电子数目为0.3N(N为阿伏加德罗常数),则反应产生气体(标准状况)为__升。
A A
(6)消毒效率常以单位质量的消毒剂得到的电子数表示。ClO 的消毒效率是Cl 的__倍。
2 2
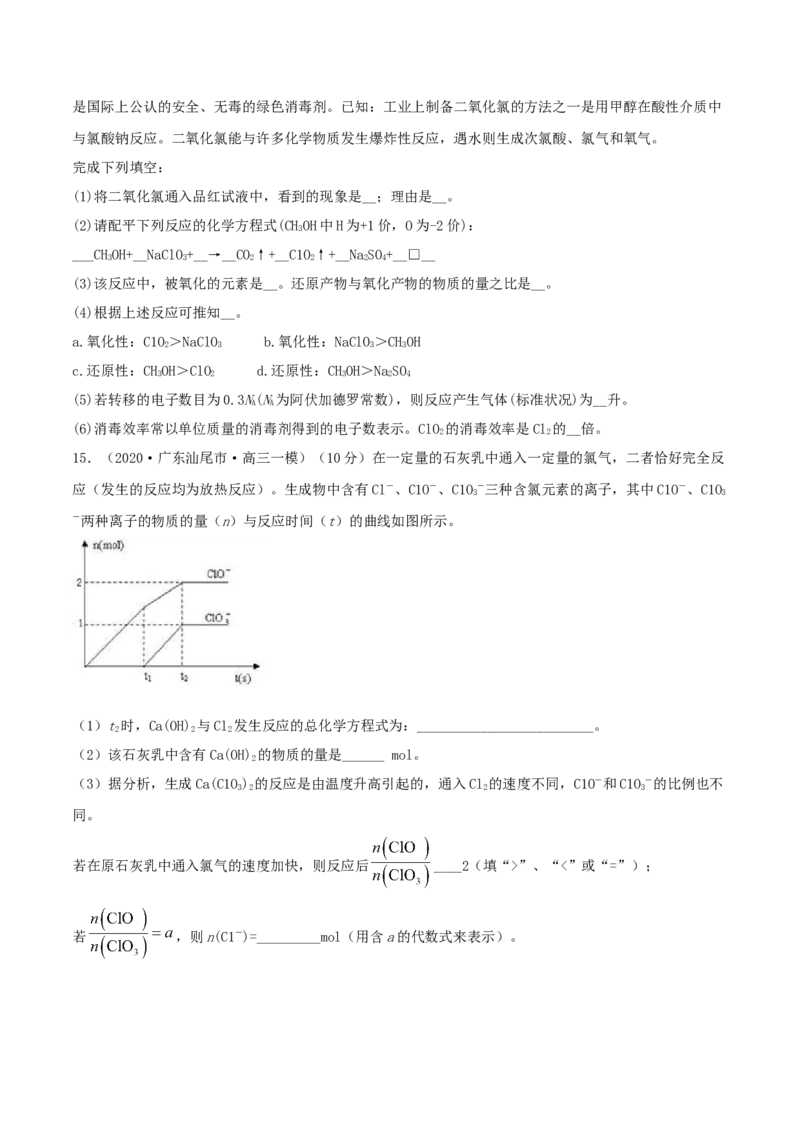
15.(2020·广东汕尾市·高三一模)(10分)在一定量的石灰乳中通入一定量的氯气,二者恰好完全反
应(发生的反应均为放热反应)。生成物中含有Cl-、C1O-、C1O-三种含氯元素的离子,其中C1O-、C1O
3 3
-两种离子的物质的量(n)与反应时间(t)的曲线如图所示。
(1)t时,Ca(OH) 与Cl 发生反应的总化学方程式为:_________________________。
2 2 2
(2)该石灰乳中含有Ca(OH) 的物质的量是______ mol。
2
(3)据分析,生成Ca(C1O) 的反应是由温度升高引起的,通入Cl 的速度不同,C1O-和C1O-的比例也不
3 2 2 3
同。
若在原石灰乳中通入氯气的速度加快,则反应后 ____2(填“>”、“<”或“=”);
若 ,则n(C1-)=_________mol(用含a的代数式来表示)。