文档内容
第 14 讲 元素周期律和元素周期表
【练基础】
1.1869年俄国化学家门捷列夫制作出了第一张元素周期表,揭示了化学元素间的内在联系,成为化
学发展史上重要里程碑之一。下列有关元素周期表的说法正确的是( )
A.元素周期表有7个横行、18个纵列,即有7个周期、18个族
B.在过渡元素中寻找半导体材料
C.俄罗斯专家首次合成了X原子,116号元素位于元素周期表中第七周期ⅥA族
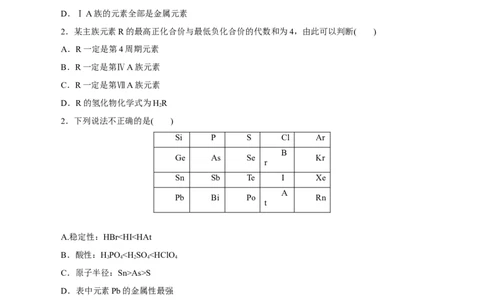
D.ⅠA族的元素全部是金属元素
2.某主族元素R的最高正化合价与最低负化合价的代数和为4,由此可以判断( )
A.R一定是第4周期元素
B.R一定是第ⅣA族元素
C.R一定是第ⅦA族元素
D.R的氢化物化学式为HR
2
2.下列说法不正确的是( )
Si P S Cl Ar
B
Ge As Se Kr
r
Sn Sb Te I Xe
A
Pb Bi Po Rn
t
A.稳定性:HBrAs>S
D.表中元素Pb的金属性最强
3.2019年是“国际化学元素周期表年”。下列对元素周期表的认识正确的是( )
A.周期表中共有18个族
B.第一、二、三周期为短周期
C.第三周期主族元素原子半径从左到右依次增大
D.第二周期主族元素从左到右,最高正化合价从+1递增到+7
4.以下验证元素的金属性、非金属性强弱的实验,所用物品不合理的是( )
A.比较钾、钠:Na、K、HO
2B.比较镁、铝:MgCl 溶液、AlCl 溶液、NaOH溶液
2 3
C.比较硫、氯:NaS溶液、NaCl溶液、pH试纸
2
D.比较溴、碘:溴水、KI-淀粉试纸
5.下列关于元素周期表和元素周期律的应用说法正确的是( )
A.为元素性质的系统研究提供指导,为新元素的发现提供线索
B.在周期表中金属与非金属的分界处,寻找可作催化剂的合金材料
C.在ⅠA、ⅡA族元素中,寻找制造农药的主要元素
D.在过渡元素中,可以找到半导体材料
6.下列说法正确的是( )
①Li、Na、K、Rb、Cs的熔、沸点逐渐变小
②若R2-和M+的电子层结构相同,则原子序数:R>M
③F 、Cl、Br 、I 熔、沸点随相对分子质量的增大而升高
2 2 2 2
④由于非金属性:Cl>Br>I,所以酸性:HCl>HBr>HI
⑤氨的液化会破坏共价键
⑥C与H形成的化合物中只存在极性共价键
⑦Na O 固体中的阴离子和阳离子个数比是1∶2
2 2
A.②⑤⑥ B.③⑤⑦
C.②④⑤ D.①③⑦
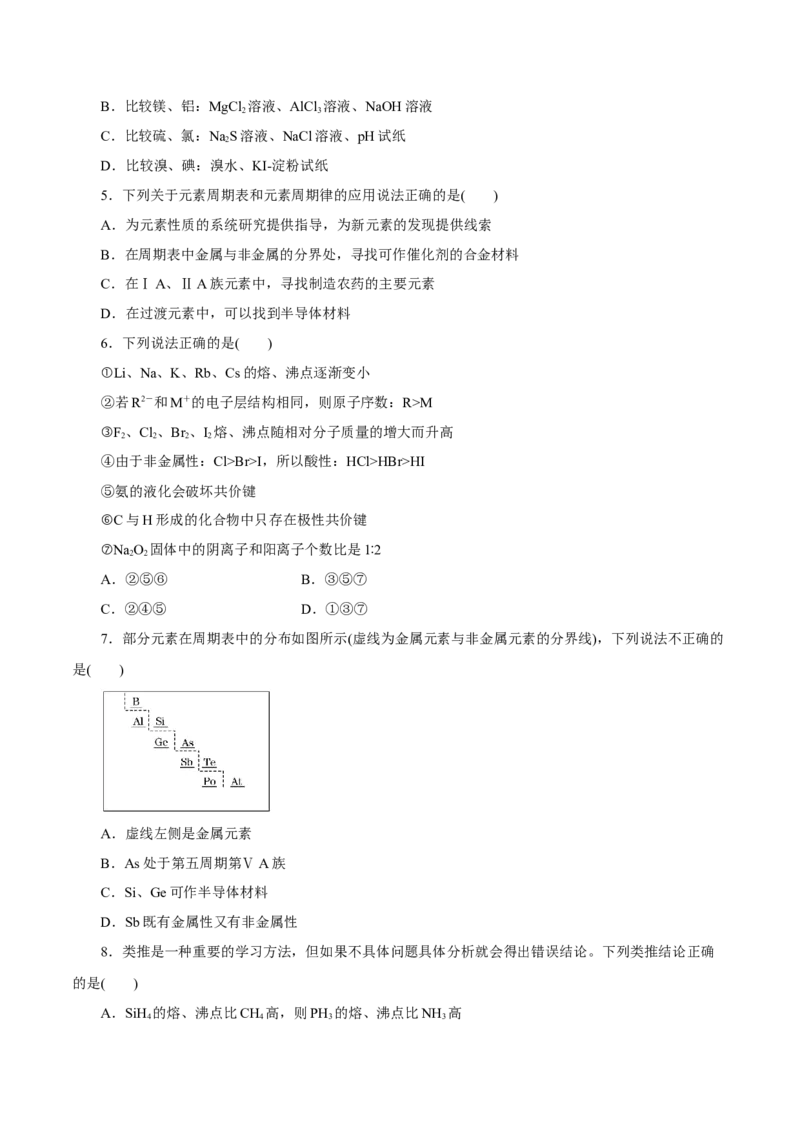
7.部分元素在周期表中的分布如图所示(虚线为金属元素与非金属元素的分界线),下列说法不正确的
是( )
A.虚线左侧是金属元素
B.As处于第五周期第ⅤA族
C.Si、Ge可作半导体材料
D.Sb既有金属性又有非金属性
8.类推是一种重要的学习方法,但如果不具体问题具体分析就会得出错误结论。下列类推结论正确
的是( )
A.SiH 的熔、沸点比CH 高,则PH 的熔、沸点比NH 高
4 4 3 3B.HO比NH 稳定,则HS也比NH 稳定
2 3 2 3
C.F 在暗处遇H 即爆炸,I 在暗处遇H 也爆炸
2 2 2 2
D.同族元素有Ca(OH) 的碱性强于Mg(OH) ,Pb(OH) 的碱性也应强于Sn(OH)
2 2 4 4
9.下列事实中,不能用元素周期律解释的是( )
A.原子半径:K>Ca>Mg
B.碱性:NaOH>Mg(OH) >Al(OH)
2 3
C.热稳定性:HF>HCl>H S
2
D.酸性:HSO >H CO>H SiO
2 3 2 3 2 3
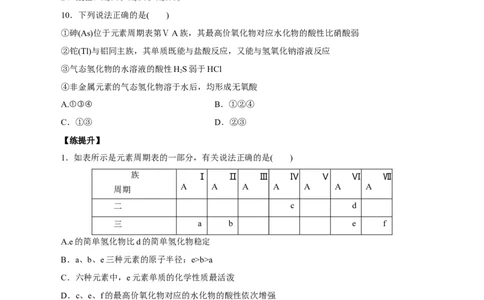
10.下列说法正确的是( )
①砷(As)位于元素周期表第ⅤA族,其最高价氧化物对应水化物的酸性比硝酸弱
②铊(Tl)与铝同主族,其单质既能与盐酸反应,又能与氢氧化钠溶液反应
③气态氢化物的水溶液的酸性HS弱于HCl
2
④非金属元素的气态氢化物溶于水后,均形成无氧酸
A.①③④ B.①②④
C.①③ D.②③
【练提升】
1.如表所示是元素周期表的一部分,有关说法正确的是( )
族
Ⅰ Ⅱ Ⅲ Ⅳ Ⅴ Ⅵ Ⅶ
周期 A A A A A A A
二 c d
三 a b e f
A.e的简单氢化物比d的简单氢化物稳定
B.a、b、e三种元素的原子半径:e>b>a
C.六种元素中,e元素单质的化学性质最活泼
D.c、e、f的最高价氧化物对应的水化物的酸性依次增强
2.短周期元素X、Y、Z、W、Q在元素周期表中的相对位置如图所示。下列说法不正确的是( )
A.W、Y对应的简单氢化物的稳定性前者高
B.阴离子的还原性:W2->Q-
C.离子半径:Y2->Z3+D.元素的非金属性:Y>W
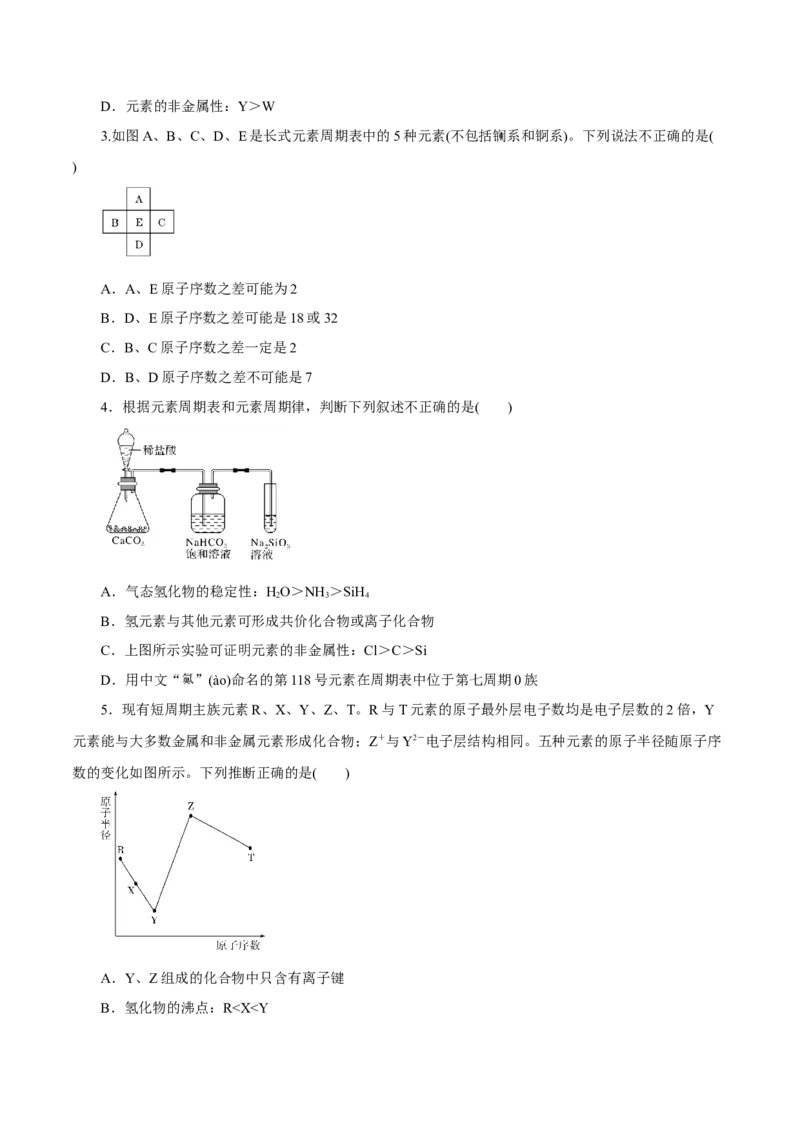
3.如图A、B、C、D、E是长式元素周期表中的5种元素(不包括镧系和锕系)。下列说法不正确的是(
)
A.A、E原子序数之差可能为2
B.D、E原子序数之差可能是18或32
C.B、C原子序数之差一定是2
D.B、D原子序数之差不可能是7
4.根据元素周期表和元素周期律,判断下列叙述不正确的是( )
A.气态氢化物的稳定性:HO>NH >SiH
2 3 4
B.氢元素与其他元素可形成共价化合物或离子化合物
C.上图所示实验可证明元素的非金属性:Cl>C>Si
D.用中文“ ”(ào)命名的第118号元素在周期表中位于第七周期0族
5.现有短周期主族元素R、X、Y、Z、T。R与T元素的原子最外层电子数均是电子层数的2倍,Y
元素能与大多数金属和非金属元素形成化合物;Z+与Y2-电子层结构相同。五种元素的原子半径随原子序
数的变化如图所示。下列推断正确的是( )
A.Y、Z组成的化合物中只含有离子键
B.氢化物的沸点:RMg
B Ca(OH) 的碱性强于Mg(OH) 金属性:Ca>Mg
2 2
C 氧化性:HClO>HCO 金属性:Cl>C
2 3
D 热稳定性强弱:HBr>HI 非金属性:Br>I
7.如图是元素周期表的一部分,下列叙述不正确的是( )
B C N O F
Al Si P S Cl
Ga Ge As Se Br
In Sn Sb Te I
Tl Pb Bi Po At
A.Pb的最高正化合价为+4
B.原子半径比较:Al>F
C.酸性强弱:HAsO H SO
2 3
b.非金属性:O>S
c.碱性:NaOH>Mg(OH)
2
d.热稳定性:NaCO>NaHCO
2 3 3
(4)硒(Se)与硫位于同一主族,均是生命必需元素。下列推断正确的是____________。
a.硒元素的最低负化合价为-2
b.二氧化硒(SeO )具有还原性
2
c.硒的氧化物对应的水化物属于强酸
(5)科学家合成了一种新化合物(如图所示),其中R、X、Y、Z为同一短周期元素,Z核外最外层电子
数是Y核外电子数的一半。①Y的元素符号为______________。
②X的氢化物的电子式:________________。