文档内容
第 14 讲 元素周期律和元素周期表
【练基础】
1.1869年俄国化学家门捷列夫制作出了第一张元素周期表,揭示了化学元素间的内在联系,成为化
学发展史上重要里程碑之一。下列有关元素周期表的说法正确的是( )
A.元素周期表有7个横行、18个纵列,即有7个周期、18个族
B.在过渡元素中寻找半导体材料
C.俄罗斯专家首次合成了X原子,116号元素位于元素周期表中第七周期ⅥA族
D.ⅠA族的元素全部是金属元素
【答案】C
【解析】元素周期表中的第Ⅷ族包含8、9、10共3个纵列,因此元素周期表虽然共18个纵列,但共
16个族,A错误;在金属和非金属的分界线附近寻找半导体材料,B错误;第七周期0族元素为118号,
则116号元素位于元素周期表中第七周期ⅥA族,C正确;第ⅠA族的元素包括H和碱金属元素,D错误。
2.某主族元素R的最高正化合价与最低负化合价的代数和为4,由此可以判断( )
A.R一定是第4周期元素
B.R一定是第ⅣA族元素
C.R一定是第ⅦA族元素
D.R的氢化物化学式为HR
2
【答案】D
【解析】主族元素中,最高正化合价+|最低负化合价|=8,元素R的最高正化合价与最低负化合价的
代数和为4,所以R元素的最高正化合价是+6价,最低负化合价是-2价,R的最外层电子数是6。R为
第ⅥA族元素S、Se、Te,但不一定是第四周期元素,其气态氢化物化学式为HR。
2
2.下列说法不正确的是( )
Si P S Cl Ar
B
Ge As Se Kr
r
Sn Sb Te I Xe
A
Pb Bi Po Rn
t
A.稳定性:HBrAs>SD.表中元素Pb的金属性最强
【答案】A
【解析】同主族元素从上到下元素的非金属性逐渐减弱,则非金属性:Br>I>At,元素的非金属性越
强,对应的氢化物越稳定,则稳定性:HAt<HI<HBr,故A错误;同主族元素从上到下元素的金属性逐
渐增强,同周期元素从左到右元素的金属性逐渐减弱,故表中元素Pb的金属性最强,故D正确。
3.2019年是“国际化学元素周期表年”。下列对元素周期表的认识正确的是( )
A.周期表中共有18个族
B.第一、二、三周期为短周期
C.第三周期主族元素原子半径从左到右依次增大
D.第二周期主族元素从左到右,最高正化合价从+1递增到+7
【答案】B
【解析】周期表中共有18列,7个主族,7个副族、1个第Ⅷ族、1个0族,除第Ⅷ族有3列,其他各
族均为1列,共有16个族,A错误;同周期元素电子层数相同,从左到右核电荷数逐渐增大,原子核对核
外电子吸引逐渐增强,原子半径逐渐减小,C错误;氧元素无最高正化合价、氟元素无正化合价,D错误。
4.以下验证元素的金属性、非金属性强弱的实验,所用物品不合理的是( )
A.比较钾、钠:Na、K、HO
2
B.比较镁、铝:MgCl 溶液、AlCl 溶液、NaOH溶液
2 3
C.比较硫、氯:NaS溶液、NaCl溶液、pH试纸
2
D.比较溴、碘:溴水、KI-淀粉试纸
【答案】C
【解析】体积大致相同的Na、K与水反应,钾反应更剧烈,表明钾的金属性比钠强,A所用物品合理;
向MgCl 溶液、AlCl 溶液中不断滴加NaOH溶液,前者生成白色沉淀,后者起初生成沉淀后来沉淀溶解,
2 3
表明Al(OH) 能表现出酸性,从而得出Mg(OH) 的碱性强,Mg的金属性比Al强,B所用物品合理;用pH
3 2
试纸测定NaS溶液、NaCl溶液的pH,前者的pH大,表明酸性:HSI,D所用物品合理。
2 2
5.下列关于元素周期表和元素周期律的应用说法正确的是( )
A.为元素性质的系统研究提供指导,为新元素的发现提供线索
B.在周期表中金属与非金属的分界处,寻找可作催化剂的合金材料
C.在ⅠA、ⅡA族元素中,寻找制造农药的主要元素
D.在过渡元素中,可以找到半导体材料【答案】A
【解析】元素周期表和元素周期律为元素性质的系统研究提供指导,为新元素的发现提供线索,A项
正确;在周期表中金属与非金属的分界处寻找半导体材料,B项错误;在非金属元素中寻找制造农药的主
要元素,C项错误;在过渡元素中寻找可作催化剂的合金材料,D项错误。
6.下列说法正确的是( )
①Li、Na、K、Rb、Cs的熔、沸点逐渐变小
②若R2-和M+的电子层结构相同,则原子序数:R>M
③F 、Cl、Br 、I 熔、沸点随相对分子质量的增大而升高
2 2 2 2
④由于非金属性:Cl>Br>I,所以酸性:HCl>HBr>HI
⑤氨的液化会破坏共价键
⑥C与H形成的化合物中只存在极性共价键
⑦Na O 固体中的阴离子和阳离子个数比是1∶2
2 2
A.②⑤⑥ B.③⑤⑦
C.②④⑤ D.①③⑦
【答案】D
【解析】Li、Na、K、Rb、Cs为金属晶体,影响熔、沸点高低的因素是金属键,原子半径越大,金属
键越弱,熔、沸点越小,则Li、Na、K、Rb、Cs熔、沸点逐渐减小,故①正确;R2-和M+的电子层结构
相同,则离子的核外电子数相等,且M处于R相邻的下一周期,所以原子序数:M>R,故②错误;F、
2
Cl、Br 、I 是组成和结构相似的分子晶体,熔、沸点随相对分子质量的增大而升高,故③正确;根据元素
2 2 2
的非金属性强弱可以比较简单气态氢化物的稳定性强弱和最高价氧化物对应水化物的酸性强弱,氢化物的
酸性与元素的非金属性无关,并且酸性:HCl<HBr<HI,故④错误;氨液化是气体转化为液体,没有化学
键的变化,故⑤错误;C与H形成的化合物有很多,例如乙烯既有极性共价键也有非极性共价键,故⑥错
误;NaO 是由钠离子和过氧根离子形成的离子化合物,阴离子和阳离子个数比是1∶2,故⑦正确。
2 2
7.部分元素在周期表中的分布如图所示(虚线为金属元素与非金属元素的分界线),下列说法不正确的
是( )
A.虚线左侧是金属元素B.As处于第五周期第ⅤA族
C.Si、Ge可作半导体材料
D.Sb既有金属性又有非金属性
【答案】B
【解析】本题考查元素周期表的应用,侧重考查金属元素与非金属元素分界线附近元素的性质。题图
中虚线左下方的元素均为金属元素,A正确;由Si处于第三周期第ⅣA族可推知,As处于第四周期第
ⅤA族,B错误;元素周期表中的金属元素和非金属元素分界线附近的元素往往既具有金属性,又具有非
金属性,可在该分界线附近寻找半导体材料(如Ge、Si等),C、D正确。
8.类推是一种重要的学习方法,但如果不具体问题具体分析就会得出错误结论。下列类推结论正确
的是( )
A.SiH 的熔、沸点比CH 高,则PH 的熔、沸点比NH 高
4 4 3 3
B.HO比NH 稳定,则HS也比NH 稳定
2 3 2 3
C.F 在暗处遇H 即爆炸,I 在暗处遇H 也爆炸
2 2 2 2
D.同族元素有Ca(OH) 的碱性强于Mg(OH) ,Pb(OH) 的碱性也应强于Sn(OH)
2 2 4 4
【答案】D
【解析】由于NH 分子间存在氢键,导致PH 的熔、沸点比NH 的低,A项错误;元素非金属性越强,
3 3 3
氢化物的稳定性越强,因非金属性:O>N,则HO比NH 稳定,而非金属性:O>S,则无法通过类比比较
2 3
HS与NH 的稳定性,B项错误;同主族元素从上到下非金属性逐渐减弱,能用元素周期律解释F 在暗处
2 3 2
遇H 即爆炸,但I 在暗处遇H 几乎不反应,C项错误;同一主族从上到下元素的金属性逐渐增强,金属性:
2 2 2
Ca>Mg,则同族元素对应的最高价氧化物的水化物Ca(OH) 的碱性强于Mg(OH) 的碱性,同理,金属性:
2 2
Pb>Sn,所以Pb(OH) 的碱性也应强于Sn(OH) 的碱性,D项正确。
4 4
9.下列事实中,不能用元素周期律解释的是( )
A.原子半径:K>Ca>Mg
B.碱性:NaOH>Mg(OH) >Al(OH)
2 3
C.热稳定性:HF>HCl>H S
2
D.酸性:HSO >H CO>H SiO
2 3 2 3 2 3
【答案】D
【解析】同一周期主族元素从左到右原子半径依次减小,同一主族元素从上到下原子半径依次增大,
A项不符合题意;元素的金属性越强,其最高价氧化物对应的水化物碱性越强,B项不符合题意;元素的
非金属性越强,其气态氢化物越稳定,C项不符合题意;元素的非金属性越强,其最高价氧化物对应的水
化物酸性越强,HSO 不是S元素最高价氧化物对应的水化物,D项符合题意。
2 310.下列说法正确的是( )
①砷(As)位于元素周期表第ⅤA族,其最高价氧化物对应水化物的酸性比硝酸弱
②铊(Tl)与铝同主族,其单质既能与盐酸反应,又能与氢氧化钠溶液反应
③气态氢化物的水溶液的酸性HS弱于HCl
2
④非金属元素的气态氢化物溶于水后,均形成无氧酸
A.①③④ B.①②④
C.①③ D.②③
【答案】C
【解析】元素的非金属性越强,其最高价氧化物对应的水化物酸性越强,①正确;Tl不与NaOH溶液
反应,②错误;HCl是强酸,HS是弱酸,③正确;NH 溶于水后形成弱碱,④错误。
2 3
【练提升】
1.如表所示是元素周期表的一部分,有关说法正确的是( )
族
Ⅰ Ⅱ Ⅲ Ⅳ Ⅴ Ⅵ Ⅶ
周期 A A A A A A A
二 c d
三 a b e f
A.e的简单氢化物比d的简单氢化物稳定
B.a、b、e三种元素的原子半径:e>b>a
C.六种元素中,e元素单质的化学性质最活泼
D.c、e、f的最高价氧化物对应的水化物的酸性依次增强
【答案】D
【解析】e是硫元素,d是氧元素,HS稳定性弱于HO,A错误;同周期元素的原子半径从左到右逐
2 2
渐减小,B错误;a~f六种元素分别为Na、Mg、C、O、S、Cl,其中金属单质中Na的化学性质最活泼,
非金属单质中Cl、O 化学性质均比S活泼,C错误。
2 2
2.短周期元素X、Y、Z、W、Q在元素周期表中的相对位置如图所示。下列说法不正确的是( )
A.W、Y对应的简单氢化物的稳定性前者高
B.阴离子的还原性:W2->Q-
C.离子半径:Y2->Z3+
D.元素的非金属性:Y>W【答案】A
【解析】W、Y对应的简单氢化物分别为HS和HO,元素非金属性越强,其简单气态氢化物的稳定
2 2
性越强,非金属性:O>S,所以水的稳定性比HS高,故A错误;S和Cl的非金属性:S<Cl,所以阴离
2
子的还原性:S2->Cl-,故B正确;O2-和Al3+核外电子排布相同,离子半径随核电荷数的增大而减小,
所以离子半径:O2->Al3+,故C正确;同主族元素,从上到下,原子半径逐渐增大,原子核对核外电子
的束缚力逐渐减弱,所以元素的非金属性逐渐减弱,故元素的非金属性:O>S,故D正确。
3.如图A、B、C、D、E是长式元素周期表中的5种元素(不包括镧系和锕系)。下列说法不正确的是(
)
A.A、E原子序数之差可能为2
B.D、E原子序数之差可能是18或32
C.B、C原子序数之差一定是2
D.B、D原子序数之差不可能是7
【答案】A
【解析】由题给5种元素的位置关系可以看出,A不是第一周期元素,因为A若为氢元素,则其位于
最左边一族,就不会有B;A若为氦元素,则其位于最右边一族,就不会有C。既然A不是氢元素或氦元
素,则A、E原子序数之差不可能为2,A错误;由表中位置关系可知,D、E原子序数之差可能是8、18
或32,B正确;B、C之间仅隔有E一种元素,故原子序数之差一定为2,C正确;B、D原子序数之差应
大于8,D正确。
4.根据元素周期表和元素周期律,判断下列叙述不正确的是( )
A.气态氢化物的稳定性:HO>NH >SiH
2 3 4
B.氢元素与其他元素可形成共价化合物或离子化合物
C.上图所示实验可证明元素的非金属性:Cl>C>Si
D.用中文“ ”(ào)命名的第118号元素在周期表中位于第七周期0族【答案】C
【解析】气态氢化物稳定性与非金属性一致,非金属性:O>N>Si,所以气态氢化物稳定性:HO>
2
NH >SiH,A正确;氢元素可与非金属元素形成共价化合物如HO等,也可以与某些金属元素形成离子
3 4 2
化合物如NaH等,B正确;不能用氢化物的酸性来验证非金属性强弱,可以采用最高价含氧酸的酸性强弱
来验证,C错误;根据元素周期表知识判断,各周期0族元素的原子序数依次为2、10、18、36、54、
86、118,所以第118号元素在周期表中位于第七周期0族,D正确。
5.现有短周期主族元素R、X、Y、Z、T。R与T元素的原子最外层电子数均是电子层数的2倍,Y
元素能与大多数金属和非金属元素形成化合物;Z+与Y2-电子层结构相同。五种元素的原子半径随原子序
数的变化如图所示。下列推断正确的是( )
A.Y、Z组成的化合物中只含有离子键
B.氢化物的沸点:RMg
B Ca(OH) 的碱性强于Mg(OH) 金属性:Ca>Mg
2 2
C 氧化性:HClO>HCO 金属性:Cl>C
2 3
D 热稳定性强弱:HBr>HI 非金属性:Br>I
【答案】C
【解析】根据与水反应的剧烈程度可判断元素金属性强弱,A项不符合题意;根据最高价氧化物对应的水化物碱性强弱可判断元素金属性强弱,B项不符合题意;应该根据最高价氧化物对应的水化物酸性强
弱来判断元素非金属性强弱,C项符合题意;气态氢化物越稳定,元素非金属性越强,D项不符合题意。
7.如图是元素周期表的一部分,下列叙述不正确的是( )
B C N O F
Al Si P S Cl
Ga Ge As Se Br
In Sn Sb Te I
Tl Pb Bi Po At
A.Pb的最高正化合价为+4
B.原子半径比较:Al>F
C.酸性强弱:HAsO F,B正确;As、Se同周期,原子序数越大,非
金属性越强,则非金属性:AsS2-
2>Cl->Na+,错误;B项,磷元素存在红磷、白磷等同素异形体,正确;C项,非金属性:Cl>S>P,则气
态氢化物的稳定性:HCl>H S>PH,正确;D项,NaPO 溶液因PO水解而使溶液呈碱性,错误。
2 3 3 4
9.现有1~20号元素A、B、C、D所对应的物质的性质或微粒结构如下表:
元素 物质性质或微粒结构
A M层上有2对成对电子
B B的离子与D的离子具有相同的电子层结构,且可以相互组合形成干燥剂
C 常温下单质为双原子分子,其氢化物水溶液呈碱性
D 元素最高正价是+7价
(1)元素A的原子最外层共有________种不同运动状态的电子,这些电子中有________种能量不同的电
子。B的离子与D的离子相互组合形成的干燥剂的化学式是________。
(2)元素C与氢元素形成带一个单位正电荷的离子,写出该微粒的电子式:__________。
(3)元素A与元素D相比,非金属性较强的是________(用元素符号表示),下列表述中能证明这一事实
的是________(填字母)。
A.常温下A的单质和D的单质状态不同
B.A的氢化物比D的氢化物稳定
C.一定条件下D能从A的氢化物水溶液中置换出A单质
D.D的氢化物水溶液酸性比A的氢化物水溶液酸性强
(4)C的氢化物固态时属于________晶体,该氢化物与A的最高价氧化物对应的水化物反应的化学方程
式是______________________________________________。
【解析】M层上有2对成对电子可推出A原子3p轨道分布了4个电子,A为S元素;根据C的氢化物
水溶液呈碱性可知,C为N元素;1~20号元素最高正价是+7价的只有Cl,所以D为Cl元素;B的离子
与D的离子具有相同的电子层结构,且可以相互组合形成干燥剂,可推出B为Ca元素。(3)根据元素周期
律和元素周期表可知,Cl的非金属性大于S;一定条件下Cl 能从HS水溶液中置换出S单质,说明Cl原
2 2
子的得电子能力大于S原子,Cl元素的非金属性大于S元素。非金属性强弱与单质的状态、氢化物水溶液
的酸性无关,氯化氢的稳定性强于硫化氢,故选C。(4)C的氢化物为NH ,固态时属于分子晶体,A的最
3
高价氧化物对应的水化物为HSO ,二者反应生成(NH )SO ,反应的化学方程式为2NH +
2 4 4 2 4 3
HSO ===(NH)SO 。
2 4 4 2 4
【答案】(1)6 2 CaCl (2) (3)Cl C (4)分子 2NH +HSO ===(NH)SO
2 3 2 4 4 2 4
10.为纪念元素周期表诞生150周年,IUPAC等向世界介绍118位优秀青年化学家,并形成一张“青
年化学家元素周期表”。中国学者雷晓光、姜雪峰、刘庄分别成为“N、S、Hg”元素的代言人。回答下列问题:
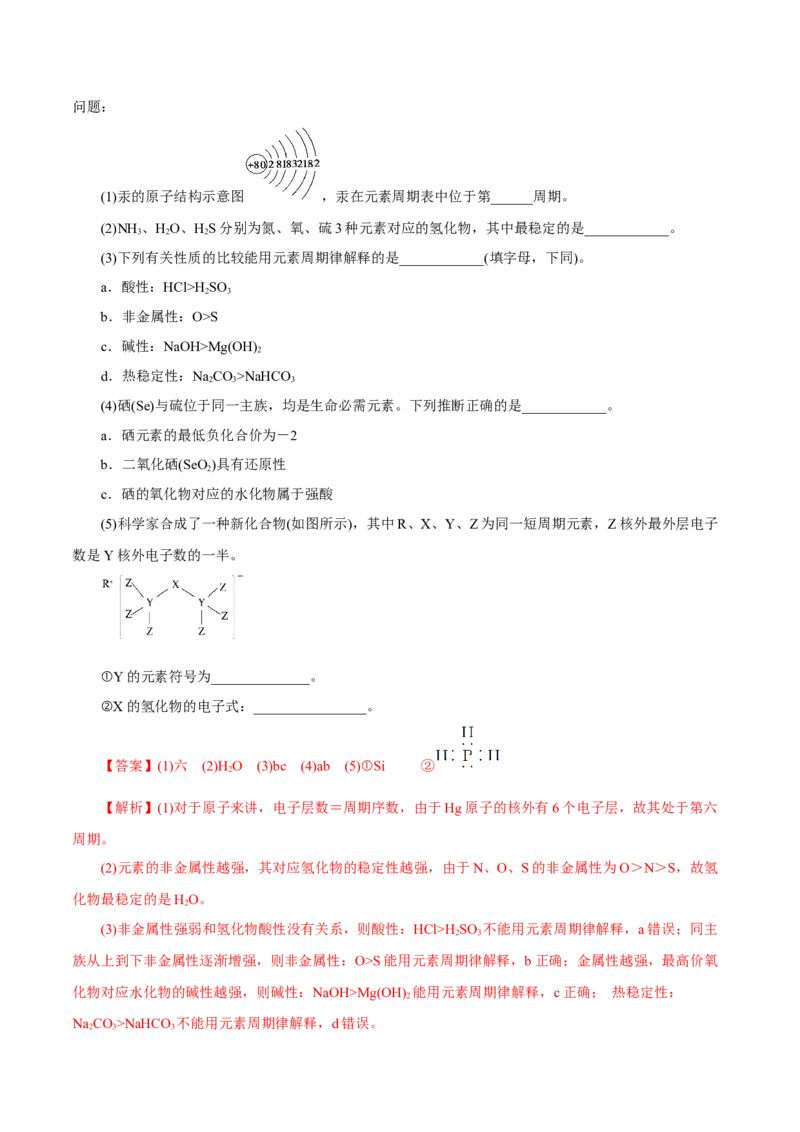
(1)汞的原子结构示意图 ,汞在元素周期表中位于第______周期。
(2)NH 、HO、HS分别为氮、氧、硫3种元素对应的氢化物,其中最稳定的是____________。
3 2 2
(3)下列有关性质的比较能用元素周期律解释的是____________(填字母,下同)。
a.酸性:HCl>H SO
2 3
b.非金属性:O>S
c.碱性:NaOH>Mg(OH)
2
d.热稳定性:NaCO>NaHCO
2 3 3
(4)硒(Se)与硫位于同一主族,均是生命必需元素。下列推断正确的是____________。
a.硒元素的最低负化合价为-2
b.二氧化硒(SeO )具有还原性
2
c.硒的氧化物对应的水化物属于强酸
(5)科学家合成了一种新化合物(如图所示),其中R、X、Y、Z为同一短周期元素,Z核外最外层电子
数是Y核外电子数的一半。
①Y的元素符号为______________。
②X的氢化物的电子式:________________。
【答案】(1)六 (2)H O (3)bc (4)ab (5)①Si ②
2
【解析】(1)对于原子来讲,电子层数=周期序数,由于Hg原子的核外有6个电子层,故其处于第六
周期。
(2)元素的非金属性越强,其对应氢化物的稳定性越强,由于N、O、S的非金属性为O>N>S,故氢
化物最稳定的是HO。
2
(3)非金属性强弱和氢化物酸性没有关系,则酸性:HCl>H SO 不能用元素周期律解释,a错误;同主
2 3
族从上到下非金属性逐渐增强,则非金属性:O>S能用元素周期律解释,b正确;金属性越强,最高价氧
化物对应水化物的碱性越强,则碱性:NaOH>Mg(OH) 能用元素周期律解释,c正确; 热稳定性:
2
NaCO>NaHCO 不能用元素周期律解释,d错误。
2 3 3(4)硒(Se)与硫位于同一主族,最外层均有6个电子,且均为非金属元素,故最高价均为+6,最低价均
为-2,故a正确;硒(Se)的最高价为+6,最低价为-2,SeO 的+4价处于中间价态,既有氧化性又有还
2
原性,故b正确;由于Se为非金属元素,故硒的最高价氧化物对应的水化物属于酸,但非金属性弱于硫,
因此硒的氧化物对应的水化物不属于强酸,故c错误。
(5)R、X、Y、Z为同一短周期元素,根据图知,Y能形成4个共价键、Z能形成1个共价键,则Y位
于第ⅣA族、Z位于第ⅦA族,且Z核外最外层电子数是Y核外电子数的一半,Z最外层7个电子,则Y
原子核外有14个电子,Y为Si元素,Z为Cl元素,该阴离子中Cl元素为-1价、Y元素为+4价,根据化
合价的代数和为-1可知,X为-3价,所以X为P元素,根据阳离子所带电荷知,R为Na元素,根据以
上分析可知:R、X、Y、Z分别是Na、P、Si、Cl元素,所以①Y的元素符号为Si;②X的氢化物为
PH ,其电子式为 。
3