文档内容
专题 06 化学反应与能量
第 15 练 化学反应与能量变化
1.下列属于可再生能源的是( )
A.煤 B.石油 C.核能 D.乙醇
2.据报道,某国一集团拟在太空建造巨大的集光装置,把太阳光变成激光用于分解海水制氢:
2HO=====2H↑+O↑,下列说法正确的是( )
2 2 2
A.水的分解反应是放热反应 B.氢气是一次能源
C.使用氢气作燃料将会增加温室效应 D.在这一反应中,光能转化为化学能
3.下列反应属于吸热反应的是( )
A.金属钠与水反应 B.化石燃料的燃烧
C.氢氧化钡晶体与氯化铵晶体混合 D.氢氧化钠与盐酸反应
4.下列关于能量的说法不合理的是( )
A.太阳能电池将化学能转化为电能
B.镁条与盐酸反应过程将化学能转化成热能
C.火力发电涉及多种能量之间的转化
D.化学反应中,断裂化学键要吸收能量,形成化学键要释放能量
5.下列关于化学反应与能量的说法中,不正确的是( )
A.镁条与盐酸的反应属于放热反应
B.断裂化学键释放能量,形成化学键需要吸收能量
C.化学反应不仅有新物质生成而且伴随着能量变化
D.反应物的总能量高于生成物的总能量,反应时向环境释放能量
6.下列说法正确的是( )
A.镍氢电池、锂离子电池和碱性锌锰干电池都是二次电池
B.化学电池的反应基础是氧化还原反应
C.燃料电池是一种高效但是会严重污染环境的新型电池
D.铅蓄电池放电的时候正极是Pb,负极是PbO
2
7.下列设备工作时,将化学能转化为电能的是( )8.下面是四个化学反应,你认为理论上不可用于设计原电池的化学反应是( )
A.Zn+Ag O+HO===Zn(OH) +2Ag B.Pb+PbO +2HSO ===2PbSO+2HO
2 2 2 2 2 4 4 2
C.Zn+CuSO ===Cu+ZnSO D.AgNO+HCl===AgCl↓+HNO
4 4 3 3
9.对原电池的电极名称,下列叙述中错误的是( )
A.电子流入的一极为正极 B.比较不活泼的一极为正极
C.电子流出的一极为负极 D.发生氧化反应的一极为正极
10.下列有关原电池的叙述中不正确的是( )
A.原电池是将化学能转化为电能的装置
B.在原电池中,电子流出的一极是负极,发生氧化反应
C.锌、铜、硫酸组成的原电池中,溶液中的 Zn2+、H+均向正极移动
D.构成原电池的两个电极必须是活泼性不同的两种金属
11.以锌片和铜片为两极,以稀硫酸为电解质溶液组成原电池,当导线中通过 2 mol电子时,下列说
法正确的是( )
A.锌片溶解了1 mol,铜片上析出1 mol H
2
B.两极上溶解和析出的物质质量相等
C.锌片溶解31 g,铜片上析出1 g H
2
D.锌片溶解了1 mol,硫酸消耗0.5 mol
12.下列关于实验现象的描述不正确的是( )
A.把铜片和铁片紧靠在一起浸入稀硫酸中,铜片表面出现气泡
B.用锌片作负极,铜片作正极,在CuSO 溶液中,铜片质量增加[来源:学科网]
4
C.把铜片插入三氯化铁溶液中,在铜片表面出现一层铁
D.把锌粒放入盛有盐酸的试管中,加入几滴氯化铜溶液,气泡放出速率加快
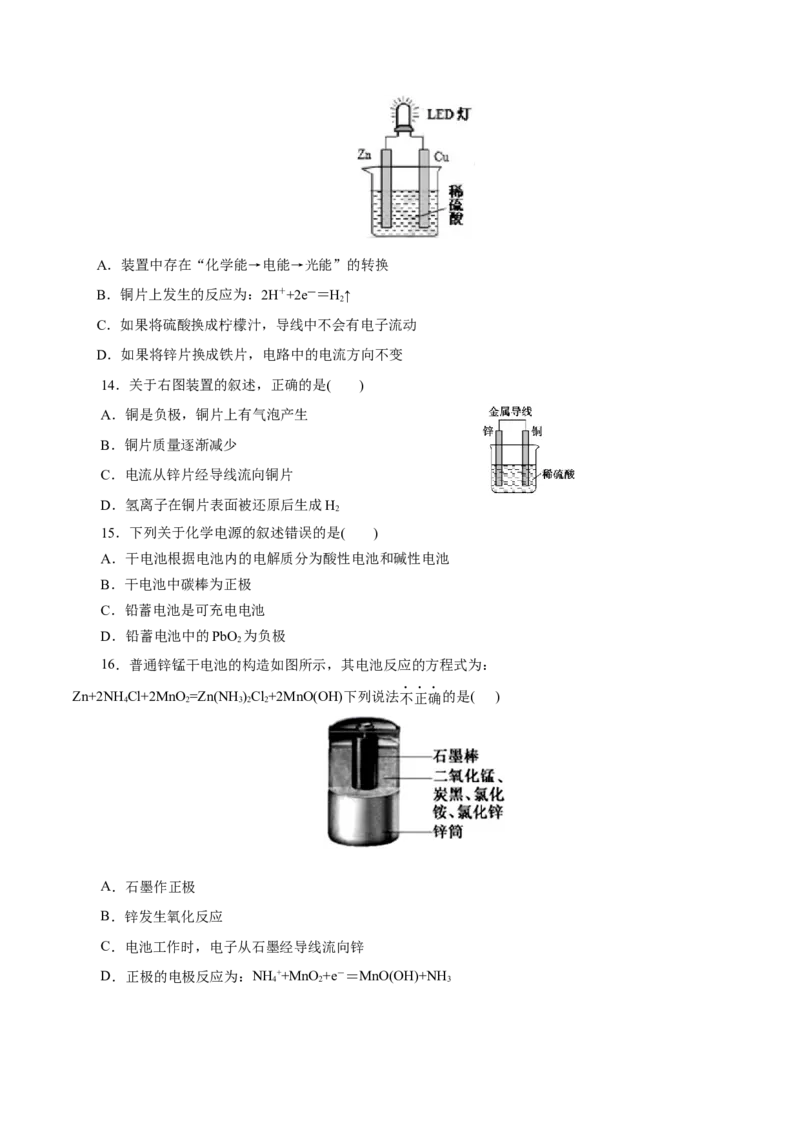
13.LED(Light Emitting Diode),发光二极管,是一种能够将电能转化为可见光的固态的半导体器件,
它可以直接把电能转化为光能。下图是课外活动小组设计的用化学电源使LED灯发光的装置。下列说法错
误的是( )A.装置中存在“化学能→电能→光能”的转换
B.铜片上发生的反应为:2H++2e―=H↑
2
C.如果将硫酸换成柠檬汁,导线中不会有电子流动
D.如果将锌片换成铁片,电路中的电流方向不变
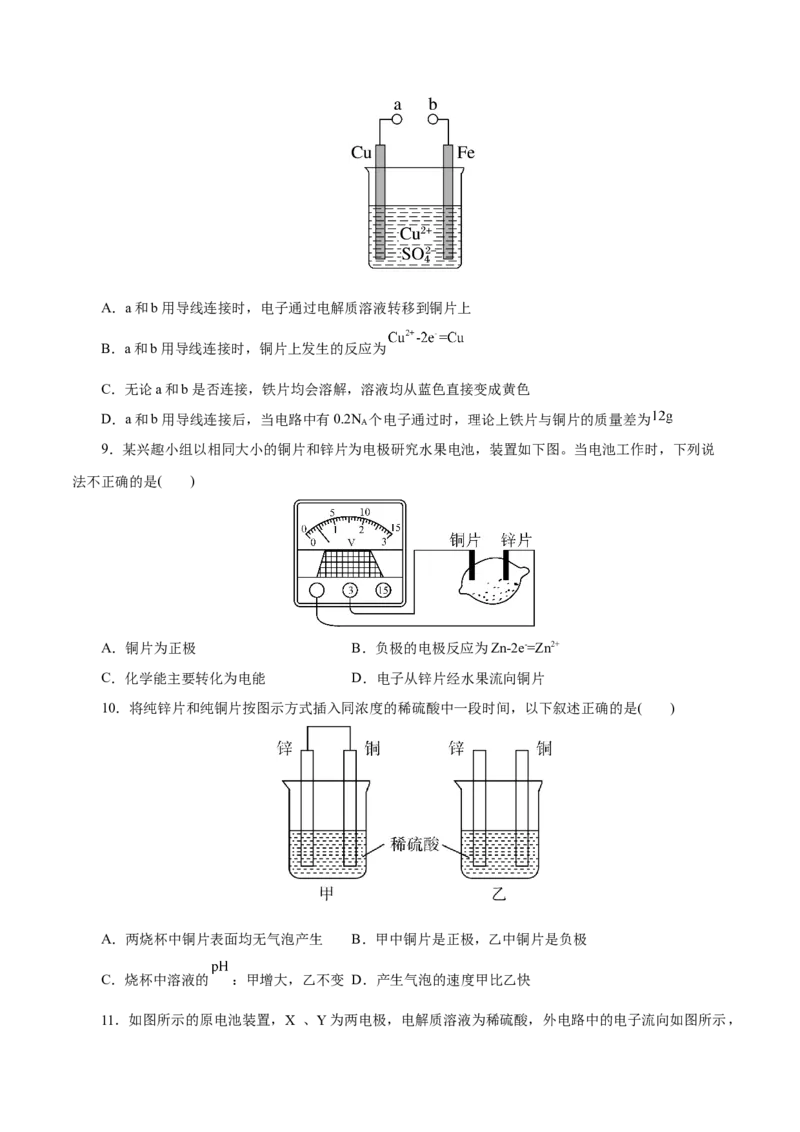
14.关于右图装置的叙述,正确的是( )
A.铜是负极,铜片上有气泡产生
B.铜片质量逐渐减少
C.电流从锌片经导线流向铜片
D.氢离子在铜片表面被还原后生成H
2
15.下列关于化学电源的叙述错误的是( )
A.干电池根据电池内的电解质分为酸性电池和碱性电池
B.干电池中碳棒为正极
C.铅蓄电池是可充电电池
D.铅蓄电池中的PbO 为负极
2
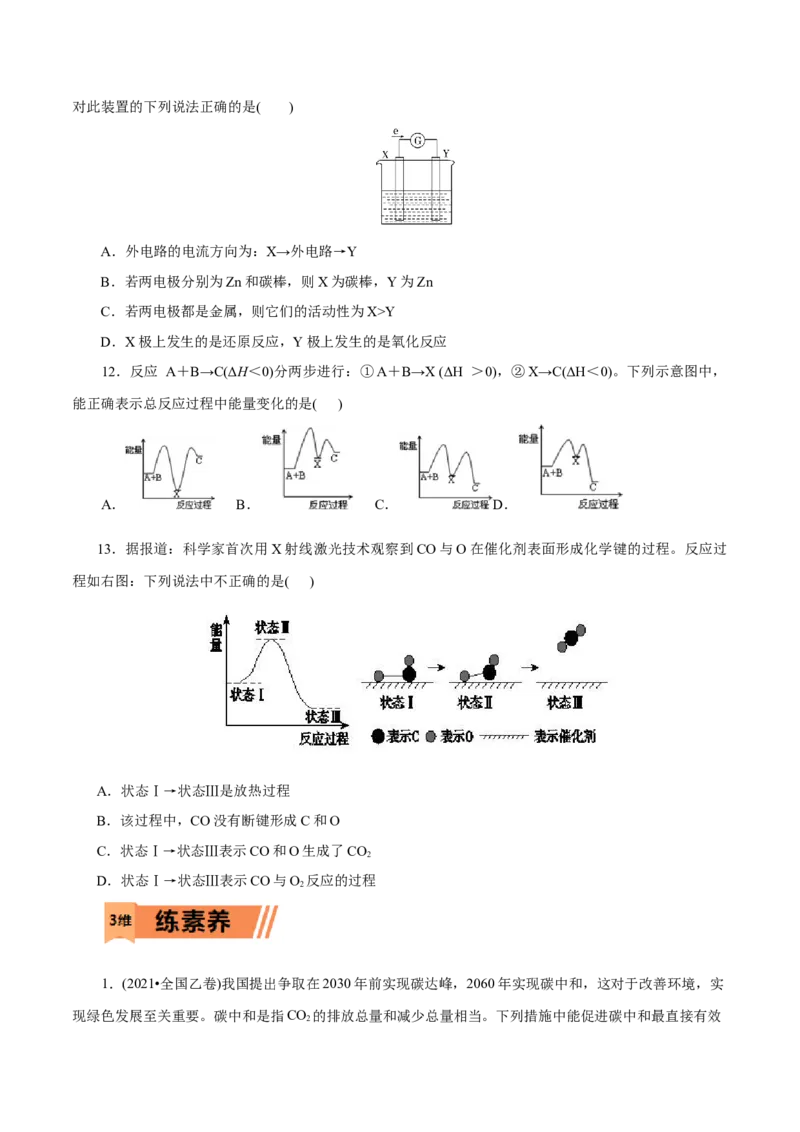
16.普通锌锰干电池的构造如图所示,其电池反应的方程式为:
Zn+2NH Cl+2MnO =Zn(NH)Cl+2MnO(OH)下列说法不正确的是( )
4 2 3 2 2
A.石墨作正极
B.锌发生氧化反应
C.电池工作时,电子从石墨经导线流向锌
D.正极的电极反应为:NH ++MnO+e-=MnO(OH)+NH
4 2 31.下列设备工作时,将化学能转化为电能的是( )
A B C D
锂离子电池 硅太阳能电池 电动车电池充电 燃气灶
2.有关下列四个常用电化学装置的叙述中,正确的是( )
A.图Ⅰ所示电池中,电子经石墨电极沿电解质溶液流向锌筒
B.图Ⅱ所示电池中,MnO 的作用是作氧化剂
2
C.图Ⅲ所示装置工作过程中,电解质溶液中Cu2+浓度始终不变
D.图Ⅳ所示电池中,Zn是还原剂,在电池工作过程中被还原
3.C H 为液化气的成分之一,其充分燃烧的方程式为 。下列叙述
3 8
正确的是( )
A.该反应为吸热反应
B.生成物的总能量高于反应物总能量
C.化学反应中的能量变化主要是由化学键变化引起的
D.能量变化必然伴随着化学反应的发生
4.1mol CO(g)与1 mol H O(g)反应生成1mol CO(g)与1 mol H (g)的过程中能量变化如图所示,下列说
2 2 2
法正确的是( )A.该反应不需要加热就能直接发生
B.该反应中只有极性键的断裂和形成
C.生成2mol CO(g)和2 mol H (g)时,放出 能量
2 2
D.CO(g)与HO(g)所具有的总能量小于CO(g)与H(g)所具有的总能量
2 2 2
5.已知化学反应2C(s)+O(g)=====2CO(g)、2CO(g)+O(g)=====2CO(g)都是放热反应。据此判断,
2 2 2
下列说法不正确的是(其他条件相同)( )
A.12 g C所具有的能量一定高于28 g CO所具有的能量
B.56 g CO和32 g O 所具有的总能量大于88 g CO 所具有的总能量
2 2
C.12 g C和32 g O 所具有的总能量大于44 g CO 所具有的总能量
2 2
D.将一定质量的C燃烧,生成CO 比生成CO时放出的热量多
2
6.在25 ℃,101 kPa下,1 mol的白磷(化学式为P)完全燃烧放出的热量比4 mol的红磷(化学式为P)
4
完全燃烧放出的热量多。化学方程式分别为P(s)+5O(g)===P O (s);4P(s)+5O(g)===P O (s)。由此判断,
4 2 4 10 2 4 10
下列说法正确的是( )
A.由红磷转化为白磷是吸热反应,等质量时红磷能量比白磷高
B.由红磷转化为白磷是放热反应,等质量时红磷能量比白磷低
C.由红磷转化为白磷是放热反应,等质量时红磷能量比白磷高
D.由红磷转化为白磷是吸热反应,等质量时红磷能量比白磷低
7.化学反应可视为旧键断裂和新键形成的过程。共价键的键能是两种原子间形成 1 mol共价键(或其
可逆过程)时释放(或吸收)的能量。已知H—H键的键能为436 kJ·mol-1、Cl—Cl键的键能为243 kJ·mol-1、
H—Cl键的键能为x,若1 mol H (g)与1 mol Cl (g)反应生成2 mol HCl(g)放出183 kJ的热量,则x为( )
2 2
A.496 kJ·mol-1 B.431 kJ·mol-1 C.862 kJ·mol-1 D.248 kJ·mol-1
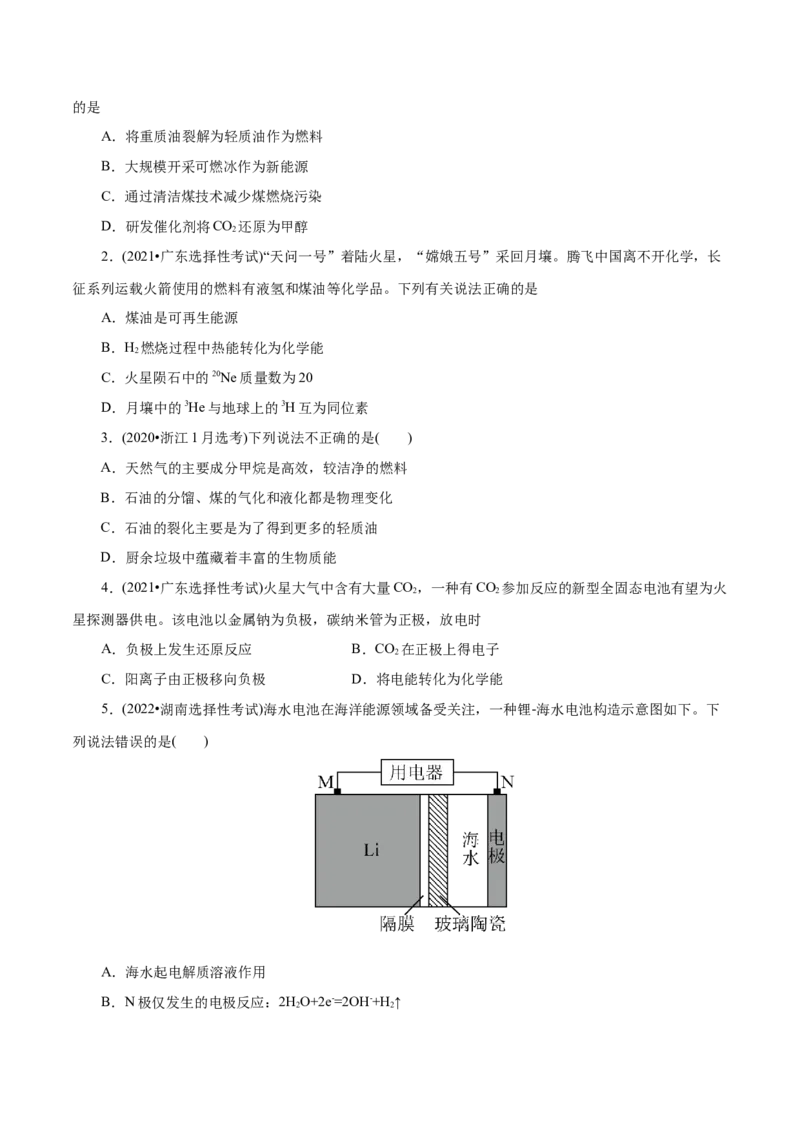
8.质量均为 的铁片、铜片和 溶液组成的装置如图所示,下列说法正确的是(
)A.a和b用导线连接时,电子通过电解质溶液转移到铜片上
B.a和b用导线连接时,铜片上发生的反应为
C.无论a和b是否连接,铁片均会溶解,溶液均从蓝色直接变成黄色
D.a和b用导线连接后,当电路中有0.2N 个电子通过时,理论上铁片与铜片的质量差为
A
9.某兴趣小组以相同大小的铜片和锌片为电极研究水果电池,装置如下图。当电池工作时,下列说
法不正确的是( )
A.铜片为正极 B.负极的电极反应为Zn-2e-=Zn2+
C.化学能主要转化为电能 D.电子从锌片经水果流向铜片
10.将纯锌片和纯铜片按图示方式插入同浓度的稀硫酸中一段时间,以下叙述正确的是( )
A.两烧杯中铜片表面均无气泡产生 B.甲中铜片是正极,乙中铜片是负极
C.烧杯中溶液的 :甲增大,乙不变 D.产生气泡的速度甲比乙快
11.如图所示的原电池装置,X 、Y为两电极,电解质溶液为稀硫酸,外电路中的电子流向如图所示,对此装置的下列说法正确的是( )
A.外电路的电流方向为:X→外电路→Y
B.若两电极分别为Zn和碳棒,则X为碳棒,Y为Zn
C.若两电极都是金属,则它们的活动性为X>Y
D.X极上发生的是还原反应,Y极上发生的是氧化反应
12.反应 A+B→C(ΔH<0)分两步进行:①A+B→X (ΔH >0),②X→C(ΔH<0)。下列示意图中,
能正确表示总反应过程中能量变化的是( )
A. B. C. D.
13.据报道:科学家首次用X射线激光技术观察到CO与O在催化剂表面形成化学键的过程。反应过
程如右图:下列说法中不正确的是( )
A.状态Ⅰ→状态Ⅲ是放热过程
B.该过程中,CO没有断键形成C和O
C.状态Ⅰ→状态Ⅲ表示CO和O生成了CO
2
D.状态Ⅰ→状态Ⅲ表示CO与O 反应的过程
2
1.(2021•全国乙卷)我国提出争取在2030年前实现碳达峰,2060年实现碳中和,这对于改善环境,实
现绿色发展至关重要。碳中和是指CO 的排放总量和减少总量相当。下列措施中能促进碳中和最直接有效
2的是
A.将重质油裂解为轻质油作为燃料
B.大规模开采可燃冰作为新能源
C.通过清洁煤技术减少煤燃烧污染
D.研发催化剂将CO 还原为甲醇
2
2.(2021•广东选择性考试)“天问一号”着陆火星,“嫦娥五号”采回月壤。腾飞中国离不开化学,长
征系列运载火箭使用的燃料有液氢和煤油等化学品。下列有关说法正确的是
A.煤油是可再生能源
B.H 燃烧过程中热能转化为化学能
2
C.火星陨石中的20Ne质量数为20
D.月壤中的3He与地球上的3H互为同位素
3.(2020•浙江1月选考)下列说法不正确的是( )
A.天然气的主要成分甲烷是高效,较洁净的燃料
B.石油的分馏、煤的气化和液化都是物理变化
C.石油的裂化主要是为了得到更多的轻质油
D.厨余垃圾中蕴藏着丰富的生物质能
4.(2021•广东选择性考试)火星大气中含有大量CO,一种有CO 参加反应的新型全固态电池有望为火
2 2
星探测器供电。该电池以金属钠为负极,碳纳米管为正极,放电时
A.负极上发生还原反应 B.CO 在正极上得电子
2
C.阳离子由正极移向负极 D.将电能转化为化学能
5.(2022•湖南选择性考试)海水电池在海洋能源领域备受关注,一种锂-海水电池构造示意图如下。下
列说法错误的是( )
A.海水起电解质溶液作用
B.N极仅发生的电极反应:2HO+2e-=2OH-+H ↑
2 2C.玻璃陶瓷具有传导离子和防水的功能
D.该锂-海水电池属于一次电池
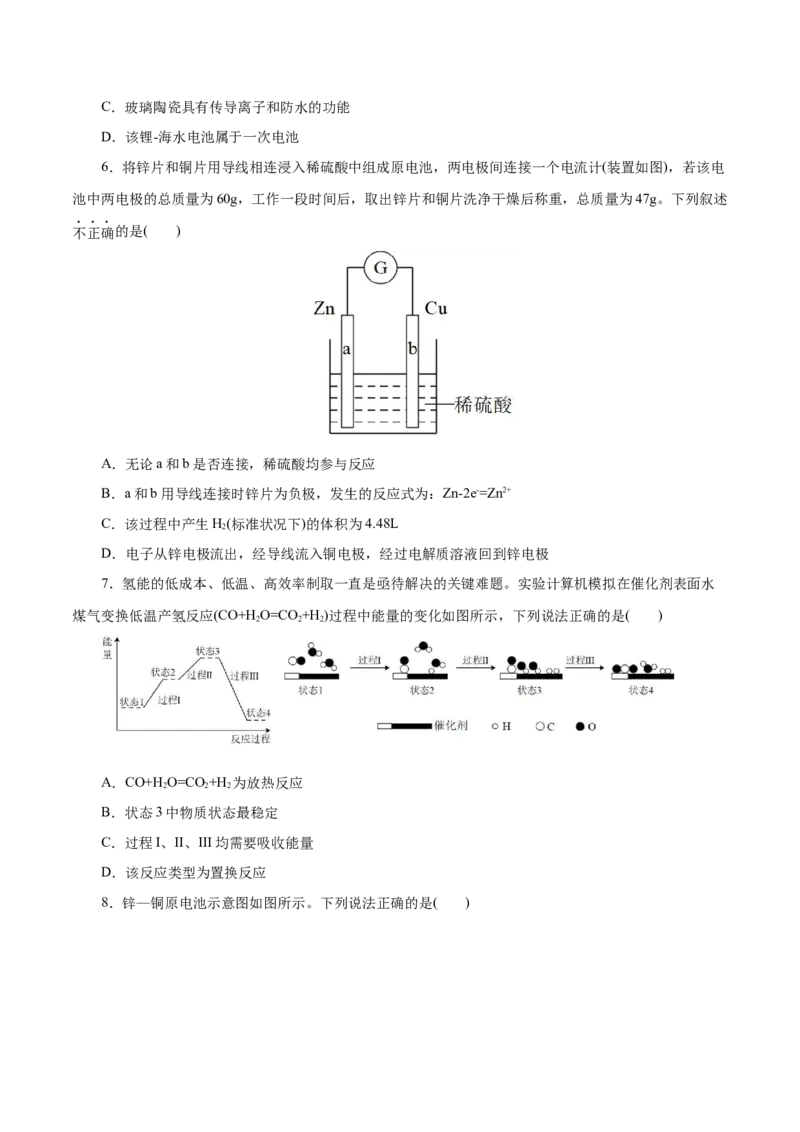
6.将锌片和铜片用导线相连浸入稀硫酸中组成原电池,两电极间连接一个电流计(装置如图),若该电
池中两电极的总质量为60g,工作一段时间后,取出锌片和铜片洗净干燥后称重,总质量为47g。下列叙述
不正确的是( )
A.无论a和b是否连接,稀硫酸均参与反应
B.a和b用导线连接时锌片为负极,发生的反应式为:Zn-2e-=Zn2+
C.该过程中产生H(标准状况下)的体积为4.48L
2
D.电子从锌电极流出,经导线流入铜电极,经过电解质溶液回到锌电极
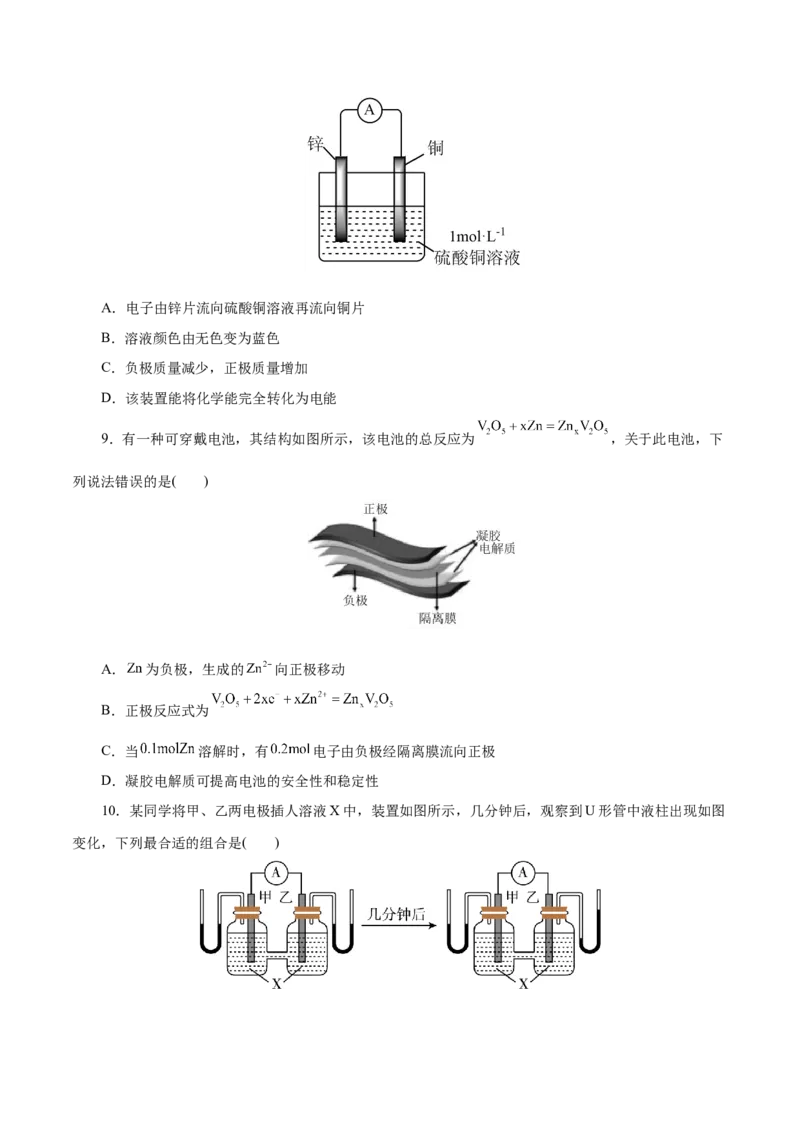
7.氢能的低成本、低温、高效率制取一直是亟待解决的关键难题。实验计算机模拟在催化剂表面水
煤气变换低温产氢反应(CO+HO=CO+H )过程中能量的变化如图所示,下列说法正确的是( )
2 2 2
A.CO+HO=CO+H 为放热反应
2 2 2
B.状态3中物质状态最稳定
C.过程I、II、III均需要吸收能量
D.该反应类型为置换反应
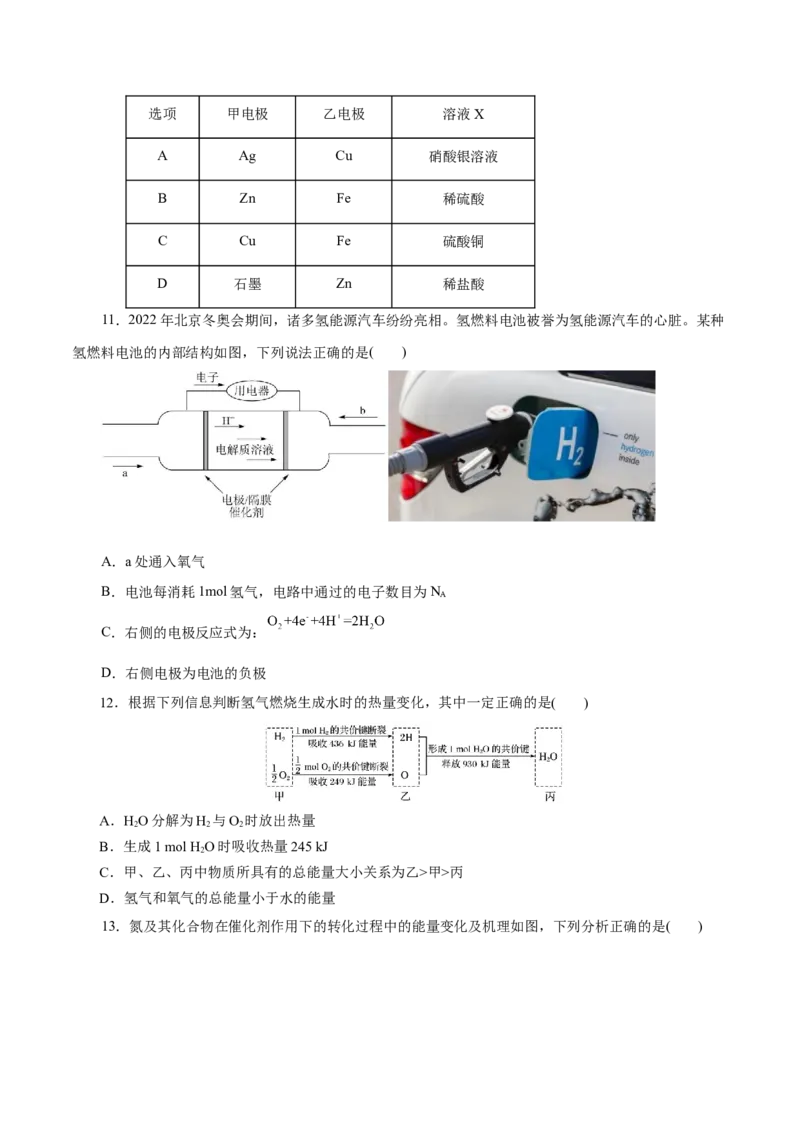
8.锌—铜原电池示意图如图所示。下列说法正确的是( )A.电子由锌片流向硫酸铜溶液再流向铜片
B.溶液颜色由无色变为蓝色
C.负极质量减少,正极质量增加
D.该装置能将化学能完全转化为电能
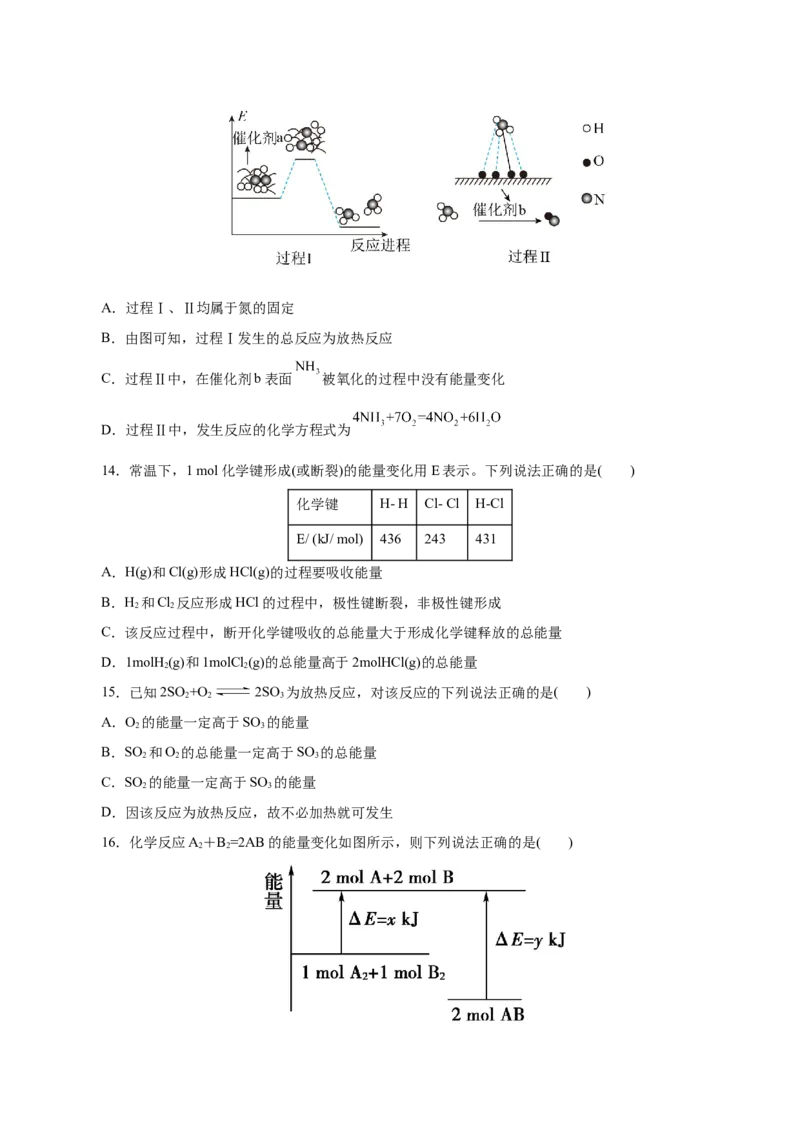
9.有一种可穿戴电池,其结构如图所示,该电池的总反应为 ,关于此电池,下
列说法错误的是( )
A. 为负极,生成的 向正极移动
B.正极反应式为
C.当 溶解时,有 电子由负极经隔离膜流向正极
D.凝胶电解质可提高电池的安全性和稳定性
10.某同学将甲、乙两电极插人溶液X中,装置如图所示,几分钟后,观察到U形管中液柱出现如图
变化,下列最合适的组合是( )选项 甲电极 乙电极 溶液X
A Ag Cu 硝酸银溶液
B Zn Fe 稀硫酸
C Cu Fe 硫酸铜
D 石墨 Zn 稀盐酸
11.2022年北京冬奥会期间,诸多氢能源汽车纷纷亮相。氢燃料电池被誉为氢能源汽车的心脏。某种
氢燃料电池的内部结构如图,下列说法正确的是( )
A.a处通入氧气
B.电池每消耗1mol氢气,电路中通过的电子数目为N
A
C.右侧的电极反应式为:
D.右侧电极为电池的负极
12.根据下列信息判断氢气燃烧生成水时的热量变化,其中一定正确的是( )
A.HO分解为H 与O 时放出热量
2 2 2
B.生成1 mol H O时吸收热量245 kJ
2
C.甲、乙、丙中物质所具有的总能量大小关系为乙>甲>丙
D.氢气和氧气的总能量小于水的能量
13.氮及其化合物在催化剂作用下的转化过程中的能量变化及机理如图,下列分析正确的是( )A.过程Ⅰ、Ⅱ均属于氮的固定
B.由图可知,过程Ⅰ发生的总反应为放热反应
C.过程Ⅱ中,在催化剂b表面 被氧化的过程中没有能量变化
D.过程Ⅱ中,发生反应的化学方程式为
14.常温下,1 mol化学键形成(或断裂)的能量变化用E表示。下列说法正确的是( )
化学键 H- H Cl- Cl H-Cl
E/ (kJ/ mol) 436 243 431
A.H(g)和Cl(g)形成HCl(g)的过程要吸收能量
B.H 和Cl 反应形成HCl的过程中,极性键断裂,非极性键形成
2 2
C.该反应过程中,断开化学键吸收的总能量大于形成化学键释放的总能量
D.1molH (g)和1molCl (g)的总能量高于2molHCl(g)的总能量
2 2
15.已知2SO +O 2SO 为放热反应,对该反应的下列说法正确的是( )
2 2 3
A.O 的能量一定高于SO 的能量
2 3
B.SO 和O 的总能量一定高于SO 的总能量
2 2 3
C.SO 的能量一定高于SO 的能量
2 3
D.因该反应为放热反应,故不必加热就可发生
16.化学反应A+B =2AB的能量变化如图所示,则下列说法正确的是( )
2 2A.该反应是吸收能量的反应
B.1molA—A键和1molB—B键断裂能放出xkJ的能量
C.2molA—B键断裂需要放出ykJ的能量
D.1molA 和1molB 的总能量高于2molAB的总能量
2 2