文档内容
第十一讲 粗盐的提纯
模块一 粗盐提纯的基本实验
知识精讲
1.粗盐的提纯实验
用海水晒盐,得到粗盐NaCl:
粗盐中主要成分是食盐,主要含有的杂质:
①难溶性杂质:泥沙等;
②可溶性杂质:NaSO 、MgCl 、CaCl 等。
2 4 2 2
实验
操作示意图 操作方法 玻璃棒的作用
步骤
称取5.0克粗盐,用量简量取10毫升水,将粗
溶解 盐和水倒入烧杯里,用玻璃棒搅拌使粗盐溶解充
分
将烧杯中的液体沿玻璃棒倒入过滤装置中,其液
过滤
面不能超过滤纸边缘,若滤液浑浊,再过滤一次
将滤液倒入蒸发皿中,然后用酒精灯加热,同时
蒸发 用玻璃棒不断搅溶液,待出现较多固体时停止加
热
用玻璃棒把固体转移到纸上,用托盘天平称量质
计算
量并记录,比较提纯前后食盐状态并计算精盐的
产率
产率= ×100%思考与交流
(1)过滤时,‘一贴二低三靠’指什么?
(2)蒸发时,一直蒸干液体才停止加热,对吗?
(3)这样提纯的食盐是否为纯净物 ?
经典例题
粗盐中难溶性杂质的去除实验
【例1】(2020·广东广州)已知室温下NaCl的溶解度约为36g。现称取3.6g粗盐,经过溶解、过滤、蒸发、
转移等步骤,除去泥沙得到精盐。下列操作正确且合理的是( )
A.溶解 B.过滤 C.蒸发 D.转移
【例2】(2018·广东)如图是利用海水提取粗盐的过程,下列说法中错误的是( )
A.图中①是结晶池
B.图中②的操作过程是溶解、过滤、结晶
C.析出晶体后的母液是氯化钠的饱和溶液
D.蒸发池是利用氯化钠的溶解度受温度影响变化大的原理
【例3】在粗盐提纯的实验中,下列操作正确的是( )A.称量 B.溶解
C.过滤 D.蒸发结晶
模块二 粗盐中杂质离子的去除
知识精讲
1.粗盐中杂质离子的去除
思考与交流
1.粗盐NaCl中含有杂质:NaSO 、MgCl 、CaCl 等。
2 4 2 2
(1)含有杂质离子有哪些?
(2)用什么离子才能除去杂质离子?
2.挑选合适的试剂除去括号内杂质:
(1)NaCl(Na SO ) (2) NaCl(MgCl ) (3)NaCl(CaCl )
2 4 2 2
(4)NaCl(BaCl ) (5)NaCl(NaOH) (6)NaCl(Na CO)
2 2 3
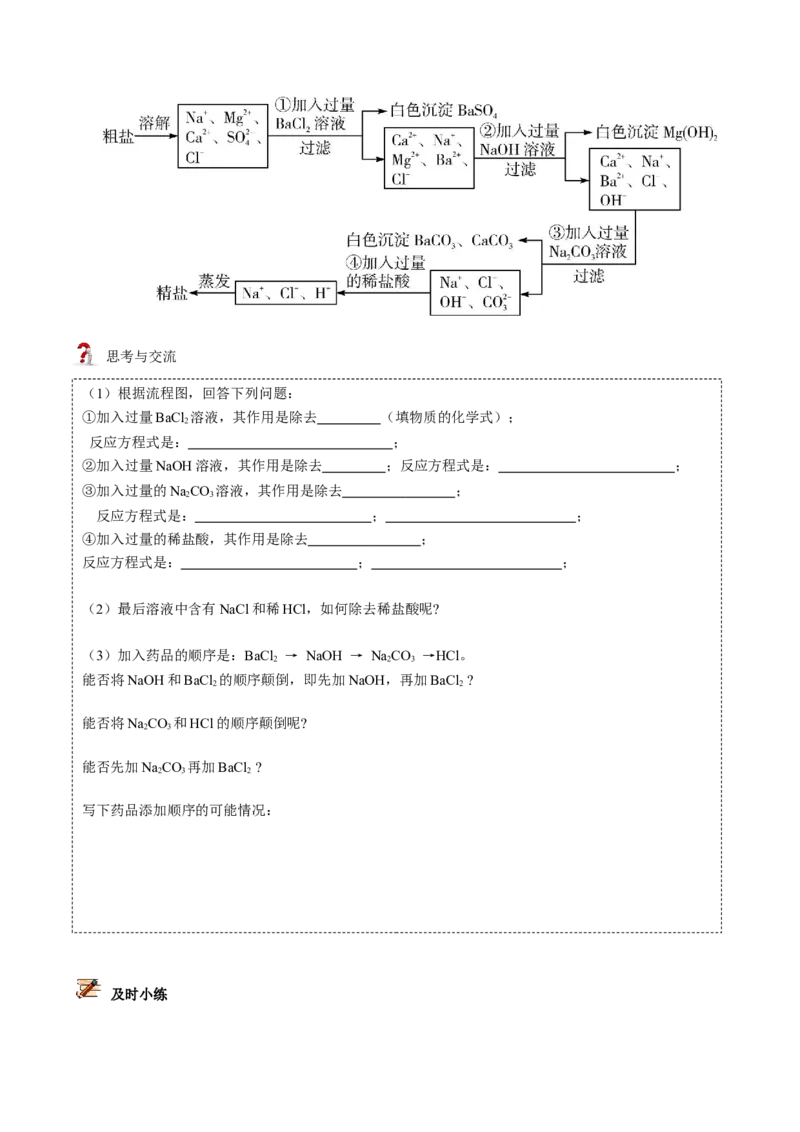
2.粗盐中杂质离子去除的流程:思考与交流
(1)根据流程图,回答下列问题:
①加入过量BaCl 溶液,其作用是除去 (填物质的化学式);
2
反应方程式是: ;
②加入过量NaOH溶液,其作用是除去 ;反应方程式是: ;
③加入过量的NaCO 溶液,其作用是除去 ;
2 3
反应方程式是: ; ;
④加入过量的稀盐酸,其作用是除去 ;
反应方程式是: ; ;
(2)最后溶液中含有NaCl和稀HCl,如何除去稀盐酸呢?
(3)加入药品的顺序是:BaCl → NaOH → NaCO →HCl。
2 2 3
能否将NaOH和BaCl 的顺序颠倒,即先加NaOH,再加BaCl ?
2 2
能否将NaCO 和HCl的顺序颠倒呢?
2 3
能否先加NaCO 再加BaCl ?
2 3 2
写下药品添加顺序的可能情况:
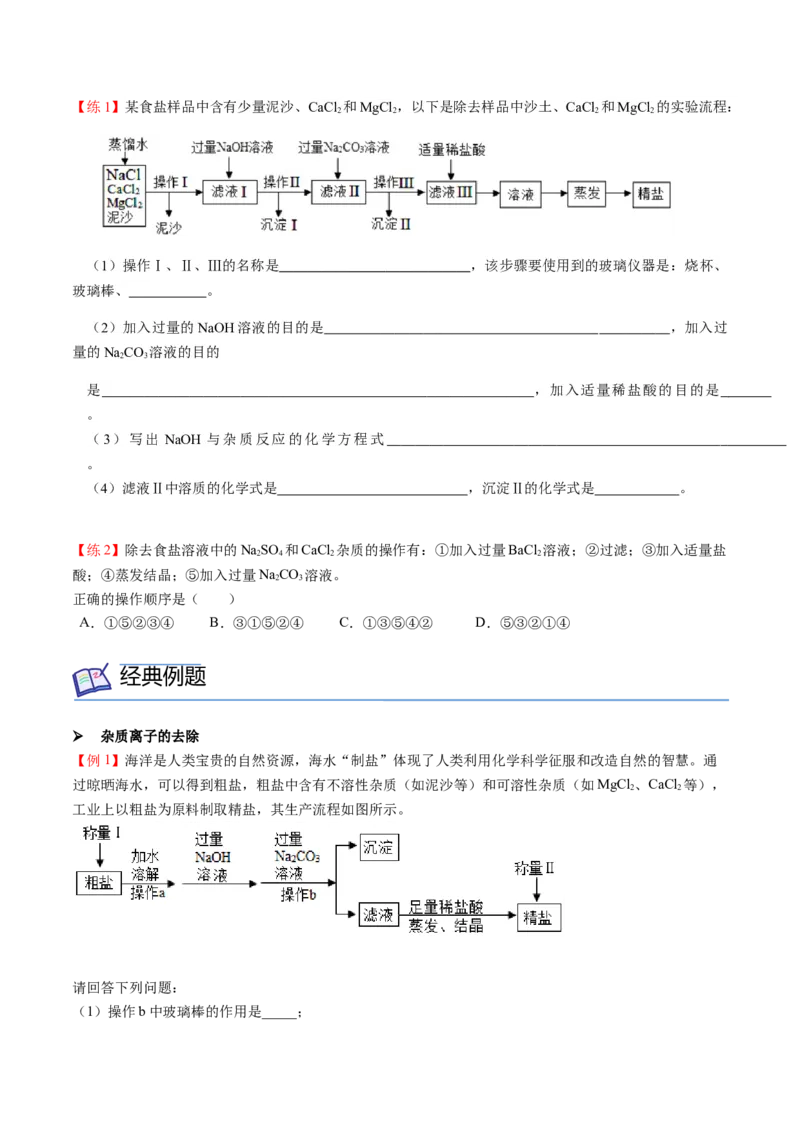
及时小练【练1】某食盐样品中含有少量泥沙、CaCl 和MgCl ,以下是除去样品中沙土、CaCl 和MgCl 的实验流程:
2 2 2 2
(1)操作Ⅰ、Ⅱ、Ⅲ的名称是 ,该步骤要使用到的玻璃仪器是:烧杯、
玻璃棒、 。
(2)加入过量的NaOH溶液的目的是 ,加入过
量的NaCO 溶液的目的
2 3
是 ,加入适量稀盐酸的目的是
。
(3)写出 NaOH 与杂质反应的化学方程式
。
(4)滤液Ⅱ中溶质的化学式是 ,沉淀Ⅱ的化学式是 。
【练2】除去食盐溶液中的NaSO 和CaCl 杂质的操作有:①加入过量BaCl 溶液;②过滤;③加入适量盐
2 4 2 2
酸;④蒸发结晶;⑤加入过量NaCO 溶液。
2 3
正确的操作顺序是( )
A.①⑤②③④ B.③①⑤②④ C.①③⑤④② D.⑤③②①④
经典例题
杂质离子的去除
【例1】海洋是人类宝贵的自然资源,海水“制盐”体现了人类利用化学科学征服和改造自然的智慧。通
过晾晒海水,可以得到粗盐,粗盐中含有不溶性杂质(如泥沙等)和可溶性杂质(如MgCl 、CaCl 等),
2 2
工业上以粗盐为原料制取精盐,其生产流程如图所示。
请回答下列问题:
(1)操作b中玻璃棒的作用是_____;(2)加入NaCO 溶液除去的离子是___(填离子符号),加入NaOH溶液发生反应的化学方程式为
2 3
_______。
(3)滤液中溶质的主要成分是_____ (填一个化学式),加入足量稀盐酸的目的是_______。
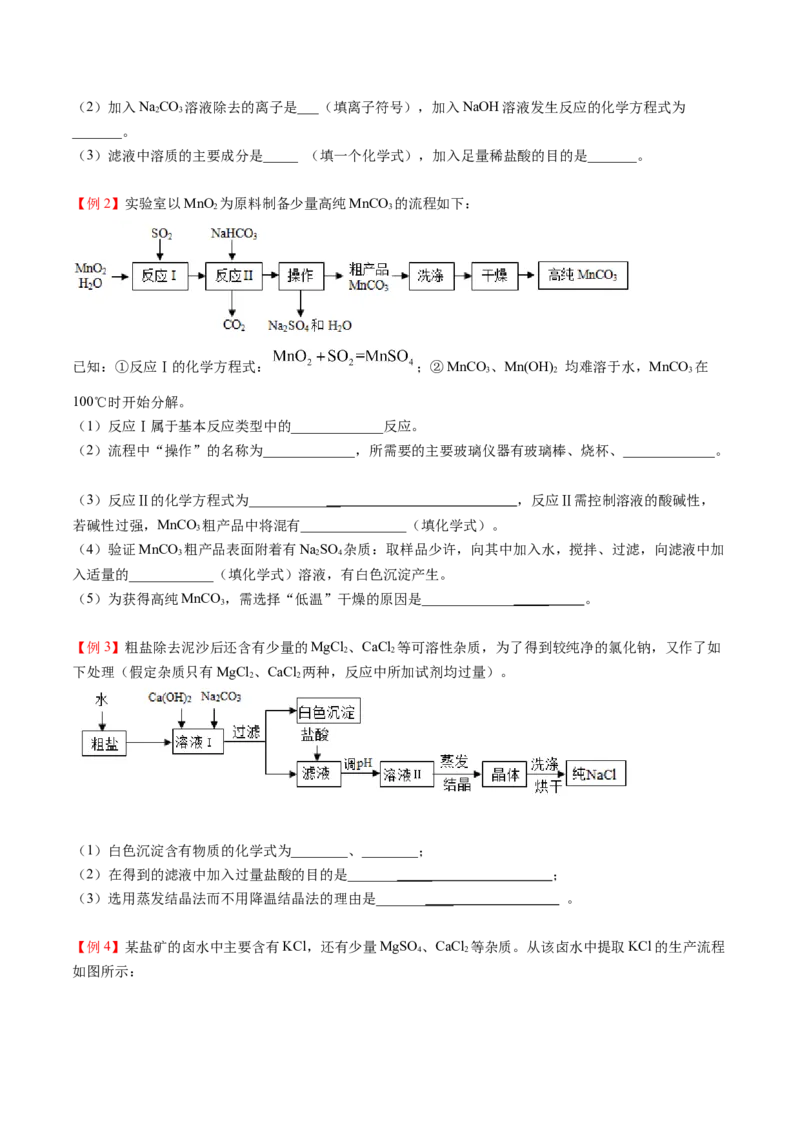
【例2】实验室以MnO 为原料制备少量高纯MnCO 的流程如下:
2 3
已知:①反应Ⅰ的化学方程式: ;②MnCO 、Mn(OH) 均难溶于水,MnCO 在
3 2 3
100℃时开始分解。
(1)反应Ⅰ属于基本反应类型中的_____________反应。
(2)流程中“操作”的名称为_____________,所需要的主要玻璃仪器有玻璃棒、烧杯、_____________。
(3)反应Ⅱ的化学方程式为_____________ ,反应Ⅱ需控制溶液的酸碱性,
若碱性过强,MnCO 粗产品中将混有_______________(填化学式)。
3
(4)验证MnCO 粗产品表面附着有NaSO 杂质:取样品少许,向其中加入水,搅拌、过滤,向滤液中加
3 2 4
入适量的____________(填化学式)溶液,有白色沉淀产生。
(5)为获得高纯MnCO ,需选择“低温”干燥的原因是__________________ 。
3
【例3】粗盐除去泥沙后还含有少量的MgCl 、CaCl 等可溶性杂质,为了得到较纯净的氯化钠,又作了如
2 2
下处理(假定杂质只有MgCl 、CaCl 两种,反应中所加试剂均过量)。
2 2
(1)白色沉淀含有物质的化学式为________、________;
(2)在得到的滤液中加入过量盐酸的目的是____________ ;
(3)选用蒸发结晶法而不用降温结晶法的理由是___________ 。
【例4】某盐矿的卤水中主要含有KCl,还有少量MgSO 、CaCl 等杂质。从该卤水中提取KCl的生产流程
4 2
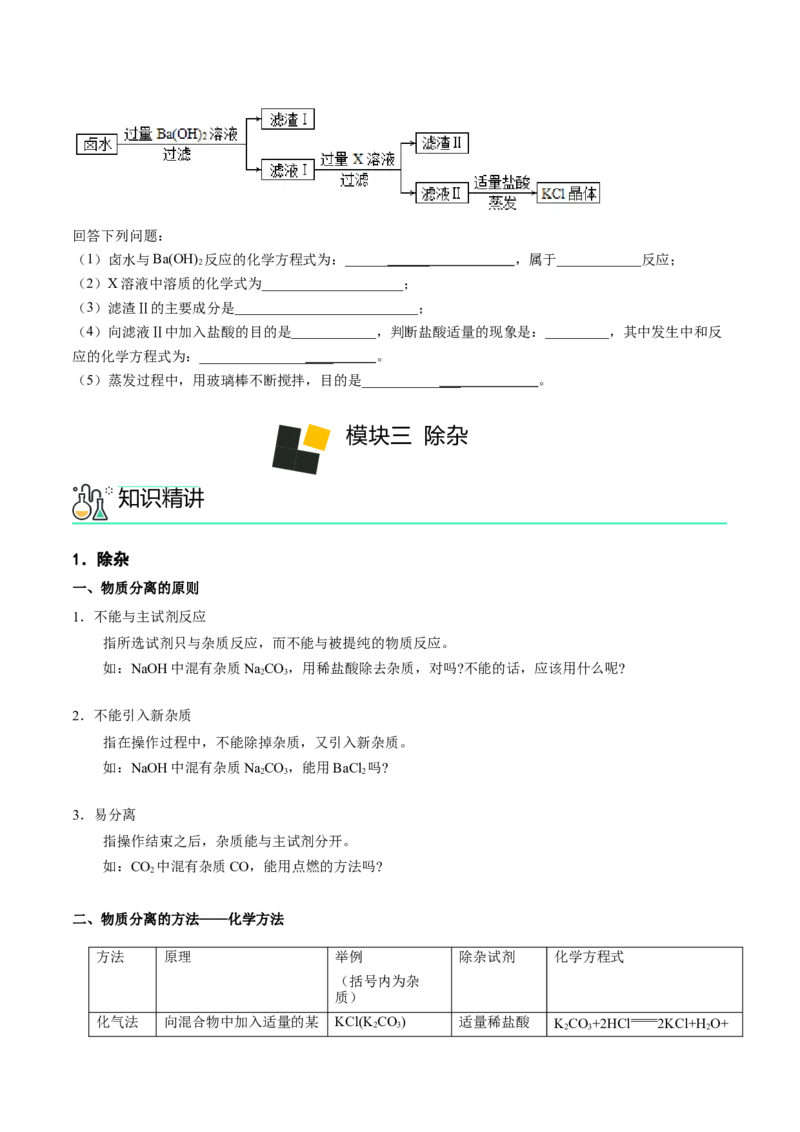
如图所示:回答下列问题:
(1)卤水与Ba(OH) 反应的化学方程式为:____________ ,属于____________反应;
2
(2)X溶液中溶质的化学式为____________________;
(3)滤渣Ⅱ的主要成分是__________________________;
(4)向滤液Ⅱ中加入盐酸的目的是____________,判断盐酸适量的现象是:_________,其中发生中和反
应的化学方程式为:___________________ 。
(5)蒸发过程中,用玻璃棒不断搅拌,目的是______________ 。
模块三 除杂
知识精讲
1.除杂
一、物质分离的原则
1.不能与主试剂反应
指所选试剂只与杂质反应,而不能与被提纯的物质反应。
如:NaOH中混有杂质NaCO,用稀盐酸除去杂质,对吗?不能的话,应该用什么呢?
2 3
2.不能引入新杂质
指在操作过程中,不能除掉杂质,又引入新杂质。
如:NaOH中混有杂质NaCO,能用BaCl 吗?
2 3 2
3.易分离
指操作结束之后,杂质能与主试剂分开。
如:CO 中混有杂质CO,能用点燃的方法吗?
2
二、物质分离的方法——化学方法
方法 原理 举例 除杂试剂 化学方程式
(括号内为杂
质)
化气法 向混合物中加入适量的某 KCl(K 2 CO 3 ) 适量稀盐酸 K 2 CO 3 +2HCl 2KCl+H 2 O+种试剂,使其中的杂质转 CO↑↑
2
变为气体逸出而除去
CO(CO) 灼热的CuO CuO+CO=Cu+CO ↑
2 2
化水法 向混合物中加入适量的某 NaCl(NaOH) 适量稀盐酸 NaOH+HCl NaCl+H O
2
种试剂,使其中的杂质转
变为水而除去
沉淀法 向混合物的溶液中加入适 NaNO 3 (NaCl) 适量硝酸银 NaCl+AgNO 3 AgCl↓+Na
量的某种试剂,使杂质与 溶液 NO
3
该试剂反应转化为沉淀,
再过滤除掉沉淀
加热(高 加热(高温)混合物使杂质 CaO(CaCO) 高温
3 CaCO CaO+CO ↑
温)法 分解(或变成气体)而除去 3 2
溶解法 向混合物中加入某种试 Cu(CuO) 稀硫酸 CuO+HSO CuSO +H O
2 4 4 2
剂,使杂质与试剂反应而
被溶解掉,以除去杂质
置换法 向混合物中加入一种试 FeSO 4 (CuSO 4 ) 适量铁粉 CuSO 4 +Fe FeSO 4 +Cu。
剂,利用该试剂与杂质发
生置换反应,而将杂质除
去
吸收法 将气体混合物通过洗气装 水蒸气 浓硫酸
置,杂质气体被装置内所
盛试剂吸收而除去
酸性气体(CO、 碱溶液
2
SO 、HCl等) (NaOH溶液)
2
碱性气体(NH 等) 酸溶液
3
(H SO 溶液)
2 4
经典例题
除杂
【例1】(2020·广东中考)下列除杂方法正确的是( )
选项 物质(括号内为杂质) 方法
A KCO 溶液(KSO ) 加BaCl 溶液,过滤
2 3 2 4 2
B N(O) 将气体通过灼热的铜网
2 2
C NaOH溶液(NaCO) 加入稀硫酸
2 3
D ZnSO 溶液(CuSO ) 加入过量的铁粉,过滤
4 4
【例2】除去下列各组物质中的杂质,所选用的试剂(足量)及操作方法均正确的是( )
选项 物质(括号内为杂质) 选用试剂 操作方法A Fe O (Fe) 稀硫酸 溶解、过滤、洗涤、干燥
2 3
B CaCl 溶液(盐酸) CaCO 过滤
2 3
C CaO(CaCO) 水 过滤、干燥
3
D KCl(KCO) Ca(NO ) 溶液 溶解、过滤、蒸发、结晶
2 3 3 2
【例3】除去下列物质中的杂质(括号中物质为杂质),所用试剂和操作方法都正确的是( )
A.CaCl 溶液(HCl):过量CaCO 过滤 B.Cu(CuO):O 加热
2 3 2
C.KCl(KOH):水 蒸发 D.ZnCl 溶液(CuCl )过量镁粉 过滤
2 2
【例4】为除去下列物质中的杂质(括号内为杂质),下列操作方法能达到目的的是( )
选项 物质(杂质) 操作方法
A CO(CO) 将气体点燃
2
B CaO(CaCO ) 加足量稀盐酸、过滤
3
C NaSO (NaCO) 加盐酸至恰好不再产生气泡为止
2 4 2 3
D FeCl (CuCl ) 加入足量铁屑,充分反应后过滤
2 2
【例5】除去下列各组物质中的杂质(括号内为杂质),所选用的试剂(足量)及操作方法均正确的是
选项 物质 选用试剂 操作方法
A Fe O(Fe) 盐酸 浸泡、过滤、洗涤、烘干
2 3
B CO(CO) NaOH溶液、浓硫酸 洗气、干燥
2
C CaO(CaCO ) 水 过滤、烘干
3
D NaCl(NaCO) Ca(NO ) 溶液 溶解、过滤、蒸发、结晶
2 3 3 2
专项训练
【训1】(2020深圳)下列方法能达到除杂目的的是( )
选项 物质(括号内为杂质) 方法
A CH(CO) 点燃混合气体
4
B 铜粉(碳粉) 在空气中灼烧固体混合物
C O(水蒸气) 将混合气体通过浓硫酸
2D NaCl(CaCl ) 加水溶解,过滤
2
【训2】有关“粗盐中难溶性杂质的去除”实验中说法不正确的是( )
A. 多加水,让粗盐加速溶解
B. 玻璃棒用了4 次,但作用各不相同
C. 粗盐经过溶解、过滤、蒸发、结晶可以得到初步提纯
D. 当蒸发皿中出现较多量固体时,停止加热,利用余热使滤液蒸干
【训3】某粗盐固体样品中含有少量CaCl 、MgCl 、NaSO 、MgSO 和泥沙,进行以下操作可得到纯净的
2 2 2 4 4
NaCl晶体:
①加过量的NaOH溶液;②加HO溶解;③加过量的BaCl 溶液;④过滤;⑤蒸发;⑥加过量的NaCO 溶
2 2 2 3
液;⑦加适量的稀盐酸,则正确的操作顺序是( )
A.②①⑥③④⑦⑤ B.②①③⑥⑦④⑤
C.①⑥②③④⑤⑦ D.②③①⑥④⑦⑤
【训4】(2020·广东中考)实验室对含有MgCl 的粗盐进行提纯,步骤如图”:
2
(1)步骤①中,称量50g粗盐需补充的主要仪器是___________。
(2)步骤②中,玻璃棒的作用是________。
(3)步骤③中,滴加过量NaOH溶液除去MgCl ,反应的化学方程式是__________ 。
2
(4)步骤⑤中,为中和过量的NaOH,应滴加的“试剂a”是______(填字母)。
A.稀盐酸 B.稀硫酸 C.稀硝酸
(5)步骤⑥的操作名称是_______,当_________ _时,停止加热。
【训5】为了除去NaCl溶液中含有少量的MgCl 、CaCl 和NaSO 等杂质,某小组同学选用NaCO 溶液、
2 2 2 4 2 3
稀盐酸、Ba(OH) 溶液三种试剂,按一定的顺序进行如图所示的实验。
2回答下列问题:
(1)实验Ⅰ中加入试剂A除去的杂质是_________ 。
(2)实验Ⅱ中加入的试剂B是_________溶液;加入过量B的目的是__________ 。
(3)滤液②中除Na+和Cl-外,还含有的离子是__________(填离子符号)。
(4)实验Ⅲ中发生的中和反应的化学方程式__________ 。
(5)由所得NaCl溶液制成氯化钠晶体,所需操作为_________。
【训6】某矿物质中的主要成分是MgO,其中还含有少量Fe O、CuO和SiO 等杂质。用该矿物质制备Mg
2 3 2
(OH) 的工艺流程简图如下:
2
回答下列问题:
(1)步骤①、②、③要得到Mg(OH) 均用到的操作是____________。
2
(2)溶液A中所含的阳离子有Fe3+、Cu2+、Mg2+和____________(填离子符号)。
(3)已知部分金属阳离子以氢氧化物形成沉淀时溶液的pH见下表:
对应离子 Fe3+ Cu2+ Mg2+
开始沉淀时的pH 1.9 4.2 9.1
完全沉淀时的pH 3.2 6.7 11.1
步骤②加入熟石灰,调节溶液的pH范围为_______________,固体C中所含成分的化学式为__________。
(4)步骤③制得Mg(OH) 的化学方程式为________________ 。当分离出Mg(OH) 后,滤
2 2
液中所含的离子有__________(填离子符号)。
【训7】氧化镁在医药、建筑等行业应用广泛。以菱镁矿(主要成分为MgCO ,含少量FeCO 和不溶性杂
3 3
质)为原料制备高纯氧化镁的实验流程图如下:
(1)FeCO 的名称是________;MgSO 固体与木炭反应的化学方程式为_____________。
3 4(2)在实验室里完成操作I,需要用到的玻璃仪器除漏斗、玻璃棒外,还有________;滤液I里,主要的
金属阳离子是_________(填离子符号)。
(3)通过加入氨水使溶液的pH______________(填“增大”或“减小”或“不变”),将杂质离子沉淀
除去。
(4)若直接煅烧100t含碳酸镁84%的菱镁矿,理论上可制得氧化镁的质量为______t。
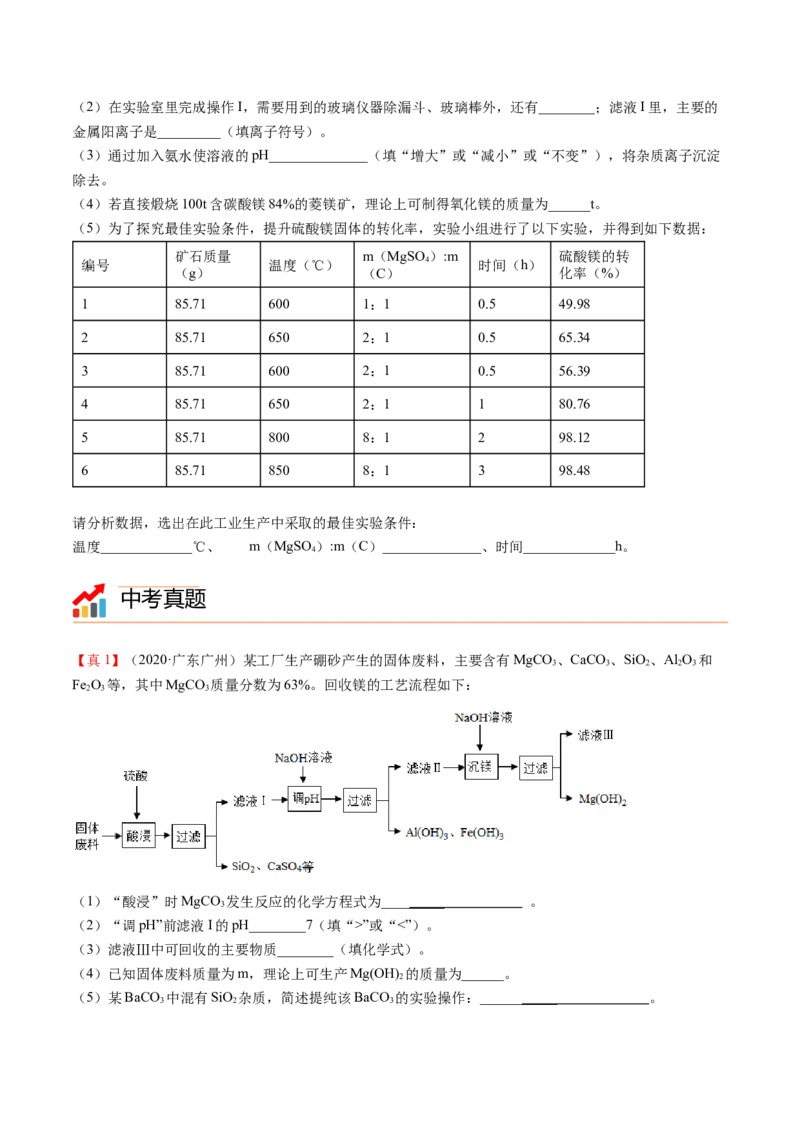
(5)为了探究最佳实验条件,提升硫酸镁固体的转化率,实验小组进行了以下实验,并得到如下数据:
矿石质量 m(MgSO ):m 硫酸镁的转
编号 温度(℃) 4 时间(h)
(g) (C) 化率(%)
1 85.71 600 1:1 0.5 49.98
2 85.71 650 2:1 0.5 65.34
3 85.71 600 2:1 0.5 56.39
4 85.71 650 2:1 1 80.76
5 85.71 800 8:1 2 98.12
6 85.71 850 8:1 3 98.48
请分析数据,选出在此工业生产中采取的最佳实验条件:
温度_____________℃、 m(MgSO ):m(C)______________、时间_____________h。
4
中考真题
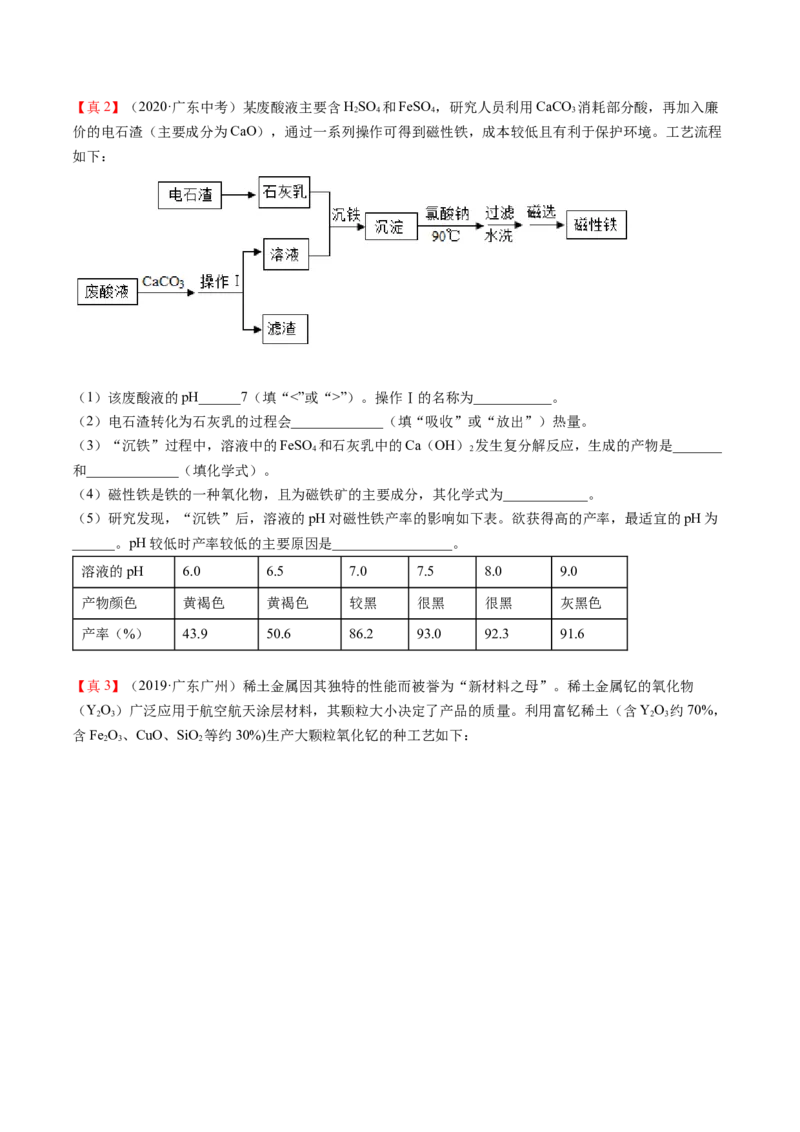
【真1】(2020·广东广州)某工厂生产硼砂产生的固体废料,主要含有MgCO 、CaCO 、SiO、Al O 和
3 3 2 2 3
Fe O 等,其中MgCO 质量分数为63%。回收镁的工艺流程如下:
2 3 3
(1)“酸浸”时MgCO 发生反应的化学方程式为_________ 。
3
(2)“调pH”前滤液I的pH________7(填“>”或“<”)。
(3)滤液Ⅲ中可回收的主要物质________(填化学式)。
(4)已知固体废料质量为m,理论上可生产Mg(OH) 的质量为______。
2
(5)某BaCO 中混有SiO 杂质,简述提纯该BaCO 的实验操作:___________ 。
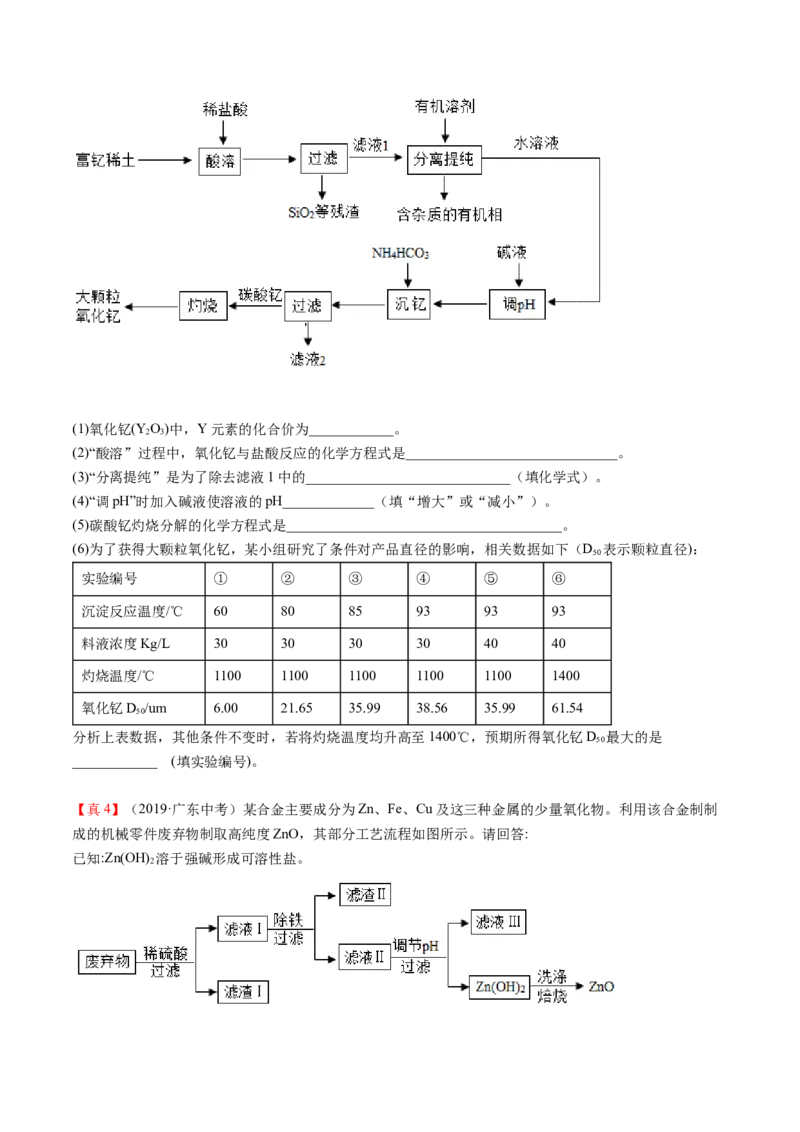
3 2 3【真2】(2020·广东中考)某废酸液主要含HSO 和FeSO ,研究人员利用CaCO 消耗部分酸,再加入廉
2 4 4 3
价的电石渣(主要成分为CaO),通过一系列操作可得到磁性铁,成本较低且有利于保护环境。工艺流程
如下:
(1)该废酸液的pH______7(填“<”或“>”)。操作Ⅰ的名称为___________。
(2)电石渣转化为石灰乳的过程会_____________(填“吸收”或“放出”)热量。
(3)“沉铁”过程中,溶液中的FeSO 和石灰乳中的Ca(OH) 发生复分解反应,生成的产物是_______
4 2
和_____________(填化学式)。
(4)磁性铁是铁的一种氧化物,且为磁铁矿的主要成分,其化学式为____________。
(5)研究发现,“沉铁”后,溶液的pH对磁性铁产率的影响如下表。欲获得高的产率,最适宜的pH为
______。pH较低时产率较低的主要原因是_________________。
溶液的pH 6.0 6.5 7.0 7.5 8.0 9.0
产物颜色 黄褐色 黄褐色 较黑 很黑 很黑 灰黑色
产率(%) 43.9 50.6 86.2 93.0 92.3 91.6
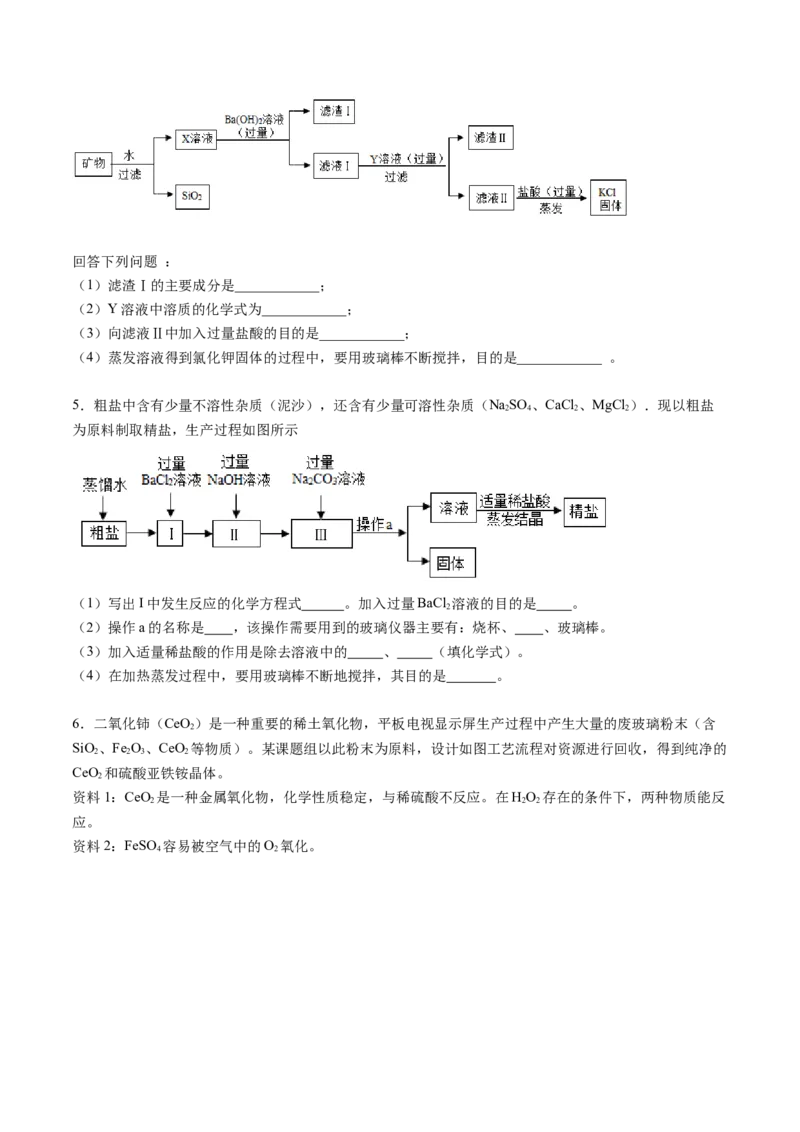
【真3】(2019·广东广州)稀土金属因其独特的性能而被誉为“新材料之母”。稀土金属钇的氧化物
(YO)广泛应用于航空航天涂层材料,其颗粒大小决定了产品的质量。利用富钇稀土(含YO 约70%,
2 3 2 3
含Fe O、CuO、SiO 等约30%)生产大颗粒氧化钇的种工艺如下:
2 3 2(1)氧化钇(Y O)中,Y元素的化合价为____________。
2 3
(2)“酸溶”过程中,氧化钇与盐酸反应的化学方程式是______________________________。
(3)“分离提纯”是为了除去滤液1中的_____________________________(填化学式)。
(4)“调pH”时加入碱液使溶液的pH_____________(填“增大”或“减小”)。
(5)碳酸钇灼烧分解的化学方程式是_______________________________________。
(6)为了获得大颗粒氧化钇,某小组研究了条件对产品直径的影响,相关数据如下(D 表示颗粒直径):
50
实验编号 ① ② ③ ④ ⑤ ⑥
沉淀反应温度/℃ 60 80 85 93 93 93
料液浓度Kg/L 30 30 30 30 40 40
灼烧温度/℃ 1100 1100 1100 1100 1100 1400
氧化钇D /um 6.00 21.65 35.99 38.56 35.99 61.54
50
分析上表数据,其他条件不变时,若将灼烧温度均升高至1400℃,预期所得氧化钇D 最大的是
50
____________ (填实验编号)。
【真4】(2019·广东中考)某合金主要成分为Zn、Fe、Cu及这三种金属的少量氧化物。利用该合金制制
成的机械零件废弃物制取高纯度ZnO,其部分工艺流程如图所示。请回答:
已知:Zn(OH) 溶于强碱形成可溶性盐。
2(1)滤渣I中一定有__________。
(2)加酸溶解废弃物时,需要通风并远离火源,其原因是__________ 。此过程中Zn还能
起到除铜作用,除铜的化学方程式为__________ ,此反应属于__________ (填基本反应类型)。
(3)调节pH可用NaOH,但不能过量,其原因是__________ 。
(4)焙烧Zn(OH) 发生分解反应的化学方程式为__________ 。
2
提分作业
1.除去下列物质中的杂质(括号内为杂质),除杂试剂及方法正确的是( )
选项 物质(括号内为杂质) 除杂试剂及方法
A 氯化钾固体(二氧化锰) 加入足量的水,溶解、过滤、洗涤、干燥
B NH (水蒸气) 通过浓硫酸
3
C 氢氧化钠溶液(碳酸钠溶液) 加入适量的氢氧化钙溶液,过滤
D 氧化铜(木炭粉) 加入稀硫酸,过滤
2.除去下列物质中的杂质,所选方法正确的是( )
A. 除去CO 气体中混有少量的CO,让气体通过氢氧化钠溶液
2
B. 除去FeCl 溶液中混有少量的CuCl ,加入过量的铁粉、过滤
2 2
C. 除去NaCl溶液中混有少量的NaCO,加入适量稀硫酸、蒸发结晶
2 3
D. 除去BaCl 固体中混有少量的KCl,加水溶解、过滤
2
3.下列各组物质除杂(括号内的物质为杂质)方法错误的是( )
选项 物质 方法
A CaO(CaCO ) 高温煅烧
3
B NaSO 溶液(NaCO) 加入适量的稀盐酸
2 4 2 3
C CO(CO) 通过灼热的氧化铜
2
D 氯化钙溶液(盐酸) 加入过量的碳酸钙后过滤
4.从盐湖中提取的某种矿物主要含有氯化钾,还有少量硫酸镁、氯化钙及不溶性杂质SiO,从该矿物中
2
提取氯化钾的流程如下图。回答下列问题 :
(1)滤渣Ⅰ的主要成分是____________;
(2)Y溶液中溶质的化学式为____________;
(3)向滤液Ⅱ中加入过量盐酸的目的是____________;
(4)蒸发溶液得到氯化钾固体的过程中,要用玻璃棒不断搅拌,目的是____________ 。
5.粗盐中含有少量不溶性杂质(泥沙),还含有少量可溶性杂质(NaSO 、CaCl 、MgCl ).现以粗盐
2 4 2 2
为原料制取精盐,生产过程如图所示
(1)写出I中发生反应的化学方程式 。加入过量BaCl 溶液的目的是 。
2
(2)操作a的名称是 ,该操作需要用到的玻璃仪器主要有:烧杯、 、玻璃棒。
(3)加入适量稀盐酸的作用是除去溶液中的 、 (填化学式)。
(4)在加热蒸发过程中,要用玻璃棒不断地搅拌,其目的是 。
6.二氧化铈(CeO)是一种重要的稀土氧化物,平板电视显示屏生产过程中产生大量的废玻璃粉末(含
2
SiO、Fe O、CeO 等物质)。某课题组以此粉末为原料,设计如图工艺流程对资源进行回收,得到纯净的
2 2 3 2
CeO 和硫酸亚铁铵晶体。
2
资料1:CeO 是一种金属氧化物,化学性质稳定,与稀硫酸不反应。在HO 存在的条件下,两种物质能反
2 2 2
应。
资料2:FeSO 容易被空气中的O 氧化。
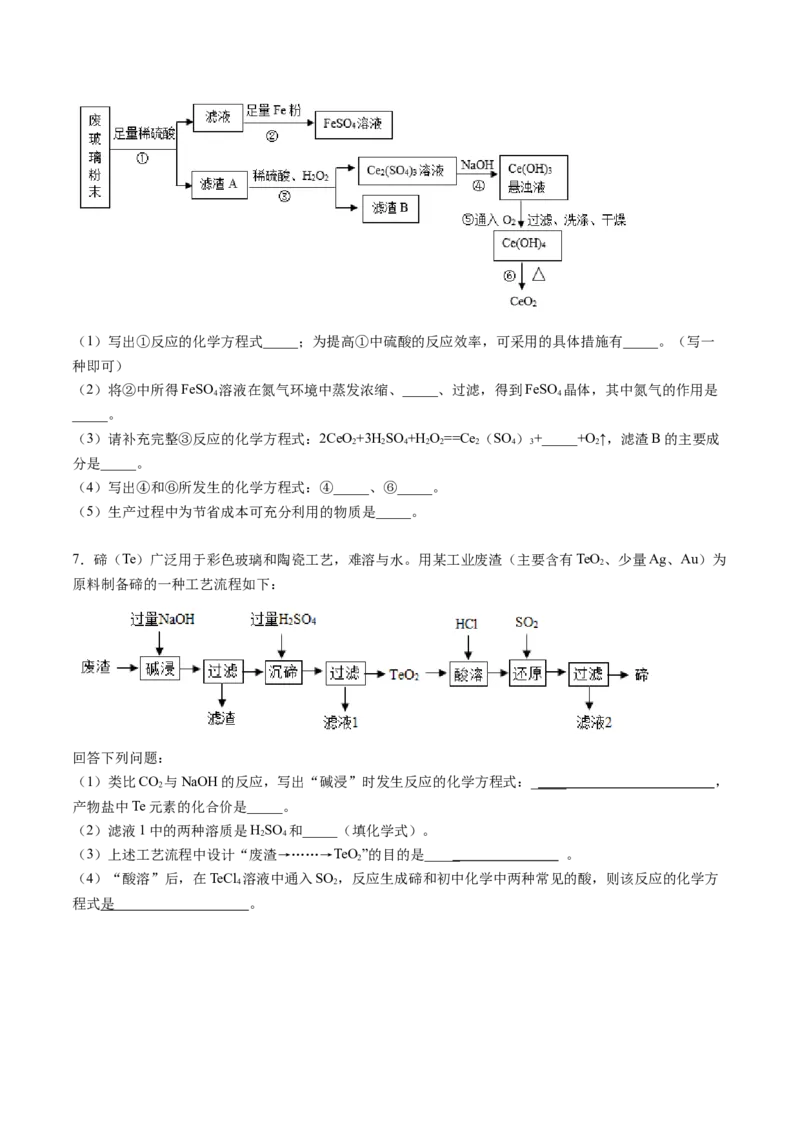
4 2(1)写出①反应的化学方程式_____;为提高①中硫酸的反应效率,可采用的具体措施有_____。(写一
种即可)
(2)将②中所得FeSO 溶液在氮气环境中蒸发浓缩、_____、过滤,得到FeSO 晶体,其中氮气的作用是
4 4
_____。
(3)请补充完整③反应的化学方程式:2CeO+3H SO +H O==Ce (SO )+_____+O ↑,滤渣B的主要成
2 2 4 2 2 2 4 3 2
分是_____。
(4)写出④和⑥所发生的化学方程式:④_____、⑥_____。
(5)生产过程中为节省成本可充分利用的物质是_____。
7.碲(Te)广泛用于彩色玻璃和陶瓷工艺,难溶与水。用某工业废渣(主要含有TeO 、少量Ag、Au)为
2
原料制备碲的一种工艺流程如下:
回答下列问题:
(1)类比CO 与NaOH的反应,写出“碱浸”时发生反应的化学方程式:_____ ,
2
产物盐中Te元素的化合价是_____。
(2)滤液1中的两种溶质是HSO 和_____(填化学式)。
2 4
(3)上述工艺流程中设计“废渣→……→TeO ”的目的是_____ 。
2
(4)“酸溶”后,在TeCl 溶液中通入SO ,反应生成碲和初中化学中两种常见的酸,则该反应的化学方
4 2
程式 是 _____ 。