文档内容
第 18 讲 化学反应速率
1.调控化学反应进行的快慢,对于工业生产和日常生活都有着十分重要的意义。在下列事实中,减慢
化学反应速率的是( )
①古代冶铁使用鼓风机 ②用冰箱冷藏食物
③SO 转化为SO 使用钒触媒 ④食品包装袋中放小袋铁粉
2 3
A.①② B.③④
C.①③ D.②④
2.中国首条“生态马路”在上海复兴路隧道建成,它运用了“光触媒”技术,在路面涂上一种光催化
剂涂料,可将汽车尾气中45%的NO和CO转化成N 和CO。下列对此反应的叙述中正确的是( )
2 2
A.使用光催化剂不改变反应速率
B.使用光催化剂能提高NO的转化率
C.升高温度能加快反应速率
D.改变压强对反应速率无影响
3.把0.6 mol 气体X和0.4 mol气体Y混合于2.0 L的密闭容器中,发生如下反应:3X(g)+Y(g)nZ(g)
+2W(g),测得5 min末生成0.2 mol W,又知以Z表示的平均反应速率为0.01 mol·L-1·min-1,则n值是(
)
A.1 B.2
C.3 D.4
4.已知反应4CO+2NO N+4CO 在不同条件下的化学反应速率如下,其中表示反应速率最快的是(
2 2 2
)
A.v(CO)=1.5 mol·L-1·min-1B.v(NO )=0.7 mol·L-1·min-1
2
C.v(N )=0.4 mol·L-1·min-1
2
D.v(CO)=1.1 mol·L-1·min-1
2
5.对反应A+BAB来说,常温下按以下情况进行反应:
①20 mL溶液中含A、B各0.01 mol ②50 mL溶液中含A、B各0.05 mol ③0.1 mol·L-1的A、B溶
液各10 mL
④0.5 mol·L-1的A、B溶液各50 mL
四者反应速率的大小关系是( )
A.②>①>④>③ B.④>③>②>①
C.①>②>④>③ D.①>②>③>④
6.一定温度下,反应N(g)+O(g)2NO(g)在密闭容器中进行,下列措施不会改变化学反应速率的是(
2 2
)
A.缩小容积使压强增大 B.恒容,充入N
2
C.恒容,充入He D.恒压,充入He
7.一定温度下,在某密闭容器中发生反应:2HI(g)H (g)+I(s) ΔH>0,若0~15 s内c(HI)由0.1
2 2
mol·L-1降到0.07 mol·L-1,则下列说法正确的是( )
A.0~15 s内用I 表示的平均反应速率为v(I)=0.001 mol·L-1·s-1
2 2
B.c(HI)由0.07 mol·L-1降到0.05 mol·L-1所需的反应时间小于10 s
C.升高温度,正反应速率加快,逆反应速率减慢
D.减小反应体系的体积,化学反应速率加快
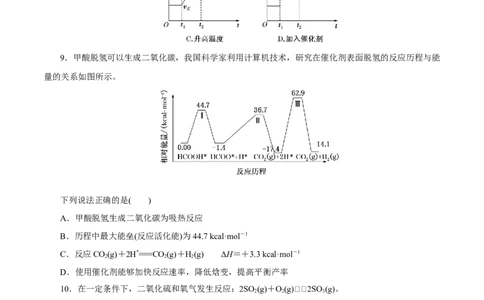
8.对于反应2SO (g)+O(g)2SO (g) ΔH<0已达到平衡,如果其他条件不变时,分别改变下列条件,
2 2 3
对化学反应速率和化学平衡产生影响,下列条件与图像不相符的是(O~t:v =v ;t 时改变条件,t 时重
1 正 逆 1 2
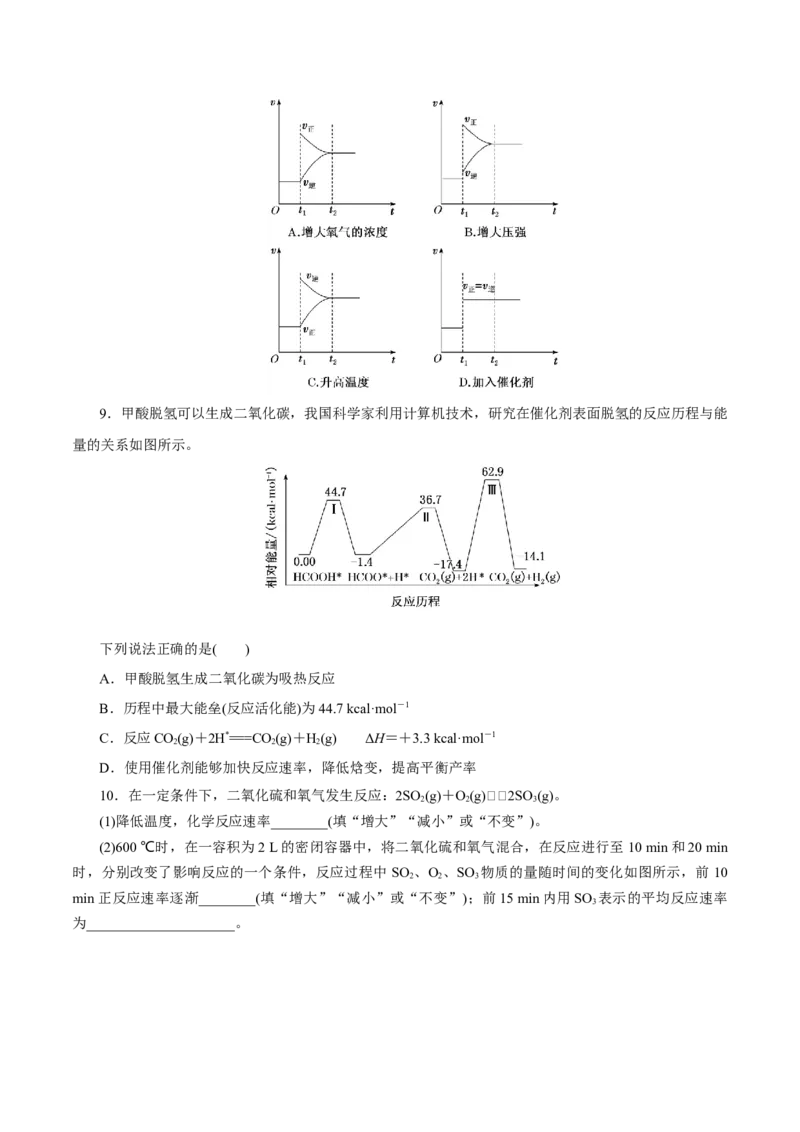
新建立平衡)( )9.甲酸脱氢可以生成二氧化碳,我国科学家利用计算机技术,研究在催化剂表面脱氢的反应历程与能
量的关系如图所示。
下列说法正确的是( )
A.甲酸脱氢生成二氧化碳为吸热反应
B.历程中最大能垒(反应活化能)为44.7 kcal·mol-1
C.反应CO(g)+2H*===CO (g)+H(g) ΔH=+3.3 kcal·mol-1
2 2 2
D.使用催化剂能够加快反应速率,降低焓变,提高平衡产率
10.在一定条件下,二氧化硫和氧气发生反应:2SO (g)+O(g)2SO (g)。
2 2 3
(1)降低温度,化学反应速率________(填“增大”“减小”或“不变”)。
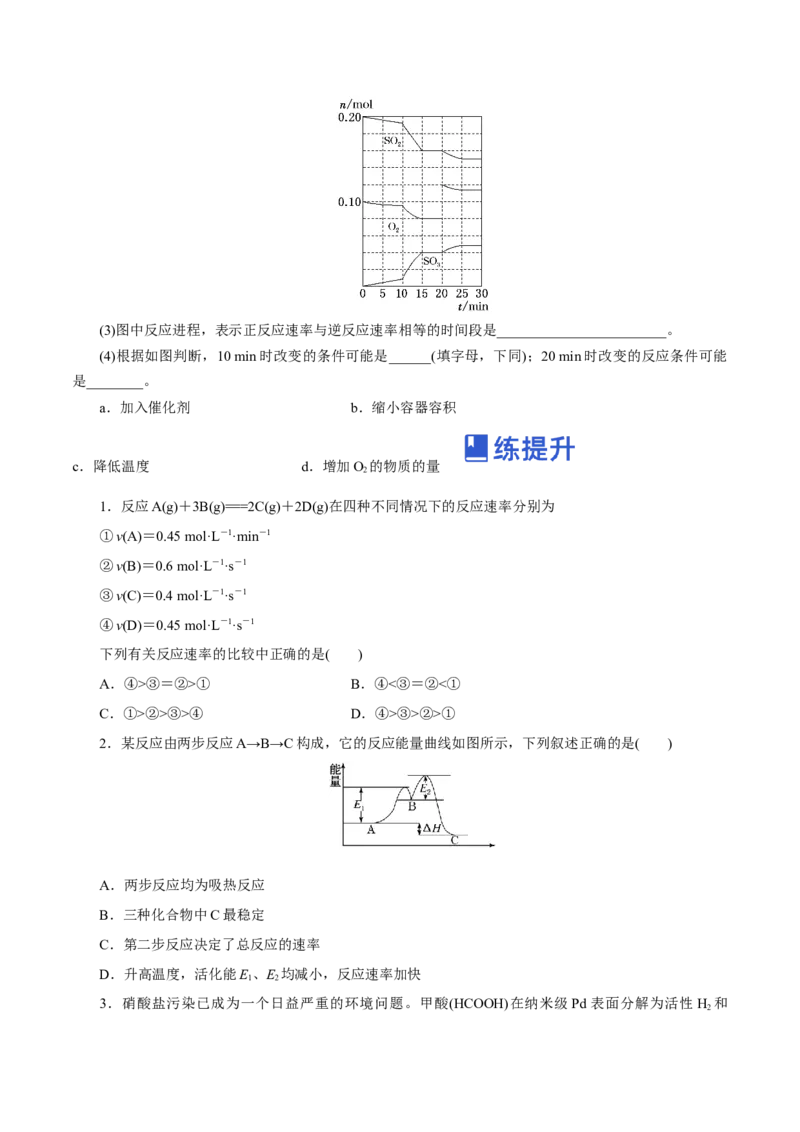
(2)600 ℃时,在一容积为2 L的密闭容器中,将二氧化硫和氧气混合,在反应进行至 10 min和20 min
时,分别改变了影响反应的一个条件,反应过程中 SO 、O 、SO 物质的量随时间的变化如图所示,前 10
2 2 3
min正反应速率逐渐________(填“增大”“减小”或“不变”);前15 min内用SO 表示的平均反应速率
3
为_____________________。(3)图中反应进程,表示正反应速率与逆反应速率相等的时间段是________________________。
(4)根据如图判断,10 min时改变的条件可能是______(填字母,下同);20 min时改变的反应条件可能
是________。
a.加入催化剂 b.缩小容器容积
c.降低温度 d.增加O 的物质的量
2
1.反应A(g)+3B(g)===2C(g)+2D(g)在四种不同情况下的反应速率分别为
①v(A)=0.45 mol·L-1·min-1
②v(B)=0.6 mol·L-1·s-1
③v(C)=0.4 mol·L-1·s-1
④v(D)=0.45 mol·L-1·s-1
下列有关反应速率的比较中正确的是( )
A.④>③=②>① B.④<③=②<①
C.①>②>③>④ D.④>③>②>①
2.某反应由两步反应A→B→C构成,它的反应能量曲线如图所示,下列叙述正确的是( )
A.两步反应均为吸热反应
B.三种化合物中C最稳定
C.第二步反应决定了总反应的速率
D.升高温度,活化能E、E 均减小,反应速率加快
1 2
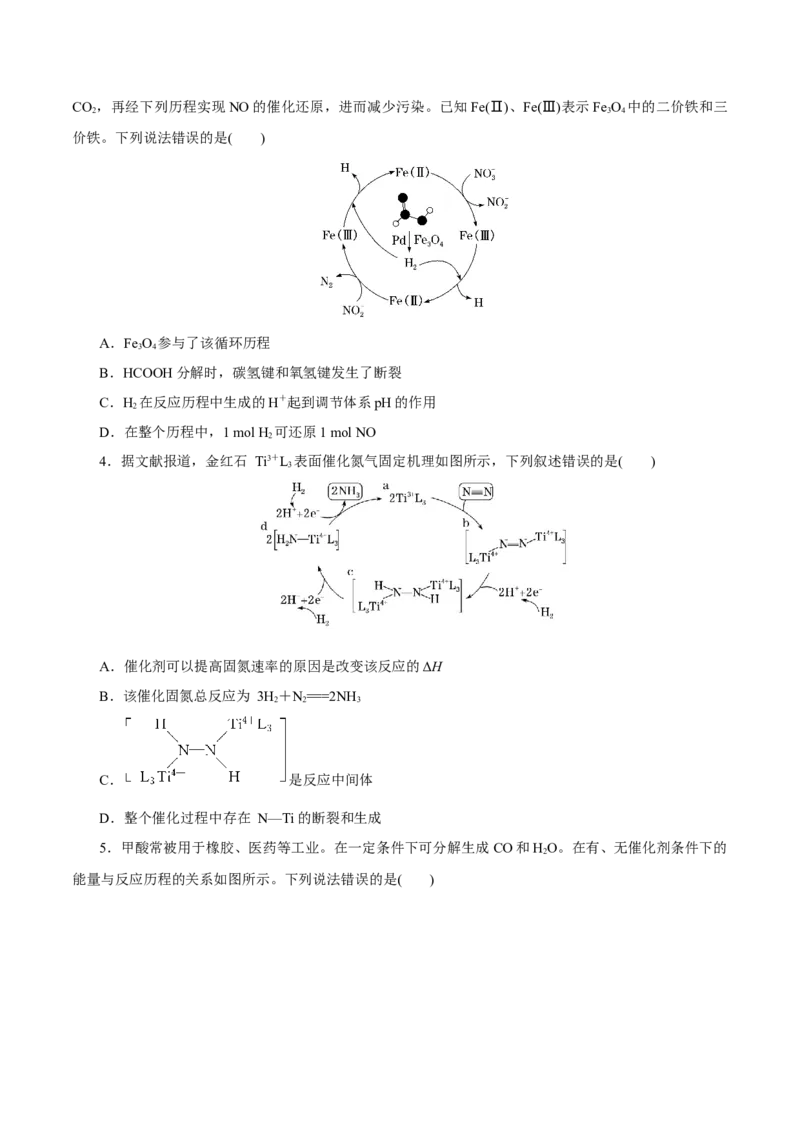
3.硝酸盐污染已成为一个日益严重的环境问题。甲酸(HCOOH)在纳米级Pd表面分解为活性H 和
2CO ,再经下列历程实现NO的催化还原,进而减少污染。已知Fe(Ⅱ)、Fe(Ⅲ)表示Fe O 中的二价铁和三
2 3 4
价铁。下列说法错误的是( )
A.Fe O 参与了该循环历程
3 4
B.HCOOH分解时,碳氢键和氧氢键发生了断裂
C.H 在反应历程中生成的H+起到调节体系pH的作用
2
D.在整个历程中,1 mol H 可还原1 mol NO
2
4.据文献报道,金红石 Ti3+L 表面催化氮气固定机理如图所示,下列叙述错误的是( )
3
A.催化剂可以提高固氮速率的原因是改变该反应的ΔH
B.该催化固氮总反应为 3H+N===2NH
2 2 3
C. 是反应中间体
D.整个催化过程中存在 N—Ti的断裂和生成
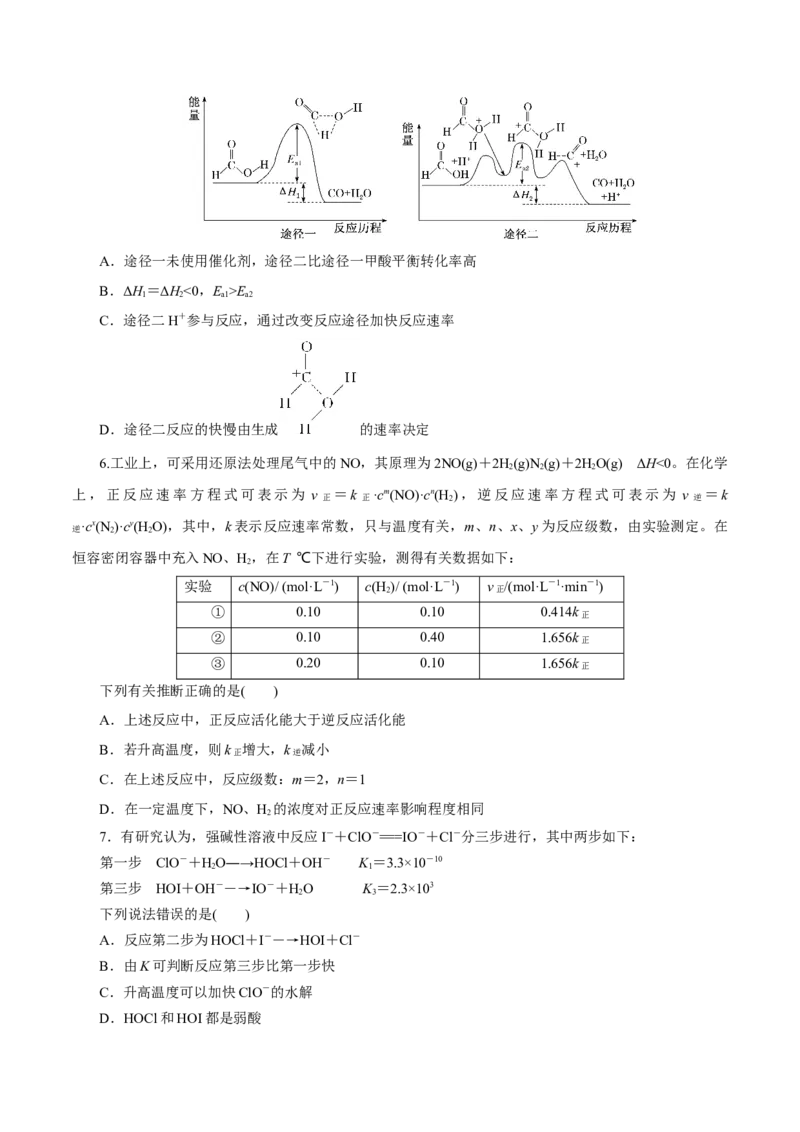
5.甲酸常被用于橡胶、医药等工业。在一定条件下可分解生成 CO和HO。在有、无催化剂条件下的
2
能量与反应历程的关系如图所示。下列说法错误的是( )A.途径一未使用催化剂,途径二比途径一甲酸平衡转化率高
B.ΔH=ΔH<0,E >E
1 2 a1 a2
C.途径二H+参与反应,通过改变反应途径加快反应速率
D.途径二反应的快慢由生成 的速率决定
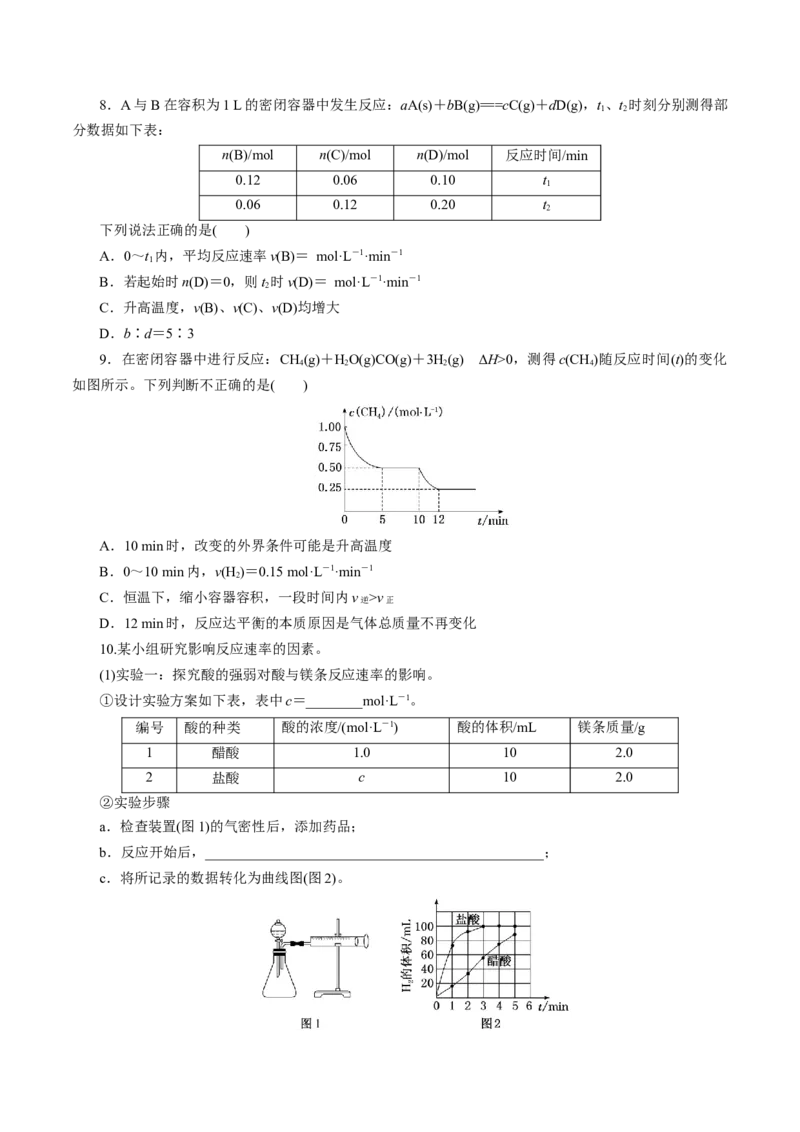
6.工业上,可采用还原法处理尾气中的NO,其原理为2NO(g)+2H(g)N (g)+2HO(g) ΔH<0。在化学
2 2 2
上,正反应速率方程式可表示为 v =k ·cm(NO)·cn(H ),逆反应速率方程式可表示为 v =k
正 正 2 逆
·cx(N )·cy(H O),其中,k表示反应速率常数,只与温度有关,m、n、x、y为反应级数,由实验测定。在
逆 2 2
恒容密闭容器中充入NO、H,在T ℃下进行实验,测得有关数据如下:
2
实验 c(NO)/ (mol·L-1) c(H )/ (mol·L-1) v /(mol·L-1·min-1)
2 正
① 0.10 0.10 0.414k
正
② 0.10 0.40 1.656k
正
③ 0.20 0.10 1.656k
正
下列有关推断正确的是( )
A.上述反应中,正反应活化能大于逆反应活化能
B.若升高温度,则k 增大,k 减小
正 逆
C.在上述反应中,反应级数:m=2,n=1
D.在一定温度下,NO、H 的浓度对正反应速率影响程度相同
2
7.有研究认为,强碱性溶液中反应I-+ClO-===IO-+Cl-分三步进行,其中两步如下:
第一步 ClO-+HO―→HOCl+OH- K =3.3×10-10
2 1
第三步 HOI+OH-―→IO-+HO K =2.3×103
2 3
下列说法错误的是( )
A.反应第二步为HOCl+I-―→HOI+Cl-
B.由K可判断反应第三步比第一步快
C.升高温度可以加快ClO-的水解
D.HOCl和HOI都是弱酸8.A与B在容积为1 L的密闭容器中发生反应:aA(s)+bB(g)===cC(g)+dD(g),t 、t 时刻分别测得部
1 2
分数据如下表:
n(B)/mol n(C)/mol n(D)/mol 反应时间/min
0.12 0.06 0.10 t
1
0.06 0.12 0.20 t
2
下列说法正确的是( )
A.0~t 内,平均反应速率v(B)= mol·L-1·min-1
1
B.若起始时n(D)=0,则t 时v(D)= mol·L-1·min-1
2
C.升高温度,v(B)、v(C)、v(D)均增大
D.b∶d=5∶3
9.在密闭容器中进行反应:CH(g)+HO(g)CO(g)+3H(g) ΔH>0,测得c(CH)随反应时间(t)的变化
4 2 2 4
如图所示。下列判断不正确的是( )
A.10 min时,改变的外界条件可能是升高温度
B.0~10 min内,v(H )=0.15 mol·L-1·min-1
2
C.恒温下,缩小容器容积,一段时间内v >v
逆 正
D.12 min时,反应达平衡的本质原因是气体总质量不再变化
10.某小组研究影响反应速率的因素。
(1)实验一:探究酸的强弱对酸与镁条反应速率的影响。
①设计实验方案如下表,表中c=________mol·L-1。
编号 酸的种类 酸的浓度/(mol·L-1) 酸的体积/mL 镁条质量/g
1 醋酸 1.0 10 2.0
2 盐酸 c 10 2.0
②实验步骤
a.检查装置(图1)的气密性后,添加药品;
b.反应开始后,________________________________________________;
c.将所记录的数据转化为曲线图(图2)。③写出0~5 min醋酸、盐酸与镁条反应的反应速率变化规律:_____________________________。
(2)实验二:探究反应条件对0.10 mol·L-1 Na SO 溶液与稀HSO 反应速率的影响,其设计与测定结果
2 2 3 2 4
如下:
编 反应温 NaSO V(蒸馏 0.10 mol·L-1
2 2 3
号 度/℃ 溶液/mL 水)/mL HSO 溶液/mL
2 4
1 25 10.0 0 10.0
2 25 5.0 a 10.0
3 45 10.0 0 10.0
乙
①写出上述实验原理的离子方程式:__________________________________________。
②上述实验1、3是探究________对化学反应速率的影响;若上述实验1、2是探究浓度对化学反应速
率的影响,则 a 的值为________;乙是实验需要测量的物理量,则表格中“乙”应填写
__________________________________________________________________。
1.(2021·浙江6月选考)一定温度下:在NO 的四氯化碳溶液(100 mL)中发生分解反应:2NO4NO +
2 5 2 5 2
O。在不同时刻测量放出的O 体积,换算成NO 浓度如下表:
2 2 2 5
t/s 0 600 1 200 1 710 2 220 2 820 x
c(N O)/
2 5
1.40 0.96 0.66 0.48 0.35 0.24 0.12
(mol·L-1)
下列说法正确的是( )
A.600~1 200 s,生成NO 的平均速率为5.0×10-4 mol·L-1·s-1
2
B.反应2 220 s时,放出的O 体积为11.8 L(标准状况)
2
C.反应达到平衡时,v (N O)=2v (NO )
正 2 5 逆 2
D.推测上表中的x为3 930
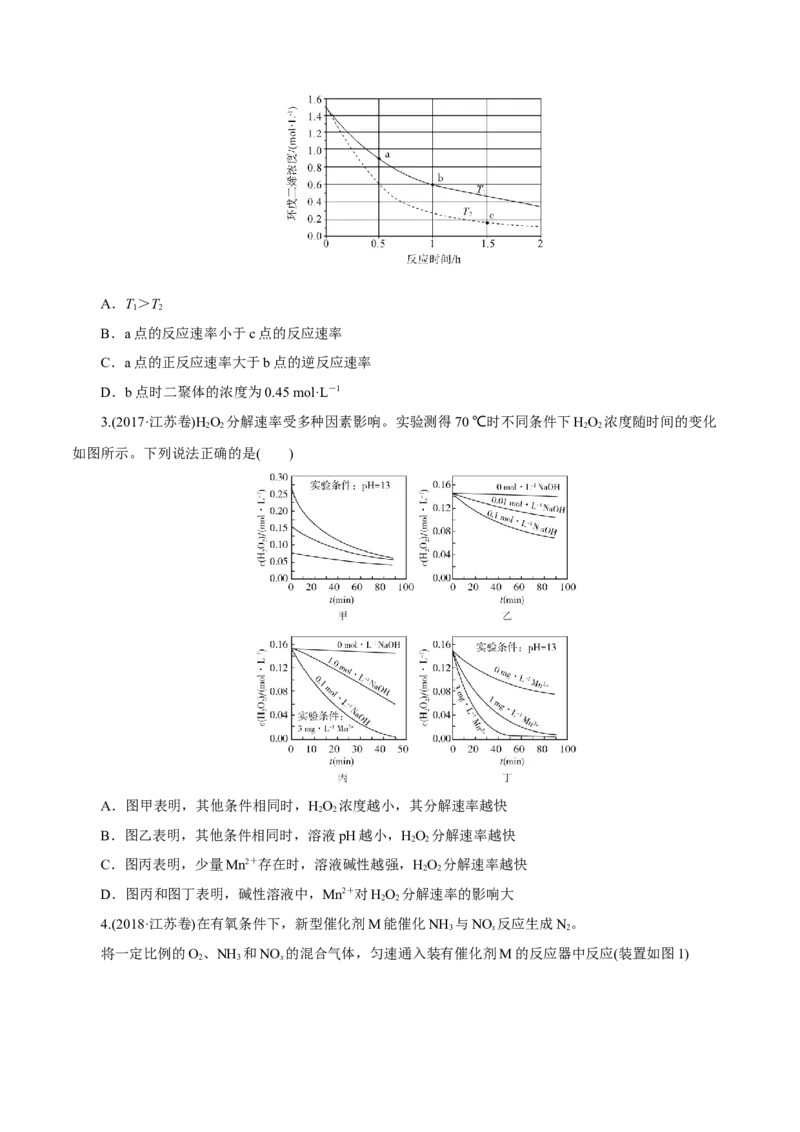
2.[2019·全国卷Ⅱ,27(3)]环戊二烯( )容易发生聚合生成二聚体,该反应为可逆反应。不同温度下,溶
液中环戊二烯浓度与反应时间的关系如图所示,下列说法正确的是________(填标号)。A.T>T
1 2
B.a点的反应速率小于c点的反应速率
C.a点的正反应速率大于b点的逆反应速率
D.b点时二聚体的浓度为0.45 mol·L-1
3.(2017·江苏卷)H O 分解速率受多种因素影响。实验测得70 ℃时不同条件下HO 浓度随时间的变化
2 2 2 2
如图所示。下列说法正确的是( )
A.图甲表明,其他条件相同时,HO 浓度越小,其分解速率越快
2 2
B.图乙表明,其他条件相同时,溶液pH越小,HO 分解速率越快
2 2
C.图丙表明,少量Mn2+存在时,溶液碱性越强,HO 分解速率越快
2 2
D.图丙和图丁表明,碱性溶液中,Mn2+对HO 分解速率的影响大
2 2
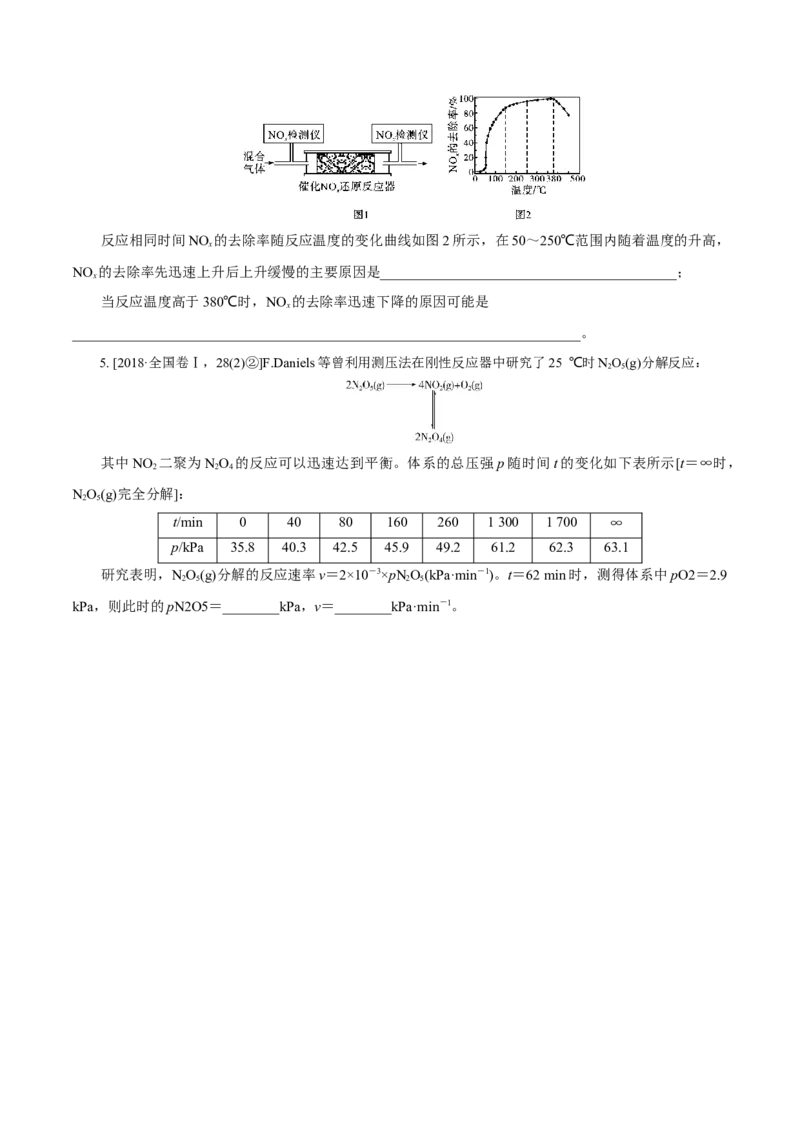
4.(2018·江苏卷)在有氧条件下,新型催化剂M能催化NH 与NO 反应生成N。
3 x 2
将一定比例的O、NH 和NO 的混合气体,匀速通入装有催化剂M的反应器中反应(装置如图1)
2 3 x反应相同时间NO 的去除率随反应温度的变化曲线如图2所示,在50~250℃范围内随着温度的升高,
x
NO 的去除率先迅速上升后上升缓慢的主要原因是__________________________________________;
x
当反应温度高于380℃时,NO 的去除率迅速下降的原因可能是
x
________________________________________________________________________。
5. [2018·全国卷Ⅰ,28(2)②]F.Daniels等曾利用测压法在刚性反应器中研究了25 ℃时NO(g)分解反应:
2 5
其中NO 二聚为NO 的反应可以迅速达到平衡。体系的总压强p随时间t的变化如下表所示[t=∞时,
2 2 4
NO(g)完全分解]:
2 5
t/min 0 40 80 160 260 1 300 1 700 ∞
p/kPa 35.8 40.3 42.5 45.9 49.2 61.2 62.3 63.1
研究表明,NO(g)分解的反应速率v=2×10-3×pNO(kPa·min-1)。t=62 min时,测得体系中pO2=2.9
2 5 2 5
kPa,则此时的pN2O5=________kPa,v=________kPa·min-1。