文档内容
重点题空热练(三) 化工流程题中的曲线分析应用
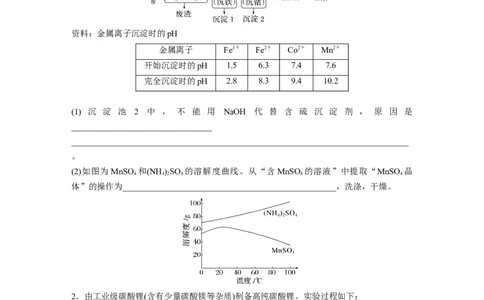
1.MnSO 是一种重要的化工产品。以菱锰矿(主要成分为MnCO ,还含有Fe O 、FeO、
4 3 3 4
CoO等)为原料制备MnSO 的工艺流程如下:
4
资料:金属离子沉淀时的pH
金属离子 Fe3+ Fe2+ Co2+ Mn2+
开始沉淀时的pH 1.5 6.3 7.4 7.6
完全沉淀时的pH 2.8 8.3 9.4 10.2
(1) 沉 淀 池 2 中 , 不 能 用 NaOH 代 替 含 硫 沉 淀 剂 , 原 因 是
_________________________________
_______________________________________________________________________________
。
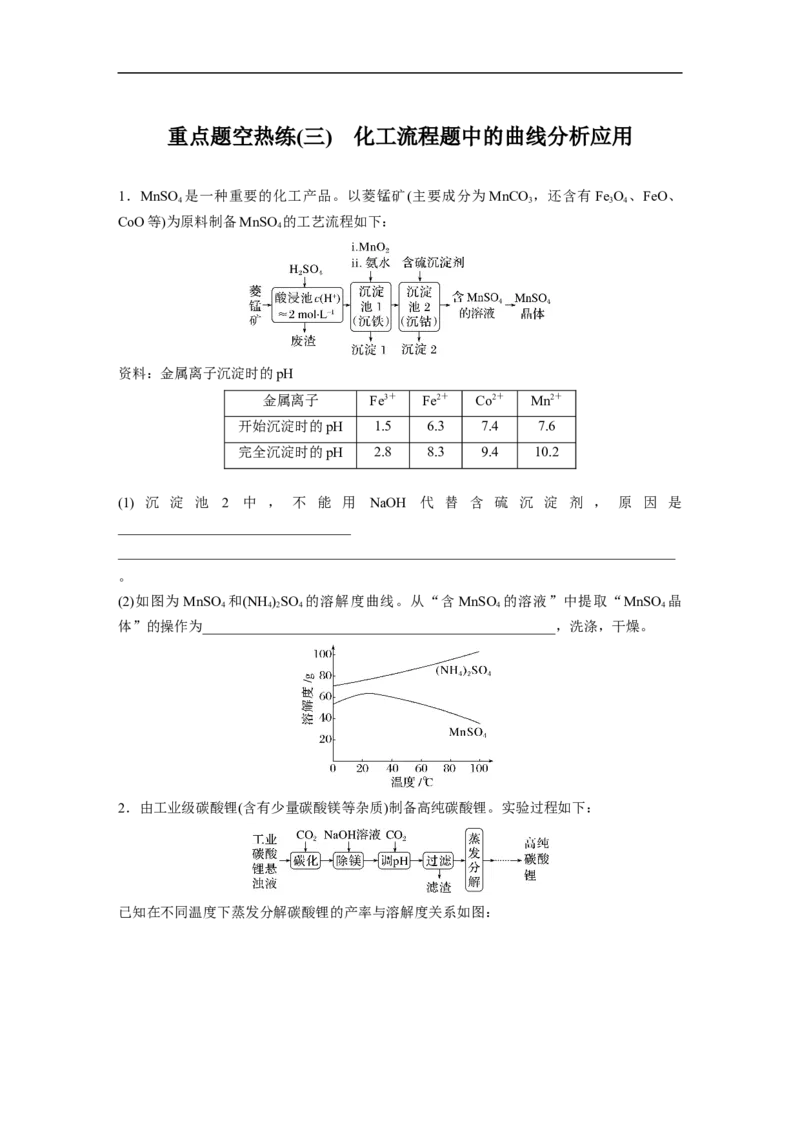
(2)如图为MnSO 和(NH )SO 的溶解度曲线。从“含MnSO 的溶液”中提取“MnSO 晶
4 4 2 4 4 4
体”的操作为__________________________________________________,洗涤,干燥。
2.由工业级碳酸锂(含有少量碳酸镁等杂质)制备高纯碳酸锂。实验过程如下:
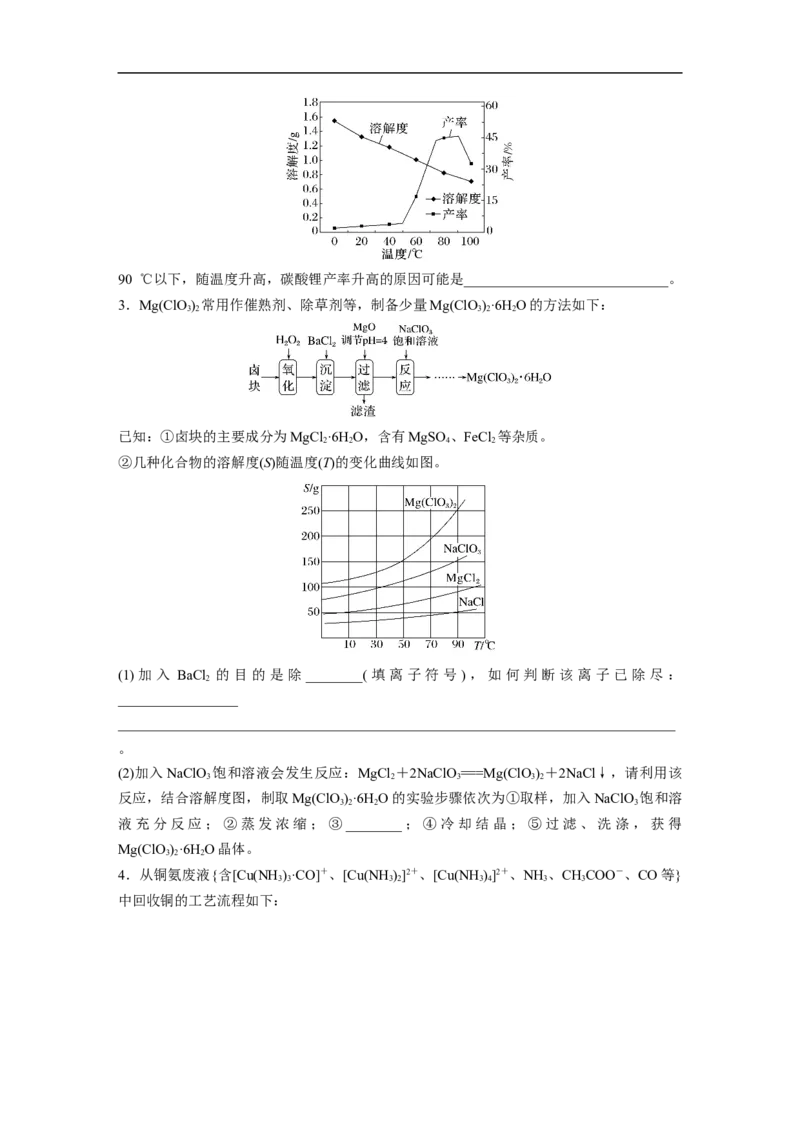
已知在不同温度下蒸发分解碳酸锂的产率与溶解度关系如图:90 ℃以下,随温度升高,碳酸锂产率升高的原因可能是_____________________________。
3.Mg(ClO) 常用作催熟剂、除草剂等,制备少量Mg(ClO)·6H O的方法如下:
3 2 3 2 2
已知:①卤块的主要成分为MgCl ·6H O,含有MgSO 、FeCl 等杂质。
2 2 4 2
②几种化合物的溶解度(S)随温度(T)的变化曲线如图。
(1)加入 BaCl 的目的是除 ________(填离子符号 ),如何判断该离子已除尽:
2
_________________
_______________________________________________________________________________
。
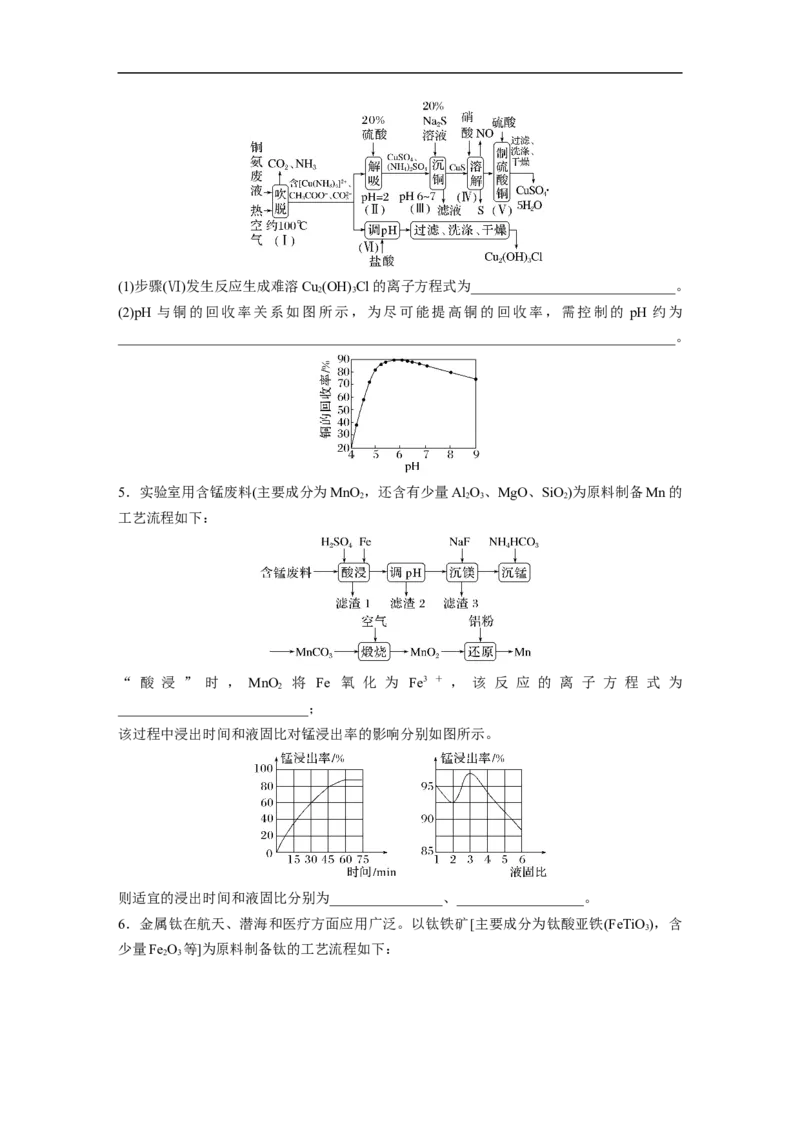
(2)加入NaClO 饱和溶液会发生反应:MgCl +2NaClO===Mg(ClO) +2NaCl↓,请利用该
3 2 3 3 2
反应,结合溶解度图,制取Mg(ClO)·6H O的实验步骤依次为①取样,加入NaClO 饱和溶
3 2 2 3
液充分反应;②蒸发浓缩;③________;④冷却结晶;⑤过滤、洗涤,获得
Mg(ClO)·6H O晶体。
3 2 2
4.从铜氨废液{含[Cu(NH )·CO]+、[Cu(NH )]2+、[Cu(NH )]2+、NH 、CHCOO-、CO等}
3 3 3 2 3 4 3 3
中回收铜的工艺流程如下:(1)步骤(Ⅵ)发生反应生成难溶Cu (OH) Cl的离子方程式为_____________________________。
2 3
(2)pH 与铜的回收率关系如图所示,为尽可能提高铜的回收率,需控制的 pH 约为
_______________________________________________________________________________。
5.实验室用含锰废料(主要成分为MnO ,还含有少量Al O、MgO、SiO)为原料制备Mn的
2 2 3 2
工艺流程如下:
“ 酸 浸 ” 时 , MnO 将 Fe 氧 化 为 Fe3 + , 该 反 应 的 离 子 方 程 式 为
2
___________________________;
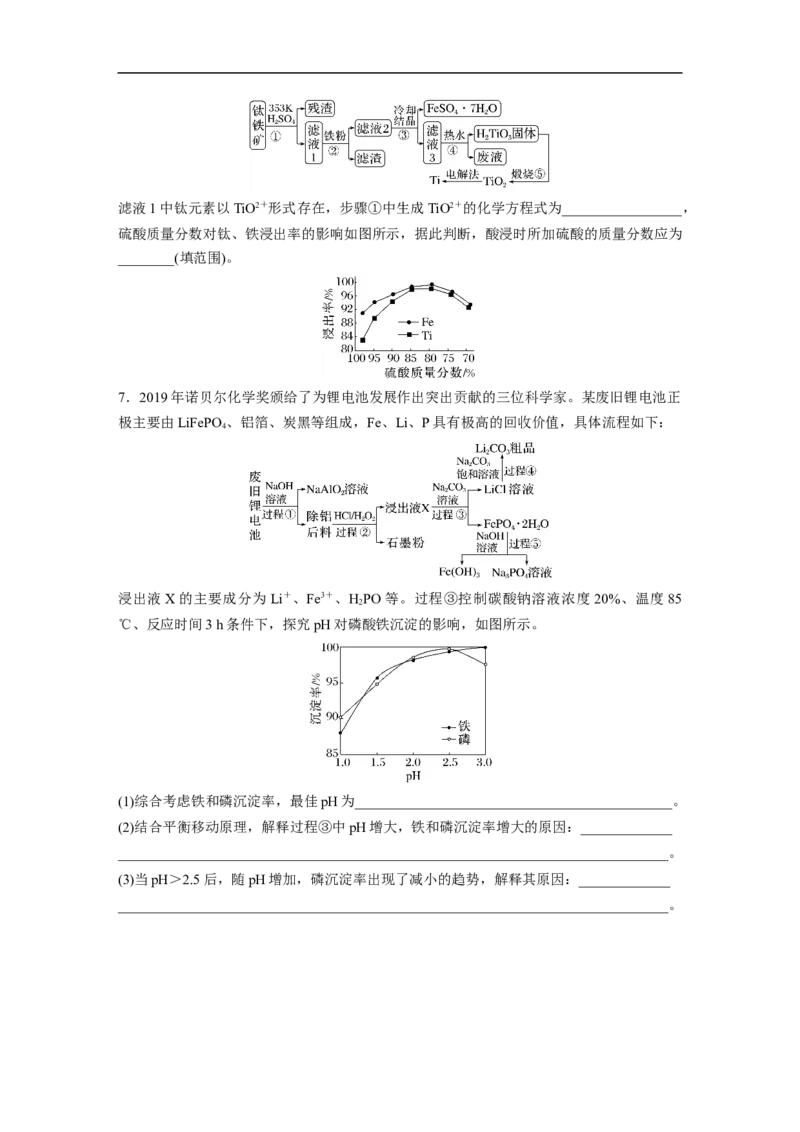
该过程中浸出时间和液固比对锰浸出率的影响分别如图所示。
则适宜的浸出时间和液固比分别为________________、__________________。
6.金属钛在航天、潜海和医疗方面应用广泛。以钛铁矿[主要成分为钛酸亚铁(FeTiO),含
3
少量Fe O 等]为原料制备钛的工艺流程如下:
2 3滤液1中钛元素以TiO2+形式存在,步骤①中生成TiO2+的化学方程式为_________________,
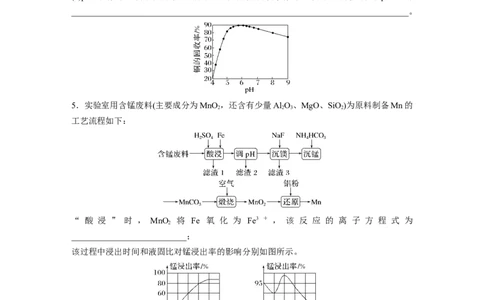
硫酸质量分数对钛、铁浸出率的影响如图所示,据此判断,酸浸时所加硫酸的质量分数应为
________(填范围)。
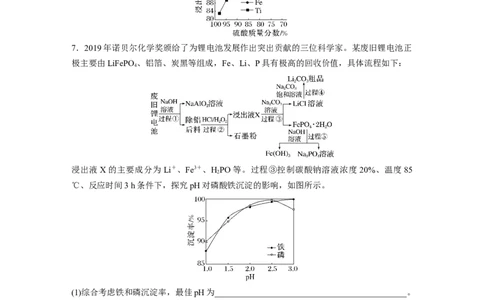
7.2019年诺贝尔化学奖颁给了为锂电池发展作出突出贡献的三位科学家。某废旧锂电池正
极主要由LiFePO 、铝箔、炭黑等组成,Fe、Li、P具有极高的回收价值,具体流程如下:
4
浸出液X的主要成分为Li+、Fe3+、HPO等。过程③控制碳酸钠溶液浓度 20%、温度85
2
℃、反应时间3 h条件下,探究pH对磷酸铁沉淀的影响,如图所示。
(1)综合考虑铁和磷沉淀率,最佳pH为_____________________________________________。
(2)结合平衡移动原理,解释过程③中pH增大,铁和磷沉淀率增大的原因:_____________
______________________________________________________________________________。
(3)当pH>2.5后,随pH增加,磷沉淀率出现了减小的趋势,解释其原因:_____________
______________________________________________________________________________。