文档内容
专题 09 化学反应的热效应
第 24 练 反应热
1.下列对能量变化的认识不正确的是( )
A.电解水时,电能转化为化学能
B.绿色植物进行光合作用时,太阳能转化为化学能
C.煤燃烧时,化学能主要转化为热能
D.白炽灯工作时,电能全部转化为光能
【答案】D
【解析】白炽灯工作时,电能转化为光能和热能, D项错误。
2.下列关于化学反应与能量变化的说法正确的是( )
A.燃烧属于放热反应
B.中和反应是吸热反应
C.断裂化学键放出能量
D.反应物总能量与生成物总能量可能相等
【答案】A
【解析】物质燃烧时向外界释放能量,属于放热反应,A项正确;中和反应都是放热反应,B项错误;
化学键断裂吸收能量,化学键形成放出能量,C项错误;化学反应中的物质变化一定伴随着能量变化,反
应物总能量与生成物总能量一定不相等,D项错误。
3.将铁粉和硫粉充分混合后加热,待反应一发生立即停止加热,反应仍可持续进行,直至反应完全,
生成新物质硫化亚铁。此现象说明( )
A.该反应是吸热反应
B.该反应是放热反应
C.铁粉和硫粉在常温下容易发生反应
D.产物硫化亚铁的总能量高于反应物铁粉和硫粉的总能量
【答案】B
【解析】铁粉和硫粉充分混合后加热,反应一开始立即停止加热,反应仍可持续进行,说明该反应是
放热反应,即产物的总能量低于反应物的总能量。4.下列说法中正确的是(中和反应反应热简称中和热)( )
A.中和热一定是强酸跟强碱反应放出的热量
B.1 mol酸与1 mol碱完全反应放出的热量是中和热
C.在稀溶液中,酸与碱发生中和反应生成1 mol H O(l)时所放出的热量叫作中和热
2
D.测定中和热时可用稀硫酸和稀Ba(OH) 溶液
2
【答案】C
【解析】中和热是指稀酸与稀碱发生中和反应生成 1 mol H O(l)时所放出的热量,可以是强酸、强碱,
2
也可以是弱酸、弱碱,故A、B两项错误,C项正确;HSO 和Ba(OH) 反应时,除生成水外,还有BaSO
2 4 2 4
沉淀生成,所以其反应热不是中和热,D项错误。
5.下列反应既属于氧化还原反应,又属于吸热反应的是( )
A.铝片与稀盐酸反应 B.Ba(OH) ·8H O与NH Cl反应
2 2 4
C.灼热的炭与CO 反应 D.甲烷在氧气中的燃烧反应
2
【答案】C
【解析】Al与盐酸的反应是放热反应,A项错误;该反应是吸热反应,但不是氧化还原反应,B项错
误;灼热的C和CO 反应生成CO,该反应既是氧化还原反应,又是吸热反应,C项正确;甲烷的燃烧是
2
放热反应,D项错误。
6.下列有关叙述正确的是( )
A.测定中和反应的反应热时,需要用到天平
B.若用50 mL 0.55 mol·L-1的氢氧化钠溶液,分别与50 mL 0.50 mol·L-1的盐酸和50 mL 0.50 mol·L-1的
硝酸充分反应,两中和反应的反应热不相等
C.用玻璃搅拌器是为了加快反应速率,减小实验误差
D.只需做一次实验,再根据公式即可得出中和反应的反应热
【答案】C
【解析】氢氧化钠溶液稍过量,能使反应进行完全,由于参加反应的n(H+)和n(OH-)相等,测得的反应
热也相等,B项错误;为了减小误差,需做2~3次实验求平均值,D项错误。
7.已知羰基硫(COS)是硫循环的重要中间体,反应H(g)+COS(g) HS(g)+ CO(g) 的能量变
2 2
化如图所示。下列说法错误的是( )A.ΔH<0
B.加入催化剂, 的值不变
C.反应物的总能量大于生成物的总能量
D.反应物的键能总和大于生成物的键能总和
【答案】D
【解析】A项,由图可知,反应物的总能量大于生成物的总能量,该反应为放热反应,反应ΔH<0,
故A正确;B项,加入催化剂,能降低反应的活化能,但不能改变反应ΔH的值,故B正确;C项,由图
可知,反应物的总能量大于生成物的总能量,故C正确;D项,由图可知,反应物的总能量大于生成物的
总能量,则反应物的键能总和小于生成物的键能总和,故D错误;故选D。
8.下列关于热化学方程式的说法错误的是( )
A.化学反应过程所吸收或放出的热量与参加反应的物质的物质的量成正比
B.热化学方程式中各物质前的化学计量数表示物质的量,可以用整数或者简单分数
C.热化学方程式未注明温度和压强时 ,ΔH表示标准状况下的数据
D.同一化学反应,反应条件不同ΔH可能相同
【答案】C
【解析】A项,化学反应过程所吸收或放出的热量与参加反应的物质的物质的量成正比,参加反应的
物质的物质的量越多,化学反应过程所吸收和放出的热量越多,故A不符合题意;B项,热化学方程式中
各物质前的化学计量数表示物质的量,可以用整数或者简单分数,不能表示分子的个数,故 B不符合题意;
C项,热化学方程式未注明温度和压强时,ΔH表示室温常压下的数据,故C符合题意;D项,ΔH只与反
应物和生成物状态有关,与反应过程无关,故D不符合题意;故选C。
9.下列说法中正确的是( )
A.在化学反应过程中,发生物质变化的同时不一定发生能量变化
B.破坏生成物全部化学键所需要的能量大于破坏反应物全部化学键所需要的能量时,该反应为吸热
反应
C.生成物的总焓大于反应物的总焓时,反应吸热,ΔH>0D.ΔH的大小与热化学方程式的化学计量数无关
【答案】C
【解析】化学反应中一定有能量变化,A错误;B项中,由ΔH=断开旧化学键吸收的能量-形成新
化学键放出的能量,得ΔH<0,故为放热反应;吸热反应的ΔH>0,C正确;ΔH的大小与化学方程式的化
学计量数成正比关系,D错误。
10.已知反应X+Y===M+N为吸热反应,下列说法中正确的是( )
A.X的能量一定低于M的能量,Y的能量一定低于N的能量
B.因为该反应为吸热反应,故一定要加热反应才能进行
C.破坏反应物中的化学键所吸收的能量小于形成生成物中化学键所放出的能量
D.X和Y的总能量一定低于M和N的总能量
【答案】D
【解析】已知X+Y===M+N ΔH>0,说明X与Y的总能量低于M与N的总能量,A错误,D正确;
破坏反应物中的化学键所吸收的能量大于形成生成物中化学键所放出的能量,C错误;吸热反应有的不需
要加热也可反应,如氢氧化钡晶体与氯化铵混合搅拌即可发生反应,B错误。故选D。
11.由氢气和氧气反应生成1 mol水蒸气放出241.8 kJ的热量,1 g水蒸气转化为液态水放出2.45
kJ的热量,则下列热化学方程式书写正确的是( )
A.H(g)+O(g)===H O(l) ΔH=-285.9 kJ·mol-1
2 2 2
B.H (g)+O(g)===H O(l) ΔH=-241.8 kJ·mol-1
2 2 2
C.H (g)+O(g)===H O(l) ΔH=285.9 kJ·mol-1
2 2 2
D.H(g)+O(g)===H O(g) ΔH=241.8 kJ·mol-1
2 2 2
【答案】A
【解析】放热反应ΔH<0,C、D错;1 mol水蒸气转化为相同条件下的1 mol液态水时要放出44.1
kJ的热量,可求出生成液态水时ΔH为-285.9 kJ·mol-1,B错,故选A项。
12.已知3.0 g乙烷在常温下完全燃烧放出的热量为155.98 kJ,则下列表示乙烷标准燃烧热的热化
学方程式书写正确的是( )
A.2C H(g)+7O(g)===4CO (g)+6HO(l) ΔH=-2 119.6 kJ·mol-1
2 6 2 2 2
B.C H(g)+O(g)===2CO(g)+3HO(l) ΔH=-1 559.8 kJ·mol-1
2 6 2 2
C.C H(g)+O(g)===2CO (g)+3HO(g) ΔH=-1 559.8 kJ·mol-1
2 6 2 2 2
D.C H(g)+O(g)===2CO (g)+3HO(l) ΔH=-1 559.8 kJ·mol-1
2 6 2 2 2
【答案】D
【解析】1 mol乙烷完全燃烧放出的热量为×155.98 kJ=1 559.8 kJ,则其标准燃烧热为1 559.8 kJ·mol-1,A项中C H 是2 mol,B项中C H 未完全燃烧,C项中水是气态,故A、B、C项均不正确。
2 6 2 6
13.已知2H(g)+O(g)===2H O(l) ΔH=-571.6 kJ·mol-1,则下列关于方程式2HO(l)===2H (g)+
2 2 2 2 2
O(g)的ΔH的说法中正确的是( )
2
A.方程式中的化学计量数表示分子数
B.该反应ΔH大于零
C.该反应ΔH=-571.6 kJ·mol-1
D.该反应可表示36 g水分解时的热效应
【答案】B
【解析】在书写热化学方程式时,若反应物和生成物对换,则ΔH的符号相反,数值不变,故B正确,
C不正确;D项未注明水为液态。
14.热化学方程式C(s)+HO(g)==CO(g)+H(g) H =+131.3 kJ·mol-1表示( )
2 2
A.碳和水反应吸收131.3kJ能量
△
B.1mol碳和1mol水反应生成一氧化碳和氢气并吸收131.3kJ热量
C.1mol固态碳和1mol水蒸气反应生成一氧化碳气体和氢气,并吸热131.3kJ
D.1个固态碳原子和1分子水蒸气反应吸热131.1kJ
【答案】C
【解析】依据反应热的概念,表示按照方程式系数的物质的量反应时吸收或放出的热量,单位是
kJ·mol-1,该方程式表示:1mol碳和1mol水蒸气反应生成1mol一氧化碳气体和1mol氢气,并吸收131.
3kJ的热量;特别要指明水的状态。
15.今有如下三个热化学方程式:
H(g)+l/2O (g)=HO(g) H=akJ/mol
2 2 2
H
2
(g)+l/2O
2
(g)=H
2
O(l) △H=bkJ/mol
2H
2
(g)+O
2
(g)=2H
2
O(l) △H=ckJ/mol
关于它们的下列表述正确的△是( )
A. 2b=c B. a、b和c均为正值 C. a=b D. 它们都是吸热反应
【答案】A
【解析】A项,热化学方程式中的化学计量数与反应热成正比,所以 2b=c ,故A正确;B项,燃烧反
应是放热反应,所以a、b和c均为负值 ,故B错误;C项,HO(g)成为HO(l)放热,所以a>b ,故C错
2 2
误;D项,它们都是放热反应,故D错误。
16.燃烧热是1 mol可燃物完全燃烧生成稳定氧化物放出的热量。下列热化学方程式中 ΔH代表燃烧
热的是( )
A.CH(g)+ O(g)=2HO(l)+CO(g) ΔH
4 2 2 1B.S(s)+ O(g)=SO(s) ΔH
2 3 2
C.C H O(s)+6O(g)=6CO (g)+6HO(l) ΔH
6 12 6 2 2 2 3
D.2CO(g)+O(g)=2CO (g) ΔH
2 2 4
【答案】C
【解析】A项,C的稳定氧化物是CO ,因此该热化学方程式不能表示燃烧热,A不符合题意;B项,
2
S燃烧产生的是SO ,不是SO ,因此该热化学方程式不能表示燃烧热,B不符合题意;C项,该方程式中
2 3
反应物是1 mol,产生的物质都是稳定存在形态,因此能够表示物质C H O(s)的燃烧热,C符合题意;D
6 12 6
项,反应物的物质的量不是1 mol,因此不能表示CO的燃烧热,D不符合题意;故选C。
17.下列热化学方程式中△H的值能表示可燃物的燃烧热的是( )
A.2H(g)+O(g)=2HO(g) H=-484 kJ·mol-1
2 2 2
B.CH(g)+2O(g)=CO (g)+2△HO(g) H=-802.3kJ·mol-1
4 2 2 2
C.2H(g)+O(g)=2HO(l) H= -571.△6 kJ·mol-1
2 2 2
△
D.CO(g)+ O(g) CO(g) H =-283 kJ·mol-1
2 2
△
【答案】D
【解析】燃烧热表示1 mol可燃物完全燃烧产生稳定的氧化物时放出的热量。A项,可燃物H 的物质
2
的量不是1 mol,且HO的稳定状态是液态而不是气态,因此不能表示燃烧热,A错误;B项,可燃物CH
2 4
的物质的量是1 mol,但反应产生的水是气态,不是稳定状态—液态,因此不能表示燃烧热,B错误;C项,
可燃物是2 mol H ,因此该反应不能表示燃烧热,C错误;D项,可燃物CO的物质的量是1 mol,燃烧产
2
生气态CO 是其稳定存在形式,故该方程式能够表示燃烧热,D正确;故选D。
2
1.25 ℃、101 kPa下,碳、氢气、甲烷和葡萄糖的燃烧热依次是ΔH=-393.5 kJ·mol-1、ΔH=-
285.8 kJ·mol-1、ΔH=-890.31 kJ·mol-1、ΔH=-2 800 kJ·mol-1,则下列热化学方程式正确的是( )
A.C(s)+O(g)===CO(g) ΔH=-393.5 kJ·mol-1
2
B.2H(g)+O(g)===2H O(g) ΔH=-571.6 kJ·mol-1
2 2 2
C.CH(g)+2O(g)===CO (g)+2HO(g) ΔH=-890.31 kJ·mol-1
4 2 2 2
D.C H O(s)+3O(g)===3CO (g)+3HO(l) ΔH=-1 400 kJ·mol-1
6 12 6 2 2 2
【答案】D
【解析】根据燃烧热的概念中生成指定产物的含义可知,C→CO(g),H→H O(l),D正确。
2 22.25℃、101 kPa时,1 g甲醇完全燃烧生成CO 和液态HO,同时放出22.68 kJ热量。下列表示该
2 2
反应的热化学方程式中正确的是( )
A.2CHOH(l)+3O (g)=2CO (g)+4HO(l) H=+1451.52 kJ·mol-1
3 2 2 2
△
B.CHOH(l)+ O(g)=CO (g)+2HO(l) H=-725.76 kJ·mol-1
3 2 2 2
△
C.2CHOH+O =2CO +4H O H=-22.68 kJ·mol-1
3 2 2 2
△
D.CHOH(l)+ O(g)=CO (g)+2HO(g) H=-725.76 kJ·mol-1
3 2 2 2
△
【答案】B
【解析】已知25℃、101 kPa时,1g液态甲醇(CHOH),其物质的量为 mol,完全燃烧生成CO 和
3 2
液态水,放出 22.68 kJ的热量,则 1mol CHOH完全燃烧生成 CO 和液态水,放出热量为 22.68 kJ
3 2
32=725.76 kJ。A项,燃烧反应为放热反应,反应焓变为负值,A错误;B项,根据上述分析可知甲醇的燃
烧热的热化学方程式为:CHOH(l)+ O(g)=CO (g)+2HO(l) H=-725.76 kJ·mol-1,B正确;C项,热化学
3 2 2 2
△
方程式中各物质需标明状态,C错误;D项,题干描述“1g甲醇完全燃烧生成CO 和液态HO,同时放出
2 2
22.68 kJ热量”,则生成气体水对应热化学方程式中的焓变无法计算,D错误;故选B。
3.根据热化学方程式:S(s)+O(g)===SO(g) ΔH=a kJ·mol-1(a=-297.2)。分析下列说法,其中
2 2
不正确的是( )
A.S(s)在O(g)中燃烧的反应是放热反应
2
B.S(g)+O(g)===SO(g) ΔH=b kJ·mol-1,则a>b
2 2
C.1 mol SO (g)所具有的能量低于1 mol S(s)与1 mol O (g)所具有的能量之和
2 2
D.16 g固体硫在空气中充分燃烧,可吸收148.6 kJ的热量
【答案】D
【解析】由题中条件可知:反应的热效应ΔH=a kJ·mol-1=-297.2 kJ·mol-1,可知该反应的正向反
应为放热反应,故D错误。
4.肼(N H)是一种高效清洁的火箭燃料。25℃、101kPa时,0.25molNH(g)完全燃烧生成氮气和气态
2 4 2 4
水,放出133.5kJ热量。下列说法正确的是( )
A.该反应的热化学方程式为NH(g)+O(g)=N(g)+2HO(g) ΔH=-534kJ·mol-1
2 4 2 2 2B.NH 的燃烧热534kJ·mol-1
2 4
C.相同条件下,1molN H(g)所含能量高于1molN (g)和2molH O(g)所含能量之和
2 4 2 2
D.该反应是放热反应,反应的发生不需要克服化学键
【答案】A
【解析】A项,由已知25℃、101kPa时,0.25molNH(g)完全燃烧生成氮气和气态水,放出133.5kJ
2 4
热量,则 1mol 肼燃烧放出的热量为 534 kJ,故该反应的热化学方程式为:NH(g)+O(g)= N (g)
2 4 2 2
+2H O(g) H=-534 kJ.mol-1,故A正确;B项,燃烧热是指生成为稳定的氧化物所放出的热量,但水蒸气都
2
不是稳定△的氧化物,N 为单质,故B错误;C项,由NH(g)+O(g)= N (g)+2HO(g) H=-534 kJ.mol-1,可知
2 2 4 2 2 2
该反应是放热反应,所以1 molNH(g)和1 mol O (g)所含能量之和高于1 mol N (g)和△2 mol H O(g)所含能量
2 4 2 2 2
之和,故C错误;D项,化学反应实质旧键断裂新键生成,旧化学键断裂时需要消耗能量,且两个过程能
量不相等,故D错误;故选A。
5.乙烷燃烧热为Q kJ·mol-1,则下列热化学方程式中正确的是( )
A.2C H(g)+7O(g)=4CO (g)+6HO(g) H=-2Q kJ·mol-1
2 6 2 2 2
B.2C H(g)+7O(g)=4CO (g)+6HO(l) △H=+2Q kJ·mol-1
2 6 2 2 2
C.C H(g)+7/2O (g)=2CO (g)+3HO(g) △ H=-Q kJ·mol-1
2 6 2 2 2
D.2C H(g)+7O(g)=4CO (g)+6HO(l) △H=-2Q kJ·mol-1
2 6 2 2 2
【答案】D △
【解析】由乙烷的燃烧热为Q kJ·mol-1,所以1mol乙烷完全燃烧生成CO 和液态水时放热为QkJ,表
2
示其燃烧热的热化学反应方程式为:C H(g)+7/2O (g)=2CO (g)+3HO(l) H=-Q kJ·mol-1,则:A项,燃烧
2 6 2 2 2
热是指:在250C、101KPa时,1mol纯净物完全燃烧生成稳定的氧化物放△出的热量,水应该为液态,故 A
错误;B项,该反应为放热反应,△H为负值,故B错误;C项,燃烧热是指:在250C、101KPa时,1mol
纯净物完全燃烧生成稳定的氧化物放出的热量,水应该为液态,故 C错误;D项,由于化学计量数增大2
倍,所以反应的焓变变为原来的2倍,△H =-2Q kJ·mol-1,故D正确。故选D。
6.已知:①2Na(s)+O (g)=Na O(s) H=-akJ•mol-1
2 2 2 1
②C(s,石墨)+O (g)=CO (g) H=-bk△J•mo1-1
2 2 2
△
③2Na(s)+C(s,石墨)+ O(g)=Na CO(s) H=-ckJ•mo1-1
2 2 3 3
△
④CO(g)+Na O(s)=Na CO(s)+ O(g) H
2 2 2 2 3 2 4
△
下列说法正确的是( )
A.石墨的燃烧热△H=-bkJ•mo1-1B.C(s,石墨)+ O(g)=CO(g) H<-bkJ•mo1-1
2
△
C.反应④中,△H=(c-a-b)kJ•mo1-1
4
D.若将①设计成原电池,则32gO 在正极反应转移4mol电子
2
【答案】A
【解析】A项,燃烧热是指1mol可燃物完全燃烧生成稳定氧化物放出的能量,A项正确;B项,生成
CO时放岀热量减小,C(s,石墨)+ O(g)=CO(g) H>-bkJ•mo1-1,B项错误;C项,根据盖斯定律,
2
△
③-①-②=④,△H=(a+b-c)kJ•mo1-1,C项错误;D项,①反应中,1 mo1O 在正极发生还原反应转移2 mo1
4 2
电子,D项错误;故选A。
7.如图表示在催化剂(NbO)表面进行的反应:H (g)+ CO(g) CO (g)+ HO(g)。已知下列反应:
2 5 2 2 2
①2H (g)+O(g) 2HO(g) ΔH
2 2 2 1
②C(s)+1/2O (g) CO(g) ΔH
2 2
③C(s)+O(g) CO(g) ΔH
2 2 3
下列说法不正确的是( )
A.ΔH<ΔH
2 3
B.图中的能量转化方式为太阳能转化为化学能
C.反应2CO (g)+O(g) 2 CO(g) ΔH=2(ΔH-ΔH)
2 2 3 2
D.反应 的
【答案】A
【解析】A项,ΔH 是1molC完不完全燃烧的焓变,ΔH 是1molC完全燃烧的焓变,放热焓变为负,
2 3
故ΔH>ΔH,A项错误;B项,由图知,太阳能提供能量实现CO 和H 反应生成CO和HO,B项正确;
2 3 2 2 2
C项,③−②再乘以2即得2CO (g)+O(g) 2 CO(g) 的ΔH=2(ΔH-ΔH),C项正确;D项,
2 2 3 2
②−③为H (g)+ CO (g) CO (g)+ H O(g)焓变为 ,D项正确:故选A。
2 2 28.设N 为阿伏加德罗常数的值。已知反应;
A
①
②
其他数据如下表:
化学键 C=O O=O C-H O-H C=C
键能/( ) 798 x 413 463 610
下列说法正确的是( )
A.aⅠ
C.生成P的速率:Ⅲ>Ⅱ D.进程Ⅳ中,Z没有催化作用
【答案】AD
【解析】A项,由图中信息可知,进程Ⅰ中S的总能量大于产物P的总能量,因此进程I是放热反应,
A说法正确;B项,进程Ⅱ中使用了催化剂X,但是催化剂不能改变平衡产率,因此在两个进程中平衡时
P的产率相同,B说法不正确;C项,进程Ⅲ中由S•Y转化为P•Y的活化能高于进程Ⅱ中由S•X转化为P•X
的活化能,由于这两步反应分别是两个进程的决速步骤,因此生成P的速率为Ⅲ<Ⅱ,C说法不正确;D项,
由图中信息可知,进程Ⅳ中S吸附到Z表面生成S•Z,然后S•Z转化为产物P•Z,由于P•Z没有转化为P+
Z,因此,Z没有表现出催化作用,D说法正确;故选AD。
3.(2021•浙江1月选考)在298.15 K、100 kPa条件下,N(g) +3H (g)=2NH (g) ΔH=-92.4 kJ·mol-1,N
2 2 3 2(g) 、H(g)和NH (g)的比热容分别为29.1、28.9和35.6J·K-1·mol-1。一定压强下,1 mol反应中,反应物
2 3
[N (g) +3H (g)]、生成物[2NH (g)]的能量随温度T的变化示意图合理的是( )
2 2 3
A. B.
C. D.
【答案】B
【解析】该反应为放热反应,反应物的总能量大于生成物的总能量,根据题目中给出的反应物与生成
物的比热容可知,升高温度反应物能量升高较快,反应结束后反应放出的热量也会增大,比较4个图像B
符合题意,故选B。
4.(2020•浙江1月选考)在一定温度下,某反应达到了化学平衡,其反应过程对应的能量变化如图。下
列说法正确的是( )
A.E 为逆反应活化能,E为正反应活化能
a
B.该反应为放热反应,ΔH=E’-E
a a
C.所有活化分子的平均能量高于或等于所有分子的平均能量
D.温度升高,逆反应速率加快幅度大于正反应加快幅度,使平衡逆移【答案】D
【解析】A项,由图可知, E 为正反应活化能,E为逆反应活化能,故A错误;B项,由图可知,反
a
应物的总能量大于生成物的总能量,该反应为放热反应,反应热ΔH=—(E’-E),故B错误;C项,在相
a a
同温度下,分子的能量并不完全相同,有些分子的能量高于分子的平均能量,称为活化分子,则所有活化
分子的平均能量高于所有分子的平均能量,故C错误;D项,该反应为放热反应,逆反应速率加快幅度大
于正反应加快幅度,使平衡向吸热的逆反应方向移动,故D正确;故选D。
5.(2020•天津卷)理论研究表明,在101kPa和298K下,HCN(g) HNC(g)异构化反应过程的能量
变化如图所示。下列说法错误的是( )
A.HCN比HNC稳定
B.该异构化反应的ΔH=+59.3 kJ·mol-1
C.正反应的活化能大于逆反应的活化能
D.使用催化剂,可以改变反应的反应热
【答案】D
【解析】A项,根据图中信息得到HCN能量比HNC能量低,再根据能量越低越稳定,因此HCN比
HNC稳定,故A正确;B项,根据焓变等于生成物总能量减去反应物总能量,因此该异构化反应的
ΔH=+59.3 kJ·mol-1-0=+59.3 kJ·mol-1,故B正确;C项,根据图中信息得出该反应是吸热反应,因此正反应
的活化能大于逆反应的活化能,故C正确;D项,使用催化剂,不能改变反应的反应热,只改变反应路径,
反应热只与反应物和生成物的总能量有关,故D错误。故选D。
6.(2020•北京卷)依据图示关系,下列说法不正确的是( )
A.石墨燃烧是放热反应
B.1molC(石墨)和1molCO分别在足量O 中燃烧,全部转化为CO,前者放热多
2 2C.C(石墨)+CO (g)=2CO(g) ΔH=ΔH-ΔH
2 1 2
D.化学反应的ΔH,只与反应体系的始态和终态有关,与反应途径无关
【答案】C
【详解】A.所有的燃烧都是放热反应,根据图示,C(石墨)+O (g)= CO (g) ΔH=-393.5kJ/mol,ΔH<
2 2 1 1
0,则石墨燃烧是放热反应,故A正确;B.根据图示,C(石墨)+O (g)=CO (g) ΔH=-393.5kJ/mol,CO(g)+
2 2 1
O(g)=CO (g) ΔH=-283.0kJ/mol,根据反应可知都是放热反应,1molC(石墨)和1molCO分别在足量O 中
2 2 2 2
燃烧,全部转化为CO,1molC(石墨)放热多,故B正确;C.根据B项分析,①C(石墨)+O (g)=CO (g)
2 2 2
ΔH=-393.5kJ/mol,②CO(g)+ O(g)=CO (g) ΔH=-283.0kJ/mol,根据盖斯定律①-②x2可得:C(石墨)
1 2 2 2
+CO (g)=2CO(g) ΔH=ΔH-2ΔH,故C错误;D.根据盖斯定律可知,化学反应的焓变只与反应体系的始态
2 1 2
和终态有关,与反应途径无关,故D正确;故选C。
7.甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应原理是:
①CHOH(g)+ HO(g)→CO (g) +3 H(g) ΔH=+49.0 kJ·mol-1
3 2 2 2
②CHOH(g)+ 1/2O (g)→CO (g) +2 H(g) ΔH=-192.9kJ·mol-1
3 2 2 2
25℃,101kPa时,下列说法正确的是 ( )
A.上述图示的反应为吸热反应
B.图中的能量变化如图所示,则Q=E -E
3 1
C.H 燃烧能放出大量的热,故CHOH转变成H 的过程必须吸收热量
2 3 2
D.根据①②推知:在25℃,101kPa时,1mol CHOH(g)完全燃烧生成CO 和HO(g)放出的热量应
3 2 2676.7kJ
【答案】D
【解析】A项,从图上可知,反应物能量比生成物能量高,反应放热,故A错误;B项,由图知,
△H=生成物总能量-反应物总能量=E-E ,故B错误;C项,反应②为放热反应,因此CHOH转变成H 的
1 2 3 2
过程不一定需要吸收热量,故C错误;D项,根据盖斯定律,将②×3-①×2可得:CHOH(g)+
3
O(g)=CO (g)+2HO(l) H=-192.9kJ/mol×3-49kJ/mol×2=-676.7kJ/mol,即 完全燃烧生成CO
2 2 2 2
△
和HO(g)放出的热量应676.7kJ,故D正确;故选D。
2
8.根据以下热化学方程式,ΔH 和ΔH 的大小比较错误的是( )
1 2
A.Br (g)+H(g)=2HBr(g) ΔH ,Br (l)+H (g)=2HBr(g) ΔH ,则有ΔH<ΔH
2 2 1 2 2 2 1 2
B.2HS(g)+3O(g)=2SO(g)+2HO(l) ΔH ,2HS(g)+O(g)=2S(s)+2HO(l) ΔH ,则有ΔH>ΔH
2 2 2 2 1 2 2 2 2 1 2
C.4Al(s)+3O (g)=2Al O(s) ΔH ,4Fe(s)+3O (g)=2Fe O(s) ΔH ,则有ΔH<ΔH
2 2 3 1 2 2 3 2 1 2
D.C(s)+O(g)=CO (g) ΔH ,C(s)+O(g)=CO(g) ΔH ,则有ΔH<ΔH
2 2 1 2 2 1 2
【答案】B
【解析】A项,依据盖斯定律分析,液态溴变化为气态溴需要吸收热量,反应是放热反应,焓变是负
值,所以△H<△H,A正确;B项,S燃烧生成二氧化硫放热,反应是放热反应,焓变是负值,所以
1 2
△H<△H,B错误;C项,铝活泼性大于铁,能量高于铁,反应是放热反应,焓变是负值,△H<
1 2 1
△H,C正确;D项,碳完全燃烧放出的热量大于不完全燃烧生成CO放出的热量,反应是放热反应,焓
2
变是负值,所以△H<△H,D正确;故选B。
1 2
9.煤的液化可以合成甲醇。下列有关说法正确的是( )
①“气化”: C(s)+2HO(g)=CO(g)+2H(g) ΔH=+90.1kJ·mol-1;
2 2 2 1
②催化液化Ⅰ:CO(g)+3H(g)= CH OH(g)+H O(g) ΔH = -49.0kJ•mol-1;
2 2 3 2 2
③催化液化Ⅱ:CO(g)+2H(g)=CH OH(g)+ O(g) ΔH = akJ•mol-1;
2 2 3 2 3
A.催化液化Ⅰ中使用催化剂,反应的活化能E、ΔH 都减小
a 2
B.反应C(s)+HO(g) +H (g)=CH OH(g) ΔH= 41.1 kJ•mol-1
2 2 3
C.ΔH>ΔH
2 3
D.KOH为电解质溶液的甲醇燃料电池中负极的电极反应为:CHOH-6e-+6OH-= CO+5H O
3 2 2
【答案】B
【解析】A项,使用催化剂,降低活化能,但对ΔH无影响,A错误;B项,根据盖斯定律①+②得,C(s)+HO(g)+H (g)=CH OH(g)ΔH=+41.1kJ•mol-1,B正确;C项,根据盖斯定律,②-③可得热化学方程式为:
2 2 3
H(g)+ O(g)=HO(g) ΔH=ΔH-ΔH =(-49.0-a) kJ·mol—1,该反应为放热反应,即ΔH<0,则有ΔH-ΔH <0,
2 2 2 2 3 2 3
即ΔH<ΔH ,C错误;D项,甲醇燃料电池中负极上甲醇被氧化,电解质溶液为KOH溶液,所以被氧化为
2 3
碳酸根而不是二氧化碳,D错误;故选B。
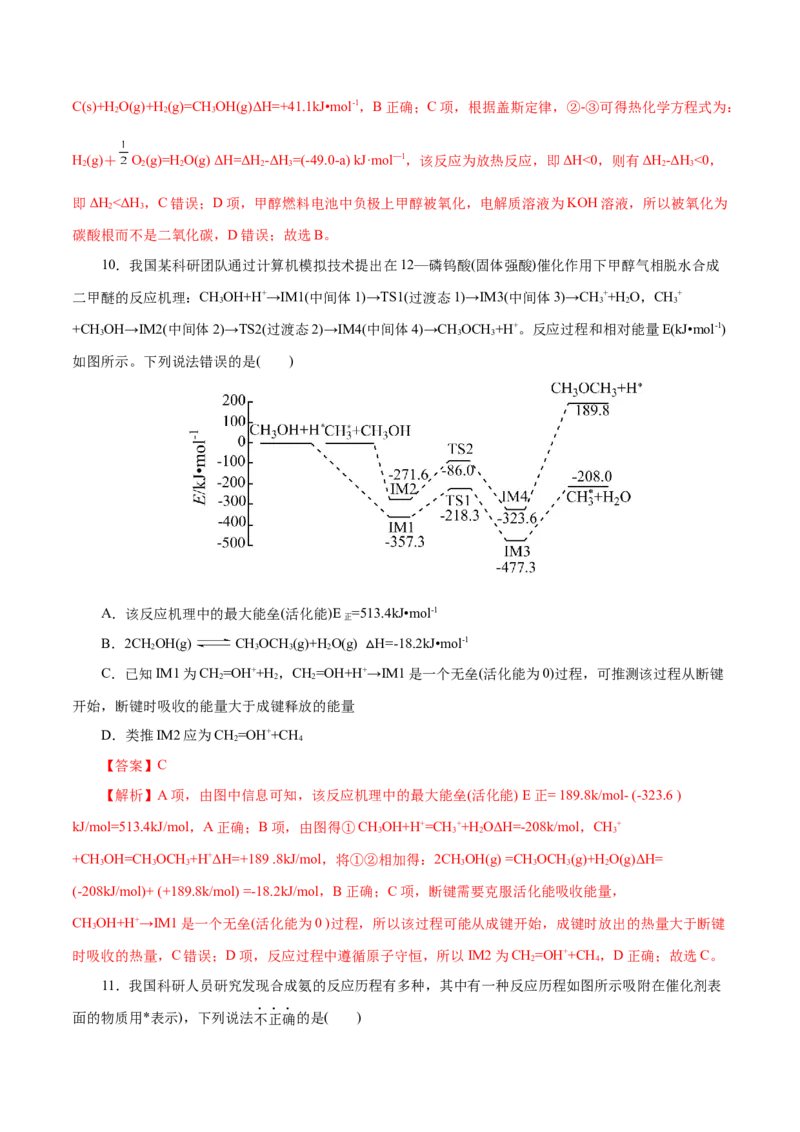
10.我国某科研团队通过计算机模拟技术提出在12—磷钨酸(固体强酸)催化作用下甲醇气相脱水合成
二甲醚的反应机理:CHOH+H+→IM1(中间体1)→TS1(过渡态1)→IM3(中间体3)→CH++H O,CH+
3 3 2 3
+CH OH→IM2(中间体2)→TS2(过渡态2)→IM4(中间体4)→CHOCH +H+。反应过程和相对能量E(kJ•mol-1)
3 3 3
如图所示。下列说法错误的是( )
A.该反应机理中的最大能垒(活化能)E =513.4kJ•mol-1
正
B.2CHOH(g) CHOCH (g)+HO(g) H=-18.2kJ•mol-1
2 3 3 2
C.已知IM1为CH=OH++H ,CH=OH+H+△→IM1是一个无垒(活化能为0)过程,可推测该过程从断键
2 2 2
开始,断键时吸收的能量大于成键释放的能量
D.类推IM2应为CH=OH++CH
2 4
【答案】C
【解析】A项,由图中信息可知,该反应机理中的最大能垒(活化能) E正= 189.8k/mol- (-323.6 )
kJ/mol=513.4kJ/mol,A正确;B项,由图得①CHOH+H+=CH ++H OΔH=-208k/mol,CH+
3 3 2 3
+CH OH=CH OCH +H+ΔH=+189 .8kJ/mol,将①②相加得:2CHOH(g) =CHOCH (g)+HO(g)ΔH=
3 3 3 3 3 3 2
(-208kJ/mol)+ (+189.8k/mol) =-18.2kJ/mol,B正确;C项,断键需要克服活化能吸收能量,
CHOH+H+→IM1是一个无垒(活化能为0 )过程,所以该过程可能从成键开始,成键时放出的热量大于断键
3
时吸收的热量,C错误;D项,反应过程中遵循原子守恒,所以IM2为CH=OH++CH ,D正确;故选C。
2 4
11.我国科研人员研究发现合成氨的反应历程有多种,其中有一种反应历程如图所示吸附在催化剂表
面的物质用*表示),下列说法不正确的是( )A.带*标记的物质是该反应历程中的中间产物或过渡态
B.N 生成NH 是通过多步还原反应生成的
2 3
C.过程I和III中能量的变化相同
D.适当提高N 分压,可以加快N(g) →★N 反应速率,N(g)转化率降低
2 2 2 2
【答案】C
【解析】A项,根据图示,N 是反应物、NH 是最终产物,带*标记的物质是该反应历程中的中间产物
2 3
或过渡态,故A正确;B项,N 生成NH 过程中N元素化合价逐渐降低,所以N 生成NH 是通过多步还
2 3 2 3
原反应生成的,故B正确;C项,过程I断裂1个氮氮键形成1个氮氢键,过程 III断裂1个氮氮键生成2
个氮氢键,能量的变化不相同,故C错误;D项,适当提高N 分压,即增大氮气浓度,可以加快N(g)
2 2
→★N 反应速率,由于氮气的初始浓度增大,N(g)转化率减小,故D正确;故选C。
2 2
12.下图是不饱和烃加氢时能量变化示意图(E代表反应物具有的总能量),具体数据如下:
反应 ΔE ΔH
CHC≡CCH +2H CH(CH)CH ΔH
3 3 2 3 2 3 3 1
CH=CH-CH=CH +2H →CH(CH)CH ΔH
2 2 2 2 2 3 2
(1)如果CHC≡CCH CH=CH-CH=CH 与H 以物质的量1:2反应,其主要产物是X。
3 2 2 2
(2)如果CHCHBrCHBrCH 与NaOH的醇溶液共热后,主要产物是Y,另一副产物是Z。
3 3
下列推断正确的是( )
A.不饱和烃加氢的反应的ΔH>0 B.Y是CHC≡CCH
3 3
C.X是CH(CH)CH=CH-CH=CH D.ΔH>ΔH
3 2 3 2 1 2【答案】C
【解析】A项,由图可知,不饱和烃加氢时反应物的总能量比生成物的总能量高,为放热反应,则
ΔH<0,A错误;B项,卤代烃消去可形成碳碳三键或两个双键,由表中信息知CHC≡CCH 的总能量大于
3 3
CH=CH-CH=CH ,反应总是向能量降低方向进行,故主要产物为二烯烃,则Y为CH=CH-CH=CH ,B错
2 2 2 2
误;C项,由图形可知两个反应均为放热反应,由表中数据可知,“-C≡C-”与H 的加成放出热量多于二烯
2
烃与H 加成放出热量,反应总是向能量降低方向进行,故加成时主要发生在碳碳三键上,则X是
2
CH(CH)CH=CH-CH=CH ,C正确;D项,不饱和烃加氢为放热反应,由ΔE的数值可知,反应1放出的
3 2 3 2
热量多,ΔH小,则ΔH<ΔH,D错误;故选C。
1 2