文档内容
专题 10 化学反应速率与平衡
第 28 练 化学反应的方向
1.下列不属于自发进行的变化是( )
A.红墨水加到清水使整杯水变红 B.冰在室温下融化成水
C.电解饱和食盐水 D.铁器在潮湿的空气中生锈
2.下列过程是非自发的是( )
A.水由高处向低处流 B.氯气和溴化钾溶液的反应
C.铁在潮湿空气中生锈 D.室温下水结成冰
3.下列关于焓变与反应方向的叙述中正确的是( )
A.化学反应的焓变与其反应的方向无关
B.化学反应的焓变直接决定了反应的方向
C.反应焓变为正值时不利于反应自发进行
D.焓变为负值的反应都能自发进行
4.下列对熵变的判断中不正确的是( )
A.少量的食盐溶解于水中:ΔS>0
B.纯碳和氧气反应生成CO(g):ΔS>0
C.气态水变成液态水:ΔS>0
D.CaCO (s)受热分解为CaO(s)和CO(g):ΔS>0
3 2
5.下列反应在任意温度下一定能自发进行的是( )
A.2NaCl+2H O 2NaOH+Cl ↑+H ↑
2 2 2
B.NH(g)+HCl(g)=NH Cl(s) ΔH<0
3 4
C.CaCO (s)=CaO(s)+CO (g) ΔH>0
3 2
D.XY(g)=X(g)+Y(g) ΔH<0
2 2 2 2
6.对于化学反应方向的确定,下列说法不正确的是( )。
A.在温度、压强一定的条件下,焓因素和熵因素共同决定一个化学反应的方向
B.温度、压强一定时,放热的熵增加反应一定能自发进行
C.反应焓变是决定反应能否自发进行的唯一因素
D.固体的溶解过程与熵变有关7.下列反应△S>0的是( )
A.HCl(g)+NH (g)=NH Cl(s) B.2CO(g)=2C(s)+O (g)
3 4 2
C.N(g)+3H(g)=2NH (g) D.CaCO (s)=CaO(s)+CO (g)
2 2 3 3 2
8.以下判断正确的是( )
A.C(s)+CO(g)=2CO(g) H>0,该反应常温下不能自发
2
B.2Mg(s)+O (g)=2MgO(s) △ H<0,该反应高温才能自发
2
C.自发反应的熵一定增大,△非自发反应的熵一定减小
D.放热反应都可以自发进行,而吸热反应不能自发进行
9.某化学反应在较低温度下自发,较高温度下非自发。有关该反应的下列说法正确的是( )
A.ΔH>0,ΔS>0 B.ΔH>0,ΔS<0 C.ΔH<0,ΔS>0 D.ΔH<0,ΔS<0
10.碳酸铵[(NH ) CO]在室温下就能自发地分解产生氨气,下列说法正确的是( )
4 2 3
A.碳酸盐都不稳定,都能自发分解
B.碳酸铵分解是因为进行了加热的操作
C.碳酸铵分解是吸热反应,此反应不应该自发进行,必须借助外力才能进行
D.碳酸铵分解是因为生成了易挥发的气体,使体系的熵增大
11.关于熵值(S)的叙述不正确的是( )
A.熵值是一个物理量,只与物质的种类有关,而与其它因素无关
B.同一种物质,其所处的状态不同,熵值不同
C.不同种物质,同一状态(T、P)下,熵值不同
D.同一物质,当物质的量一定时,温度越高,熵值越大
12.下列说法正确的是( )
A.放热且熵增加的反应,一定能自发进行 B.放热反应的焓变小于零,熵变大于零
C.放热反应的焓变大于零,熵变小于零 D.放热及熵减小的反应,一定能自发进行
13.下列对于化学反应方向说法正确的是( )
A.反应2A(g)+B(g)=3C(s)+D(g)在一定条件下能自发进行,说明该反应的ΔH>0
B.常温下反应2NaSO (s)+O(g)=2Na SO (s)能自发进行,则ΔH<0
2 3 2 2 4
C.反应2Mg(s)+CO (g)=C(s)+2MgO(s)在一定条件下能自发进行,则该反应的ΔH>0
2
D.一定温度下,反应2NaCl(s)=2Na(s)+Cl (g)的ΔH<0,ΔS>0
2
1.下列关于焓判据和熵判据的说法中,不正确的是( )A.放热的自发过程可能是熵减小的过程,吸热的自发过程一定为熵增加的过程
B.由焓判据和熵判据组合成的复合判据更适合判断所有过程的自发性
C.在室温下碳酸钙的分解反应不能自发进行,但同样是这个吸热反应,其在较高温度(1200 K)下能自
发进行
D.放热过程(ΔH<0)或熵增加(ΔS>0)的过程一定是自发的
2.下列说法正确的是( )
A.凡是放热反应都是自发的,因为吸热反应都是非自发的
B.自发反应的熵一定增大,非自发反应的熵一定减小
C.常温下,反应C(s)+CO(g) 2CO(g)不能自发进行,则该反应的ΔH>0
2
D.反应2Mg(s)+CO (g)=C(s)+2MgO(s)能自发进行,则该反应的ΔH>0
2
3.下列关于化学反应方向及其判据的说法中正确的是( )
A.1molSO 在不同状态时的熵值:S[SO (s)]>S[SO (1)]>S[SO (g)]
3 3 3 3
B.常温下,反应C(s)+CO(g)=2CO(g)不能自发进行,则该反应的ΔH>0
2
C.放热反应都可以自发进行,而吸热反应不能自发进行
D.2KClO(s)=2KCl(s)+3CO (g) ΔH>0能否自发进行与温度无关
3 2
4.化学反应进行的方向是一个比较复杂的问题。下列有关说法正确的是( )
A.反应 的
B. CO 在不同状态时的熵值:
2
C.反应 ΔH>0能否自发进行与温度有关
D.ΔH<0或ΔS>0的反应一定能自发进行
5.某化学反应A(s)=D(g)+E(g) ΔH-TΔS=(-4500+11T)kJ·mol-1(其中ΔH为焓变,ΔS为熵变,T为热力
学温度,单位为K),要防止反应发生,温度必须( )
A.高于409 K B.低于136 K
C.高于136 K而低于409 K D.低于409 K
6.灰锡结构松散,不能用于制造器皿;而白锡结构坚固,可以制造器皿。现把白锡制造的器皿放在
0 ℃、101 kPa的室内存放,它会不会变成灰锡而不能继续使用( )
(已知在0 ℃、101 kPa条件下白锡转化为灰锡的反应,焓变和熵变分别为 ΔH=-2 180.9 J·mol-1,ΔS
=-6.61 J·mol-1·K-1)
A.会变 B.不会变
C.不能确定 D.升高温度才会变7.下列叙述不正确的是( )
A.Zn(s)+CuSO(aq)=ZnSO (aq)+Cu(s) H=-216kJ•mol-1,则反应总能量>生成物总能量
4 4
B.常温下反应2NaSO (s)+O(g)=2Na SO△(s)能自发进行,则△H<0
2 3 2 2 4
C.CaCO (s)=CaO(s)+CO (g) H>0,△S>0,则不论在何种条件下都不可能自发
3 2
△
D.己知C(s)+O(g)=CO (g) H;C(s)+ O(g)=CO(g) H;则△H<△H
2 2 1 2 2 1 2
△ △
8.下列反应的△H<0、△S>0的是( )
A.CO(g)+C(s)=2CO(g) B.2Na(s)+2H O(l)=2Na+(aq)+2OH-(aq)+H (g)
2 2 2
C.N(g)+3H(g) 2NH (g) D.C(s)+HO(g) CO(g)+H(g)
2 2 3 2 2
9.下列有关说法不正确的是( )
A.Na与HO的反应是熵增的放热反应,该反应能自发进行
2
B.非自发反应在某些条件下也能够实现
C.室温下,冰溶于水的过程是一个自发反应
D.已知反应NH (g)+HCl(g)=NH Cl(s)在室温下可自发进行,则该反应的ΔH<0
3 4
10.下列说法错误的是( )
A.食物在常温下变质是自发进行的
B.1molH O在不同状态时的值:S[H O(s)]<S[H O(g)]
2 2 2
C.放热过程( H<0)或熵增加( S>0)的过程一定是自发的
D.CaCO (s)═△CaO(s)+CO (g) H△>0能否自发进行与温度有关
3 2
11.下列有关说法不正确的是△( )
A.反应CO(g)+C(s) 2CO(g) ΔS>0、ΔH<0
2
B.Na与HO的反应⇌是熵增的放热反应,该反应能自发进行
2
C.某吸热反应能自发进行,因此该反应是熵增反应
D.反应NH (g)+HCl(g)=NH Cl(s)在室温下可自发进行,则该反应的ΔH<0
3 4
12.已知NH HCO (s)=NH (g)+HO(g)+CO(g) ΔH=+185.57 kJ·mol-1,下列说法中正确的是( )
4 3 3 2 2
A.该反应ΔH>0且ΔS>0,因此该反应任何温度下都不能自发进行
B.一定条件下,该反应能自发进行,是因为该反应是一个熵增加的反应
C.其他条件不变,使用催化剂可以改变化学反应进行的方向
D.能自发进行的反应一定是放热反应,不能自发进行的反应一定是吸热反应
13.下列对化学反应预测正确的是( )
选项 化学反应方程式 已知条件 预测A M(s)=X(g)+Y(s) ΔH>0 它是非自发反应
B W(s)+xG(g)=2Q(g) ΔH<0,自发反应 x可能等于1、2、3
C 4X(g)+5Y(g)=4W(g)+6G(g) 能自发反应 ΔH一定小于0
D 4M(s)+N(g)+2W(l)=4Q(s) 常温下,自发进行 ΔH>0
1.(2022·浙江省1月选考)AB型强电解质在水中的溶解(可视作特殊的化学反应)表示为AB(s)=An+(aq)
+Bn-(aq),其焓变和熵变分别为ΔH和ΔS。对于不同组成的AB型强电解质,下列说法正确的是( )
A.ΔH和ΔS均大于零
B.ΔH和ΔS均小于零
C.ΔH可能大于零或小于零,ΔS大于零
D.ΔH和ΔS均可能大于零或小于零
2.(2021•浙江6月选考)相同温度和压强下,关于物质熵的大小比较,合理的是( )
A.1molCH(g)<1molH(g) B.1molHO(g)<2molHO(g)
4 2 2 2
C.1molHO(s)>1molHO(l) D.1molC(s,金刚石)>1molC(s,石黑)
2 2
3.(2021•北京卷)已知2NO (g) NO(g) H<0。下列说法正确的是( )
2 2 4
A.1mol混合气体含有1molN原子 △
B.完全断开2molNO 分子中的共价键所吸收的热量比完全断开1molN O 分子中的共价键所吸收的热
2 2 4
量多
C.将气体体积压缩至一半,气体颜色变深是因为平衡发生了移动
D.将气体温度升高,气体颜色会变深
4.(2020•浙江1月选考)在干燥的HCl气流中加热MgCl ·6H O,能得到无水MgCl 。下列说法不正确
2 2 2
的是( )
A.MgCl ·nH O(s)=MgCl ·(n-1)H O(s)+HO(g) ΔH>0
2 2 2 2 2
B.MgCl ·2H O(s)=Mg(OH) (s)+2HCl(g),HCl气流可抑制反应进行
2 2 2
C.MgCl ·H O(s)=Mg(OH)Cl(s)+HCl(g),升高温度,反应更易发生
2 2
D.MgCl ·4H O(s)=MgCl ·2H O(s)+2HO(g),HCl气流可抑制反应进行
2 2 2 2 2
5.关于化学反应进行的方向叙述正确的是( )A.加入催化剂可以使反应2SO +O 2SO 在低温下由非自发变为自发,从而提高产率
2 2 3
B.ΔH<0,ΔS>0时,反应可以自发进行,例如Ba(OH) 固体与NH Cl固体混合
2 4
C.常温下,反应4Fe(OH) (s)+2HO(l)+O(g) 4Fe(OH) (s)的ΔH<0
2 2 2 2
D.因为ΔH和 都与反应的自发性有关,因此ΔH或 均可单独做为判断自发性的判据
6.下列关于焓判据和熵判据的说法中,不正确的是( )
A.放热的自发过程可能是熵减小的过程,吸热的自发过程一定为熵增加的过程
B.4Fe(OH) (s)+2HO(l)+O(g)=4Fe(OH) (s) ΔH=-444.3kJ·mol-1ΔS=-280.1J·mol-1·K-1在常温常压下能自
2 2 2 3
发进行
C.在室温下碳酸钙的分解反应不能自发进行,但同样是这个吸热反应在较高温度(1200K)下则能自发
进行
D.放热过程(ΔH<0)或熵增加(ΔS>0)的过程一定是自发的
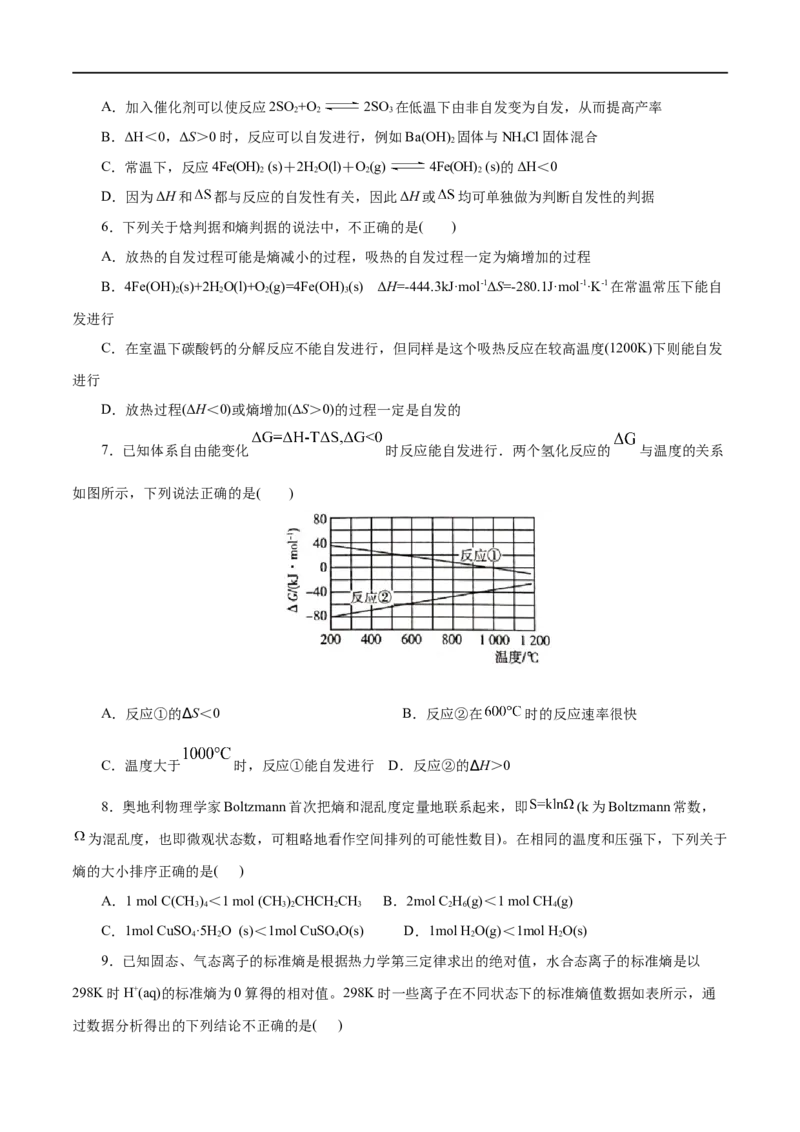
7.已知体系自由能变化 时反应能自发进行.两个氢化反应的 与温度的关系
如图所示,下列说法正确的是( )
A.反应①的∆S<0 B.反应②在 时的反应速率很快
C.温度大于 时,反应①能自发进行 D.反应②的∆H>0
8.奥地利物理学家Boltzmann首次把熵和混乱度定量地联系起来,即 (k为Boltzmann常数,
为混乱度,也即微观状态数,可粗略地看作空间排列的可能性数目)。在相同的温度和压强下,下列关于
熵的大小排序正确的是( )
A.1 mol C(CH )<1 mol (CH )CHCH CH B.2mol C H(g)<1 mol CH (g)
3 4 3 2 2 3 2 6 4
C.1mol CuSO ·5H O (s)<1mol CuSO O(s) D.1mol HO(g)<1mol HO(s)
4 2 4 2 2
9.已知固态、气态离子的标准熵是根据热力学第三定律求出的绝对值,水合态离子的标准熵是以
298K时H+(aq)的标准熵为0算得的相对值。298K时一些离子在不同状态下的标准熵值数据如表所示,通
过数据分析得出的下列结论不正确的是( )标准熵值/J·mol·L-1 Li+ Na+ K+ Be2+ Mg2+ Ca2+ Al3+
固态离子标准熵S (s) 29.1 51.3 64.7 9.5 32.7 41.6 28.3
气态离子标准熵S (g) 138.8 153.7 160.3 136.3 148.6 154.9 164.6
水合态离子标准熵S (aq) 13.4 59 102.5 -129.7 -138.1 -53.1 -321.7
A.金属离子由固态到气态,标准熵值增加
B.同周期金属离子价态越高,水合态离子的标准熵值越小
C.同主族金属离子半径越小,水合态离子的标准熵值越小
D.同主族金属元素固态或气态离子的标准熵值随原子序数增大而增大