文档内容
第二十八讲 难溶电解质溶解平衡
及反应过程中溶液粒子浓度变化的图像分析
【基础巩固】
1.医院中常用硫酸钡(俗称钡餐)作为内服造影剂,其不溶于水和脂质,所以不会被胃肠道黏膜吸收,因此对
人基本无毒性。已知:K (BaCO)=5.1×10-9;K (BaSO)=1.1×10-10。下列推断正确的是( )
sp 3 sp 4
A.BaCO 的溶度积常数表达式为K (BaCO)=n(Ba2+)·n(CO)
3 sp 3
B.可用2%~5%的NaSO 溶液给钡离子中毒患者洗胃
2 4
C.若误服含c(Ba2+)=1.0×10-5 mol·L-1的溶液时,会引起钡离子中毒
D.不用碳酸钡作为内服造影剂,是因为K (BaCO)>K (BaSO)
sp 3 sp 4
【答案】 B
【解析】 A 项,溶度积常数为离子浓度幂之积,BaCO 的溶度积常数表达式为 K (BaCO)=c(Ba2
3 sp 3
+)·c(CO),故A错误;B项,用NaSO 溶液给钡离子中毒患者洗胃,可使钡离子形成不溶于水的硫酸钡沉
2 4
淀,减小Ba2+浓度,可起到解毒的作用,故B正确;C项,c(Ba2+)=1.0×10-5 mol·L-1的溶液钡离子浓度
很小,不会引起钡离子中毒,故C错误;D项,因胃酸可与CO反应生成水和二氧化碳,使CO浓度降低,
从而使平衡BaCO (s)Ba2+(aq)+CO(aq) 向溶解方向移动,使Ba2+浓度增大,Ba2+有毒,与K 大小无关,
3 sp
故D错误。
2.(2023·浙江·高考真题)碳酸钙是常见难溶物,将过量碳酸钙粉末置于水中达到溶解平衡:
[已知 , , 的电离常
数 ],下列有关说法正确的是
A.上层清液中存在
B.上层清液中含碳微粒最主要以 形式存在
C.向体系中通入 气体,溶液中 保持不变
D.通过加 溶液可实现 向 的有效转化
【答案】 B
【解析】 A.上层清液为碳酸钙的饱和溶液,碳酸根离子水解生成碳酸氢根离子,因此
资料整理【淘宝店铺:向阳百分百】,A错误;B.根据K =4.7×10-11可得 ,则碳酸根的水解平衡
a2
常数为 ,说明碳酸根的水解程度较大,则上层清液中含碳微
粒主要为碳酸氢根离子,B正确;C.向体系中通入CO, ,c( )减小,
2
CaCO
3
(s)⇌Ca2+(aq)+CO (aq)正向移动,溶液中钙离子浓度增大,C错误;D.由题干可知,
, ,碳酸钙比硫酸钙更难溶,加入硫酸钠后碳酸钙不会转化
成硫酸钙,D错误;故答案选B。
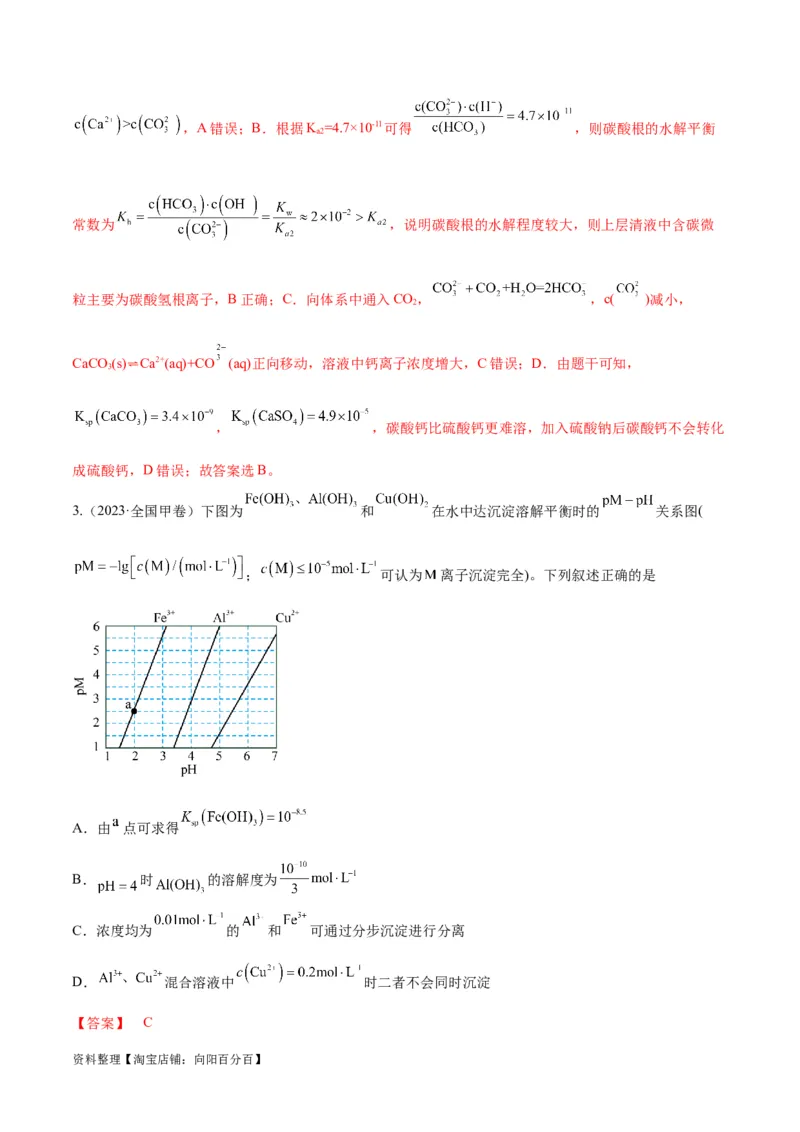
3.(2023·全国甲卷)下图为 和 在水中达沉淀溶解平衡时的 关系图(
; 可认为 离子沉淀完全)。下列叙述正确的是
A.由 点可求得
B. 时 的溶解度为
C.浓度均为 的 和 可通过分步沉淀进行分离
D. 混合溶液中 时二者不会同时沉淀
【答案】 C
资料整理【淘宝店铺:向阳百分百】【解析】 A.由点a(2,2.5)可知,此时pH=2,pOH=12,则 = =
= ,故A错误;B.由点(5,6)可知,此时pH=5,pOH=9,则 =
= = , 时 的溶解度为 =10-3 ,故B错误;C.
由图可知,当铁离子完全沉淀时,铝离子尚未开始沉淀,可通过调节溶液pH的方法分步沉淀 和 ,
故C正确;D.由图可知, 沉淀完全时, ,pM 5,此时pH约为4.7,在此pH下
刚开始沉淀的浓度为 ,而题中 > ,则 会同时沉淀,
故D错误;答案选C。
4.(2024·福建泉州·统考一模)室温下,用 溶液滴定盐酸酸化的 溶液的
pH-t曲线如图所示。下列说法正确的是
已知:①室温时 ②
A. 的水解平衡常数
B.若b点 ,则x=3.2
C.ab段仅发生反应:
D.从a到c点,水的电离程度一直在减小
资料整理【淘宝店铺:向阳百分百】【答案】 B
【解析】 A.Fe3+水解反应为Fe3+(aq)+3H
2
O⇌Fe(OH)
3
+3H+(aq),水解平衡常数
,故A错误;B.b点生成Fe(OH) 沉淀,
3
K [Fe(OH) ]=c(Fe3+)•c3(OH-),若b点c(Fe3+)=10-5mol⋅L-1,则c(OH-)=
sp 3
,c(H+)= ,pH=-
lgc(H+)=3.2,即x=3.2,故B正确;C.向盐酸酸化的FeCl 溶液中逐滴加入NaOH溶液时,NaOH先与盐酸
3
反应,后与FeCl 反应,则ab段发生的反应为H++OH-=H O、Fe3++3OH-=Fe(OH) ↓,故C错误;D.盐酸酸
3 2 3
化的FeCl 溶液中逐滴加入NaOH溶液时,NaOH先与盐酸反应,后与FeCl 反应,酸碱抑制水的电离,
3 3
Fe3+促进水的电离,所以从a到c点,水的电离程度先增大后减小,故D错误;故选:B。
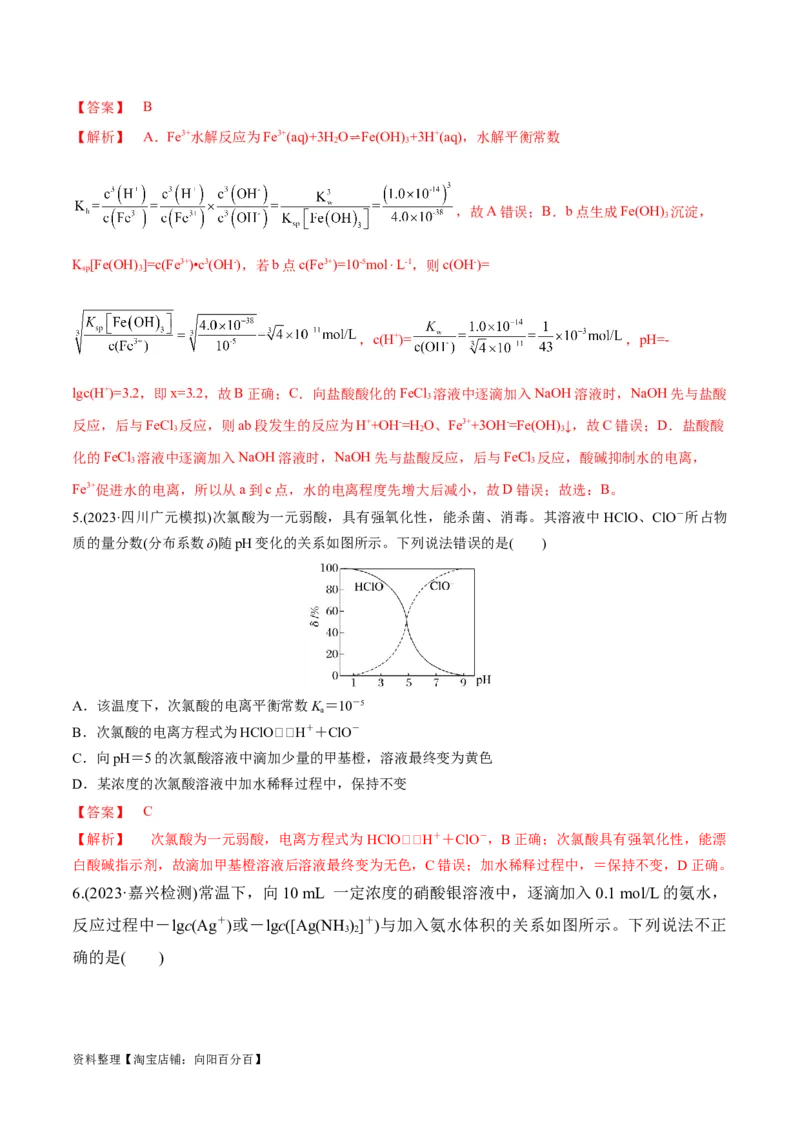
5.(2023·四川广元模拟)次氯酸为一元弱酸,具有强氧化性,能杀菌、消毒。其溶液中HClO、ClO-所占物
质的量分数(分布系数δ)随pH变化的关系如图所示。下列说法错误的是( )
A.该温度下,次氯酸的电离平衡常数K=10-5
a
B.次氯酸的电离方程式为HClOH++ClO-
C.向pH=5的次氯酸溶液中滴加少量的甲基橙,溶液最终变为黄色
D.某浓度的次氯酸溶液中加水稀释过程中,保持不变
【答案】 C
【解析】 次氯酸为一元弱酸,电离方程式为HClOH++ClO-,B正确;次氯酸具有强氧化性,能漂
白酸碱指示剂,故滴加甲基橙溶液后溶液最终变为无色,C错误;加水稀释过程中,=保持不变,D正确。
6.(2023·嘉兴检测)常温下,向10 mL 一定浓度的硝酸银溶液中,逐滴加入 0.1 mol/L的氨水,
反应过程中-lgc(Ag+)或-lgc([Ag(NH ) ]+)与加入氨水体积的关系如图所示。下列说法不正
3 2
确的是( )
资料整理【淘宝店铺:向阳百分百】A.NH的浓度:b点小于m点
B.原硝酸银溶液的浓度是0.1 mol/L
C.m点:c(NO)-c(Ag+)-c(NH)<0.01 mol·L-1
D.a―→c的过程中,溶液pH始终增大
【答案】 A
【解析】 向10 mL 一定浓度的硝酸银溶液中,逐滴加入0.1 mol·L-1的氨水,首先发生反应:
Ag++NH ·H O===AgOH↓+NH,然后发生反应 AgOH+2NH ·H O===Ag(NH )+2H O+OH
3 2 3 2 3 2
-;b点-lgc(Ag+)达到最大值,可认为此时Ag+与NH ·H O恰好完全反应生成AgOH沉淀和
3 2
硝酸铵,b点后氨水过量生成[Ag(NH )]。A.b点溶液溶质为 NH NO ,b到m过程发生反应
3 4 3
AgOH+2NH ·H O=Ag(NH )+2H O+OH-,随着氨水的加入,并没有引入铵根离子,虽然溶
3 2 3 2
液碱性增强铵根离子的水解受到促进,但是溶液体积增加导致铵根离子的浓度仍然减小,即
b点铵根离子的浓度大于溶液m点铵根离子的浓度,A错误;B.b点完全反应,此时加入的氨
水为 10 mL,氨水的浓度 0.1 mol/L,原硝酸银溶液也为 10 mL,根据方程式 Ag++
NH ·H O=AgOH↓+NH可知,硝酸银溶液的浓度为 0.1 mol/L,B正确;C.m点溶液存在电荷
3 2
守恒c(OH-)+c(NO)=c(Ag+)+c[Ag(NH )]+c(NH)+c(H+),此时加入了过量的氨水,溶液应
3
呈碱性,则有:c(NO)-c(Ag+)-c(NH)=c[Ag(NH )]+c(H+)-c(OH-)=10-2+c(H+)-c(OH
3
-)<10-2 mol/L,C正确;D.a→c的过程中,溶液中不断加入氨水,溶液碱性一直增加,pH
始终增大,D正确。
7.(2023·河北·校联考一模)下列离子方程式,不能正确解释相应现象的是
A.长期放置的 溶液中含有 :
B. 溶液中 :
C.向 溶液中加入适量 得到蓝色沉淀:
D.长期放置的 溶液中出现红棕色固体:
资料整理【淘宝店铺:向阳百分百】【答案】 D
【解析】 A. 溶液放置过程中, 被空气中氧气氧化为 ,选项A正确;B. 水解导
致其浓度减小,选项B正确;C. 水解使溶液显酸性,加入的 消耗了 促进 的水解导致形
成 沉淀,选项C正确;D.红棕色固体是 水解生成的 ,
,选项D错误;答案选D。
8.(2023·沧州部分学校测试)亚硒酸(H SeO )是一种二元弱酸。常温下,向 H SeO 溶液中逐滴
2 3 2 3
加入KOH溶液,混合溶液中lgX[X为或]与pH的变化关系如图所示。下列说法正确的是(
)
A.曲线b表示lg[]与pH的变化关系
B.H SeO 的第一步电离平衡常数K =102.37
2 3 a1
C.根据图中信息可以判断KHSeO 溶液呈碱性
3
D.pH=5.23时,溶液中存在:c(K+)+c(H+)=c(OH-)+3c(HSeO)
【答案】 D
【解析】 A.亚硒酸(H SeO )是一种二元弱酸,根据 H SeO +KOH===KHSeO +H O、
2 3 2 3 3 2
KHSeO +KOH===K SeO +H O,结合pH=2.37时,a线的lgX为0,b线的lgX为-3,则a
3 2 3 2
表示lg,b表示lg,故A错误;B.H SeO 的第一步电离为H SeO H++HSeO,lg为0时,
2 3 2 3
pH=2.37,则平衡常数K ==10-2.37,故B错误;C.根据图示信息, KHSeO 的K =10-
a1 3 a2
5.23,K ==10-11.63,电离大于水解,溶液呈酸性,故C错误;D.pH=5.23时,溶液中存在离
h2
子为H+、OH-、HSeO、K+、SeO,lg=0,有c(HSeO)=c(SeO),结合电荷守恒得c(K+)+
c(H+)=c(OH-)+c(HSeO)+2c(SeO)= c(OH-)+3c(HSeO),故D正确。
9.(2023·株洲攸县一中月考)室温下,用 0.1 mol/L的NH ·H O滴定10.00 mL 0.1 mol/L 稀盐酸,
3 2
资料整理【淘宝店铺:向阳百分百】滴定过程中加入NH ·H O的体积与溶液中lg的关系如图所示[已知:该温度下,K (NH ·H O)
3 2 b 3 2
=1.8×10-5,不考虑溶液混合时体积和温度的变化],下列说法错误的是( )
A.a点溶液中,各离子的物质的量浓度由大到小的顺序为c(H+)>c(Cl-)>c(OH-)
B.b点溶液中,所含有的溶质为NH Cl和NH ·H O
4 3 2
C.c点溶液中,=3
D.a、b、c三点溶液中,水的电离程度由大到小的顺序为a>c>b
【答案】 D
【解析】 A.a点溶液中,溶质为HCl,HCl完全电离出H+和Cl-,水也会发生微弱电离,电
离出H+和OH-,所以溶液中各离子的物质的量浓度由大到小的顺序为 c(H+)>c(Cl-)>c(OH
-),选项A正确;B.b点溶液中,c(H+)=c(OH-),溶液呈中性。氨水加入盐酸中,当两者恰
好完全反应时,溶质为氯化铵溶液,呈酸性,所以氨水过量,则溶质为 NH Cl 和NH ·H O,
4 3 2
选项B正确;C.c点加入了30 mL 的氨水,则此时溶液中的含氮微粒总数是含氯微粒总数的3
倍,即=3,选项C正确;D.a点溶质为HCl,强烈抑制水的电离;b点溶液呈中性,溶质为
NH Cl 和NH ·H O,水的电离受到促进和抑制的程度相等;c点相对于b点加入了更多的氨
4 3 2
水,水的电离受到抑制,但NH ·H O为弱电解质,水的电离受到的抑制程度小于a点,则
3 2
a、b、c三点溶液中,水的电离程度由大到小的顺序为b>c>a,选项D错误。
10.(2023·永州第一次适应性考试)常温下,用 HCl 或 NaOH 调节 0.100 mol·L-1HCOONH 的
4
pH,忽略 NH ·H O 分解及溶液体积变化,溶液中 c(HCOO-)、c(HCOOH)、c(NH)、
3 2
c(NH ·H O)四种微粒pX与pH关系如下图所示[pX=-lgc(X)]。
3 2
已知:①x、y点的坐标:x(3.75,1.3),y(9.25,1.3);②K (HCOOH)>K (NH ·H O)。下列说
a b 3 2
法正确的是( )
资料整理【淘宝店铺:向阳百分百】A.曲线①表示pc(HCOO-)随pH的变化
B.K (NH ·H O)的数量级为10-10
b 3 2
C.z点的横坐标为6.2
D.pH=7时,溶液中离子浓度大小:c(HCOO-)<c(NH)
【答案】 A
【解析】 0.100 mol·L-1HCOONH 的溶液中加入 HCl,溶液酸性增强,HCOONH +
4 4
HCl===HCOOH+NH Cl,HCOOH浓度变大、HCOO-浓度减小、NH水解受到抑制浓度稍微
4
变大;加入氢氧化钠,溶液碱性增强,HCOONH +NaOH===HCOONa+NH ·H O,NH ·H O
4 3 2 3 2
浓度变大、NH浓度减小、HCOO-水解受到抑制稍微变大;结合图像可知,①②③④分别为
HCOO-、NH ·H O、NH、HCOOH。A.由分析可知,曲线①表示pc(HCOO-)随pH的变化,
3 2
A正确;B.已知:x、y点的坐标:x(3.75,1.3),y(9.25,1.3);K (NH ·H O)= ,NH ·H O、
b 3 2 3 2
NH浓度相等时,位于y点,pH=9.25,pOH=4.75,故K (NH ·H O)=10-4.75,其数量级为10
b 3 2
-5,B错误;C.由x点的坐标:x(3.75,1.3)可知,pH=3.75,此时HCOO-、HCOOH浓度相
等,则K (HCOOH)= =10-3.75;z点NH ·H O、HCOOH浓度相等,同时HCOO-、NH浓度
a 3 2
相等,=×===10,结合K =10-14,可知c(H+)=10-6.5,其横坐标为6.5,C错误;D.初始
W
溶液为HCOONH ,由图像可知,pH=7时,溶液中c(NH ·H O)>c(HCOOH),则溶液中离子
4 3 2
浓度大小:c(HCOO-)>c(NH),D错误。
11.(2023·荆荆宜三校上学期9月联考)某二元酸H X在水中的电离方程式是 H X===H++HX
2 2
-,HX- H++X2-,常温下,向20.00 mL 0.1 mol·L-1H X溶液中滴入0.1 mol·L-1NaOH溶液,
⇌ 2
pOH 与所加NaOH溶液体积的关系如图所示。下列说法错误的是( )
水
已知pOH 表示溶液中由水电离出的c(OH-) 的负对数,即pOH =-lgc(OH-) 。
水 水 水 水
资料整理【淘宝店铺:向阳百分百】A.常温下,0.1 mol·L-1H X溶液的pH为1.4
2
B.溶液中水的电离程度:d>c>b
C.e点溶液呈碱性
D.d点溶液中存在:2c(Na+)=c(HX-)+c(X2-)
【答案】 D
【解析】 酸和碱都会抑制水的电离;向 20.00 mL 0.1 mol·L-1H X 溶液中滴入 0.1 mol·L-
2
1NaOH溶液,滴加 NaOH溶液20.00 mL 恰好生成NaHX,对应图像 b点;滴加NaOH溶液
40.00 mL 恰好生成Na X,此时由于X2-的水解对水的电离的促进作用最大,对应图像 d点;
2
此后氢氧化钠过量,水的电离又受到抑制;由 H X===H++HX-,HX-H++X2-可知,
2
H X的一级电离完全进行、二级电离部分进行。
2
A.由图可知,常温下,0.1 mol·L-1H X溶液的pOH=12.6,则pH为1.4,A正确;B.由图像可
2
知,b点溶质为NaHX,pOH =11.2,溶液中c(H+)=10-2.8 mol/L,则溶液为酸性,水的电
水
离受到抑制;c点溶质为NaHX、Na X, pOH =7,溶液中c(OH-)=10-7 mol/L,则溶液为中
2 水
性;d点溶质为Na X,水的电离受到促进,电离程度最大;故水的电离程度,d>c>b,B正确;
2
C.e 点溶质为 NaOH、Na X,水电离出的 c(OH-) =10-7 mol/L,则溶液中 c(OH-)>10-7
2 水
mol/L,溶液显碱性,C正确;D.d点溶质为Na X,根据物料守恒可知,c(Na+)=2c(HX-)+
2
2c(X2-),D错误。
12.(2023·广州质检)某浓度的二元弱酸HB溶液在不同pH下,测得pC(M)变化如图所示[已知: pC(M)=
2
-lg c(M),M代指HB或HB-或B2-],下列说法正确的是( )
2
A.曲线 Ⅱ 表示pC(HB-)与pH关系
B.pH=5时,c(HB-)c(HSO)>c(OH-),B项正确;C.常温下pH=7.0,溶液呈中性,c(OH-)=c(H+),依
据电荷守恒:c(Na+)+ c(H+)= c(HSO)+2c(SO)+ c(OH-),c(Na+)= c(HSO)+2c(SO),C
项错误;D.由图可知,在通入SO 气体的过程中,溶液的酸性不断增强,对水的电离抑制程
2
度逐渐增大,故水的电离平衡逆向移动,D项正确。
4.(2023·陕西·统考三模)已知琥珀酸[(CH COOH)]是二元弱酸,以HA代表其化学式,且pX代表-lg
2 2 2
或-lg 。常温下,用NaOH溶液滴定琥珀酸溶液,混合溶液的pH与pX的关系如图所示。
下列有关说法正确的是
A.该溶液中
B.水的电离程度d>c
C.当 被完全中和时,
D.滴定至c点时,c(Na+)<2c(A2-)+c(HA-)
【答案】 D
资料整理【淘宝店铺:向阳百分百】【分析】 HA为二元弱酸,电离方程式为: , , ,
2
,所以 , ,因为 ,所以a线为代表
,b线代表 ,据此分析答题。A. , 同一溶液中, 相
同, ,所以 ,故A错误;B. , ,d点酸性强于c点,溶液酸性越
强,对水的电离抑制成都越大,所以水的电离程度d<c,故B错误;C.当 被完全中和时,生成
,列出质子守恒为 ,故C错误;D. 此时 ,所以
,列出电荷守恒: 此时PH=4.2,所以, ,推
知 ,故D正确;答案为D。
5..(2023·河南·校联考模拟预测)用强碱滴定某一元弱酸时,弱酸被强碱部分中和后得到“弱pH酸盐和
弱酸”组成的缓冲溶液,其中存在pH=pK 一lg 。25°C时0.1mol·L-1的NaOH溶液滴定16.00mL某未
a
知浓度的HA溶液,滴定过程中消耗NaOH溶液的体积与混合溶液pH之间的关系如图所示(已知:pK=-
a
lgK,100.48=3,酸性HA>HCN)。下列说法错误的是
a
资料整理【淘宝店铺:向阳百分百】A.25℃时,HA电离常数的数量级为10-5
B.b点溶液中存在c(HA)+c(H+)>c(A-)+c(OH-)
C.c点溶液中离子浓度的大小关系为c(HA)>c(A-)>c(H+)>c(OH-)
D.若将HA改为等体积、等浓度的HCN,则pH随NaOH溶液体积的变化曲线竖直上移
【答案】 C
【解析】 温度不变,酸的电离常数不变,设酸的浓度为 ,由 ,可得
,a点 、pH=4.27,b点 、溶液的pH=4.75,存在
,化简得 ,解得c=0.2,以此解答。A.
即 ,HA电离常数的数量级为 ,故A正确;B.由分析可知
,b点时 ,故 ,此时溶液显酸性, ,
故 ,故B正确;C.由B项分析可知b点时,故 ,则随氢氧化钠
溶液体积增大,c点时溶液 ,由图可知溶液呈酸性 ,酸电离程度较小,所以离
子浓度的大小关系为: ,故C错误;D.由HA的酸性强于HCN可知,HA的
资料整理【淘宝店铺:向阳百分百】电离常数大于HCN,由 可知,当 相等时,酸的电离常数越大,溶液pH越小,则
若将HA改为等体积等浓度的HCN,则pH随NaOH溶液体积的变化曲线竖直上移,故D正确;故选C。
6..(2023·河南·校联考模拟预测)食用级NaHSO 产品用作防腐剂、抗氧化剂等。根据常温时下列实验得
3
到的粒子浓度关系正确的是
实验操作和现象 粒子浓度的关系
向蓝色石蕊试纸上滴入2滴0.1 mol ·L-1NaHSO 溶液,试纸
① 3 c(Na+) >c( ) >c( ) >c(HSO )
变红 2 3
向10 mL0.1 mol ·L-1NaHSO 溶液中加入等体积等浓度的 c(Na+)-c( ) -c( ) -c(H SO ) =0.05
② 3 2 3
NaOH溶液 mol ·L-1
向0.1 mol ·L-1NaHSO 溶液中加入等浓度的NaOH溶液至
③ 3 c( ) +c( )=c(Na+)
pH=7
A.①③ B.②③ C.①② D.①②③
【答案】 C
【解析】 NaHSO 溶液中存在 电离平衡 和水解平衡过程, 、 、
3
;向蓝色石蕊试纸上滴入2滴0.1 mol ·L-1NaHSO 溶液,试纸变红,证明0.1
3
mol ·L-1NaHSO 溶液呈酸性, ,溶液中 电离大于水解,故c(Na+) > c( ) >c( )
3
>c(H SO ),①正确;向10 mL0.1 mol ·L-1NaHSO 溶液中加入等体积等浓度的NaOH溶液,两溶液等体积混
2 3 3
合,混合后溶液中钠离子浓度降为原来的一半,则c(Na+)=0.1 mol ·L-1,c(OH-)=0.05 mol ·L-1,根据题意c(
) +c( ) +c(HSO )=c(OH-),故c(Na+)-c( ) -c( ) -c(H SO ) =0.05 mol ·L-1,②正确;向0.1
2 3 2 3
mol ·L-1NaHSO 溶液中加入等浓度的NaOH溶液至pH=7,溶液中存在电荷守恒
3
,溶液pH=7,即 ,则 ,
资料整理【淘宝店铺:向阳百分百】故③错误。故选C。
7.(2023·江苏·统考高考真题)室温下,用含少量 的 溶液制备 的过程如题图所示。已
知 , 。下列说法正确的是
A. 溶液中:
B.“除镁”得到的上层清液中:
C. 溶液中:
D.“沉锰”后的滤液中:
【答案】C
【解析】A. 溶液中存在电荷守恒: ,A错误;B.“除
镁”得到的上层清液中为 的饱和溶液,有 ,故 ,B
错误;C. 溶液中存在质子守恒: ,故
,C正确;D.“沉锰”后的滤液中还存在F-、 等离子,故电
荷守恒中应增加其他离子使等式成立,D错误。 故选C。
8..(2023·河北衡水·河北衡水中学校考模拟预测)25℃时,用 调节 二元弱酸 溶
液的 ,假设不同 下均有 。使用数字传感器测得溶液中含R微
资料整理【淘宝店铺:向阳百分百】粒的物质的量浓度随 的变化如图所示。下列分析不正确的是
A.25℃时, 溶液的
B. 溶液和 溶液中 :前者大于后者
C. 的溶液中,
D.25℃时 的 ,在足量的 溶液中滴加少量 溶液,
发生反应:
【答案】 D
【解析】 用 调节 二元弱酸 溶液的 ,随pH升高,HR的浓度降低、HR-的浓
2
度先增大后降低、R2-的浓度升高,b表示HR的物质的量浓度随 的变化,a表示HR-的物质的量浓度随
2
的变化,c表示R2-的物质的量浓度随 的变化。根据a、c曲线的交点pH=4.2,25℃时, 的
;b、c曲线的交点 ,则
, 。A.由a、c曲线的交点可知,25℃时, 的
资料整理【淘宝店铺:向阳百分百】,故A正确;B. 的水解常数 , 的
,HR电离程度大于 水解程度,所以 溶液和 溶液中,
2
前者大于后者,故B正确;C.因为 ,所以当溶液中
时, ,根据电荷守恒,
,所以 ,故C正确;D.25℃
时 的 ,酸性: ,在足量的 溶液中滴加少量
溶液生成次氯酸和NaR,发生反应: ,故D错误;选D。
2
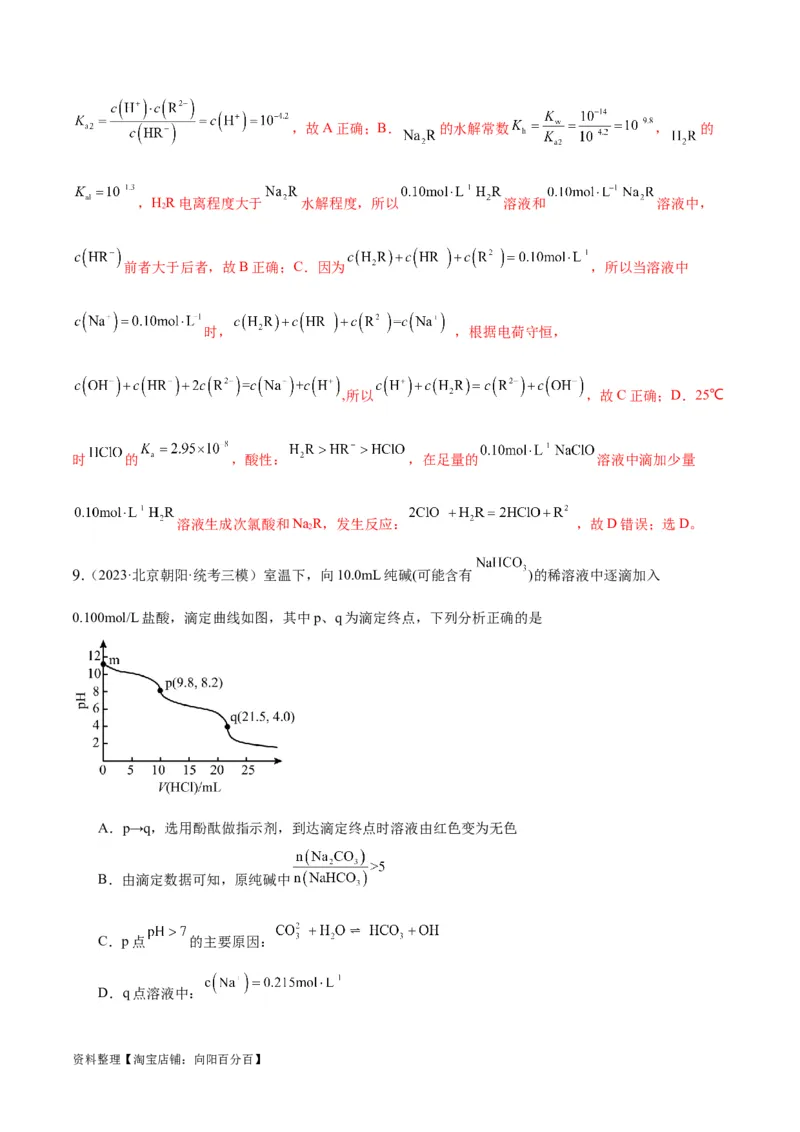
9.(2023·北京朝阳·统考三模)室温下,向10.0mL纯碱(可能含有 )的稀溶液中逐滴加入
0.100mol/L盐酸,滴定曲线如图,其中p、q为滴定终点,下列分析正确的是
A.p→q,选用酚酞做指示剂,到达滴定终点时溶液由红色变为无色
B.由滴定数据可知,原纯碱中
C.p点 的主要原因:
D.q点溶液中:
资料整理【淘宝店铺:向阳百分百】【答案】 B
【解析】 由图可知,p点溶液中的碳酸钠与盐酸恰好反应生成碳酸氢钠,反应得到氯化钠和碳酸氢钠的
混合溶液,反应方程式为NaCO+HCl=NaHCO +NaCl,q点溶液中的碳酸氢钠与盐酸恰好反应生成氯化钠、
2 3 3
二氧化碳和水,反应得到氯化钠和碳酸的混合溶液,反应方程式为NaHCO +HCl=NaCl+CO ↑+H O,由反
3 2 2
应消耗盐酸的体积可知,纯碱稀溶液中碳酸钠的物质的量为0.100mol/L×9.8×10—3L=9.8×10—4mol,碳酸氢
钠的物质的量为0.100mol/L×21.5×10—3L—9.8×10—4mol×2=1.9×10—4mol。A.由分析可知,p→q发生的反应
为溶液中的碳酸氢钠与盐酸反应生成氯化钠、二氧化碳和水,则滴定时应选用甲基橙做指示剂,不能选用
酚酞做指示剂,故A错误;B.由分析可知,原纯碱中碳酸钠的物质的量为9.8×10—4mol,碳酸氢钠的物质
的量为1.9×10—4mol,则 ,故B正确;C.由分析可知,p点所得溶液为氯化
钠和碳酸氢钠的混合溶液,溶液pH大于7是因为碳酸氢根离子在溶液中的水解程度大于电离程度,水解
的离子方程式为 ,故C错误;D.由分析可知,原纯碱中碳酸钠的物质的量为
9.8×10—4mol,碳酸氢钠的物质的量为1.9×10—4mol,则由原子个数守恒可知,q点溶液中钠离子的浓度为
≈0.068mol/L,故D错误;故选B。
10..(2023·北京海淀·北京市十一学校校考三模)为探究温度、浓度对铝和碳酸钠溶液反应的影响,某兴
趣小组查询了相关资料,并进行了实验探究。以下三组实验均采用了相同形状且等质量的打磨后的铝片。
【文献资料】
(I)铝和碱液的反应实质是铝先和水反应生成 和 ,生成的 和 反应生成 -而
溶解。
(II)碳酸氢钠溶液常温下就能缓慢分解,温度越高分解速率越大。
温度/ 溶液
实验 实验现象
① 25 0.5 5 有细小的气泡
有较多气泡,气体不能使澄清石灰水变浑
② 25 a 5
浊;用试管收集的气体靠近火焰有爆鸣声
③ 80 2.0 5 有大量白色絮状沉淀和气泡,气体可使澄
资料整理【淘宝店铺:向阳百分百】清石灰水变浑浊;气体通过 溶液除
杂后用试管收集,靠近火焰有爆鸣声
下列说法不正确的是
A.
B.实验③的反应速率比实验②更大的原因之一是实验③中 浓度更大
C.实验③中的气体为 混合气体,白色沉淀的产生可能是由于 往溶液上方移动时与
反应生成
D.将实验②中的 溶液换成相同浓度的 溶液,无白色沉淀生成
【答案】D
【解析】A.由表格数据可知,实验②和③的反应温度不同,实验目的是探究温度对铝和碳酸钠溶液反应
的影响,由探究实验的变量唯一化原则可知,实验②和③的碳酸钠溶液浓度相等,则a=2.0,故A正确;
B.由表格数据可知,实验②和③的反应温度不同,实验目的是探究温度对铝和碳酸钠溶液反应的影响,
碳酸钠在溶液中的水解反应是吸热反应,升高温度,溶液中的氢氧根离子浓度增大,与铝反应速率增大,
则实验③的反应速率比实验②更大的原因之一是实验③中氢氧根离子浓度更大,故B正确;C.由实验现
象可知实验③中的气体为二氧化碳和氢气的混合气体,二氧化碳气体是碳酸钠水解生成的碳酸氢钠受热分
解生成而得,反应生成的二氧化碳往溶液上方移动时能与溶液中的四羟基合铝离子反应生成氢氧化铝白色
絮状沉淀,故C正确;D.碳酸氢根离子能与溶液中的四羟基合铝离子反应生成氢氧化铝白色絮状沉淀,
则将实验②中的碳酸钠溶液换成相同浓度的碳酸氢钠溶液有白色沉淀生成,故D错误;故选D。
11.(2023·上海浦东新·统考二模)将pH传感器、氯离子传感器、氧气传感器分别插入盛有氯水的广口瓶
中,用强光照射,测得的实验数据如图所示。下列说法正确的是
A.图甲中pH减小是由于光照促进了HClO的电离
资料整理【淘宝店铺:向阳百分百】B.图乙中 增大主要是由于反应消耗了水
C.图丙中氧气的体积分数增大是由于HClO的分解
D.该体系中存在两个电离平衡和两个化学平衡
【答案】C
【解析】图甲中可观察到随着时间的进行,氯水的pH减小,酸性增强;图乙中随着时间的进行,溶液中
氯离子浓度增大,图丙中,氧气逐渐增多,所以久置的氯水中次氯酸发生分解产生了氢离子、氯离子和氧
气,据此分析解答。A.pH减小是由于光照促进了HClO的分解,产生了氢离子,A错误;B. 增
大主要是由于HClO的分解反应产生了氯离子,B错误;C. HClO光照分解生成HCl和氧气,所以导致
氧气的体积分数随着时间的进行不断增大,C正确;D.该体系中存在次氯酸的电离平衡和水的电离平衡
两个电离平衡,氯气与水反应的一个化学平衡,D错误;故选C。
12.(2023·浙江·校联考模拟预测) 是一元弱碱。难溶盐RA的饱和溶液中 随 而变化,
不发生水解。25℃时, 与 有如图所示线性关系。下列叙述不正确的是
A. 时,
B. 的电离平衡常数
C.当溶液 时,
D. 的溶解积
【答案】 C
资料整理【淘宝店铺:向阳百分百】【解析】 A.pH=6时, , ,由图可知此时 ,
,A正确;B.由图可知,当 =0时, ,
此时 ,则 ,选择曲线上 的点代入等
式可得, ,解得 ,B正确;C.难溶盐RA的
饱和溶液中因为阳离子的水解显酸性,所以当溶液显中性时,说明加入了碱,若加溶液 ,则
表示电荷守恒成立,若加其它碱则不成立,C错误;D.由图可知,当
=0时, ,此时 ,则 ,D
正确; 故选C。
13.一种从乙醛工业中产生的废钯(Pd)催化剂(钯5%~6%,炭93%~94%,铁、铜、锌、镍1%
~2%)中提取PdCl 和CuCl 的工艺流程如图所示:
2 2
已知:钯、铜、锌、镍可与氨水形成Pd(NH )等络离子。请回答:
3
(1)“酸溶”时,Pd转化为PdCl ,其化学方程式为_________________________________;
2
该过程需控温70~80 ℃,温度不能太低或太高的原因为
_________________________________
__________________________________________________。
(2)“络合”时,溶液的 pH 需始终维持 8~9,则络合后溶液中含铁离子的浓度
≤__________________________。[已知:Fe(OH) 、Fe(OH) 的K 分别为4×10-17、2.8×10-39]
2 3 sp
【答案】 (1)Pd+3HCl+HNO =PdCl +NOCl+2H O 温度太低反应速率过慢,温度太高王
3 2 2
水易分解挥发
资料整理【淘宝店铺:向阳百分百】(2)2.8×10-21 mol·L-1
【解析】 (1)“酸溶”时,Pd 被氧化为 PdCl ,根据流程图可知,酸溶时的还原产物为
2
NOCl,其化学方程式为 Pd+HNO +3HCl===PdCl +NOCl+2H O,该过程需控温 70~80
3 2 2
℃,温度过低会导致反应速率比较慢,温度过高时,王水会挥发分解。(2)加入王水后,溶液
中铁元素以Fe3+ 形式存在,加氨水络合后,溶液pH维持在 8~9,当pH=8 时,c(Fe3+) 最
大,最大为 ==2.8×10-21(mol·L-1),故络合后含铁离子浓度≤2.8×10-21 mol·L-1。
14.二次电池锂离子电池广泛应用于手机和电脑等电子产品中。某常见锂离子电池放电时电池
的总反应为: Li CoO + Li C === LiCoO +C (x<1)。2018年中国回收了全球可回收锂离子
1-x 2 x 6 2 6
电池总量的69%。但现阶段我国废旧电池回收仍属于劳动密集型产业,效率仍需提高。一种
回收该锂离子电池中的锂和钴的流程:
已知:①Na S O 是一种中等强度的还原剂,遇强酸分解
2 2 3
② Li CO 溶解度随温度升高而减小
2 3
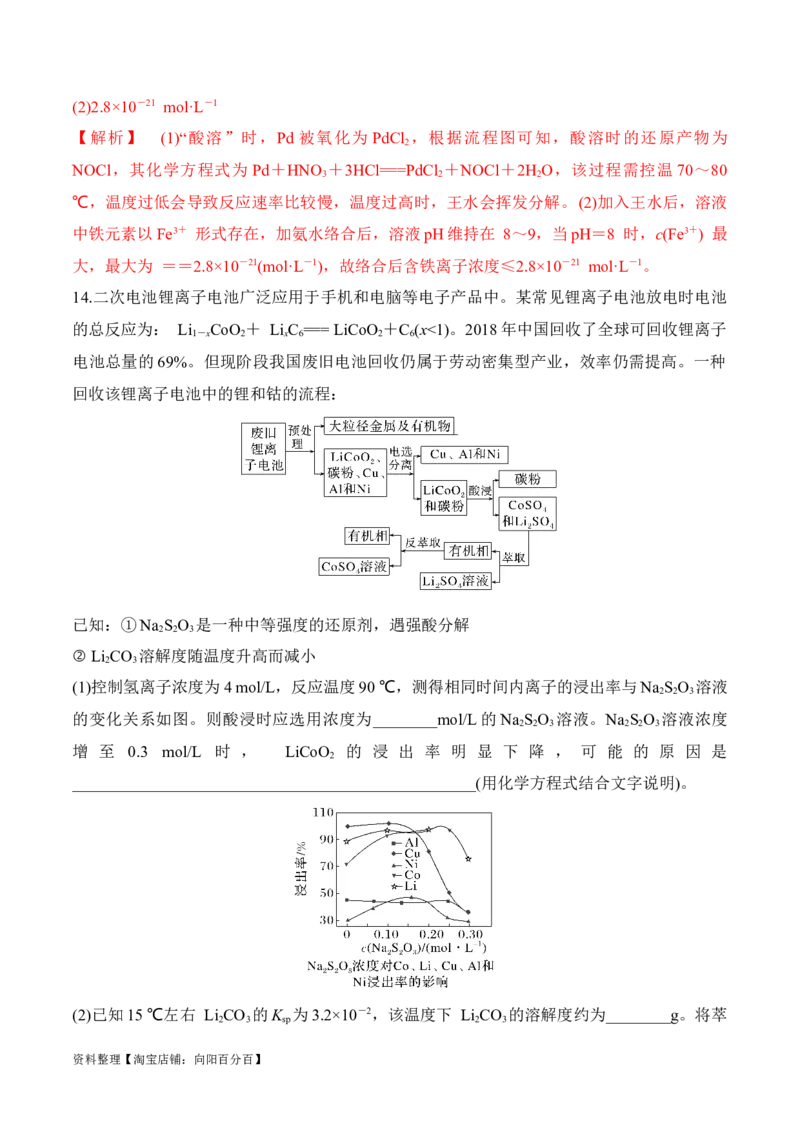
(1)控制氢离子浓度为4 mol/L,反应温度90 ℃,测得相同时间内离子的浸出率与Na S O 溶液
2 2 3
的变化关系如图。则酸浸时应选用浓度为________mol/L的Na S O 溶液。Na S O 溶液浓度
2 2 3 2 2 3
增 至 0.3 mol/L 时 , LiCoO 的 浸 出 率 明 显 下 降 , 可 能 的 原 因 是
2
__________________________________________________(用化学方程式结合文字说明)。
(2)已知15 ℃左右 Li CO 的K 为3.2×10-2,该温度下 Li CO 的溶解度约为________g。将萃
2 3 sp 2 3
资料整理【淘宝店铺:向阳百分百】取后的 Li SO 溶液加热至95 ℃,加入饱和Na CO 溶液,反应10 min,________________(填
2 4 2 3
操作)得 Li CO 粉末。
2 3
【答案】 (1)0.25 Na S O +H SO ===Na SO +S↓+SO ↑+H O,反应中产生硫单质,附着
2 2 3 2 4 2 4 2 2
在固体表面阻止反应进行
(2)1.48 趁热过滤、洗涤、干燥
【解析】 (1)通过酸浸,加入Na S O 溶液,将Cu、Al、Ni与 Li、Co分离,提高 Li、Co
2 2 3
离子的浸出率,当 Li、Co离子的浸出率最高时,Na S O 溶液的浓度为0.25 mol/L;Na S O
2 2 3 2 2 3
溶液浓度增至0.3 mol/L时,Na S O 是一种中等强度的还原剂,遇强酸分解,发生反应为:
2 2 3
Na S O +H SO ===Na SO +S↓+SO ↑+H O,反应中产生硫单质,附着在固体表面阻止反应
2 2 3 2 4 2 4 2 2
进行,导致 LiCoO 的浸出率明显下降;(2)溶解度是指一定温度下达到饱和时,100 g水中溶
2
解溶质的质量,15 ℃左右,100 g 水的体积 100 mL,根据 Li CO (s)2Li+(aq)+CO(aq),
2 3
c(Li+)=2c(CO),K (Li CO )=c2(Li+)×c(CO)=[2c(CO)]2×c(CO)=4[c(CO)]3=3.2×10-2,c(CO)
sp 2 3
===0.2 (mol/L),则溶解的 Li CO 的物质的量=0.2 mol/L×0.1 L=0.02 mol,溶解的 Li CO
2 3 2 3
的质量=0.02 mol×74 g/mol=1.48 g;将萃取后的 Li SO 溶液加热至95 ℃,加入饱和Na CO
2 4 2 3
溶液,反应10 min, Li CO 溶解度随温度升高而减小,应趁热过滤,洗涤,干燥获得 Li CO
2 3 2 3
粉末。
15.(2023秋·广东湛江·高三湛江一中校考开学考试)糠酸(熔点133℃,沸点231℃,在热水中溶解度较
大,微溶于冷水)和糠醇(熔点-29℃,沸点171℃)均为重要的化工中间体,工业上可利用糠醛(沸点
161.7℃,易被氧化)发生歧化反应制取这两种物质(该反应为强放热反应),反应原理如下:
实验步骤:
步骤1:向三颈烧瓶中加入 (约 )新蒸馏的糠醛,通过仪器A向三颈烧瓶中缓慢滴加
的 溶液。搅拌并保持反应温度为8~12℃,回流 ,得到粗产品。
步骤2:将粗产品倒入盛有 水的烧杯中,然后将液体转移至分液漏斗中,用乙醚萃取4次,分液得到
水层和醚层。
资料整理【淘宝店铺:向阳百分百】步骤3:向水层中分批滴加25%的盐酸,调至溶液的 ,冷却、结晶、抽滤、冷水洗涤,得到糠酸粗
品;向醚层中加入无水碳酸钾干燥,过滤除掉碳酸钾后,分离乙醚(乙醚的沸点为34.6℃)和糠醇。
回答下列问题:
(1)仪器A的名称为 。与直形冷凝管相比,使用仪器B的优点是 。
(2)该反应必须严格控制反应温度为8~12℃,实验中采用了哪些保障措施? 。
(3)步骤3中分离乙醚和糠醇的实验操作为 。
(4)步骤3中洗涤粗糠酸用冷水的原因是 。进一步将粗糠酸提纯,应采用的方法是 。
(5)取 提纯后的糠酸样品,配成 溶液,准确量取 于锥形瓶中,加入几滴酚酞溶液,用
标准溶液滴定,平行滴定三次,平均消耗 标准溶液 。糠酸的纯度为
。该中和滴定实验中,若其他实验操作均正确,则下列实验操作造成测得的糠酸的纯度比实际偏低的是
(填标号)。
A.蒸馏水洗净后,末用 标准溶液润洗碱式滴定管
B.指示剂酚酞溶液滴加过多(酚酞是一种弱酸)
C.锥形瓶内壁用蒸馏水洗净后,再用配制好的糠酸样品溶液润洗2~3次,将润洗液倒掉,再装入
糠酸样品溶液,进行中和滴定
D.滴定前仰视碱式滴定管液面读数,滴定后俯视碱式滴定管液面读数
【答案】(1) 恒压滴液漏斗(或恒压漏斗) 内管与冷却水的接触面积更大,冷凝效果更好
(2) 缓慢滴加 溶液,采用冰水浴给反应装置降温 (3)蒸馏
(4) 减少产品因溶解而造成的损失 重结晶
(5)99.2% D
资料整理【淘宝店铺:向阳百分百】【解析】(1)仪器A是为了平衡气压,液体顺利流入三颈烧瓶中,所以根据仪器构造与作用可知,仪器
A的名称为恒压滴液漏斗(或恒压漏斗);仪器B中内管与冷却水的接触面积更大,冷凝效果更好;(2)要
想控制反应温度为8~12℃,需要缓慢滴加 溶液,采用冰水浴给反应装置降温;(3)乙醚和糠醇互
溶,且沸点不同,所以可采用蒸馏的方式分离混合物;(4)糠酸在冷水中的溶解度小,因此用冷水洗涤
糠酸,可降低因溶解而造成的损失。将不纯的固体进一步提纯,应采用的方法是重结晶。(5)根据题干
数据可计算出糠酸的纯度为 ;
A.蒸馏水洗净后,末用 标准溶液润洗碱式滴定管,则滴定管中的标准溶液浓度变小,滴定时消耗
标准溶液的体积偏大,测得的糠酸的纯度比实际偏高,A错误;
B.指示剂酚酞溶液滴加过多(酚酞是一种弱酸),则消耗 标准溶液的体积偏大,测得的糠酸的纯度比
实际偏高,B错误;
C.锥形瓶内壁用蒸馏水洗净后,再用配制好的糠酸样品溶液润洗2~3次,将润洗液倒掉,再装入
糠酸样品溶液,进行中和滴定,则雉形瓶中糠酸样品溶液的体积偏大,滴定结束时消耗 标
准溶液的体积偏大,测得的糠酸的纯度比实际偏高,C错误;
D.D.滴定前仰视碱式滴定管液面读数,滴定后俯视碱式滴定管液面读数,则二次读数之差偏小,造成消
耗 标准溶液的体积的读数偏小,测得的糠酸的纯度比实际偏低,D正确。
资料整理【淘宝店铺:向阳百分百】